Flt4 (VEGFR-3) COMO DIANA PARA LA OBTENCIÓN DE IMÁGENES DE TUMORES Y TERAPIA ANTITUMORAL.
Un compuesto eficaz para inhibir la unión de una proteína ligando del receptor tirosina quinasa Flt4 (Flt4) a Flt4 expresado en células endoteliales vasculares de un mamífero para usar en un procedimiento de tratamiento de un mamífero que padece de una enfermedad neoplásica que se caracteriza por la expresión de Flt4 en células endoteliales de vasos sanguíneos adyacentes a un neoplasma maligno,
inhibiendo la proliferación mediada por Flt4 de dichas células endoteliales vasculares, en el que dicho compuesto comprende un polipéptido seleccionado del grupo constituido por: (a) un polipéptido que comprende un anticuerpo anti-Flt4 o un fragmento de unión a antígeno de un anticuerpo anti-Flt4; (b) un polipéptido que comprende un fragmento de Flt4 soluble, en el que dicho fragmento y dicho polipéptido son capaces de unirse a un ligando de Flt4; (c) un polipéptido que comprende un fragmento o análogo de un polipéptido precursor del factor de crecimiento endotelial vascular C (VEGF-C) de vertebrado,en el que dicho polipéptido y dicho fragmento o análogo se unen a, pero no son capaces de estimular, dicho Flt4 expresado en células huésped nativas; (d) un polipéptido que comprende un fragmento o análogo de un polipéptido precursor del factor de crecimiento endotelial vascular D (VEGF-D) de vertebrado en el que dicho polipéptido y dicho fragmento o análogo se unen a, pero no son capaces de estimular, dicho Flt4 expresado en células huésped nativas; (e) un anticuerpo anti-VEGF-C o polipéptido que comprende un fragmento de unión a antígeno del mismo; y (f) un anticuerpo anti-VEGF-D o polipéptido que comprende un fragmento de unión a antígeno del mismo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US1999/023525.
Solicitante: VEGENICS LIMITED.
Nacionalidad solicitante: Australia.
Dirección: LEVEL 1 10 WALLACE AVENUE TOORAK, VICTORIA 3142 AUSTRALIA.
Inventor/es: ALITALO,Kari,Haartman Institute, KAIPAINEN,Arja,Surgical Research Laboratory, VALLTOLA,Reija,Haartman Institute, JUSSILA,Lotta,Haartman Institute.
Fecha de Publicación: .
Fecha Solicitud PCT: 8 de Octubre de 1999.
Clasificación Internacional de Patentes:
- A61K38/17C
- A61K38/19 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Citoquinas; Linfoquinas; Interferones.
- C07K16/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
Clasificación PCT:
- A61K38/17 A61K 38/00 […] › que provienen de animales; que provienen de humanos.
- A61K38/18 A61K 38/00 […] › Factores de crecimiento; Reguladores de crecimiento.
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61K47/48
- A61K51/10 A61K […] › A61K 51/00 Preparaciones que contienen sustancias radioactivas utilizadas para la terapia o para el examen in vivo. › Anticuerpos o inmunoglobulinas; Sus fragmentos.
- G01N33/574 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para el cáncer.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
Clasificación antigua:
- A61K38/17 A61K 38/00 […] › que provienen de animales; que provienen de humanos.
- A61K38/18 A61K 38/00 […] › Factores de crecimiento; Reguladores de crecimiento.
- A61K39/395 A61K 39/00 […] › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61K47/48
- A61K51/10 A61K 51/00 […] › Anticuerpos o inmunoglobulinas; Sus fragmentos.
- G01N33/574 G01N 33/00 […] › para el cáncer.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
PDF original: ES-2357406_T3.pdf
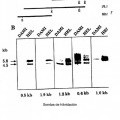
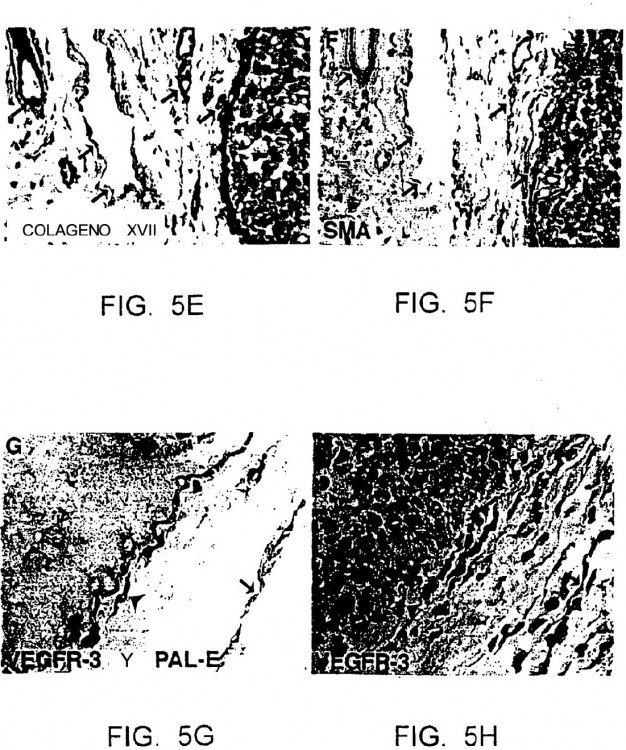
Fragmento de la descripción:
La presente invención se refiere, en general, a genes para receptores, específicamente a genes para receptores tirosina quinasas, a su inserción en vectores de ADN recombinante y a la producción de las proteínas resultantes en cepas huésped de microorganismos y células huésped eucariotas. Más específicamente, la presente invención se refiere a Flt4, un receptor tirosina quinasa; a secuencias de nucleótidos que codifican Flt4; a anticuerpos que reconocen específicamente dichos receptores; y a procedimientos que usan dichas sondas y anticuerpos y otros compuestos de unión a FIt4, por ejemplo para identificar vasos linfáticos y venulas endoteliales altas (HEV) en tejidos animales y humanos y aumentar o prevenir el crecimiento de células que expresan Flt4 en trastornos patológicos.
El comportamiento celular responsible del desarrollo, mantenimiento y reparación de células diferenciadas y tejidos está regulado, en su mayor parte, por señales intercelulares transportadas por medio de factores de crecimiento y ligandos similares y sus receptores. Los receptores están ubicados sobre la superficie celular de células receptoras y se unen a péptidos o polipéptidos conocidos como factores de crecimiento y otros ligandos similares a hormonas. Los resultados de esta interacción son cambios bioquímicos rápidos en las células receptoras, así como un reajuste rápido y a largo plazo de la expresión génica celular. Distintos receptores asociados con varias superficies celulares pueden unirse a factores de crecimiento específicos.
La fosforilación de tirosina es una de las formas clave de transducción de señal a través de la membrana plasmática. Varios genes de tirosina quinasa codifican receptores transmembranales para factores de crecimiento polipeptídicos y hormonas, tales como factor de crecimiento epidérmico (EGF), insulina, factor de crecimiento l similar a insulina (IGF-I), factores de crecimiento derivados de plaquetas (PDGF-A y -B) y factores de crecimiento fibroblásticos (FGF) [Heldin y col., Cell Regulation, 1: 555-566 (1990); Ullrich y col., Cell, 61: 243-54 (1990)]. Los receptores de varios factores de crecimiento hematopoyéticos son tirosina quinasas; éstas incluyen c-fms, que es el receptor del factor 1 estimulador de colonias [Sherr y col., Cell, 41: 665-676 (1985)] y c-kit, un receptor del factor de crecimiento hematopoyético primitivo [Huang y col., Cell, 63: 225-33 (1990)].
Estos receptores difieren en su especificidad y su afinidad. En general, los receptores tirosina quinasas son glucoproteínas que consisten en un dominio extracelular capaz de unirse a un(os) factor(es) de crecimiento específico(s), un dominio transmembranal que es generalmente una porción alfa-helicoidal de la proteína, un dominio yuxtamembranal (donde puede ser regulado el receptor por, por ejemplo, fosforilación proteica), un dominio de tirosina quinasa (que es el componente enzimático del receptor) y una cola carboxi-terminal, que en muchos receptores está implicada en el reconocimiento y la unión de los sustratos por la tirosina quinasa.
En varios receptores tirosina quinasas, los procesos de ayuste alternativo y poliadenilación alternativa son capaces de producir varios polipéptidos distintos a partir del mismo gen. Éstos pueden contener o no los diversos dominios enumerados anteriormente. Como consecuencia, algunos dominios extracelulares pueden expresarse como proteínas separadas segregadas por las células y algunas formas de los receptores pueden carecer de dominio de tirosina quinasa y contener sólo el dominio extracelular insertado en la membrana plasmática a través del dominio transmembranal más una cola carboxi-terminal corta.
La fisiología del sistema vascular, la vasculogenesis y la angiogenesis embriónica, la coagulación sanguínea, la cicatricación de heridas y la reproducción, así como varias enfermedades, implican al endotelio vascular que recubre los vasos sanguíneos. El desarrollo del árbol vascular tiene lugar mediante angiogénesis y, de acuerdo con algunas teorías, la formación del sistema linfático comienza poco después del desarrollo arterial y venoso, brotando a partir de las venas. Véase Sabin, F.R., Am. J. Anat., 9:43 (1909); y van der Putte, S.C.J, Adv. Anat. Embryol. Cell Biol., 51:3 (1975).
Después del periodo fetal, las células endoteliales proliferan muy lentamente, excepto durante angiogénesis asociada con neovascularización. Los factores de crecimiento que estimulan la angiogénesis ejercen sus efectos a través de receptores tirosina quinasas específicos de la superficie de células endotelial.
Entre los ligandos para receptores tirosina quinasas, se ha demostrado que el factor de crecimiento derivado de plaquetas (PDGF) es angiogénico, aunque débilmente, en la membrana corioalantoica de pollo. El factor de crecimiento transformante α (TGFα) es un factor angiogénico segregado por diversos tipos de células tumorales y por macrófagos. El factor de crecimiento de hepatocitos (HGF), el ligando del receptor codificado protooncogénicamente cmet es también muy angiogénico, induciendo respuestas similares a las del TGFα en cultivos de células endoteliales.
La evidencia muestra que existen factores de crecimiento y receptores específicos de células endoteliales que pueden ser responsables principales de la estimulación del crecimiento, la diferenciación y de determinadas funciones diferenciadas de células endoteliales. El factor de crecimiento estudiado con más detalle es el factor de crecimiento endotelial vascular (VEGF), un miembro de la familia de los PDGF. El factor de crecimiento endotelial vascular es una glucoproteína dimérica de subunidades de 23 kDa unidas a disulfuro, descubierta debido a su actividad mitogénica hacia las células endoteliales y su capacidad para inducir permeabilidad a los vasos (de aquí su nombre alternativo de factor de permaeabilidad vascular). Se ha informado de otros efectos del VEGF que incluyen la mobilización de Ca2+ intracelular, la inducción de la síntesis del activador plasminógeno y del inhibidor-1 del activador plasminógeno, la estimulación del transporte de hexosa en células endoteliales y la promoción de la migración de monocitos in vitro. Cuatro isoformas de VEGF, codificadas por distintas variantes de ayuste de ARNm, parecen ser capaces igualmente de mitógenesis estimulante de células endoteliales. Las isoformas de VEGF de 121 y 165 aminoácidos se segregan en una forma soluble, mientras que las isoformas de 189 y 206 restos de aminoácidos permanecen asociadas con la superficie celular y tienen una gran afinidad por la heparina. Las formas solubles que no se unen a heparina y que se unen a heparina se han descrito para el factor de crecimiento de placenta relacionado (PIGF; 131 y 152 aminoácidos, respectivamente), que se expresan en placenta, tumores trofoblásticos y células endoteliales humanas cultivadas.
El patrón de expresión de VEGF sugiere su implicación en el desarrollo y mantenimiento del sistema vascular normal y en angiogénesis de tumores. Durante el desarrollo murino, el endodermo de 7,5 días postcoitales expresa VEGF y el neuroectodermo ventricular produce VEGF en el estadio de crecimiento hacia dentro de los capilares. El día dos del desarrollo de la codorniz, el área vascularizada del saco de la yema, así como la totalidad del embrión muestran expresión de VEGF. Además, las células epiteliales próximas al endotelio fenestrado en ratones adultos muestran expresión de VEGF persistente, sugiriendo un papel en el mantenimiento de este fenotipo endotelial específico y en su función.
Se han caracterizado dos receptores de alta afinidad para VEGF, VEGFR-1/Flt1 (tirosina quinasa-1 similar a fins) y VEGFR-2/Kdr/Flk-1 (dominio del inserto quinasa que contiene receptor/quinasa-1 de hígado fetal). Estos receptores se clasifican en la familia del receptor de PDGF. No obstante, los receptores de VEGF tienen siete bucles similares a inmunoglobulina en los dominios extracelulares (como oposición a cinco en otros miembros de la familia PDGF) y un inserto de quinasa más largo. La expresión de receptores de VEGF tiene lugar principalmente en células endoteliales vasculares, aunque algunos también pueden estar presentes en monocitos y en líneas celulares de melanomas. Se ha informado que sólo las células endoteliales proliferan en respuesta a VEGF, y las células endoteliales de fuentes diferentes muestras respuestas diferentes. De este modo, las señales mediadas a través de VEGFR-1 y VEGFR-2 parecen ser específicas del tipo celular.
Los VEGFR-1 y VEGFR-2 se unen a VEGF165 con afinidad alta (Kd aproximadamente... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto eficaz para inhibir la unión de una proteína ligando del receptor tirosina quinasa Flt4 (Flt4) a Flt4 expresado en células endoteliales vasculares de un mamífero para usar en un procedimiento de tratamiento de un mamífero que padece de una enfermedad neoplásica que se caracteriza por la expresión de Flt4 en células endoteliales de vasos sanguíneos adyacentes a un neoplasma maligno, inhibiendo la proliferación mediada por Flt4 de dichas células endoteliales vasculares, en el que dicho compuesto comprende un polipéptido seleccionado del grupo constituido por:
(a) un polipéptido que comprende un anticuerpo anti-Flt4 o un fragmento de unión a antígeno de un anticuerpo anti-Flt4;
(b) un polipéptido que comprende un fragmento de Flt4 soluble, en el que dicho fragmento y dicho polipéptido son capaces de unirse a un ligando de Flt4;
(c) un polipéptido que comprende un fragmento o análogo de un polipéptido precursor del factor de crecimiento endotelial vascular C (VEGF-C) de vertebrado,en el que dicho polipéptido y dicho fragmento o análogo se unen a, pero no son capaces de estimular, dicho Flt4 expresado en células huésped nativas;
(d) un polipéptido que comprende un fragmento o análogo de un polipéptido precursor del factor de crecimiento endotelial vascular D (VEGF-D) de vertebrado en el que dicho polipéptido y dicho fragmento o análogo se unen a, pero no son capaces de estimular, dicho Flt4 expresado en células huésped nativas;
(e) un anticuerpo anti-VEGF-C o polipéptido que comprende un fragmento de unión a antígeno del mismo; y
(f) un anticuerpo anti-VEGF-D o polipéptido que comprende un fragmento de unión a antígeno del mismo.
2. Un compuesto que se une a Flt4 para usar en un procedimiento diagnóstico en vivo de detección de una enfermedad neoplásica que se caracteriza por la expresión de Flt4 en células endoteliales de vasos sanguíneos adyacentes a un neoplasma maligno.
3. Uso de un compuesto eficaz para inhibir la unión de una proteína ligando del receptor tirosina quinasa Flt4 (Flt4) a Flt4 expresado en células endoteliales vasculares de un mamífero para la fabricación de un medicamente para tratar a un mamífero que padece de una enfermedad neoplásica que se caracteriza por la expresión de Flt4 en células endoteliales de vasos sanguíneos adyacentes a un neoplasma maligno, inhibiendo la proliferación mediada por Flt4 de dichas células endoteliales vasculares, en el que dicho compuesto comprende un polipéptido seleccionado del grupo constituido por:
(a) un polipéptido que comprende un anticuerpo anti-Flt4 o un fragmento de unión a antígeno de un anticuerpo anti-Flt4;
(b) un polipéptido que comprende un fragmento de Flt4 soluble, en el que dicho fragmento y dicho polipéptido son capaces de unirse a un ligando Flt4;
(c) un polipéptido que comprende un fragmento o análogo de un polipéptido precursor del factor de crecimiento endotelial vascular C (VEGF-C) de vertebrado en el que dicho polipéptido y dicho fragmento o análogo se unen a, pero no son capaces de estimular, dicho Flt4 expresado en células huésped nativas.
(d) un polipéptido que comprende un fragmento o análogo de un polipéptido precursor del factor de crecimiento endotelial vascular D (VEGF-D) de vertebrado, en el que dicho polipéptido y dicho fragmento o análogo se unen a, pero no son capaces de estimular, dicho Flt4 expresado en células huésped nativas;
(e) un anticuerpo anti-VEGF-C o polipéptido que comprende un fragmento de unión a antígeno del mismo; y
(f) un anticuerpo anti-VEGF-D o polipéptido que comprende un fragmento de unión a antígeno del mismo.
4. Uso de un compuesto que se une a Flt4 para la fabricación de una composición para usar en un procedimiento diagnóstico en vivo de detección de una enfermedad neoplásica que se caracteriza por la expresión de Flt4 en células endoteliales de vasos sanguíneos adyacentes a un neoplasma maligno.
5. Un procedimiento in vitro de detección de una enfermedad neoplásica que se caracteriza por la expresión de Flt4 en células endoteliales de vasos sanguíneos adyacentes a un neoplasma maligno, usando un compuesto que se une a Flt4.
6. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en la reivindicación 1 o un uso tal como se reivindica en la reivindicación 3, en el que el mamífero ha sido analizado para detectar células endoteliales que expresan Flt4 en vasos sanguíneos adyacentes a un neoplasma maligno del mamífero, y mostrar de este modo que tiene un neoplasma maligno que se caracteriza por la presencia de células endoteliales que expresan Flt4 en vasos sanguíneos adyacentes a un neoplasma maligno.
7. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en cualquiera de las reivindicaciones 1, 2 ó 6, para usar tal como se reivindica en cualquiera de las reivindicaciones 3, 4 ó 6, o un procedimiento tal como se reivindica en la reivindicación 5, en el que dicha enfermedad neoplásica se selecciona del grupo que consiste en carcinomas, carcinomas de células escamosas, linfomas, melanomas y sarcomas.
8. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en cualquiera de las reivindicaciones 1, 2, 6 ó 7, para usar tal como se reivindica en una cualquiera de las reivindicaciones 3, 4, 6 ó 7, o un procedimiento tal como se reivindica en la reivindicación 5 ó 7, en el que dicha enfermedad neoplásica es un carcinoma de mama que se caracteriza por la expresión de Flt4 en células endoteliales vasculares.
9. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en cualquiera de las reivindicaciones 1, 2 ó 6 – 8, para usar tal como se reivindica en una cualquiera de las reivindicaciones 3, 4 ó 6 - 8, o un procedimiento tal como se reivindica en cualquiera de las reivindicaciones 5, 7 u 8, en el que dicho medicamento o composición es para la administración a un ser humano.
10. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en cualquiera de las reivindicaciones 1, 2 ó 6 – 9, para usar tal como se reivindica en una cualquiera de las reivindicaciones 3, 4 ó 6 - 9, o un procedimiento tal como se reivindica en cualquiera de las reivindicaciones 5 ó 7 - 9, en el que dicho compuesto comprende un anticuerpo biespecífico o un fragmento del mismo, y dicho anticuerpo o fragmento incluye un dominio de unión a antígeno que se une específicamente a Flt4 y un dominio de unión a antígeno que se une específicamente a un antígeno marcador endotelial vascular sanguíneo seleccionado del grupo constituido por PAL-E, VEGFR-1, VEGFR-2, endoglina y Factor de von Willebrand.
11. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en cualquiera de las reivindicaciones 1, 2 ó 6 – 10, para usar tal como se reivindica en una cualquiera de las reivindicaciones 3, 4 ó 6 – 10, o un procedimiento tal como se reivindica en cualquiera de las reivindicaciones 5 ó 7—10, en el que dicho compuesto comprende un anticuerpo anti-Ftl4 o un fragmento de unión a antígeno del mismo.
12. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en la reivindicación 10 ó 1, para usar tal como se reivindica en la reivindicación 10 u 11, o un procedimiento tal como se reivindica en la reivindicación 10 u 11, en el que el anticuerpo anti-Flt4 es un anticuerpo humanizado.
13. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en la reivindicación 10 ó 12, para usar tal como se reivindica en la reivindicación 10 ó 12, o un procedimiento tal como se reivindica en la reivindicación 10 ó 12, en el que dicho compuesto comprende además un antineoplásico conjugado a dicho anticuerpo o fragmento del mismo.
14. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en cualquiera de las reivindicaciones 1, 2 ó 6 – 13, para usar tal como se reivindica
en una cualquiera de las reivindicaciones 3, 4 ó 6 - 13, o un procedimiento tal como se reivindica en cualquiera de las reivindicaciones 5 ó 7 - 13, en el que dicho compuesto comprende además una etiqueta detectable.
15. Uso tal como se reivindica en la reivindicación 3 o la reivindicación 4 o cualquiera de las reivindicaciones 6 - 14 cuando dependen de las reivindicaciones 3 ó 4, en el que dicho medicamento o composición comprende además un diluyente, coadyuvante o medio vehicular farmacéuticamente aceptable.
16. Un compuesto para usar en un procedimiento diagnóstico en vivo tal como se reivindica en la reivindicación 2, el uso tal como se reivindica en la reivindicación 4 o un procedimiento tal como se reivindica en la reivindicación 5, en el que el procedimiento de detección de una enfermedad neoplásica es un procedimiento para obtener imágenes de tumores en tejidos de un organismo vertebrado, que comprende las etapas de:
(a) poner en contacto el tejido del vertebrado sospechoso de contener un tumor con una composición que comprende un compuesto de unión a Flt4;
(b) detectar dicho compuesto de unión a Flt4 unido a células de dicho tejido; y
(c) obtener imágenes de tumores sólidos identificando células endoteliales de vasos sanguíneos unidas por medio de dicho compuesto de unión a Flt4.
17. Un compuesto para usar en un procedimiento diagnóstico en vivo tal como se reivindica en la reivindicación 16, el uso tal como se reivindica en la reivindicación 16 o un procedimiento tal como se reivindica en la reivindicación 16, en el que dicho tejido comprende tejido humano.
18. Un compuesto para usar en un procedimiento diagnóstico en vivo tal como se reivindica en la reivindicación 16 ó 17, el uso tal como se reivindica en la reivindicación 16 ó 17,
o un procedimiento tal como se reivindica en la reivindicación 16 ó 17, en el que el procedimiento comprende además la etapa de lavar dicho tejido, después de dicha etapa de poner en contacto y antes de dicha etapa de obtener imágenes, en condiciones que eliminan de dicho tejido el compuesto de unión a Flt4 que no está unido a Flt4 en dicho tejido.
19. Un compuesto para usar en un procedimiento diagnóstico en vivo tal como se reivindica en una cualquiera de las reivindicaciones 16 - 18, el uso tal como se reivindica en una cualquiera de las reivindicaciones 16 - 18, o un procedimiento tal como se reivindica en una cualquiera de las reivindicaciones 16 - 18, en los que dicho compuesto de unión a Flt4 es un compuesto que se une a Flt4 tal como se define en una cualquiera de las reivindicaciones 10 - 14.
20. Un compuesto para usar en un procedimiento diagnóstico en vivo tal como se reivindica en una cualquiera de las reivindicaciones 16 - 19, el uso tal como se reivindica en
una cualquiera de las reivindicaciones 16 - 19, o un procedimiento tal como se reivindica en una cualquiera de las reivindicaciones 16 – 19, en el que el procedimiento comprende además las etapas de:
poner en contacto el tejido con un segundo compuesto que se une específicamente a un marcador endotelial de vasos sanguíneos que está sustancialmente ausente de endotelios linfáticos; y detectar dicho segundo compuesto unido a células de dicho tejido;
en el que dicha etapa de obtener imágenes comprende identificar vasos sanguíneos etiquetados con el compuesto de unión a Flt4 y el segundo compuesto, en el que los vasos sanguíneos etiquetados con el compuesto de unión a Flt4 y el segundo compuesto se correlacionan con la presencia y localización de un tumor en el tejido.
21. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en la reivindicación 1 o un uso tal como se reivindica en la reivindicación 3, en el que el compuesto es un fragmento de Flt4 soluble, y el fragmento es capaz de unirse a un ligando de Flt4.
22. Un compuesto para usar en un procedimiento de tratamiento tal como se reivindica en la reivindicación 1 o un uso tal como se reivindica en la reivindicación 3, en el que el compuesto es una molécula de ácido nucleico que codifica un fragmento de Flt4 soluble, y el fragmento es capaz de unirse a un ligando de Flt4.
23. Uso de una composición que comprende un polipéptido constituido por un fragmento de un dominio extracelular de Flt4, en el que el fragmento es capaz de unirse a un ligando de Flt4, para la fabricación de un medicamento para el tratamiento de una enfermedad neoplásica que se caracteriza por la expresión de Flt4 en células endoteliales vasculares.
24. Uso de un polipéptido constituido por un fragmento de un dominio extracelular de Flt4, en el que el fragmento es capaz de unirse a un ligando de Flt4, para la fabricación de un medicamento para el tratamiento de una enfermedad neoplásica que se caracteriza por la expresión de Flt4 en células.
25. Una composición tal como se reivindica en la reivindicación 23 o un uso tal como se reivindica en la reivindicación 24, en la que la enfermedad neoplásica es un carcinoma, carcinoma de células escamosa, carcinoma de mama, linfoma, melanoma o sarcoma.
26. Una composición tal como se reivindica en la reivindicación 23 o la reivindicación 25 o uso tal como se reivindica en la reivindicación 24 o la reivindicación 25, en la que el polipéptido está conjugado a un profármaco o agente antiangiogénico.
27. Una composición tal como se reivindicación en la reivindicación 23, reivindicación 25 ó 26, o uso tal como se reivindica en cualquiera de las reivindicaciones 24 – 26, que es para la administración conjunta con un agente antiangiogénico.
28. Un anticuerpo biespecífico, o un fragmento del mismo, que se une a Flt4 y se une a un antígeno marcador endotelial de vasos sanguíneos seleccionado del grupo que consiste en PAL-E, VEGFR-1, VEGFR-2, endoglina y Factor de von Willebrand.
29. Un anticuerpo biespecífico o un fragmento tal como se reivindica en la 5 reivindicación 28, que está conjugado a un agente citotóxico.
30. Un anticuerpo biespecífico o un fragmento tal como se reivindica en la reivindicación 28 ó 29, que está conjugado a un profármaco.
31. Una composición que comprende un anticuerpo biespecífico o un fragmento tal
como se reivindica en cualquiera de las reivindicaciones 28 – 30 y un excipiente, diluyente o 10 vehículo farmacéuticamente aceptable.
Patentes similares o relacionadas:
Métodos y composiciones para tratar y prevenir enfermedades asociadas con la integrina AVB8, del 29 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un anticuerpo aislado que se une específicamente a la integrina β8 humana e inhibe la adhesión del péptido asociado a latencia (LAP) a ανβ8, en donde el […]
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Bloqueo de CD73, del 22 de Julio de 2020, de Innate Pharma: Un anticuerpo aislado que específicamente se une a un polipéptido CD73 humano en la superficie de una célula y que tiene capacidad de neutralizar […]
Composición de anticuerpos monoclonales dirigidos contra BDCA-2, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Composición de anticuerpos monoclonales dirigidos contra la proteína BDCA-2, presentando dichos anticuerpos un porcentaje de fucosilación inferior al 60% […]
Anticuerpos anti-PD-L1 y usos de los mismos, del 22 de Julio de 2020, de MERCK PATENT GMBH: Un anticuerpo anti-PD-L1 aislado o su fragmento de union a antigeno que comprende una secuencia de region variable de cadena pesada y de cadena ligera, en donde: […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]