USO DE POLIMEROS ACTIVADOS PARA LA SEPARACION DE MULTIMEROS PROTEICOS Y POLIPEPTIDICOS.
Uso de un polímero activado para separar un multímero polipeptídico asociado no covalentemente,
que comprende múltiples subunidades polipeptídicas, en múltiples subunidades polipeptídicas, en el que
- el polímero activado comprende una fracción química mediante la cual el polímero puede enlazarse covalentemente a la subunidad polipeptídica en el multímero polipeptídico asociado no covalentemente.
- el polímero activado es un polietilenglicol activado, un polidextran activado o una poli-L-lisina activada, y
- cada una de las subunidades polipeptídicas comprende una cadena polipeptídica única; y/o un grupo de al menos dos cadenas polipeptídicas únicas, en las que al menos dos cadenas polipeptídicas únicas están enlazadas covalentemente, una a la otra, y en las que al menos una de las subunidades polipeptídicas comprende un anticuerpo de cadena única que comprende al menos una región variable de anticuerpo
Tipo: Resumen de patente/invención. Número de Solicitud: W06001359EP.
Solicitante: MICROMET AG.
Nacionalidad solicitante: Alemania.
Dirección: STAFFELSEESTRASSE 2,81477 MUNCHEN.
Inventor/es: WOLF, ANDREAS, RAUM, TOBIAS, HOFFMANN,PATRICK, HEPP,NEE HENCKEL,JULIA.
Fecha de Publicación: .
Fecha Concesión Europea: 4 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- A61K47/48H4P
- C07K1/107D4
- C07K16/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
Clasificación PCT:
- A61K47/48
- C07K1/107 C07K […] › C07K 1/00 Procedimientos generales de preparación de péptidos. › por modificación química de los péptidos precursores.
- C07K16/46 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › Inmoglobulinas híbridas (híbridos de una inmunoglobulina con un péptido distinto de una inmunoglobulina C07K 19/00).
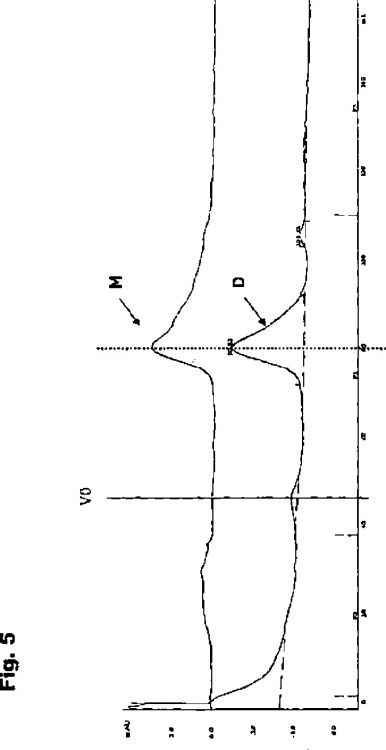
Fragmento de la descripción:
Uso de polímeros activados para la separación de multímeros proteicos y polipeptídicos.
La presente invención se refiere a un uso de polímeros activados. Específicamente, la presente invención se refiere a un uso de polímeros activados en el campo de la preparación de proteínas y/o polipéptidos.
Tras una expresión recombinante, las moléculas proteicas y/o polipeptídicas existen frecuentemente en una o más isoformas, es decir, estas moléculas exhiben frecuentemente heterogenicidad de producto. Como ejemplo particularmente bien estudiado, se conoce que los anticuerpos de cadena única, o scFvs, existen tras una expresión recombinante como una mezcla de especies monoméricas y multiméricas, principalmente diméricas. Las especies monoméricas resultan de la asociación covalente o no covalente de las regiones variables del anticuerpo en la misma cadena polipeptídica, unas con las otras. Por otra parte, las especies diméricas resultan de una asociación de la primera cadena polipeptídica y de la segunda cadena polipeptídica, comprendiendo cada una, por ejemplo, dos regiones variables A y B complementarias del anticuerpo, una con la otra, de manera que la región variable A de la primera cadena polipeptídica se asocia con la región variable B de la segunda cadena polipeptídica, y viceversa. Estas especies son conocidas normalmente como un diacuerpo (Hudson et al. (1999) J. Immunol. Met. 231, 177-189).
En los casos en que los polipéptidos están destinados a un uso terapéutico posterior, dicha heterogenicidad de producto es generalmente no deseable, ya que los productos heterogéneos exhiben frecuentemente propiedades farmacocinéticas o actividades biológicas distintas. En el desarrollo de un polipéptido terapéutico, es importante poder predecir como actuará este polipéptido in vivo (es decir, su modo de acción cualitativo) así como la magnitud de esta actividad biológica (es decir, su eficacia cuantitativa y su distribución en el cuerpo). Dichas predicciones son frecuentemente difíciles de realizar con seguridad para productos heterogéneos (Moore et al. (1999) Biochemistry. 38, 13960-13967).
Sin embargo, también puede ser problemático crear un producto homogéneo que permanezca como tal. Esto es así debido a que la heterogenicidad del polipéptido es frecuentemente el resultado de un equilibrio termodinámico entre el polipéptido monomérico y el multimérico; tras la retirada de una de las especies, el equilibrio se restablece entre ambas especies (Lee et al. (2002) J. Mol. Biol. 320,107-127). Esto se aplica tanto a la fracción retirada como a la fracción restante, de manera que un tiempo después de una separación cromatográfica, cada fracción exhibirá aproximadamente la misma relación monómero:multímero, siendo esta relación el resultado de la equilibración isomérica entre ambas o entre todas las especies de polipéptidos. Entonces, una simple retirada cromatográfica de una de las especies polipeptídicas representa frecuentemente solo una solución temporal al problema de la heterogenicidad del producto, ya que frecuentemente existe un impulso termodinámico natural hacia un producto heterogéneo. Este problema puede ser salvado mediante la conversión de un producto purificado deseado en una forma en la que la equilibración termodinámica entre las isoformas ya no pueda ocurrir, por ejemplo, en un producto liofilizado. A continuación, este producto liofilizado es reconstituido inmediatamente antes de la administración en el punto de tratamiento, de manera que se eliminan una equilibración termodinámica no deseada y un incremento concomitante en la heterogenicidad del producto o al menos se mantienen en un mínimo absoluto. Sin embargo, la separación de la isoforma no deseada de una mezcla heterogénea resulta frecuentemente en una pérdida considerable de producto polipeptídico.
Independientemente de los problemas de la heterogenicidad polipeptídica, el desarrollador de los polipéptidos terapéuticos se encuentra frecuentemente con la necesidad de modular las propiedades farmacocinéticas y/o inmunogénicas del polipéptido destinado a ser administrado. Por ejemplo, el polipéptido destinado para terapia puede ser eliminado del suero del paciente demasiado rápidamente para provocar cualquier efecto terapéutico, un problema que generalmente se convierte en más intratable cuanto más pequeño es el peso molecular del polipéptido. La tasa de eliminación de un polipéptido terapéutico del suero de un paciente puede ser acelerada sin desearlo si el polipéptido desencadena una respuesta inmunogénica, es decir, si el sistema inmune del paciente monta una respuesta inmune al material extraño. Por cada una de estas razones, es frecuentemente deseable derivar un polipéptido destinado para la administración a un paciente, de manera que se extienda la vida media en suero y se reduzca la inmunogenicidad del polipéptido, siendo lo primero un resultado, al menos en parte, de lo último.
Estos objetivos se han cumplido mediante una conjugación de polímeros orgánicos extendidos con polipéptidos terapéuticos. Para citar un ejemplo en la literatura, se ha usado una conjugación de polipéptidos con polietilenglicol ("PEG") con este fin (Roberts et al. (2002) Adv. Drug Delivers Rev. 54, 459-476). La conjugación con polímeros orgánicos extendidos incrementa el peso molecular efectivo de los polipéptidos mientras que, al mismo tiempo, los protege del reconocimiento por el sistema inmune, cada uno de los cuales tiene el efecto de que la vida media en suero del polipéptido se extiende ventajosamente.
Por lo tanto, el desarrollador de polipéptidos terapéuticos se encuentra frecuentemente con el reto doble de generar un producto homogéneo mejorando al mismo tiempo las propiedades farmacocinéticas y/o inmunogénicas de este producto. Combinadas, estas consideraciones necesitan numerosas etapas secuenciales de aislamiento, purificación y conjugación, cada una de las cuales resulta en una pérdida de producto y tiempo y, en general, en una complejidad y un coste añadidos a todo el proceso de producción. Por lo tanto, es un objeto de la invención proporcionar una manera alternativa, más concertada, de abordar los problemas mencionados anteriormente.
Los inventores de la presente invención han descubierto ahora sorprendentemente que la conjugación de polipéptidos con polímeros extendidos resulta no solo en las ventajas ya reconocidas para dichos polímeros (es decir, mejora de las propiedades farmacocinéticas y/o inmunogénicas de un producto), sino también en la separación de polipéptidos multiméricos en polipéptidos monoméricos conjugados en una manera permanente.
Por consiguiente, un aspecto de la presente invención se refiere al uso de un polímero activado para separar un multímero polipeptídico asociado no covalentemente, que comprende múltiples subunidades polipeptídicas, en dichas múltiples subunidades polipeptídicas, según las reivindicaciones adjuntas.
Según este aspecto de la invención, se usa un polímero, preferentemente un polímero orgánico, en una forma activada. El término "activada" se refiere a cualquier forma del polímero que comprenda una fracción química mediante la cual el polímero pueda ser enlazado covalentemente a una subunidad polipeptídica en el multímero polipeptídico asociado no covalentemente. Debido a que un polímero que comprende dicha fracción retendrá esta fracción tras enlazarse covalentemente a la subunidad polipeptídica, el término "polímero activado", tal como se usa en la presente memoria, se refiere al polímero tanto antes como también después del acoplamiento a la subunidad polipeptídica, es decir, un polímero activado que ya ha formado un enlace covalente con una subunidad polipeptídica será denominado todavía como un "polímero activado". Preferentemente, la fracción química para el enlace covalente al polipéptido reaccionará bajo condiciones fisiológicas o condiciones cercanas a las fisiológicas, o al menos bajo condiciones que no serán dañinas para las subunidades polipeptídicas del multímero polipeptídico asociado no covalente- mente.
La expresión "multímero polipeptídico asociado no covalentemente" debe entenderse que abarca cualquier especie polipeptídica que comprende al menos dos cadenas polipeptídicas que pueden separarse una de la otra sin romper ningún enlace químico covalente. La asociación puede ser de una naturaleza ordenada, por ejemplo del tipo observado entre dos polipéptidos que son complementarios estéricamente y/o electrostáticamente uno respecto al otro. Como un ejemplo de dicha asociación ordenada, puede...
Reivindicaciones:
1. Uso de un polímero activado para separar un multímero polipeptídico asociado no covalentemente, que comprende múltiples subunidades polipeptídicas, en múltiples subunidades polipeptídicas, en el que
- - el polímero activado comprende una fracción química mediante la cual el polímero puede enlazarse covalentemente a la subunidad polipeptídica en el multímero polipeptídico asociado no covalentemente.
- - el polímero activado es un polietilenglicol activado, un polidextran activado o una poli-L-lisina activada, y
- - cada una de las subunidades polipeptídicas comprende una cadena polipeptídica única; y/o un grupo de al menos dos cadenas polipeptídicas únicas, en las que al menos dos cadenas polipeptídicas únicas están enlazadas covalentemente, una a la otra, y en las que al menos una de las subunidades polipeptídicas comprende un anticuerpo de cadena única que comprende al menos una región variable de anticuerpo.
2. Uso según la reivindicación 1, en el que el polímero activado tiene un peso molecular de al menos 3.000 g/mol y comprende de 25 a 70% en peso de átomos polares, en el que los átomos polares son átomos que participan en interacciones de enlace de hidrógeno con moléculas de agua en solución acuosa.
3. Uso según la reivindicación 1 ó 2, en el que cada una de las múltiples subunidades polipeptídicas en su forma separada está enlazada al polímero activado.
4. Uso según la reivindicación 3, en el que cada una de las múltiples subunidades polipeptídicas en su forma separada está enlazada covalentemente al polímero activado.
5. Uso según cualquiera de las reivindicaciones anteriores, en el que el anticuerpo de cadena única comprende una o más regiones variables de anticuerpo.
6. Uso según cualquiera de las reivindicaciones anteriores, en el que cada una de las subunidades polipeptídicas está enlazada covalentemente al polímero activado mediante un grupo amino, un grupo sulfhidrilo, un grupo carboxilo, un grupo hidroxilo o un grupo aldehído comprendido dentro/en la subunidad polipeptídica.
7. Uso según la reivindicación 6, en el que
- el polímero activado que es capaz de formar un enlace químico covalente con un grupo amino comprendido dentro de la subunidad polipeptídica comprende un grupo hidroxisucinimidilo, un grupo carboxilo, un grupo epóxido, un grupo ceto o un grupo aldehído;
- el polímero activado que es capaz de formar un enlace químico covalente con un grupo sulfhidrilo comprendido dentro de la subunidad polipeptídica comprende un grupo maleimida, un grupo vinil sulfona o un grupo sulfhidrilo;
- el polímero activado que es capaz de formar un enlace químico covalente con un grupo con un grupo carboxilo comprendido dentro de la subunidad polipeptídica comprende un grupo amino o un grupo hidroxilo; y/o
- el polímero activado que es capaz de formar un enlace químico covalente con un grupo hidroxilo comprendido dentro de la subunidad polipeptídica comprende un grupo carboxilo, un grupo aldehído o un grupo ceto.
8. Uso según cualquiera de las reivindicaciones 3-7, en el que cada subunidad polipeptídica está enlazada covalentemente al polímero activado mediante un carbohidrato comprendido dentro de la subunidad polipeptídica, cuyo carbohidrato ha sido modificado químicamente para comprender al menos un grupo aldehído.
9. Uso según la reivindicación 8, en el que el polímero activado es capaz de formar un enlace químico covalente con el carbohidrato que comprende el grupo aldehído que comprende un grupo amino o un grupo hidracida.
10. Uso según la reivindicación 9, en el que el enlace covalente entre el aldehído y el grupo amino o grupo hidracida es estabilizado mediante aminación reductiva.
11. Uso según la reivindicación 1, en el que el polietilenglicol se selecciona de entre el grupo que comprende mPEG-SPA (mPEG-propionato de succinimidilo), mPEG-SBA (mPEG-butanoato de succinimidilo), mPEG-SMB (mPEG-alfa-metilbutanoato de succinimidilo), mPEG2-NHS (mPEG2-N-hidroxisuccinimida), mPEG-OPTE (mPEG-tioéster), mPEG-CM-HBA-NHS (mPEG-carboximetil-3-ácido hidroxibutanoico-N-hidroxisuccinato), mPEG-ACET (mPEG-acetaldehído dietil acetal), mPEG2-acetaldehído (equivalente a mPEG2-dietil acetal), mPEG-propionaldehído, mPEG2-propionaldehído, mPEG-butiraldehído, mPEG2-butiraldehído, mPEG-cetonas, mPEG-MAL (mPEG-maleimida), mPEG2-MAL (mPEG2-maleimida) y mPEG-tioles.
12. Uso según cualquiera de las reivindicaciones anteriores, en el que el polímero activado tiene un peso molecular de 3.500 g/mol, 5.000 g/mol, 20.000 g/mol o 40.000 g/mol.
13. Uso según la reivindicación 11 o la reivindicación 12, en el que el mPEG-MAL es mPEG-MAL o mPEG2-MAL que tiene un peso molecular de 40.000 g/mol.
14. Uso según cualquiera de las reivindicaciones anteriores, en el que el polímero activado comprende
- de 27 a 60% en peso de átomos polares, particularmente de 32 a 45% en peso de átomos polares, de 35 a 38% en peso de átomos polares, o
- de 36 a 37% en peso de átomos polares;
- de 27 a 28% en peso de átomos polares;
- de 48 a 50% en peso de átomos polares; o
- de 54 a 56% en peso de átomos polares,
en el que los átomos polares son átomos que participan en interacciones de enlace de hidrógeno con moléculas de agua en solución acuosa.
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
 Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Animales no humanos que tienen un locus de cadena ligera lambda de inmunoglobulina modificado por ingeniería, del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Un roedor cuyo genoma de la línea germinal comprende un locus de cadena ligera λ de inmunoglobulina endógeno que comprende:
(a) uno o más segmentos […]
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Formulación anti-IFNAR1 estable, del 24 de Junio de 2020, de ASTRAZENECA AB: Una formulacion de anticuerpo que comprende: a. De 100 mg/ml a 200 mg/ml de anifrolumab; b. Lisina HCl 40 mM a 60 mM; c. Trehalosa […]
Proteínas y péptidos modificados, del 24 de Junio de 2020, de GLAXO GROUP LIMITED: Un dominio variable de inmunoglobulina único, que se une a TNFR1 y que se selecciona de cualquiera de las siguientes secuencias de aminoácidos: (a) DOM1h-131-206 caracterizada […]
Métodos para purificar una proteína objetivo de una o más impurezas en una muestra, del 17 de Junio de 2020, de EMD Millipore Corporation: Un metodo para purificar una proteina objetivo que contiene una region Fc de una o mas impurezas en una muestra, el metodo comprende las etapas de: a) poner en contacto […]
Dominios variables de inmunoglobulina, del 10 de Junio de 2020, de Ablynx NV: Dominio variable individual de inmunoglobulina de cadena pesada (ISVD), en que el residuo aminoacídico en la posición 89 es L y el residuo […]
Criterio de valoración terapéutico equivalente para inmunoterapia de enfermedades basada en antiCTLA-4, del 10 de Junio de 2020, de E. R. Squibb & Sons, L.L.C: Un anticuerpo antiCTLA-4 para su uso en el tratamiento de cáncer en un sujeto, tratamiento que comprende inducir un acontecimiento liminar […]