PRODUCCION DE AUTOANTICUERPOS DE REPERTORIOS DE SEGMENTOS DE ANTICUERPOS EXPRESADOS EN LA SUPERFICIE DE FAGOS.
Procedimiento de obtención de un miembro de una pareja de unión específica (miembro sbp),
cuyo miembro sbp tiene un sitio de unión a antígeno con especificidad de unión para un autoantígeno diana de una especie de mamífero, donde el miembro sbp es un dominio VH de un anticuerpo de la especie de mamífero, comprendiendo el procedimiento:
(a) proporcionar una biblioteca de partículas de bacteriófagos filamentosos, expresando cada una de las partículas de bacteriófagos filamentosos en su superficie un miembro sbp, y conteniendo cada partícula de bacteriófago filamentoso ácido nucleico con la secuencia que codifica el miembro sbp expresado en la superficie de esa partícula de bacteriófago filamentoso, donde proporcionar la biblioteca comprende preparar dicho ácido nucleico a partir de secuencias de anticuerpos de un mamífero de la especie no inmunizada con el autoantígeno diana y no tener una enfermedad autoinmune contra el autoantígeno diana, sin determinar que los anticuerpos con especificidad de unión para dicho autoantígeno diana son detectables cuando circulan en un mamífero de la especie;
(b) seleccionar, mediante unión con dicho autoantígeno diana, uno o más miembros sbp con especificidad de unión para dicho autoantígeno diana
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E06001908.
Solicitante: CAMBRIDGE ANTIBODY TECHNOLOGY LIMITED
MEDICAL RESEARCH COUNCIL.
Nacionalidad solicitante: Reino Unido.
Dirección: MILSTEIN BUILDING GRANTA PARK,CAMBRIDGE CB1 6GH.
Inventor/es: MCCAFFERTY, JOHN, GRIFFITHS, ANDREW DAVID, MARKS, JAMES DAVID, WINTER, GREGORY, PAUL, GRIGG,GEOFFREY WALTER, HOOGENBOOM,HENDRICUS RENERUS JACOBUS M.
Fecha de Publicación: .
Fecha Solicitud PCT: 2 de Diciembre de 1992.
Fecha Concesión Europea: 7 de Abril de 2010.
Clasificación Internacional de Patentes:
- C07K16/00A
- C07K16/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
- C07K16/24B
- C07K16/26 C07K 16/00 […] › contra hormonas.
- C07K16/28 C07K 16/00 […] › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C07K16/28A14
- C07K16/28G
- C07K16/28H
- C07K16/30A
- C07K16/30S20
- C07K16/34 C07K 16/00 […] › contra antígenos de grupo sanguíneo.
- C07K16/42K14
Clasificación PCT:
- C07K16/18 C07K 16/00 […] › contra materiales animales o humanos.
- C07K16/24 C07K 16/00 […] › contra citoquinas, linfoquinas o interferones.
- C07K16/28 C07K 16/00 […] › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C07K16/30 C07K 16/00 […] › de células tumorales.
- C12N15/13 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Inmunoglobulinas.
- C12N15/62 C12N 15/00 […] › Secuencias de ADN que codifican proteínas de fusión.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda.
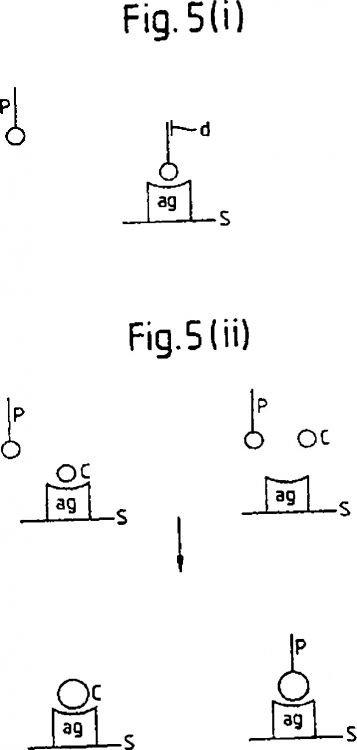
Fragmento de la descripción:
Producción de autoanticuerpos de repertorios de segmentos de anticuerpos expresados en la superficie de fagos.
Esta invención hace referencia al aislamiento de moléculas de anticuerpo dirigidas contra autoantígenos, en particular anticuerpos humanos dirigidos contra autoantígenos humanos. La tecnología de la expresión en fagos para la selección de moléculas de anticuerpo se describió en la patente internacional WO92/01047, PCT/GB92/00883, PCT/GB92/01755 y GB92/0206372.6. Los solicitantes demuestran que los anticuerpos dirigidos contra autoantígenos pueden aislarse mediante tecnología de expresión en fagos.
Los autoanticuerpos humanos son de particular valor para propósitos terapéuticos y diagnósticos in vivo, ya que evitan problemas que sobrevienen de la antigenicidad de anticuerpos foráneos, por ejemplo de ratón. Los anticuerpos más utilizados para la terapia son aquellos que se dirigen a moléculas efectoras de superficie celular, como los receptores, adhesinas e integrinas, y los que se dirigen contra moléculas efectoras biológicas circulantes, como las hormonas, los factores de crecimiento y las citoquinas. Ha sido extremadamente difícil obtener anticuerpos humanos dirigidos contra autoantígenos. Esta invención proporciona una vía potente de obtención de dichos anticuerpos.
Existe una demanda para aislar un fragmento de anticuerpo con especificidad contra autoantígenos. Los animales no producen anticuerpos normalmente contra autoantígenos, un fenómeno denominado tolerancia (G.J. Nossal Science 245, 147-153, 1989). Las enfermedades autoinmunes pueden resultar de la rotura de la tolerancia. Por lo general, la vacunación con un autoantígeno no resulta en la producción de anticuerpos circulantes. Por ello es difícil de generar anticuerpos contra autoantígenos, en particular en humanos. Es posible generar anticuerpos que reconozcan antígenos humanos en un animal como el ratón, especialmente si el antígeno humano no está estrechamente relacionado con cualquier equivalente en el animal. Si se requiere un anticuerpo humano, entonces es necesario "humanizar" el anticuerpo, por ejemplo mediante trasplante de CDR (patente GB2188638B).
La tecnología de anticuerpos de fagos tal como se describe en la patente internacional W092701047 ofrece la posibilidad de aislar anticuerpos humanos directamente. En esta solicitud, se demuestra por primera vez que los anticuerpos contra autoantígenos pueden aislarse de bibliotecas de fagos derivadas, por ejemplo, de fuentes no inmunizadas y de bibliotecas preparadas por recombinación sintética de secuencias de genes-V, preferiblemente recombinación de secuencias VH con secuencias, DH y JH, y VL con JL. Estos anticuerpos son específicos para su antígeno. Esta aplicación muestra que las bibliotecas únicas derivadas de esta manera pueden actuar como fuente de antígenos foráneos y de autoantígenos y permite la exploración de una biblioteca amplia para aislar anticuerpos contra cualquier antígeno.
En la patente internacional WO92/01047 se describió que los fragmentos de anticuerpo pueden expresarse en la superficie de bacteriófagos y que éstos pueden unirse al antígeno. Los fragmentos de anticuerpo pueden seleccionarse directamente utilizando esta característica. La capacidad para aislar los fragmentos de anticuerpo (Fab, Fv, scFv y VH) utilizando su expresión sobre la superficie del bacteriófago filamentoso ha abierto la posibilidad de aislar especificidades de anticuerpos (es decir, anticuerpos dirigidos contra un antígeno en particular) que hasta ahora eran difíciles o imposibles de aislar. En particular, la patente internacional WO92/01047 demuestra que las especificidades de anticuerpo pueden aislarse de un humano que no ha sido inmunizado específicamente ("no inmunizado"), incluso espe- cificidades para antígenos como el 2-fenil-5-oxazolona con el que los humanos no estarían normalmente expuestos.
En realizaciones de la presente invención, los repertorios de anticuerpos sintéticos o naturales derivados de secuencias de una especie de mamífero, tal como humano, ratón, rata, oveja, cerdo, cabra, caballo u otras secuencias, se expresan en la superficie de una partícula de bacteriófago filamentoso, referido aquí como un paquete de expresión genética replicable (rgdp) y la especificidad de unión para él mismo se selecciona mediante la unión al autoantígeno. En este proceso, los repertorios de genes V se derivan de genes V reordenados in vitro o in vivo y o mediante mutación de (a) un gen o genes V reordenados. Una característica clave de los repertorios de genes V es que son extremadamente diversos en su secuencia, generalmente en más de 106 miembros distintos. Incluso, es posible que una biblioteca suficientemente grande pueda proporcionar una fuente de especificidades dirigida contra cualquier autoantígeno. Los repertorios de genes V se clonan en el rgdp de un vector de fago filamentoso, de modo que los repertorios de anticuerpos se expresan en la superficie de rgdp. Los rgdps que codifican especificidades de anticuerpo raras que se unen a su propio anticuerpo, pueden seleccionarse en virtud de la unión a su propio antígeno. Los repertorios de anticuerpos pueden clonarse en un replicón sencillo o un formato de doble replicón como el descrito en la patente internacional WO92/01047 y la PCT/GB92/00883.
Los genes V pueden clonarse en el material genético del rgdp, y expresarse como dominios únicos, por ejemplo, dominios variables de cadena pesada únicos, denominados ligandos de dominios únicos o "dAbs" (véase WO90/01544).
Los dos dominios podrían expresarse como cadenas polipeptídicas separadas (unidas en fragmentos Fab a través de asociación no covalente de dominios y/o enlaces disulfuro), o como parte de la misma cadena (fragmentos V de cadena sencilla en donde los dos dominios están contenidos dentro de la misma cadena polipeptídica).
En la patente internacional WO92/01047 y en los ejemplos 1 a 8 de esta solicitud se ha utilizado la fusión de fragmentos de anticuerpo con la proteína del gen 3 del bacteriófago filamentoso para expresar y seleccionar fragmentos de anticuerpo. Una aproximación alternativa sería fusionar fragmentos de anticuerpo con la proteína del gen 8 u otras moléculas de superficie del bacteriófago filamentoso.
El aislamiento de anticuerpos humanos dirigidos contra antígenos humanos es una tarea en demanda. Existe sólo un limitado número de antígenos humanos contra los anticuerpos humanos circulantes hallados de forma natural. Existen anticuerpos dirigidos contra no-autoantígenos de origen humano. Se han aislado anticuerpos dirigidos contra el grupo sanguíneo humano B de una biblioteca de expresión de fagos preparada de individuos del grupo sanguíneo O (J.D. Marks y col., J. Mol. Biol. 222, 581-597, 1991), que reconoce el grupo sanguíneo B como foráneo.
Esta invención trata de un procedimiento general para aislar anticuerpos dirigidos contra autoantígenos que son específicos para el antígeno concerniente. Muchos pacientes muestran concentraciones significativas de auto-anticuerpos circulantes. Se estima que del 10 al 30% de linfocitos B en individuos normales, sanos están implicados en generar auto-anticuerpos (I.R. cohen y A. Cooke Immunol. Today 7, 363-364, 1986). Sin embargo, los "auto-anticuerpos naturales" producidos no son de uso terapéutico ya que a menudo son IgM, de baja reactividad y polireactivos (P. Casali y A.L. Notkins Ann. Rev. Immunol. 7, 515-531, 1989); S. Avrameas Immunol.Today, 12, 154-159). Una respuesta autoinmune puede producirse en enfermedades autoinmunes o después de infecciones y pocos anticuerpos monoclonales dirigidos contra autoantígenos o auto-anticuerpos se han aislado de pacientes con enfermedad autoinmune (K. james & G.T.BellJ. Immunol Methods 100, 5-40, 1987). Estos auto-anticuerpos son frecuentemente específicos, pero pueden unirse sólo a un rango limitado de epitopos sobre el antígeno (M. Bouanani y col., Artrhitis Rheum. 34 1585-1593, 1991).
La preparación de bibliotecas de genes V derivadas del ARNm de células plasmáticas que secretan anticuerpos IgG (o IgM) puede conducir al aislamiento de fragmentos de anticuerpo derivados de auto-anticuerpos. Por ejemplo, los auto-anticuerpos pueden aislarse de pacientes con enfermedades inmunes, por ejemplo anticuerpos anti-receptor de la acetilcolina podrían aislarse de repertorios de anticuerpos generados a partir del ARNm de IgG de pacientes con miastenia gravis. Por ejemplo, un fragmento de anticuerpo específico para la peroxidasa humana del tiroides se ha aislado de una biblioteca de bacteriófago lambda de un paciente con enfermedad...
Reivindicaciones:
1. Procedimiento de obtención de un miembro de una pareja de unión específica (miembro sbp), cuyo miembro sbp tiene un sitio de unión a antígeno con especificidad de unión para un autoantígeno diana de una especie de mamífero, donde el miembro sbp es un dominio VH de un anticuerpo de la especie de mamífero, comprendiendo el procedimiento:
2. Procedimiento de obtención de un miembro de una pareja de unión específica (miembro sbp), cuyo miembro sbp tiene un sitio de unión a antígeno con especificidad de unión para un autoantígeno diana de una especie de mamífero, donde el miembro de sbp es un dominio VL de un anticuerpo de la especie de mamífero, comprendiendo el procedimiento:
3. Procedimiento según la reivindicación 1 o la reivindicación 2, donde el ácido nucleico deriva de genes V reordenados de un mamífero no inmunizado.
4. Procedimiento según la reivindicación 1 o la reivindicación 2, donde la biblioteca se prepara mediante recombinación artificial o sintética de secuencias de genes V.
5. Método según la reivindicación 4, donde la biblioteca deriva de las secuencias de los genes V de la línea germinal.
6. Método según cualquiera de las reivindicaciones anteriores, donde dicha especie de mamífero es humano.
7. Procedimiento según cualquiera de las reivindicaciones anteriores, donde los miembros sbp seleccionados en (b) expresados en la superficie de partículas de bacteriófagos filamentosos se seleccionan o criban para proporcionar una partícula de bacteriófago filamentoso individual que expresa un miembro sbp o una población mixta de dichas partículas de bacteriófagos filamentosos, conteniendo dicha partícula de bacteriófago filamentoso ácido nucleico que codifica el miembro sbp que se expresa en su superficie.
8. Procedimiento según cualquiera de las reivindicaciones anteriores, donde el ácido nucleico que codifica un miembro sbp seleccionado o cribado y que deriva de una partícula de bacteriófago filamentosos que expresa en su superficie un miembro sbp seleccionado o cribado se utiliza para expresar un miembro sbpo o un fragmento o derivado del mismo en un organismo huésped recombinante.
9. Procedimiento según la reivindicación 8, donde se extrae ácido nucleico de una o más partículas de bacteriófagos filamentosos y se utiliza para proporcionar un ácido nucleico codificante en un método adicional para obtener un miembro sbp individual o una población mixta de miembros sbp, o un ácido nucleico que codifica dicho miembro sbp individual o dicha población mixta de miembros sbp.
10. Procedimiento según la reivindicación 8 o la reivindicación 9, donde el producto final de expresión se modifica para producir un derivado del mismo.
11. Procedimiento según cualquiera de las reivindicaciones 1 a 10, donde el autoantígeno es el Factor de Necrosis Tumoral Alfa (TNFa).
12. Procedimiento según cualquiera de las reivindicaciones 1 a 10, donde el autoantígeno es tiroglobulina.
13. Procedimiento según cualquiera de las reivindicaciones 1 a 10, donde el autoantígeno es un receptor.
14. Procedimiento según cualquiera de las reivindicaciones 1 a 10, donde el autoantígeno es mucina.
15. Procedimiento según cualquiera de las reivindicaciones 1 a 10, donde el autoantígeno es antígeno carcinoembrionario (CEA).
16. Procedimiento según cualquiera de las reivindicaciones 1 a 10, donde el autoantígeno es CD4.
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Métodos y composiciones para tratar y prevenir enfermedades asociadas con la integrina AVB8, del 29 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un anticuerpo aislado que se une específicamente a la integrina β8 humana e inhibe la adhesión del péptido asociado a latencia (LAP) a ανβ8, en donde el […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]
Proteínas de unión al antígeno ST2, del 22 de Julio de 2020, de AMGEN INC.: Un anticuerpo aislado que se une a un antígeno ST2 que tiene la secuencia de aminoácidos 19-556 del SEQ ID NO: 1, comprendiendo dicho anticuerpo una secuencia de […]
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Bloqueo de CD73, del 22 de Julio de 2020, de Innate Pharma: Un anticuerpo aislado que específicamente se une a un polipéptido CD73 humano en la superficie de una célula y que tiene capacidad de neutralizar […]