NUEVOS DERIVADOS DE 3-((1,2,4)TRIAZOLO(4,3-A)PIRIDIN-7-IL)BENZAMIDA.
Nuevos derivados de 3-([1,2,4]triazolo[4,3-A]piridin-7-IL)benzamida.
Esta invención se refiere a nuevos inhibidores de la proteína quinasa p38 activada por mitógenos, que tienen la fórmula general (I)
**FIGURA**
a procesos para su preparación; a composiciones farmacéuticas que los comprenden; y a su uso en terapia
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200700565.
Solicitante: LABORATORIOS ALMIRALL, S.A..
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: EASTWOOD, PAUL, ROBERT, GONZALEZ RODRIGUEZ,JACOB, VIDAL JUAN,BERNAT, ESTEVE TRIAS,CRISTINA.
Fecha de Solicitud: 2 de Marzo de 2007.
Fecha de Publicación: .
Fecha de Concesión: 2 de Marzo de 2010.
Clasificación Internacional de Patentes:
- A61K31/437 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › conteniendo el sistema heterocíclico un ciclo de cinco eslabones teniendo el nitrógeno como heteroátomo del ciclo, p. ej. indolicina, beta-carbolina.
- C07D471/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 471/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del sistema condensado, teniendo al menos un ciclo de seis miembros con un átomo de nitrógeno, no previstos en los grupos C07D 451/00 - C07D 463/00. › Sistemas condensados en orto.
Clasificación PCT:
- A61K31/437 A61K 31/00 […] › conteniendo el sistema heterocíclico un ciclo de cinco eslabones teniendo el nitrógeno como heteroátomo del ciclo, p. ej. indolicina, beta-carbolina.
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- C07D471/04 C07D 471/00 […] › Sistemas condensados en orto.
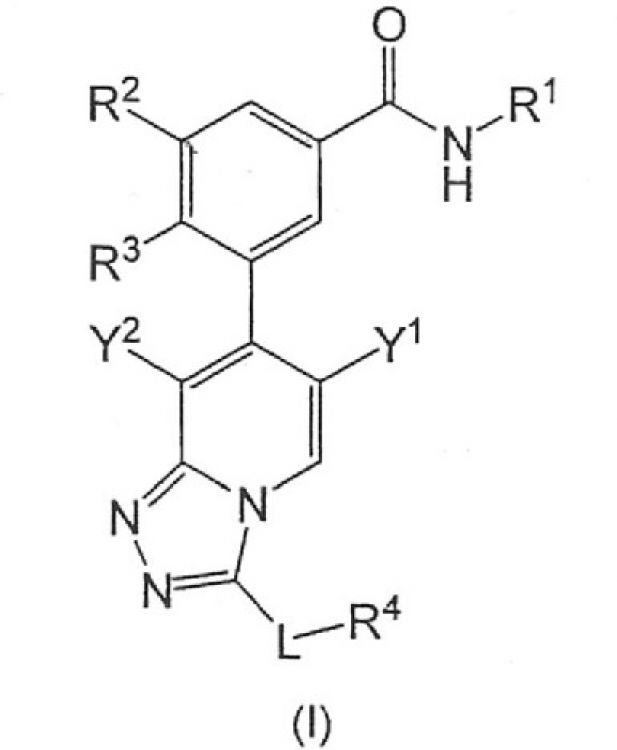
Fragmento de la descripción:
Nuevos derivados de 3-([1,2,4]triazolo[4,3-a]piridin-7-il)benzamida.
La presente invención se refiere a nuevos inhibidores de la proteína-quinasa p38 activada por mitógenos.
Las proteína-quinasas activadas por mitógenos (abreviadamente en lo sucesivo MAP por la expresión inglesa Mitogen-Activated Protein Kinases) son enzimas conservadas evolutivamente que traducen señales de membrana en respuesta a la expresión de genes. En mamíferos se pueden distinguir cuatro familias de MAPK: quinasas relacionadas con señales extracelulares (ERK1/2), quinasas aminoterminales de Jun (JNK1/2/3), proteínas p38 (alfa, beta, gamma y delta) y ERK5. La regulación de estas proteínas es ejercida por una cascada de tres etapas compuesta por MAPK, quinasa MAPK, y quinasa-quinasa MAPK.
La MAPK denominada p38 se identificó originalmente como la diana de los fármacos anti-inflamatorios supresores de citoquinas (abreviadamente en lo sucesivo CSAID por la expresión inglesa Cytokine Suppressive Anti-inflammatory Drugs), que tiene un papel central en la transducción de señales que conduce a la producción de TNF-alfa y otras citoquinas (Lee et al, 1984). La p38 es activada por fosforilación en Thr en Tyr por MKK3, MKK4, o MKK6 (Kyriakis y Avruch, 2001) en respuesta al estrés y los estímulos pro-inflamatorios. A su vez, la p38 fosforila sus efectores en los residuos de Ser y Thr, a saber las proteína-quinasas fosfatasas y los factores de transcripción, tales como ATF-2, MEF2, MAPKAPK2, MSK1/2 o MNK1/2. En conjunto esta cascada de activación da como resultado el control de la expresión de genes a través de cuatro mecanismos diferentes: activación de factores de transcripción; estabilización de mRNA; traducción de mRNA; y fosforilación de histonas en los sitios de unión NF-kB en la cromatina (Shi y Gaestel, 2002; Sacanni et al, 2001).
Existen cuatro diferentes isoformas de p38 codificadas por genes separados: p38 alfa, beta, gama y delta, mostrando cada una de ellas un modelo distinto de expresión en tejidos. Tal como se determina por mRNA y por los niveles de proteínas (Beardmore et al, 2005; Wang et al, 1997), p38 alfa y beta se expresan ubicuamente, siendo la expresión de la p38 beta más relevante en los tejidos del sistema nervioso central (SNC) (cerebro, córtex, cerebelo, hipocampo, etc.). La expresión de p38 gamma es más prominente en el músculo esquelético, mientras que la p38 delta se localiza principalmente en el corazón, riñón, pulmón y glándulas supra-renales. Al nivel celular, la p38 alfa y delta parecen ser las isoformas más relevantes en las células inmunes (monocitos, macrófagos, neutrófilos y células T) (Hale et al, 1999). La inhibición farmacológica con inhibidores específicos de p38alfa/beta, así como los estudios de señalización como dianas de genes han indicado que la p38alfa es la isoforma que regula las respuestas inflamatorias más probablemente a través de su sustrato MAPKAP-K2 (Kotlyarov et al, 1999). Análogamente, esta isoforma es necesaria en el desarrollo embriónico temprano puesto que los ratones que no tienen un gen que codifica la p38alfa (ratones KO p38 alpha) mueren el día 12,5 de la fase embrionaria debido a una insuficiencia placental y a defectos vasculares (Allen et al, 2000; Tamura et al, 2000; Adams et al, 2000), un fenotipo que se reproduce también en ratones KO MKK3/MKK6 doble (Brancho et al, 2003). En contraste, los ratones KO p38 beta, gamma y delta no muestran deficiencias en el desarrollo (Beardmore et al, 2005; Sabio et al, 2005). Los ratones KO p38 beta parecen responder similarmente a estímulos pro-inflamatorios (LPS) como los controles de tipo natural, lo que indica que esta isoforma no tiene una función en la inflamación (Beardmore et al, 2005).
La contribución de la vía de la MAPK p38 a la inflamación ha sido estudiada tanto in vitro como in vivo empleando diferentes series químicas de inhibidores de p38 (Pargellis y Regan, 2003; Kumar et al, 2003). La molécula inhibidora más ampliamente usada, SB203580, es, de hecho, un inhibidor dual de p38alfa/beta. La inhibición de p38 anulada liberación de TNF-alfa, así como otras citoquinas pro-inflamatorias como IL-1, IL-6, e IL-8, en PBMC, sangre completa, o en la línea celular monocítica humana THP-1.
En virtud de la implicación de p38 en la producción de TNFalpha, se han ensayado los inhibidores de p38 en modelos de animales con enfermedades en las cuales el TNFalpha tiene un papel patofisiológico. La inhibición de p38 disminuye la artritis inducida por colágeno en múridos y la gravedad de la artritis inducida por coadyuvantes en ratas (Pargellis y Regan, 2003). Además, los inhibidores de p38 mejoran también la resorción ósea en modelos de animales con artritis, debido probablemente a la implicación de la MAPK p38 en la diferenciación de osteoclastos. La inhibición de p38 atenúa la respuesta inflamatoria en un modelo de múridos de la enfermedad de Crohn y disminuye la producción de TNF-alfa en biopsias de pacientes humanos con la enfermedad de Crohn (Hollenbach et al, 2005; Waetzig et al, 2002).
Debido al uso exclusivo de la vía de p38 por los neutrófilos, la p38 ha sido también considerada una diana para la enfermedad pulmonar obstructiva crónica (EPOC) (Nick et al, 2002). La inhibición de p38 reduces la neutrofilia, las citoquinas inflamatorias, la MMP-9 y la fibrosis del pulmón (Underwood et al, 2000). En modelos de irradiación de piel, la inhibición de p38 protege la epidermis contra la exposición a la radiación ultravioleta aguda bloqueando la apoptosis y las respuestas inflamatorias (Hildesheim et al, 2004). La inhibición de p38 invierte también los defectos hematopoyéticos en la médula ósea de pacientes con síndromes mielodisplásticos, en los que la sobre-producción de TNF-alfa tiene un papel patofisiológico (Katsoulidis et al, 2005).
En las malignidades hematopoyéticas, un estudio ha puesto de manifiesto que los inhibidores de p38 pueden bloquear la proliferación de células de mieloma múltiple mediante la inhibición de la producción de IL-6 y VEGF en las células estromales de la médula ósea (Hideshima et al, 2002).
La p38 está implicada en mecanismos celulares claves, tales como apoptosis, fibrosis e hipertrofia celular, que son comunes a las patologías cardiacas y vasculares. La inhibición farmacológica de p38 ha demostrado ser útil en mejorar el daño por isquemia-reperfusión, la isquemia focal cerebral, el síndrome coronario agudo, la insuficiencia cardiaca crónica y la remodelación posterior al infarto de miocardio (See et al, 2004).
Se ha descrito que la inhibición experimental de p38 es eficaz en reducir el dolor en modelos de animales de neuropatías que se basa en la expresión de COX-2 y la producción de TNF-alfa por células gliales (Schafers et al, 2003; Jin et al, 2003; Tsuda et al, 2004).
Por lo tanto, los compuestos de la invención pueden ser útiles en la profilaxis o el tratamiento de cualquier enfermedad o desorden, en el cual la quinasa p38 desempeña un papel, incluyendo condiciones causadas por una producción excesiva o no regulada de citoquinas pro-inflamatorias, incluyendo por ejemplo la producción excesiva o no regulada de TNF, IL-1, IL-6 e IL-8 en un ser humano, u otro mamífero. La invención se extiende a dicho uso y al uso de los compuestos para la fabricación de un medicamento para tratar enfermedades o trastornos mediados por citoquinas.
Además, la invención se extiende a la administración a un ser humano de una cantidad eficaz de un inhibidor de p38 para tratar dicho trastorno o enfermedad.
Las enfermedades o trastornos en los cuales la quinasa p38 desempeña una función bien directamente o bien vía citoquinas pro-inflamatorias incluyendo las citoquinas TNF, IL-1, IL-6 e IL-8 incluyen sin limitación a las mismas, enfermedades autoinmunes, enfermedades inmunes e inflamatorias, trastornos óseos destructivos, trastornos neoplásticos, trastornos neurodegenerativos, enfermedades virales, enfermedades infecciosas, enfermedades cardiovasculares, trastornos relacionados con la angiogénesis, y trastornos relacionados con el dolor.
Las enfermedades autoinmunes que pueden impedirse o tratarse incluyen pero sin limitación a las mismas, artritis reumatoide, artritis psoriática, espondilitis anquilosante, síndrome de Reiter, fibromialgia, enfermedad inflamatoria del intestino, tal como colitis ulcerante, y enfermedad de Crohn, esclerosis múltiple, diabetes,...
Reivindicaciones:
1. Un compuesto de fórmula (I)
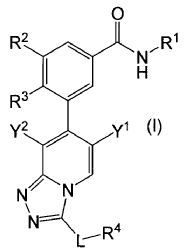
en donde:
R1 se selecciona del grupo que consiste en grupo alquilo C1-4, cicloalquilo C3-7 y
R2 se selecciona del grupo que consiste en átomos de hidrógeno y átomos de halógeno;
R3 se selecciona del grupo que consiste en grupos metilo y átomos de halógeno;
L se selecciona del grupo que consiste en
R4 se selecciona del grupo que consiste en átomos de hidrógeno, grupos alquilo C1-4 opcionalmente sustituidos con átomos de flúor, grupos cicloalquilo C3-6 opcionalmente sustituidos con átomos de flúor o grupos alquilo C1-4; grupos arilo que están opcionalmente sustituidos con átomos de halógeno o grupos seleccionados de alquilo C1-4, trifluorometilo y difluorometilo y grupos heteroarilo que están opcionalmente sustituidos con átomos de halógeno o grupos seleccionados de alquilo C1-4, trifluorometilo y difluorometilo;
o
Y1 y Y2 se seleccionan independientemente del grupo que consiste en átomos de hidrógeno, átomos de flúor, y átomos de cloro;
y sus sales y N-óxidos farmacéuticamente aceptables.
2. Un compuesto de acuerdo con la reivindicación 1, en donde R1 se selecciona del grupo que consiste en cicloalquilo C3-6 y
3. Un compuesto de acuerdo con la reivindicación 2, en donde R1 representa un grupo cicloalquilo C3-4.
4. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1-3, en donde R2 representa un átomo de hidrógeno o un átomo de flúor.
5. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1-4, en donde R3 es un grupo metilo.
6. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1-5, en donde L es un enlace directo y R4 se selecciona del grupo que consiste en grupos alquilo C1-4, cicloalquilo C3-6 opcionalmente sustituido con un grupo metilo y un grupo arilo que está opcionalmente sustituido con átomos de halógeno.
7. Un compuesto de acuerdo con la reivindicación 6, en donde R4 se selecciona del grupo que consiste en grupos alquilo C1-4 ramificados y un grupo fenilo que está opcionalmente sustituido con átomos de cloro o flúor.
8. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1-7, en donde Y1 y Y2 se seleccionan independientemente del grupo que consiste en átomo de hidrógeno y átomo de flúor.
9. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1-8, en donde R1 representa un grupo ciclopropilo, R2 se selecciona de átomo de hidrógeno y átomo de flúor, R3 representa un grupo metilo, L es un enlace directo, R4 se selecciona del grupo que consiste en grupos alquilo C1-4 ramificados o un grupo fenilo que está opcionalmente sustituido con átomos de cloro o flúor y Y1 y Y2 se seleccionan independientemente de átomo de hidrógeno y átomo de flúor.
10. Un compuesto de acuerdo con la reivindicación 1, que es uno de:
11. Un compuesto de acuerdo con una cualquiera de las reivindicaciones 1 a 10, para uso en el tratamiento de un estado patológico o enfermedad susceptible de mejorar por inhibición de la proteína quinasa p38 activada por mitógenos.
12. Una composición farmacéutica que comprende un compuesto tal como se ha definido en una cualquiera de las reivindicaciones 1 a 10, mezclado con un vehículo o diluyente farmacéuticamente aceptable.
13. Uso de un compuesto tal como se ha definido en una cualquiera de las reivindicaciones 1 a 10, en la fabricación de un medicamento para el tratamiento de un estado patológico o enfermedad susceptible de mejorar por inhibición de la proteína quinasa p38 activada por mitógenos.
14. Uso de acuerdo con la reivindicación 13, en donde el estado patológico o enfermedad es artritis reumatoide, daño por isquemia-reperfusión, isquemia cerebral focal, síndrome coronario agudo, EPOC, enfermedad de Crohn, síndrome del intestino irritable, síndrome del malestar respiratorio en adultos, osteoporosis, la enfermedad de Alzheimer, espondilitis reumatoide, psoriasis, aterosclerosis, osteoartritis o mieloma múltiple.
15. Un producto de combinación que comprende:
por uso simultáneo, separado o secuencial en el tratamiento del cuerpo humano o animal.
Patentes similares o relacionadas:
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Compuestos de heteroaril carboxamida como inhibidores de RIPK2, del 29 de Julio de 2020, de BOEHRINGER INGELHEIM INTERNATIONAL GMBH: Un compuesto de fórmula (I): **(Ver fórmula)** o sus sales farmacéuticamente aceptables, en la que: X es N y Y es CH; o X es CH y Y es N; […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
Ureas cíclicas como inhibidores de ROCK, del 22 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de acuerdo con la Fórmula (I): **(Ver fórmula)** o un enantiómero, un diastereómero, un estereoisómero, un tautómero, una sal farmacéuticamente aceptable […]
Formas sólidas de un compuesto modulador de quinasas, del 22 de Julio de 2020, de PLEXXIKON, INC: Una forma cristalina del Compuesto I: **(Ver fórmula)** que es la Forma C del Compuesto I caracterizado por un difractograma de rayos […]
Derivado heteroarilo o sal farmacéuticamente aceptable del mismo, método de preparación del mismo y composición farmacéutica para prevenir o tratar enfermedades asociadas con PI3 quinasas, que contiene el mismo como principio activo, del 22 de Julio de 2020, de KOREA RESEARCH INSTITUTE OF CHEMICAL TECHNOLOGY: Un compuesto representado por la fórmula 1, un isómero óptico del mismo o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la fórmula […]
Procedimiento de preparación de la forma A de grapiprant, del 22 de Julio de 2020, de Aratana Therapeutics Inc: Un procedimiento de preparación de una Forma A cristalina sustancialmente pura de grapiprant, comprendiendo el procedimiento: i. poner en contacto grapiprant a temperatura […]