NUEVAS HERRAMIENTAS DE EXPRESION PARA APLICACIONES MULTIPROTEICAS.
Polinucleótido para aplicaciones multigénicas, que comprende una disposición funcional según la figura I:
comprendiendo dicha disposición:
(a) por lo menos dos casetes de expresión: T1 - MCS1 - P1 y P2 - MCS2 - T2 en una disposición de cabeza con cabeza, cabeza con cola o cola con cola, comprendiendo cada uno un sitio de clonación múltiple MCS1 o MCS2, flanqueado por un promotor P1 y una secuencia de terminador T1 para MCS1 y flanqueado por un promotor P2 y una secuencia de terminador T2 para MCS2,
(b) por lo menos un módulo de multiplicación M intermedio de los promotores P1 y P2 que comprende por lo menos dos sitios de restricción A y B,
(c) por lo menos dos sitios de restricción X e Y, flanqueando cada uno uno de los casetes de expresión, en el que:
(i) los sitios de restricción A y X, así como B e Y son compatibles, pero
(ii) los productos de ligación de AY y de BX no son divididos enzimáticamente por los enzimas de restricción a, b, x o y, específicos para los sitios de restricción A, B, X e Y, e
(iii) los sitios de restricción A y B, así como X e Y no son compatibles
Tipo: Resumen de patente/invención. Número de Solicitud: W04013381EP.
Solicitante: EIDGENOSSISCHE TECHNISCHE HOCHSCHULE ZURICH.
Nacionalidad solicitante: Suiza.
Dirección: ETH TRANSFER, RAMISTRASSE 101,8092 ZURICH.
Inventor/es: RICHMOND,TIMOTHY, BERGER,IMRE, FITZGERALD,DANIEL,J.
Fecha de Publicación: .
Fecha Concesión Europea: 9 de Septiembre de 2009.
Clasificación Internacional de Patentes:
- C12N15/866 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Vectores báculovirales.
Clasificación PCT:
- A01K67/027 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01K CRÍA DE ANIMALES; AVICULTURA; APICULTURA; PISCICULTURA; PESCA; ANIMALES PARA CRIA O REPRODUCCIÓN, NO PREVISTOS EN OTRO LUGAR; NUEVAS VARIEDADES DE ANIMALES. › A01K 67/00 Cría u obtención de animales, no prevista en otro lugar; Nuevas razas de animales. › Nuevas razas de vertebrados.
- A61K31/7088 A […] › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- C12N15/10 C12N 15/00 […] › Procedimientos para el aislamiento, la preparación o la purificación de ADN o ARN (preparación química de ADN o ARN C07H 21/00; preparación de polinucleótidos no estructurales a partir de microorganismos o con la ayuda de enzimas C12P 19/34).
- C12N15/866 C12N 15/00 […] › Vectores báculovirales.
Clasificación antigua:
- A01K67/027 A01K 67/00 […] › Nuevas razas de vertebrados.
- A61K31/7088 A61K 31/00 […] › Compuestos que tienen al menos tres nucleósidos o nucleótidos.
- C12N15/10 C12N 15/00 […] › Procedimientos para el aislamiento, la preparación o la purificación de ADN o ARN (preparación química de ADN o ARN C07H 21/00; preparación de polinucleótidos no estructurales a partir de microorganismos o con la ayuda de enzimas C12P 19/34).
- C12N15/866 C12N 15/00 […] › Vectores báculovirales.
Fragmento de la descripción:
Nuevas herramientas de expresión para aplicaciones multiproteicas.
La presente invención se refiere a polinucleótidos para aplicaciones multigénicas, que comprende una nueva disposición funcional, así como vectores, células huésped y animales recombinantes que comprenden dichos polinucleótidos.
Asimismo, la presente invención se refiere a procedimientos para generar casetes de expresión multigénica, procedimientos para producir complejos multiproteicos in vitro e in vivo, y procedimientos para producir una vacuna.
Además, la presente invención comprende procedimientos para cribar interacciones entre complejos de proteínas o modificaciones de proteínas, y procedimientos para el cribado in vitro o in vivo de compuestos candidatos que pueden presentar entre complejos de proteínas o de modificaciones de proteínas, o capaces de inhibir interacciones entre complejos de proteínas o de inhibir modificaciones de proteínas.
Además, la presente invención se refiere a la utilización de los polinucleótidos, vectores, células huésped o animales recombinantes de la invención para: (i) la preparación de un medicamento para la terapia génica, (ii) la producción recombinante de complejos multiproteicos, (iii) la producción de una vacuna, o (iv) el cribado de compuestos de interés.
Finalmente, e igualmente importante, la invención se refiere a un kit de partes que comprende por lo menos un polinucleótido, un vector y/o una célula huésped según la invención.
Antecedentes de la invención
La identificación de nuevos complejos multiproteicos en las células eucarióticas se ha acelerado considerablemente, en particular debido a la aparición del análisis genómico de las interacciones proteína-proteína, a la introducción de potentes procedimientos de purificación de proteínas de afinidad múltiple y al desarrollo de técnicas analíticas ultrasensibles. Basándose en búsquedas exhaustivas de dos híbridos, se ha estimado que el número de parejas de interacción para una proteína determinada de la levadura de panadería es de entre cinco y ocho (Schwikowski et al., A network of protein-protein interactions in yeast, Nat. Biotechnol. 18:1257-1261, 2000; Bader et al., Analyzing protein-protein interaction data obtained from different sources, Nat. Biotechnol. 20:991-997, 2002; Von Mering et al., Comparative assessment of large-scale data sets of protein-protein interacions, Nature 417:399-403, 2002; Grigoriev, A., On the number of protein-protein interacions in the yeast proteome, Nucleic Acids Res. 31:4157-4161, 2003). De esta manera, ha surgido el concepto de la célula como una colección de máquinas proteicas multicomponente, con una proteína para esencialmente cada proceso importante. Lo expuesto anteriormente plantea retos significativos para las tecnologías de producción de proteínas centradas en estudios moleculares de tipo estructural y funcional de los complejos multiproteicos eucarióticos, debido a que las cantidades intracelulares típicamente son refractarias a la extracción a gran escala a partir de la fuente.
Se han utilizado vectores policistrónicos portadores de varios genes que codifican componentes de complejos multiproteicos para casos seleccionados de administración en la terapia génica (De Felipe, P., Polycistronic viral vectors, Curr. Gene Ther. 2:355-378, 2002; Planelles, V., Hybrid lentivirus vectors, Methods Mol. Biol. 229:273-284, 2003). Recientemente se ha utilizado un vector policistrónico para la expresión de un complejo de factor transcripcional compuesto de cuatro subunidades en E. coli (Selleck et al., A histone fold TAF octamer within the yeast TFIID transcriptional coactivator, Nat. Struct. Biol. 8:695-700, 2001). Los constructos de ADN en estos estudios se generaron mediante procedimientos convencionales utilizando endonucleasas y ligasa. Sin embargo, los complejos de proteínas en los eucariotas con frecuencia contienen diez o más subunidades con polipéptidos individuales de tamaños variables, de hasta varios cientos de kDa, lo que limita severamente la aplicabilidad de las estrategias convencionales de clonación y en gran parte descarta a E. coli como sistema huésped útil para la expresión de proteínas heterólogas.
Los baculovirus recombinantes resultan particularmente atractivos para la producción de nivel elevado de conjuntos grandes de proteínas (O'Reilly et al., Baculovirus expression vectors. A laboratory manual. Oxford Press, New York, 1994). Los genes regulados por promotores tardíos del virus de la polihedrosis nuclear de Autographa californica (AcNVP) con frecuencia se expresan abundantemente, se procesan fielmente y se direccionan a su compartimiento celular apropiado. Incluso partículas de arquitectura compleja, tales como las estructuras de cápside, se han ensamblado con éxito en células de insecto utilizando el sistema baculovirus (Roy et al., Baculovirus multigene expression vectores and their use for understanding the assembly process of architecturally complex virus particles, Gene 190:119-129, 1997). La expresión de varios genes en una célula puede conseguirse mediante coinfección con virus que transportan un gen foráneo cada uno. Sin embargo, este enfoque inevitablemente conduce a considerables variaciones en los niveles de producción de las proteínas individuales como resultado de la varianza estadística entre células infectadas en la estequiometría vírica. Una alternativa mejor es la infección con un baculovirus que contenga todos los genes heterólogos seleccionados (Roy et al., ver anteriormente; Bertolotti-Ciarlet et al., Immunogenicity and protective efficacy of rotavirus 2/6-virus-like particles produced by a dual baculovirus expression vector and administered intramuscularly, intranasally, or orally to mice, Vaccine 21:3885-3990, 2003). Lo expuesto anteriormente resulta posible debido a la naturaleza flexible de la cubierta de AcNVP, que permite alojar inserciones de ADN de gran tamaño en el genoma circular de 130 kb de ADNds. Tradicionalmente, la generación de baculovirus recombinante se lleva a cabo en dos etapas. En primer lugar se clonan los genes foráneos en un vector de transferencia de tamaño reducido propagado en E. coli y después se insertan en el genoma de baculovirus, de gran tamaño, mediante recombinación homóloga en células de insecto en una reacción que proporciona progenie recombinante al 30%-80% en el caso de que se utilice ADN vírico parental linearizado (O'Reilly et al., ver anteriormente). Este procedimiento se simplificó sustancialmente mediante la introducción de un vector lanzadera baculovírico (bácmido bMON14272) propagado en E. coli (Luckow et al., Efficient generation of infectious recombinant baculoviruses by site-specific transposon-mediated insertion of foreign genes into a baculovirus genome propagated in E. coli, J. Virol. 67:4566-4579, 1993). El bácmido contiene el sitio de unión de Tn7 para la transposición de genes foráneos procedentes de un vector de transferencia (Bac-to-BacTM, Invitrogen) (Luckow et al., ver anteriormente; Bac-to-BacTM Baculovirus Expression Systems Manual, Invitrogen, Life Technologies Incorporated, 2000). Para la coexpresión se introdujo un vector de transferencia bicistrónico, pFastBacTM Dual, que contenía los promotores víricos tardíos polihedrina (polh) y p10 en dos casetes de expresión separados con conjuntos de sitios de restricción destinados a la subclonación secuencial de dos genes foráneos.
Para la producción de complejos multiproteicos que contienen subunidades grandes y además muchas subunidades, todavía existe una fuerte necesidad de vectores de transferencia que permitan ensamblar genes de una manera modular no secuencial, para aliviar las limitaciones impuestas por la escasez de sitios de restricción útiles en una colección de secuencias codificantes, cada una de las cuales comprende varios miles de pares de bases.
Por lo tanto, un objetivo de la presente invención consiste en proporcionar nuevas herramientas y procedimientos para la generación rápida y flexible de complejos multiproteicos.
También existe una necesidad de nuevas herramientas y procedimientos para producir complejos multiproteicos de diez o más subunidades con polipéptidos individuales de tamaños de hasta varios cientos de kDa.
Otro objetivo de la presente invención consiste en proporcionar nuevas herramientas y procedimientos para generar complejos multiproteicos grandes con muchas subunidades y simultáneamente minimizar los requisitos...
Reivindicaciones:
1. Polinucleótido para aplicaciones multigénicas, que comprende una disposición funcional según la figura I:
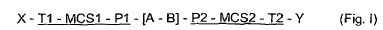
comprendiendo dicha disposición:
en el que:
2. Polinucleótido según la reivindicación 1, en el que los sitios de restricción A y B en el módulo de multiplicación M se seleccionan de entre el grupo que consiste en BstZ17I, Spe, ClaI y NruI o enzimas de restricción que presentan sitios de división idénticos a los de dichos enzimas ("isoesquizómeros").
3. Polinucleótido según la reivindicación 1 ó 2, en el que los sitios de restricción X e Y se seleccionan de entre el grupo que consiste en PmeI y AvrlI o enzimas de restricción que presentan sitios de división idénticos a los de dichos enzimas ("isoesquizómeros").
4. Polinucleótido según cualquiera de las reivindicaciones 1 a 3, en el que los promotores P1 y P2 se seleccionan de entre el grupo que consiste en promotores baculovíricos muy tardíos polh, p10 y pXIV, promotor baculovírico tardío vp39, promotor baculovírico híbrido tardío/muy tardío vp39polh, promotores baculovíricos tempranos Pcap/polh, pcna, etl, p35, egt, da26; CMV, SV40, UbC, EF-1a, RSVLTR, MT, PDS47, Ac5, PGAL y PADH.
5. Polinucleótido según cualquiera de las reivindicaciones 1 a 4, en el que las secuencias de terminador T1 y T2 se seleccionan de entre SV40, HSVtk o BGH (hormona de crecimiento bovina).
6. Polinucleótido según cualquiera de las reivindicaciones 1 a 5, que comprende además por lo menos un sitio para su integración en un vector o célula huésped.
7. Polinucleótido según la reivindicación 6, en el que el sitio de integración se selecciona de entre el grupo que consiste en los elementos transposones de Tn7, sitios de unión específica de integrasa ? y SSR (recombinasas específicas de sitio), preferentemente el sitio de recombinación específica cre-lox (LoxP) o el sitio de recombinación específica de recombinasa FLP (FRT).
8. Polinucleótido según cualquiera de las reivindicaciones 1 a 7, en el que dicho polinucleótido comprende:
9. Vector que comprende una secuencia de polinucleótido según cualquiera de las reivindicaciones 1 a 8.
10. Vector según la reivindicación 9, en el que dicho vector es un virus seleccionado de entre el grupo que consiste en adenovirus, virus adenoasociado (AAV), parvovirus autónomo, virus del herpes simplex (HSV), retrovirus, radinovirus, virus de Epstein-Barr, lentivirus, virus del bosque de Semliki y baculovirus.
11. Vector según la reivindicación 10, en el que el vector es un vector de expresión baculovírico.
12. Vector según la reivindicación 11, en el que los dos genes baculovíricos v-cath y chiA se encuentran funcionalmente alterados.
13. Vector según las reivindicaciones 9 a 12, que comprende además un sitio para las SSR (recombinasas específicas de sitio), preferentemente LoxP para la recombinación específica de sitio cre-lox.
14. Vector según las reivindicaciones 12 y 13, en el que el sitio cre-lox se encuentra situado en uno o en ambos de los genes baculovíricos v-cath y chiA.
15. Vector según cualquiera de las reivindicaciones 9 a 14, que comprende un elemento transposón, preferentemente el sitio de unión de Tn7.
16. Vector según la reivindicación 9, en el que dicho vector presenta la secuencia según la SEC ID nº 1 (pFBDM).
17. Vector según la reivindicación 9, en el que dicho vector presenta la secuencia según la SEC ID nº 2 (pUCDM).
18. Célula huésped que comprende un polinucleótido según cualquiera de las reivindicaciones 1 a 8 y/o un vector según cualquiera de las reivindicaciones 9 a 17.
19. Célula huésped según la reivindicación 18, seleccionada de entre el grupo que consiste en células de mamífero, preferentemente células humanas, células de roedor, células porcinas, células bovinas, células ovinas, y células de C. elegans; células de levadura, preferentemente S. cerevisiae, S. pombe, C. albicans y P. pastoris; células de insecto; y células de E. coli.
20. Animal no humano recombinante que comprende un polinucleótido según cualquiera de las reivindicaciones 1 a 8 y/o un vector según cualquiera de las reivindicaciones 9 a 17.
21. Animal no humano según la reivindicación 20, en el que el animal se selecciona de entre los mamíferos, preferentemente roedor, porcino y bovino y C. elegans.
22. Procedimiento para generar casetes de expresión multigénica, que comprende las etapas siguientes:
23. Procedimiento para producir complejos multiproteicos in vitro, que comprende las etapas siguientes:
Patentes similares o relacionadas:
PARTÍCULAS TIPO-VIRUS (VLP) DEL VIRUS DE LA ANEMIA INFECCIOSA DEL SALMÓN (ISAV) COMPRENDIENDO LA PROTEÍNA DE MATRIZ Y UNA O MÁS PROTEÍNAS ANTIGÉNICAS SE DICHO VIRUS; MÉTODO DE OBTENCIÓN, COMPOSICIÓN, VACUNA Y ALIMENTO PARA PECES BACULOVIRUS RECOMBINANTE; Y KIT DE VACUNACIÓN, del 2 de Julio de 2020, de UNIVERSIDAD DE SANTIAGO DE CHILE: El presente invento se refiere al campo de la medicina veterinaria, particularmente, con vacunas y sanidad animal en el ámbito de la acuicultura. […]
Composiciones inmunogénicas de PCV2 multivalentes y métodos para producir dichas composiciones, del 27 de Mayo de 2020, de Boehringer Ingelheim Animal Health USA Inc: Una vacuna combinada multivalente para uso en un método para (i) la prevención de una infección por PCV2, o de reinfección por PCV2 o (ii) la reducción o eliminación […]
Producción de productos biofarmacéuticos a base de baculovirus sin viriones baculovíricos contaminantes, del 12 de Febrero de 2020, de GENETHON: Un método para la producción un producto biofarmacéutico, que comprende: (a) infectar una célula de insecto productora de sustancia biofarmacéutica con al menos un baculovirus, […]
Tratamiento de PRDC en cerdos, del 4 de Diciembre de 2019, de Boehringer Ingelheim Animal Health USA Inc: Uso de una composición inmunogénica que consiste en el ORF-2 de PCV2 expresado en baculovirus recombinante y uno o más vehículos veterinariamente aceptables […]
Expresión de proteínas recombinantes en pupas de Trichoplusia ni, del 13 de Noviembre de 2019, de Alternative Gene Expression, S.L: Pupa que comprende un baculovirus recombinante y/o un bácmido derivado del virus multicápside de la polihedrosis nuclear de Autographa californica (AcMNPV), en la que la pupa […]
Sistema de baculovirus para expresión de un vector de terapia genética, del 14 de Febrero de 2018, de GENETHON: Genoma de baculovirus recombinante que comprende: - uno o varios casetes de expresión de los genes rep y cap de AAV necesarios para la […]
Composiciones inmunogénicas de PCV2 multivalentes, del 24 de Enero de 2018, de BOEHRINGER INGELHEIM VETMEDICA, INC.: Una vacuna de combinación para usar en un método para (i) disminuir la gravedad de los síntomas clínicos asociados con la infección por PCV2, y / o […]
Producción de productos biofarmacéuticos a base de baculovirus sin viriones baculovíricos contaminantes, del 29 de Marzo de 2017, de GENETHON: Procedimiento para la producción de un producto biofarmacéutico, que comprende: (a) infectar una célula de insecto productora de sustancia […]