NANOPARTICULAS CONSTITUIDAS POR UN NUCLEO MAGNETICO Y UN RECUBRIMIENTO POLIMERICO.
Dichas nanopartículas tienen un diámetro medio inferior a 1 micrometro y comprenden un recubrimiento y un núcleo magnético,
en la que dicho recubrimiento comprende un látex de etilcelulosa y dicho núcleo magnético comprende, al menos, una partícula de un metal sensible a campos magnéticos con un diámetro inferior a 0,95 micrometros. Dichas nanopartículas pueden ser utilizadas como sistemas transportadores de fármacos, entre otras aplicaciones
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200702051.
Solicitante: UNIVERSIDAD DE GRANADA.
Nacionalidad solicitante: España.
Provincia: GRANADA.
Inventor/es: GALLARDO LARA,VISITACION, ARIAS MEDIANO,JOSE LUIS, RUIZ MARTINEZ,MA. ADOLFINA, LOPEZ-VIOTA GALLARDO,MARGARITA.
Fecha de Solicitud: 23 de Julio de 2007.
Fecha de Publicación: .
Fecha de Concesión: 13 de Mayo de 2010.
Clasificación Internacional de Patentes:
- A61K33/26 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 33/00 Preparaciones medicinales que contienen ingredientes activos inorgánicos. › Hierro; Sus compuestos.
- A61K47/48W8B
- A61K49/18P6
- H01F1/00E10
- H01F1/42 ELECTRICIDAD. › H01 ELEMENTOS ELECTRICOS BASICOS. › H01F IMANES; INDUCTANCIAS; TRANSFORMADORES; EMPLEO DE MATERIALES ESPECIFICOS POR SUS PROPIEDADES MAGNETICAS. › H01F 1/00 Imanes o cuerpos magnéticos, caracterizados por los materiales magnéticos pertinentes; Empleo de materiales específicos por sus propiedades magnéticas. › de materiales orgánicos u organometálicos (H01F 1/44 tiene prioridad).
Clasificación PCT:
- A61K33/26 A61K 33/00 […] › Hierro; Sus compuestos.
- A61K47/48
- A61K49/18 A61K […] › A61K 49/00 Preparaciones para examen in vivo. › caracterizadas por un aspecto físico particular, p. ej. emulsiones, microcápsulas, liposomas.
- H01F1/00 H01F […] › Imanes o cuerpos magnéticos, caracterizados por los materiales magnéticos pertinentes; Empleo de materiales específicos por sus propiedades magnéticas.
- H01F1/42 H01F 1/00 […] › de materiales orgánicos u organometálicos (H01F 1/44 tiene prioridad).
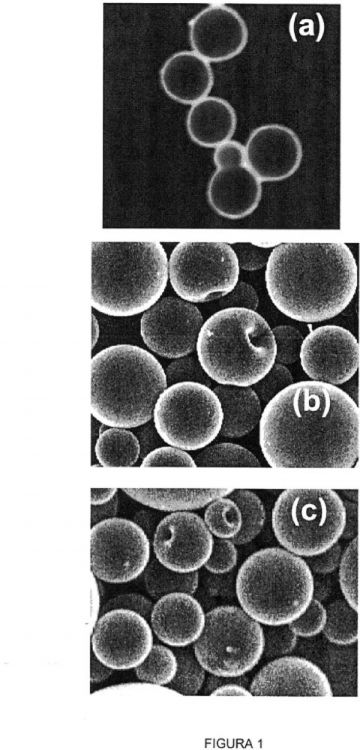
Fragmento de la descripción:
Nanopartículas constituidas por un núcleo magnético y un recubrimiento polimérico.
Campo de la invención
La presente invención se refiere a nanopartículas, un método para su producción y sus aplicaciones.
Antecedentes de la invención
La tecnología de los transportadores magnéticos se originó en la década de 1940 a partir de estudios sobre el tratamiento de aguas residuales, donde se pretendía absorber materia orgánica en pequeñas partículas de magnetita para lograr su separación del resto de líquido procesado. Dentro de las aplicaciones biológicas de esta tecnología destacan el tratamiento de aguas residuales, la inmovilización enzimática, la separación magnética por afinidad de biomoléculas, la selección de un tipo de células de entre una población celular, el transporte de fármacos y los biosensores.
Con el desarrollo de los métodos físicos y químicos para la caracterización del óxido de hierro coloidal, durante la década de los 60, comenzaron a aparecer las primeras aplicaciones biomédicas de los fluidos magnéticos en radiodiagnóstico y emboloterapia. La aparición de microcápsulas magnéticas como soportes de moléculas biológicas dio lugar al uso de matrices y de numerosos recubrimientos poliméricos biológicos y sintéticos, para ser utilizados como transportadores magnéticos en dispositivos biomédicos, agentes de contraste superparamagnéticos orales e intravenosos, y transportadores de fármacos.
La encapsulación de partículas inorgánicas por polímeros orgánicos, dota a las partículas recubiertas de nuevas propiedades. El recubrimiento incrementa la compatibilidad de las partículas inorgánicas con compuestos orgánicos, reduce su susceptibilidad a la coagulación o precipitación, y las protege contra la oxidación superficial. Por lo tanto, la encapsulación incrementa la dispersabilidad y la estabilidad química, y reduce al mismo tiempo la toxicidad de estos materiales (Tartaj P., Morales M.P., Veintemillas-Verdaguer S., González-Carreño T., Serna C.J., J. Phys. D: Appl. Phys., 36, R182, 2003).
En esta línea, las patentes US 5.705.222 y US 6.045.925 proponen la obtención de partículas de entre 1 y 100 nanometros (nm) con una distribución de tamaños muy dispersa, constituidas por un núcleo de óxido metálico y un recubrimiento polimérico de diversa naturaleza (ácido poliacrílico, ácido polimetacrílico, polivinilalcohol, poliamida o polipéptido), mediante contacto en suspensión entre ambos materiales.
La patente US 5.952.131 describe un método de obtención, mediante polimerización en emulsión a 80ºC, de partículas constituidas por un núcleo y un recubrimiento de diferente naturaleza polimérica (alquilmetacrilatos, etc.), con un tamaño de hasta 2 micrometros (µm).
Sin embargo, materiales de esta naturaleza carecen de especial interés biomédico ya que no presentan una respuesta magnética adecuada a campos y gradientes magnéticos alcanzables técnicamente, por ejemplo a la velocidad de flujo presente en los sistemas fisiológicos. Además, el tamaño de estos sistemas generalmente es demasiado elevado como para poder utilizarse en aplicaciones biomédicas, por ejemplo en el diseño de sistemas transportadores de fármacos que precisan de una distribución a nivel capilar y una perfusión uniforme al lugar deseado. Además, carecen de máxima biocompatibilidad y mínima antigenicidad, y sus productos de degradación son tóxicos y no biodegradables. Por otro lado, su reproducibilidad a gran escala es complicada y costosa.
La patente US 5.814.687 describe un método de obtención de partículas constituidas por magnetita, ferrita de cobalto o ferrita de manganeso, como núcleo magnético, y un recubrimiento constituido por polímeros y copolímeros de metacrilatos, mediante la polimerización en emulsión o en suspensión del monómero en presencia de los núcleos. Las partículas obtenidas poseen un tamaño entre 0,5 y 30 µm y se sugiere su aplicación al diagnóstico inmunológico, a la purificación y el aislamiento, y al transporte de fármacos.
La patente US 4.871.716 propone la dispersión de núcleos de magnetita en partículas poliméricas (albúmina, polilisina, poliarginina o polihistidina) para la obtención de nanopartículas con un tamaño entre 0,05 y 500 µm.
Algunos de estos materiales no presentan una magnetización elevada, por lo que es preciso utilizar campos y gradientes magnéticos elevados para lograr, por ejemplo, su direccionabilidad en los sistemas fisiológicos. En otros su elevado tamaño, al menos 1 µm, no permite una adecuada aplicación, por ejemplo, como sistemas transportadores de fármacos ya que difícilmente se lograría una adecuada distribución a nivel capilar. Las partículas quedarían retenidas en la red de vasos sanguíneos pequeños, pudiendo incluso producir un colapso de la red capilar. Además, los fenómenos de extravasación, necesarios para un óptimo efecto terapéutico del principio activo, desde el capilar hasta el tejido u órgano diana sólo se han observado en partículas de tamaño inferior a 1 µm (Gupta A.K., Gupta M., Biomaterials, 26, 3995, 2005). Para aplicaciones biológicas es necesario estudiar las características de biocompatibilidad y toxicidad de estos materiales y sus productos de degradación y algunos son inadecuados para estas aplicaciones. Finalmente, algunas de las técnicas de obtención de estos materiales compuestos pueden no ser lo suficientemente baratas y simples para su reproducción a gran escala.
Por otro lado, estos sistemas compuestos no poseen exclusivamente aplicaciones biomédicas. Por ejemplo, la patente US 6.232.026 describe un procedimiento de obtención de partículas en las que el recubrimiento está constituido por ferritas, mientras que el núcleo tiene una naturaleza polimérica (polivinilideno, resina silicónica o polimetacrilato) para electrografía; mientras que la patente US 5.998.076 describe la obtención de partículas de óxidos metálicos recubiertas con polímeros de diferente naturaleza (poliestireno, polivinilacetato, polietileno, polimetacrilato, etc. o copolímeros de éstos), con un tamaño entre 30 y 100 µm, para su empleo en la obtención de imágenes xerográficas.
La principal aplicación biomédica de los látex de etilcelulosa es el diseño de formas farmacéuticas de diferente naturaleza. Destaca su uso en la formulación de inyectables y preparados oftálmicos, aportando a éstos últimos un mayor tiempo de contacto ocular. Es importante también su aplicación en la elaboración de formas farmacéuticas orales para la obtención de películas de recubrimiento de principios activos y comprimidos matriciales, que constituyen formas farmacéuticas de liberación modificada. Este recubrimiento polimérico puede también permitir enmascarar sabores desagradables, mejorar la estabilidad del fármaco o separar físicamente componentes que son incompatibles en estado sólido. Además, son numerosas las formulaciones líquidas y los aerosoles elaborados utilizando estos sistemas. Por ejemplo, las patentes US 7.074.430, US 7.108.865, US 7.097.851 y ES 2.206.047, entre otras, describen la utilización de este tipo de látex de tilcelulosa en el diseño de formas farmacéuticas orales de acción controlada que permiten el transporte de fármacos.
Sin embargo, el látex de etilcelulosa bajo esas condiciones de uso, ve enormemente mermadas sus aplicaciones biomédicas, las cuales quedan limitadas casi exclusivamente al diseño de formas farmacéuticas y sistemas transportadores de fármacos. Además, y en este sentido, las formas de dosificación convencionales (comprimidos, jarabes, etc.) de las que forma parte, presentan el inconveniente de precisar una administración crónica para mantener una concentración de fármaco que garantice y mantenga el efecto terapéutico. Esta pauta de tratamiento puede provocar un bajo índice de cumplimiento terapéutico o generar considerables fluctuaciones en las concentraciones plasmáticas de fármaco entre dosis, lo que dará lugar a una respuesta subterapéutica o a reacciones adversas. Otra posible causa de aparición de efectos secundarios es la distribución de una proporción importante del fármaco en regiones no deseadas del organismo. Además, esta distribución sistémica o una pobre absorción provoca que la concentración de fármaco en el lugar de acción sea baja y no produzca el efecto terapéutico deseado.
En la patente US 4.177.177 se describe la producción de partículas poliméricas que comprenden etilcelulosa en las que no se incorporan metales magnéticos.
Escasos han sido los intentos de mejorar...
Reivindicaciones:
1. Una nanopartícula con un diámetro medio inferior a 1 micrometro que comprende un recubrimiento y un núcleo magnético, en la que dicho recubrimiento comprende un látex de etilcelulosa y dicho núcleo magnético comprende, al menos, una partícula de un metal sensible a campos magnéticos con un diámetro inferior a 0,95 micrometros.
2. Nanopartícula según la reivindicación 1, en la que dicho látex de etilcelulosa es un polímero de celulosa de fórmula (I)

en donde cada grupo R se selecciona independientemente entre hidrógeno y etilo, estando el grado de etoxilación comprendido entre el 10% y el 90%, preferentemente entre el 30% y el 70%, más preferentemente entre el 40% y el 60%; y "n" está comprendido entre 20 y 50.
3. Nanopartícula según la reivindicación 1 ó 2, en la que dicho metal sensible a campos magnéticos se selecciona entre el grupo que consiste en hierro carbonilo, magnetita, maghemita, ferritas de níquel, ferritas de cobalto, ferritas de cadmio, ferritas de hierro, ferritas de níquel-zinc-cobre, ferritas de bario, ferritas de estroncio, ferritas de cobalto-níquel, y mezclas de los mismos.
4. Nanopartícula según cualquiera de las reivindicaciones 1 a 3, en la que el diámetro medio de las partículas de metal sensible a los campos magnéticos es inferior a 0,8 micrometros, preferentemente inferior a 0,7 micrometros, más preferentemente comprendido entre 0,1 y 0,6 micrometros, aún más preferentemente entre 0,2 y 0,55 micrometros.
5. Nanopartícula según cualquiera de las reivindicaciones 1 a 4, cuyo diámetro medio está comprendido entre 200 y 950 nanometros, preferentemente entre 250 y 800 nanometros, más preferentemente entre 275 y 700 nanometros, aún más preferentemente entre 300 y 600 nanometros
6. Nanopartícula según cualquiera de las reivindicaciones 1 a 5, en la que la proporción en peso (látex de etilcelulosa):(metal sensible a campos magnéticos) está comprendida entre 6:1 y 1:6, preferentemente entre 4:1 y 1:4, más preferentemente 4:2 aproximadamente.
7. Un método para la producción de nanopartículas según cualquiera de las reivindicaciones 1 a 6, que comprende:
en donde la etapa b) puede realizarse antes o después de la etapa a), o de forma simultánea.
8. Método según la reivindicación 7, en el que el disolvente inmiscible en agua utilizado en la etapa a) es una mezcla de benceno y etanol.
9. Método según cualquiera de las reivindicaciones 7 u 8, en el que dicho alcano C1-C20 lineal o ramificado se selecciona del grupo formado por n-butano, i-butano, 2,2-dimetilbutano, 2,3-dimetilbutano, n-pentano, i-pentano, 2-metilpentano, 3-metilpentano, n-hexano, 2-metilhexano, 3-metilhexano, n-heptano, 2-metilheptano, n-octano, 2-metiloctano, n-nonano, 2-metilnonano, n-decano, n-undecano, n-duodecano, metilciclohexano y sus mezclas.
10. Método según cualquiera de las reivindicaciones 7 a 9, en el que la concentración del látex de etilcelulosa en la fase orgánica (etapa a)) está comprendida entre 15% y 20% en peso respecto al peso total de dicha fase orgánica.
11. Método según cualquiera de las reivindicaciones 7 a 10, en el que dicho ácido inorgánico es ácido nítrico (HNO3).
12. Método según la reivindicación 11, en el que dicho ácido nítrico (HNO3) está presente en una concentración comprendida entre 10-5 N y 10-1 N, preferentemente entre 10-4 N y 10-2 N, más preferentemente alrededor de 10-3 N.
13. Método según cualquiera de las reivindicaciones 7 a 10, en el que dicha base inorgánica es hidróxido sódico (NaOH).
14. Método según la reivindicación 7, en el que dicho tensioactivo se selecciona entre un dextrano, un éster de polioxietilensorbitano, un éster de sorbitano, un polietilenglicol, laurilsulfato sódico (LSNa), cetiltrimetil amonio y sus mezclas.
15. Método según la reivindicación 14, en el que dicho tensioactivo se selecciona entre LSNa, polietilenglicol 4000 y sus mezclas.
16. Método según la reivindicación 7, que comprende, además, la eliminación del disolvente utilizado en la etapa a).
17. Método según la reivindicación 7 ó 16, que comprende, además, someter la mezcla obtenida a un campo magnético.
18. Un sistema transportador de fármacos que comprende, al menos, una nanopartícula según cualquiera de las reivindicaciones 1 a 6, y, al menos, un fármaco.
19. Sistema según la reivindicación 18, en el que dicho fármaco es una agente antitumoral, antineoplásico o anticancerígeno, un agente antiinflamatorio, un fármaco utilizado en el tratamiento de la artrosis o artritis, un agente antiparkinsoniano, un fármaco útil para emboloterapia o un fármaco para el catabolismo de tumores mediante hipertermia.
20. Sistema según la reivindicación 18, que comprende un único fármaco.
21. Sistema según la reivindicación 18, que comprende dos o más fármacos diferentes.
22. Una composición farmacéutica que comprende, al menos, un sistema transportador de fármacos según cualquiera de las reivindicaciones 18 a 21, junto con, al menos, un vehículo farmacéuticamente aceptable.
23. Una composición que comprende al menos una nanopartícula según cualquiera de las reivindicaciones 1 a 6 y un vehículo.
24. Empleo de nanopartículas según cualquiera de las reivindicaciones 1 a 6, en el tratamiento de aguas residuales, en la fabricación de biosensorés, en la inmovilización de enzimas, en la separación magnética por afinidad de biomoléculas, en la selección de un tipo de células de entre una población celular, en xerografía o en electrografía.
25. Empleo de nanopartículas según cualquiera de las reivindicaciones 1 a 6, como agente de contraste por resonancia magnética o en la elaboración de un agente de contraste por resonancia magnética.
Patentes similares o relacionadas:
Mazindol como único principio activo o en combinación con hierro para el tratamiento del déficit de atención/hiperactividad, del 10 de Junio de 2020, de NLS Pharmaceutics AG: Composición que comprende mazindol como único principio activo para su utilización para el tratamiento preventivo y/o curativo del trastorno del déficit de la […]
Composición farmacéutica que comprende partículas de quelante de fosfato, del 3 de Junio de 2020, de Vifor Fresenius Medical Care Renal Pharma, Ltd: Una composición farmacéutica para administración oral, que comprende un quelante de fosfato, donde dicho quelante de fosfato comprende partículas que tienen una distribución […]
Clústeres cuánticos atómicos estables, su método de obtención y uso de los mismos, del 6 de Mayo de 2020, de UNIVERSIDADE DE SANTIAGO DE COMPOSTELA: Clústeres cuánticos atómicos, AQCs, estables caracterizados por estar compuestos por menos de 500 átomos de metal, su procedimiento de obtención caracterizado […]
Formulaciones que contienen triazinonas y hierro, del 22 de Abril de 2020, de BAYER ANIMAL HEALTH GMBH: Formulación que contiene toltrazurilo y hierro (III)-dextrano para su uso para el tratamiento simultáneo de infecciones por coccidios y deficiencias de hierro […]
Suplemento dietético, del 15 de Abril de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Una composición oral que comprende: - al menos una bacteria probiótica seleccionada de los géneros: Lactobacillus y Bifidobacterium, y - pirofosfato férrico […]
Régimen de dosificación de trimaltol férrico, del 1 de Abril de 2020, de Shield TX (UK) Limited: El trimaltol férrico para usar en el tratamiento o la prevención de la deficiencia de hierro con o sin anemia en pacientes que presentan enfermedad […]
Composición de agua mineral que contiene hierro biodisponible, del 18 de Marzo de 2020, de Snowdonia Research Sarl: Una composición de agua mineral artificial no tóxica que contiene hierro biodisponible, consistiendo dicha composición en una disolución acuosa que tiene un pH de 1 a 5 que […]
Triazinas para el tratamiento de enfermedades protozoarias, del 18 de Marzo de 2020, de CEVA Santé Animale SA: Una composición que comprende toltrazuril y un complejo de hierro, que es una solución coloidal acuosa de oxihidróxido beta-férrico y ácido glucoheptónico […]