METODO PARA TRATAR EL SISTEMA NERVIOSO CENTRAL MEDIANTE LA ADMINISTRACION DE ANALOGOS ESTRUCTURALES DE IGF.
Uso de un análogo estructural de IGF en la preparación de un medicamento para tratar el sistema nervioso central,
en el que el medicamento es para tratar o prevenir lesión neuronal en el sistema nervioso central, excepto cuando la enfermedad es esclerosis lateral amiotrófica, en el que el medicamento es para administración en columna no intracraneal y no intravertebral
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US01/26750.
Solicitante: COLORADO STATE UNIVERSITY RESEARCH FOUNDATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: P.O. BOX 483,FORT COLLINS, CO 80522.
Inventor/es: ISHII, DOUGLAS N.
Fecha de Publicación: .
Fecha Concesión Europea: 7 de Abril de 2010.
Clasificación PCT:
- A61K38/30 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Factores de crecimiento análogos a la insulina (somatomedinas), p. ej. IGF-1, IGF-2.
- A61P25/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del sistema nervioso.
Clasificación antigua:
- A61K38/00 A61K […] › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
Fragmento de la descripción:
Método para tratar el sistema nervioso central mediante la administración de análogos estructurales de IGF.
Sumario de la invención
Esta invención está dirigida al uso en la fabricación de un medicamento para tratar el sistema nervioso central mediante la administración en columna no intracraneal y no intravertebral de uno o más análogos estructurales de IGF. Más particularmente, la invención está dirigida a tratar trastornos o enfermedades del cerebro o la médula espinal mediante la administración en columna no intracraneal o no intravertebral de uno o más análogos estructurales de IGF.
Loddick y col. en Proc. Nat. Acad Sci. USA, 95, febrero de 1998, pág. 1894-1898, dan a conocer el uso de análogos estructurales de IGF-I para el tratamiento de apoplejía y enfermedades neurodegenerativas después de administración intracerebroventricular. El documento WO91/12018 da a conocer el uso de análogos estructurales de IGF-I para el tratamiento de enfermedades intestinales después de inyección subcutánea. Lemmay y col. en Bioscience information service, 1991, dan a conocer el efecto anabólico de análogos estructurales de IGF-I aplicados mediante bombas osmóticas después de traumatismo quirúrgico por resección intestinal. El documento US-A-4876242 da a conocer la fabricación de análogos sintéticos de IGF-I y su estimulación de algunos procesos de crecimiento. El documento US-A-5420111 da a conocer el uso de análogos estructurales de IGF-I o IGF-II para el tratamiento del retardo del crecimiento fetal. El documento US-A-5473054 da a conocer el tratamiento de restenosis de arterias coronarias, neoplasia y metástasis cerebrales por análogos estructurales de IGF-I.
Descripción de los dibujos
Fig. 1. Detección dependiente de la concentración de (A) hIGF-I, (B) Des(1-3)hIGF-I, (C) [Leu24]hIGF-I y (D) [Leu60]hIGF-I por ELISA. Se ensayaron las muestras por triplicado a cada concentración. Se determinó el coeficiente de correlación, r, mediante regresión lineal usando un programa de software informático.
Fig. 2. Distribución dependiente de la dosis de hIGF-I inmunorreactivo en LCR y plasma después de inyecciones subcutáneas en ratas adultas. Se extrajeron plasma y LCR para ELISA 90 min después de una sola inyección subcutánea en bolo de la dosis indicada de hIGF-I, y se ensayó cada muestra por triplicado. Se muestran medias
Fig. 3. Efecto de la administración simultánea de hIGF-II sobre la captación de hIGF-I en LCR. Se inyectaron por vía subcutánea a las ratas 150 µg de hIGF-I solo (n = 8) o la combinación de 150 µg de hIGF-I y 400 µg de hIGF-II (n = 6). Se extrajeron plasma y LCR 90 min después para el ensayo. Los valores son medias
Fig. 4. Distribución comparativa en LCR y plasma después de la administración de Des(1-3)hIGF-I (n = 4), hIGF-I (n =3) o vehículo (n = 2). Se inyectaron por vía subcutánea cantidades equivalentes (200 µg por rata) de Des(1-3)hIGF-I o hIGF-I, y se extrajeron plasma y LCR para el ensayo 90 min después. Se compararon las medias de grupo usando la prueba a posteriori de Newman-Keuhl. *P<0,002 y 0,003 para Des y hIGF-I, respectivamente, frente al control en LCR. *P<0,002 para hIGF-I frente al control en plasma.
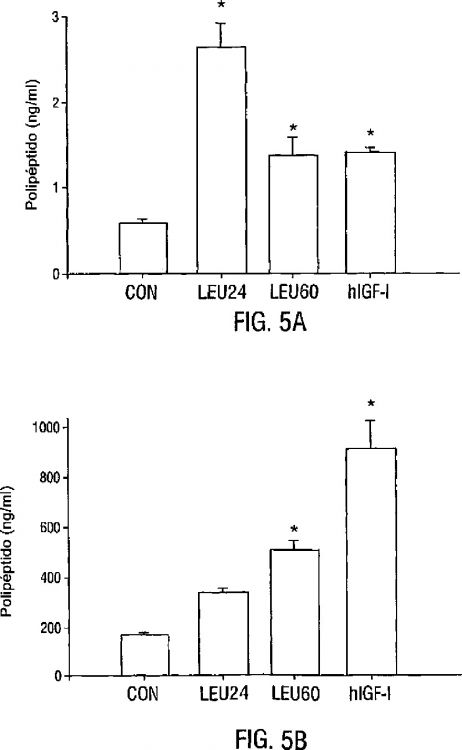
Fig. 5. Captación de [Leu24]hIGF-I y [Leu60]hIGF-I en LCR. Se inyectaron por vía subcutánea [Leu24]hIGF-I (200 µg por rata; n = 3 ratas), [Leu60]hIGF-I (100 µg por rata; n = 4) o hIGF-I (200 µg por rata; n = 3) o vehículo (n = 9), y 90 min después se extrajeron plasma y LCR para el ensayo. Parte A, LCR; Parte B, plasma. Se detectaron las diferencias entre medias de grupo usando la prueba a posteriori de Newman-Keuhl. *P<0,002 para hIGF-I frente a [Leu24]hIGF-I en LCR. *P<0,0004 para [Leu24] y [Leu60] frente al control y 0,0007 para hIGF-I frente al control en LCR. En plasma, *P<0,0002 y 0,0005 para [Leu24] y [Leu60], respectivamente, frente a hIGF-I. *P<0,0005 y 0,0002 para [Leu60] y hIGF-I, respectivamente, frente al control.
Descripción detallada de la invención
Esta invención está dirigida al uso en la fabricación de un medicamento para tratar el sistema nervioso central mediante la administración en columna no intracraneal y no intravertebral de uno o más análogos estructurales de IGF. Más particularmente, la invención está dirigida a tratar trastornos o enfermedades del cerebro o de la médula espinal mediante la administración en columna no intracraneal o no intravertebral de uno o más análogos estructurales de IGF. Con los fines de esta invención, los "análogos estructurales de IGF" se definen como moléculas que tienen una homología de secuencia sustancial con factores de crecimiento de tipo insulina de origen natural (IGF), incluyendo IGF-I e IGF-II humanos y animales (incluyendo, pero sin limitación, de vaca, cerdo, perro, oveja, caballo, ciervo, cabra, rata, ratón y pollo). Más preferiblemente, los análogos estructurales de IGF tienen secuencias aminoacídicas de moléculas de IGF que se han modificado mediante delecciones, sustituciones y/o adiciones de menos de 15 aminoácidos.
Según la invención, la vía de administración preferida del análogo estructural de IGF es en un sitio fuera de la barrera hematoencefálica (BBB), de la barrera hematonerviosa del sistema nervioso central (B-CNS-B) y de la barrera hematomedular (B-SC-B). Puede usarse cualquiera de las vías de administración comunes conocidas por la ciencia farmacéutica que pueda suministrar análogos estructurales de IGF a la circulación incluyendo, pero sin limitación, percutánea, intradérmica, subcutánea, intravenosa, intramuscular, intraarterial, intraperitoneal, parenteral, bucal, sublingual, rectal, oral, nasal, por inhalación, por una bomba o matriz implantada subcutáneamente o por un constructo plasmídico que contiene un gen de análogo estructural de IGF que se administra a un sitio fuera de la BBB, B-CNS-B y B-SC-B. Por ejemplo, la cavidad nasal y el pulmón están muy vascularizados, y los análogos estructurales de IGF administrados a la cavidad nasal o mediante inhalación pueden captarse rápidamente por los microvasos locales, dando como resultado la captación de análogos de IGF por el líquido cefalorraquídeo (LCR) a través de la BBB o B-CNS-B. Esta invención no está limitada a una vía de administración particular más que la administración sea en un sitio fuera de la BBB, B-CNS-B y B-SC-B.
En una realización preferida, puede administrarse un análogo estructural de IGF solo o en combinación con otros análogos de IGF. El análogo de IGF puede combinarse también con uno o más excipientes, agentes colorantes, sales, disolventes, portadores, estabilizadores y otros ingredientes que pueden usarse en formulaciones y son conocidos en la ciencia farmacéutica. En un realización preferida adicional, se administra el análogo estructural de IGF en una cantidad de aproximadamente 0,01 µg/kg/día a aproximadamente 4 mg/kg/día.
En una realización preferida, la invención está dirigida a tratar trastornos o enfermedades del cerebro o la médula ósea después del nacimiento, tales como enfermedad de Alzheimer, enfermedad de Parkinson, demencia relacionada con el SIDA, demencia senil, apoplejía, traumatismo, síndromes ganglionares corticobasales, demencia progresiva, demencia familiar con paraparesia espástica, parálisis supranuclear progresiva, esclerosis múltiple, encefalopatía hepática, enfermedad de Pick, enfermedad de Huntington, esclerosis cerebral difusa de Schilder, encefalomielitis hemorrágica necrosante aguda, tumores cerebrales y similares. Esta invención no incluye esclerosis lateral amiotrófica.
Los análogos estructurales de IGF que pueden usarse en la presente invención incluyen, pero sin limitación, des(1-3)IGF-I, que es un análogo de IGF-I que carece del tripéptido N-terminal; [Arg3]IGF-I, que es un análogo de IGF-I en el que Arg está sustituida por Glu en posición 3; [Leu24]IGF-I, que es un análogo de IGF-I en el que Leu está sustituida por Thr en posición 24; [Leu60]IGF-I, que es un IGF-I mutante con Leu sustituida por Tyr en posición 60; R3IGF-I largo, que es un IGF-I mutante con Arg sustituida por Glu en posición 3, así como una extensión de 13 aminoácidos en el...
Reivindicaciones:
1. Uso de un análogo estructural de IGF en la preparación de un medicamento para tratar el sistema nervioso central, en el que el medicamento es para tratar o prevenir lesión neuronal en el sistema nervioso central, excepto cuando la enfermedad es esclerosis lateral amiotrófica, en el que el medicamento es para administración en columna no intracraneal y no intravertebral.
2. El uso de la reivindicación 9, en el que la lesión es debida a un trastorno o enfermedad del sistema nervioso central.
3. El uso de la reivindicación 1 ó 2, en el que la lesión es debida a un tumor o cáncer.
4. El uso de una cualquiera de las reivindicaciones 1 a 3, en el que la lesión neuronal en el sistema nervioso central es debida a un trastorno o enfermedad en el cerebro o la médula espinal después del nacimiento.
5. El uso de la reivindicación 4, en el que la lesión neuronal en el cerebro es debida a encefalopatía hepática, enfermedad de Pick, enfermedad de Huntington, esclerosis cerebral difusa de Schilder, enfermedad de Alzheimer, enfermedad de Parkinson, demencia relacionada con el SIDA, demencia senil, apoplejía, traumatismo, síndromes ganglionares corticobasales, demencia progresiva, demencia familiar con paraparesia espástica, parálisis supranuclear progresiva, esclerosis múltiple o encefalomielitis hemorrágica necrosante aguda.
6. El uso de cualquiera de las reivindicaciones 1 a 5, en el que el análogo estructural de IGF es des(1-3)IGF-I humano.
7. El uso de cualquiera de las reivindicaciones 1 a 5, en el que el análogo estructural de IGF es [Arg3]IGF-I, [Leu24]IGF-I, [Leu60]IGF-I, R3IGF-I largo, des(1-6)IGF-II, [Gly1]IGF-II, [Arg6]IGF-II o [Leu27]IGF-II humanos.
8. El uso de cualquiera de las reivindicaciones 1 a 7, en el que el medicamento es tal que el análogo estructural de IGF puede administrarse en una cantidad de aproximadamente 0,01 µg/kg/día hasta aproximadamente 4 mg/kg/día.
9. El uso de cualquiera de las reivindicaciones 1 a 8, en el que la administración en columna no intracraneal y no intravertebral es percutánea, subcutánea, intramuscular, intravenosa, intraarterial, intradérmica, por inhalación o intranasal.
10. Análogo estructural de IGF para uso en el tratamiento o la prevención administrativo en columna no intracraneal y no intravertebral de lesión neuronal en el sistema nervioso central, excepto cuando la enfermedad es esclerosis lateral amiotrófica.
11. El análogo estructural de IGF de la reivindicación 10, en el que el análogo estructural de IGF es [Arg3]IGF-I, [Leu24]IGF-I, [Leu60]IGF-I, R3IGF-I largo, des(1-6)IGF-II, [Gly1]GF-II, [Arg6]IGF-II, [Leu27]IGF-II o des(1-3)IGF-I humanos.
12. El análogo estructural de IGF para uso en las reivindicaciones 10 u 11, en el que la lesión es debida a un trastorno o enfermedad del sistema nervioso central.
13. El análogo estructural de IGF para uso en las reivindicaciones 10 u 11, en el que la lesión es debida a un tumor o cáncer.
14. El análogo estructural de IGF para uso en cualquiera de las reivindicaciones 10 a 12, en el que la lesión neuronal en el sistema nervioso central es debida a un trastorno o enfermedad en el cerebro o la médula espinal después del nacimiento.
15. El análogo estructural de IGF para uso en la reivindicación 14, en el que la lesión neuronal en el cerebro es debida a encefalopatía hepática, enfermedad de Pick, enfermedad de Huntington, esclerosis cerebral difusa de Schilder, enfermedad de Alzheimer, enfermedad de Parkinson, demencia relacionada con el SIDA, demencia senil, apoplejía, traumatismo, síndromes ganglionares corticobasales, demencia progresiva, demencia familiar con paraparesia espástica, parálisis supranuclear progresiva, esclerosis múltiple o encefalomielitis hemorrágica necrosante aguda.
Patentes similares o relacionadas:
Derivados de 8-amino-2-oxo-1,3-diazaespiro-[4.5]-decano, del 29 de Julio de 2020, de GRUNENTHAL GMBH: Un compuesto según la fórmula general (I) **(Ver fórmula) donde R1 y R2 significan independientemente -H; -alquilo C1-C6, lineal o ramificado, […]
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
Derivado de 5-etiol-4-metil-pirazol-3-carboxamida que tiene actividad como agonista de TAAR, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un compuesto de fórmula I: **(Ver fórmula)** que es 5-etil-4-metil-N-[4-[(2S) morfolin-2-il]fenil]-1H-pirazol-3-carboxamida, o una sal de adición de ácido farmacéuticamente […]
Nuevos moduladores de receptores de fosfato de esfingosina, del 15 de Julio de 2020, de THE SCRIPPS RESEARCH INSTITUTE: Una composicion farmaceutica que comprende un compuesto de formula 265: **(Ver fórmula)** o una sal, estereoisomero, hidrato o solvato farmaceuticamente aceptable […]
Composición que comprende cinamaldehído y cinc, del 8 de Julio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Composición que comprende cinamaldehído y cinc para la utilización en la mejora de uno o más de rendimiento cognitivo, cognición, humor o memoria en un […]
Derivado de amina cíclica y uso farmacéutico del mismo, del 1 de Julio de 2020, de TORAY INDUSTRIES, INC.: Un derivado de amina cíclica representado por la siguiente fórmula general (I): **(Ver fórmula)** donde R1 representa un grupo alquiloxi que tiene de 1 a 3 átomos […]
Cápsulas blandas entéricas de liberación controlada de ésteres de fumarato, del 1 de Julio de 2020, de Banner Life Sciences LLC: Una composición farmacéutica oral que comprende una cápsula blanda entérica que encapsula fumarato de monometilo suspendido en una matriz líquida […]