CÉLULAS PROGENITORAS PROCEDENTES DE LA GELATINA DE WHARTON DE CORDÓN UMBILICAL HUMANO.
Un procedimiento para obtener una población de células progenitoras humanas,
que comprende la etapa de extraer dicha población de la gelatina de Wharton
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CA2004/000182.
Solicitante: DAVIES, JOHN E.
SARUGASER, RAHUL
BAKSH, DOLORES
HOSSEINI, MORRIS
LICKORISH, ANTONY DAVID SUTTON.
Nacionalidad solicitante: Canadá.
Dirección: 285 GARDEN AVENUE TORONTO, ONTARIO M6R 1J4 CANADA.
Inventor/es: DAVIES, JOHN, E., BAKSH,DOLORES, SARUGASER,RAHUL, LICKORISH,ANTONY DAVID SUTTON, HOSSEINI,MORRIS.
Fecha de Publicación: .
Fecha Solicitud PCT: 10 de Febrero de 2004.
Fecha Concesión Europea: 25 de Agosto de 2010.
Clasificación Internacional de Patentes:
- C12N5/06B18P
- C12N5/06B21P
- C12N5/06B2L
Clasificación PCT:
- C12N5/07 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células o tejidos animales.
Clasificación antigua:
- C12N5/06
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
DESCRIPCIÓN CAMPO DE LA INVENCIÓN [0001] Esta invención se centra en la recolección de una población de células humanas que proliferan rápidamente procedentes de tejido conjuntivo del cordón umbilical (CU); el cultivo de dichas células en condiciones osteogénicas o de formación de hueso; la demostración de un alto porcentaje de células dentro de estas poblaciones que son inmunológicamente incompetentes, como se muestra por su falta de antígenos de histocompatibilidad de superficie celular; y la capacidad de estas células para usarlas como una fuente de células para diferentes terapias basadas en células.
ANTECEDENTES DE LA INVENCIÓN [0002] El CU es una de las primeras estructuras que se forma después de la gastrulación (formación de las tres capas germinativas embrionarias). Cuando se inicia el plegado, el disco embrionario queda conectado por el intestino medio primitivo (origen embrionario) al saco vitelino primitivo (origen extraembrionario) por los vasos vitelinos y alantoideos que a su vez se desarrollan para formar los vasos umbilicales {Pereda, 2002 50/id} {Tuchmann-Duplessis, 1972 77/id} {Tuchmann-Duplessis, 1972 77/id} {Haynesworth, 1998 51/id}. Estos vasos están soportados en, y rodeados por lo que en general se considera un tejido mesenquimal primitivo de la derivación extraembrionaria primaria llamada gelatina de Wharton (WJ) {Weiss, 1983 80/id}. A partir de esta etapa temprana, el CU crece durante la gestación, para convertirse en el cordón de 30-50 cm observado en el nacimiento. Por lo tanto, se puede esperar que la GW (gelatina de Wharton) contenga no solo las células de tipo fibroblastos o de tipo miofibroblastos que se han descrito en la bibliografía (véase a continuación), sino también poblaciones de células progenitoras que pueden dar lugar a las células del volumen en expansión de la GW necesarias para soportar el crecimiento del cordón durante el desarrollo embrionario y fetal. [0003] La GW fue descrita por primera vez por Thomas Wharton, que publicó su tratado Adenographia en 1956. Posteriormente se ha definido como un tejido conjuntivo gelatinoso, laxo, mucoso, compuesto de células dispersas en una sustancia triturada amorfa compuesta de proteoglicanos, incluyendo ácido hialurónico {Schoenberg, 1960 81/id}, y diferentes tipos de colágenos (Nanaev y col., 1997). Las células dispersas en la matriz se han descrito como de “tipo fibroblasto” que son de forma estrellada en el cordón colapsado y alargadas en el cordón distendido (Parry, 1970). Las células musculares lisas se observaron inicialmente en la matriz (Chacko y Reynolds, 1954), aunque esto fue discutido por Parry (1970) quien las describió como “fibroblastos algo inusuales” que superficialmente se parecen a células musculares lisas. Después de esto, se hizo poco trabajo de caracterización de estas células hasta 1993 cuando Takechi y col. (1993) realizaron investigaciones inmunohistoquímicas sobre estas células. Describieron las células como de “tipo fibroblastos” que eran “fusiformes o de forma estrellada con procesos citoplasmáticos largos y una red ondulada de fibras de colágeno en una sustancia triturada amorfa” (Takechi y col., 1993). Para la tinción inmunohistoquímica usaron anticuerpos primarios contra actina y miosina (proteínas contráctiles citoplasmáticas), vimentina (característica de fibroblastos de origen mesenquimal embrionario) y desmina (específica de células de origen miógeno) con el fin de determinar qué tipos de miosina están asociados con los fibroblastos de la GW. Observaron niveles altos de actomiosina químicamente extraíble, y aunque los fibroblastos contienen actomiosina citoplasmática, no se tiñen para la actina y miosina, mientras que los fibroblastos de la GW se teñían positivamente para ambas. Además, se observaron tinciones positivas tanto para vimentina como para desmina conduciendo a la conclusión de que estos fibroblastos modificados en la GW derivaban de tejido mesenquimal primitivo (Takechi y col., 1993). Un estudio posterior más reciente de Nanaev y col. (1997) demostraba 5 etapas de diferenciación de las células progenitoras mesenquimales proliferativas en cordones prematuros. Sus descubrimientos apoyaban la sugerencia de que existen miofibroblastos en la matriz de la GW. La caracterización inmunohistoquímica de las células de la GW muestra notables similitudes con la de los pericitos que se sabe que son una fuente principal de células osteogénicas en la morfogénesis ósea y también forman nódulos óseos denominados unidades formadoras de colonias de osteoblastos (UFC-O) (Aubin, 1998) en cultivo (Canfield y col., 2000). [0004] Publicaciones recientes han descrito procedimientos para recoger células del CU, en lugar de la sangre del CU. Mitchell y col. (Mitchell y col., 2003) describen un procedimiento en el que primero separan y descartan los vasos umbilicales para recoger el tejido restante. Este último, que incluirá tanto GW restante (parte de la cual se habrá descartado con los vasos, puesto que los vasos umbilicales están totalmente envueltos en GW) como epitelio amniótico, después se trocea para producir fragmentos de tejido pequeños que se transfieren a placas de cultivo tisular. Estos fragmentos de tejido después se usan como explantes primarios a partir de los cuales las células migran al sustrato de cultivo. [0005] En otra publicación, Romanov y col. (Romanov y col., 2003) indican que consiguieron aislar células de tipo células madres mesenquimales de vasculatura del cordón, aunque también indicaban que sus cultivos no contenían células de la GW. Específicamente, usan una sola digestión con colagenasa de 15 min de dentro de la vena umbilical, que da una población mixta de células endoteliales y subendoteliales vasculares. Romanov y col. mostraron que aparecía un escaso número de células de tipo fibroblastos de esta recolección de células después de 7 días. [0006] Además, la patente de EE.UU. 5.919.702 describe un procedimiento para aislar “precondrocitos” de la GW de CU humano, y su uso para producir cartílago. En particular, el procedimiento comprende abrir longitudinalmente cortando una sección de 2,54 cm de cordón , separar por disección los vasos sanguíneos y la “envoltura”, que después se descartan, y recoger la GW en un envase estéril donde se corta en secciones de 2-3 mm2 para el cultivo. En un procedimiento preferido, las células se aíslan poniendo una sección de 2-3 mm2 de la GW en un portaobjetos de vidrio en la parte inferior de una placa Petri, cubriéndola con otro portaobjetos, y cultivándola durante 10-12 días con el fin de permitir que los “precondrocitos” migren al exterior de la superficie de la placa de cultivo. [0007] Un objetivo de la presente invención es proporciona una población de células que comprende células progenitoras humanas. [0008] Otro objetivo de la presente invención es proporcionar una fuente a partir de la cual se puedan extraer células progenitoras humanas. [0009] Un objeto adicional de la presente invención es proporcionar un procedimiento para aislar células progenitoras humanas. [0010] Un objeto adicional de la presente invención es proporcionar células osteoprogenitoras humanas útiles para la producción de tejido óseo. [0011] Un objeto adicional de la presente invención es proporcionar células progenitoras inmunoincompetentes humanas terapéuticamente útiles.
RESUMEN DE LA INVENCIÓN [0012] No se ha ideado un procedimiento para extraer células de la gelatina de Wharton de cordón umbilical humano, que dé una población de células única caracterizada por la rápida proliferación, la presencia de células osteoprogenitoras y otras células progenitoras humanas, incluyendo células inmunoincompetentes que no presenten ninguno de los marcadores de histocompatibilidad mayor (doble negativo para el antígeno leucocitario humano (HLA)). La población de células es una fuente útil de células progenitoras a partir de las cuales cultivar hueso y otros tejidos conjuntivos, y para la transferencia autógena y alógena de células progenitoras a los pacientes, para propósitos terapéuticos. [0013] Más en particular, y según un aspecto de la presente invención, se proporciona un extracto de gelatina de Wharton, en el que el extracto comprende células progenitoras humanas y se obtiene por digestión enzimática de la gelatina de Wharton próxima a la vasculatura del cordón umbilical humano, en una región llamada convenientemente la zona perivascular. El procedimiento de extracción da como resultado adecuadamente un extracto que carece esencialmente de células de la sangre del cordón umbilical, células epiteliales o células endoteliales del CU y células derivadas de la estructura vascular...
Reivindicaciones:
1. Un procedimiento para obtener una población de células progenitoras humanas, que comprende la etapa de extraer dicha población de la gelatina de Wharton en la zona perivascular del cordón umbilical humano, en el que la población comprende células osteoprogenitoras comprometidas y células progenitoras que tienen un fenotipo doble negativo para MHC, y además en el que dicha población se expande más rápidamente que otras poblaciones de células progenitoras extraídas de la gelatina de Wharton.
2. El procedimiento según la reivindicación 1, en el que la etapa de extracción se lleva a cabo en vasos diseccionados del cordón umbilical.
3. El procedimiento según la reivindicación 1 o reivindicación 2, en el que dicha gelatina de Wharton se somete a digestión enzimática en un medio de extracción de células adecuado.
4. El procedimiento según la reivindicación 3, en el que la digestión enzimática da como resultado la liberación de células de la matriz de colágeno de dicha gelatina de Wharton.
5. El procedimiento según la reivindicación 4, en el que la etapa de extracción de células se lleva a cabo a 37ºC en disolución salina tamponada con fosfato y colagenasa de 0,1 a 1,0 mg/ml, durante un periodo de 12 a 36 horas.
6. Un procedimiento para producir una población de células que comprende células progenitoras humanas, que comprende la etapa de cultivar células obtenidas por el procedimiento según una cualquiera de las reivindicaciones 1 a 5.
7. El procedimiento según cualquier reivindicación precedente, que comprende la etapa adicional de tratar dicha población de células para enriquecerla en células osteoprogenitoras.
8. El procedimiento de una cualquiera de las reivindicaciones 1 a 6, que comprende la etapa adicional de tratar dicha población para el enriquecimiento en
células progenitoras que tienen un fenotipo doble negativo para MHC.
9. El procedimiento según la reivindicación 8, en el que dicha población se somete a una etapa de congelación/descongelación para el enriquecimiento en células progenitoras que tienen el fenotipo doble negativo para MHC.
10. Una población de células aisladas que comprende células progenitoras humanas, en la que la población de células (1) se puede extraer de la gelatina de Wharton en la zona perivascular del cordón umbilical humano, (2) se expande más rápidamente que otras poblaciones de células progenitoras extraídas de la gelatina de Wharton, (3) comprende células osteoprogenitoras comprometidas, y (4) comprende células progenitoras que tienen un fenotipo doble negativo para MHC.
11. Una población de células que es una subpoblación de la población de células según la reivindicación 10, en la que dicha subpoblación está enriquecida en células progenitoras que tienen un fenotipo doble negativo para MHC.
12. Una población de células según una cualquiera de las reivindicaciones 10 a 11, en un estado criconservado.
13. Un procedimiento para producir células óseas, que comprende la etapa de cultivar una población de células según la reivindicación 10, en condiciones para inducir su diferenciación en células óseas.
14. El procedimiento según la reivindicación 13, en el que dichas células se cultivan en ausencia de complementos osteogénicos.
15. Un procedimiento para producir adipocitos, que comprende la etapa de cultivar una población de células según la reivindicación 10, en condiciones para inducir su diferenciación en adipocitos.
16. Un procedimiento para producir mioblastos, que comprende la etapa de cultivar una población de células según la reivindicación 10, en condiciones para inducir su diferenciación en mioblastos.
17. El uso de una población de células según una cualquiera de las reivindicaciones 10 a 12, en la preparación de un medicamento para el tratamiento de una afección, enfermedad o trastorno médico.
5 18. El procedimiento según una cualquiera de las reivindicaciones 1 a 6, que comprende la etapa adicional de tratar dicha población para enriquecerla en células progenitoras que tienen un fenotipo alterado para MHC.
19. El procedimiento según las reivindicaciones 1 a 9 y 13 a 18, en el que la
población de células progenitoras humanas carece esencialmente de células derivadas 10 de la estructura vascular del cordón.
20. Una población de células aisladas según una cualquiera de las reivindicaciones 10 a 12, en la que la población carece esencialmente de células derivadas de la estructura vascular del cordón.
Patentes similares o relacionadas:
MICROCÁPSULAS ESFÉRICAS O NO ESFÉRICAS QUE COMPRENDEN PÉPTIDOS GLP-1, SU PRODUCCIÓN Y SU USO, del 17 de Agosto de 2011, de BIOCOMPATIBLES UK LIMITED: Microcápsula esférica que comprende como mínimo un revestimiento superficial y un núcleo, en la que el como mínimo un revestimiento superficial comprende […]
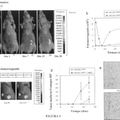 MODELO ANIMAL DE ANGIOGENESIS HUMANA Y SUS APLICACIONES, del 2 de Febrero de 2011, de UNIVERSIDAD AUTONOMA DE MADRID: La presente invención se relaciona con un modelo animal de angiogénesis humana para la monitorización cuantitativa y no invasiva de dicho proceso de angiogénesis in vivo mediante […]
MODELO ANIMAL DE ANGIOGENESIS HUMANA Y SUS APLICACIONES, del 2 de Febrero de 2011, de UNIVERSIDAD AUTONOMA DE MADRID: La presente invención se relaciona con un modelo animal de angiogénesis humana para la monitorización cuantitativa y no invasiva de dicho proceso de angiogénesis in vivo mediante […]
PROCEDIMIENTO PARA LA OBTENCION DE CELULAS MADRE MESENQUIMALES A PARTIR DE LA FRACCION MONONUCLEAR DE LA MEDULA OSEA HUMANA, del 15 de Marzo de 2010, de BANC DE SANG I TEIXITS: Procedimiento para la obtención de células madre mesenquimales a partir de la fracción mononuclear de la médula ósea humana. La presente invención se refiere […]
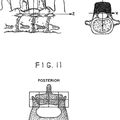 REGENERACION E INCREMENTO DE HUESO UTILIZANDO CELULAS MADRE MESENQUIMALES, del 2 de Diciembre de 2009, de OSIRIS THERAPEUTICS, INC.: SE PRESENTAN COMPOSICIONES Y METODOS PARA ACRECENTAR LA FORMACION DE HUESOS A BASE DE ADMINISTRAR CELULAS MADRE MESENQUIMATOSAS HUMANAS AISLADAS (HMSCS) CON UN MATERIAL […]
REGENERACION E INCREMENTO DE HUESO UTILIZANDO CELULAS MADRE MESENQUIMALES, del 2 de Diciembre de 2009, de OSIRIS THERAPEUTICS, INC.: SE PRESENTAN COMPOSICIONES Y METODOS PARA ACRECENTAR LA FORMACION DE HUESOS A BASE DE ADMINISTRAR CELULAS MADRE MESENQUIMATOSAS HUMANAS AISLADAS (HMSCS) CON UN MATERIAL […]
 CELULAS MADRE MESENQUIMALES COMO VEHICULOS PARA LA TRANSFERENCIA DE CANALES IONICOS EN ESTRUCTURAS SINCITIALES, del 30 de Noviembre de 2009, de THE TRUSTEES OF COLUMBIA UNIVERSITY IN THE CITY OF NEW YORK
THE RESEARCH FOUNDATION OF STATE UNIVERSITY OF NEW YORK: Una composición que comprende una célula madre mesenquimal en la que se ha introducido un ácido nucleico que codifica un canal de HCN en una cantidad suficiente […]
CELULAS MADRE MESENQUIMALES COMO VEHICULOS PARA LA TRANSFERENCIA DE CANALES IONICOS EN ESTRUCTURAS SINCITIALES, del 30 de Noviembre de 2009, de THE TRUSTEES OF COLUMBIA UNIVERSITY IN THE CITY OF NEW YORK
THE RESEARCH FOUNDATION OF STATE UNIVERSITY OF NEW YORK: Una composición que comprende una célula madre mesenquimal en la que se ha introducido un ácido nucleico que codifica un canal de HCN en una cantidad suficiente […]
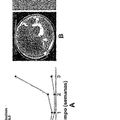 POBLACIONES DE CELULAS PROGENITORAS, EXPANSION DE LAS MISMAS Y CRECIMIENTO DE TIPOS DE CELULAS NO HEMATOPOYETICAS Y TEJIDOS PROVENIENTES DE LAS MISMAS, del 13 de Noviembre de 2009, de BAKSH, DOLORES
DAVIES, JOHN E.
ZANDSTRA, PETER: Método para expandir células progenitoras no hematopoyéticas humanas, comprendiendo dicho método la etapa de someter una población de células […]
POBLACIONES DE CELULAS PROGENITORAS, EXPANSION DE LAS MISMAS Y CRECIMIENTO DE TIPOS DE CELULAS NO HEMATOPOYETICAS Y TEJIDOS PROVENIENTES DE LAS MISMAS, del 13 de Noviembre de 2009, de BAKSH, DOLORES
DAVIES, JOHN E.
ZANDSTRA, PETER: Método para expandir células progenitoras no hematopoyéticas humanas, comprendiendo dicho método la etapa de someter una población de células […]
PROCEDIMIENTO PARA LA PREPARACION DE LINEAS CELULARES HUMANAS PERMANENTES, del 24 de Septiembre de 2010, de CEVEC PHARMACEUTICALS GMBH: Procedimiento para la preparación de una línea celular humana permanente, en el que se transfectan simultáneamente amniocitos aislados con (i) […]
CÉLULAS MADRE OBTENIDAS DE PULPA DE DIENTES TEMPORALES O PERMANENTES Y DE GERMEN DENTAL, QUE PUEDEN PRODUCIR TEJIDO ÓSEO HUMANO, del 17 de Junio de 2011, de TESLAB S.R.L: Una población de células madre de origen mesenquimatoso y no hemático, que se puede obtener a partir de pulpa de dientes temporales humanos, o de pulpa de dientes permanentes […]