FORMULACIONES FARMACEUTICAS EN CAPAS QUE COMPRENDEN UNA CAPA INTERMEDIA DE DISOLUCION RAPIDA.
Una formulación farmacéutica en capas para la administración de dos o más ingredientes farmacéuticos activos que comprende:
una primera capa farmacéutica que comprende un primer ingrediente farmacéutico activo;
una segunda capa farmacéutica que comprende un segundo ingrediente farmacéutico activo; y
una capa intermedia de liberación rápida dispuesta entre dichas capas farmacéuticas primera y segunda, en la que dicha capa intermedia de liberación rápida está configurada para disolverse rápidamente in vivo, y, con ello, dejar a dichas capas farmacéuticas primera y segunda sustancialmente intactas, pero físicamente separadas
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/084177.
Solicitante: OREXIGEN THERAPEUTICS, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3344 NORTH TORREY PINES COURT, SUITE 200,LA JOLLA, CA 92037.
Inventor/es: WEBER, ECKARD, MCKINNEY,ANTHONY A, TOLLEFSON,GARY, SOLTERO,RICK.
Fecha de Publicación: .
Fecha Concesión Europea: 17 de Marzo de 2010.
Clasificación Internacional de Patentes:
- A61K31/137 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Arilalquilaminas, p. ej. Anfetamina, epinefrina, salbutamol, efedrina.
- A61K31/138 A61K 31/00 […] › Ariloxialquilaminas, p. ej. propranolol, tamoxifeno, fenoxibenzamina (atenolol A61K 31/165; pindolol A61K 31/404; timolol A61K 31/5377).
- A61K31/155 A61K 31/00 […] › Amidinas ( ), p. ej. Guanidina (H 2 N—C(=NH)—NH 2 ), isourea (HN=C(OH)NH 2 ), isotiourea (HN=C(SH)—NH 2 ).
- A61K31/35 A61K 31/00 […] › que tienen ciclos con seis eslabones con un oxígeno como único heteroátomo de un ciclo.
- A61K31/423 A61K 31/00 […] › condensados con carbociclos.
- A61K31/485 A61K 31/00 […] › Derivados del morfinano, p. ej. morfina, codeína.
- A61K31/5513 A61K 31/00 […] › 1,4-Benzodiazepinas, p. ej. diazepam.
- A61K45/06 A61K […] › A61K 45/00 Preparaciones medicinales que contienen ingredientes activos no previstos en los grupos A61K 31/00 - A61K 41/00. › Mezclas de ingredientes activos sin caracterización química, p. ej. compuestos antiflojísticos y para el corazón.
- A61K9/20K4B
Clasificación PCT:
- A61K31/137 A61K 31/00 […] › Arilalquilaminas, p. ej. Anfetamina, epinefrina, salbutamol, efedrina.
- A61K31/138 A61K 31/00 […] › Ariloxialquilaminas, p. ej. propranolol, tamoxifeno, fenoxibenzamina (atenolol A61K 31/165; pindolol A61K 31/404; timolol A61K 31/5377).
- A61K31/155 A61K 31/00 […] › Amidinas ( ), p. ej. Guanidina (H 2 N—C(=NH)—NH 2 ), isourea (HN=C(OH)NH 2 ), isotiourea (HN=C(SH)—NH 2 ).
- A61K31/35 A61K 31/00 […] › que tienen ciclos con seis eslabones con un oxígeno como único heteroátomo de un ciclo.
- A61K31/423 A61K 31/00 […] › condensados con carbociclos.
- A61K31/485 A61K 31/00 […] › Derivados del morfinano, p. ej. morfina, codeína.
- A61K31/5513 A61K 31/00 […] › 1,4-Benzodiazepinas, p. ej. diazepam.
- A61K9/24 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › en dosis unitarias constituidas por capas u hojas.
Fragmento de la descripción:
Formulaciones farmacéuticas en capas que comprenden una capa intermedia de disolución rápida.
Campo de la invención
La presente invención versa acerca de formulaciones farmacéuticas que tienen dos o más capas farmacéuticas intercaladas con una o más capas intermedias en las que las capas farmacéuticas incluyen, sin limitación, composiciones farmacéuticas útiles para lograr la pérdida de peso, para la supresión del apetito y/o para tratar afecciones relacionadas con la obesidad en las personas.
Descripción de la técnica relacionada
En las aplicaciones farmacéuticas se conocen ciertos tipos de comprimidos en capas. Algunas aplicaciones farmacéuticas separan entre sí, dentro de un comprimido, las capas que pueden interactuar de forma potencial. Por ejemplo, la patente estadounidense nº 6.576.256 da a conocer la separación mutua entre compuestos que potencialmente pueden interactuar entre sí usando capas planas separadas de un comprimido, capas concéntricas, perlas o gránulos recubiertos y/o usando tampones. Thombre, A. G., L. E. Appel, et al. (2004), "Osmotic drug delivery using swellable-core technology", J. Control Release 94(1): 75-89, dan a conocer un comprimido con un núcleo que contiene un fármaco y un componente hinchable con el agua y uno o más orificios de administración en diferentes configuraciones del núcleo, incluyendo formulaciones de dos y tres capas de comprimido en comprimido (CIC). La patente estadounidense nº 6.706.283 da a conocer un dispositivo de administración osmótica fabricado con geometría bicapa en el que el núcleo comprende una capa hinchable "encajonada" entre dos capas de fármacos. El revestimiento de un comprimido bicapa puede incluir una membrana permeable al agua, pero es sustancialmente impermeable al fármaco y/o a los excipientes contenidos en el mismo. La patente estadounidense nº 6.630.165 da a conocer formas y procedimientos de dosificación para proporcionar una reboxetina de liberación sostenida que incluye un núcleo comprimido de tres capas con una primera capa componente con un fármaco, una segunda capa componente con una dosis de choque y una tercera capa barrera componente que separa la capa con el fármaco de la capa con la dosis de choque. La capa barrera es inerte con respecto a la composición de la capa con el fármaco y sustancialmente impermeable, de modo que se impide que se mezclen el fármaco y los componentes de la capa con la dosis de choque.
Entre las formas de comprimidos de múltiples capas, un tipo incluye una primera capa para proporcionar la liberación inmediata de un fármaco y una segunda capa para proporcionar la liberación controlada del fármaco. La patente estadounidense nº 6.514.531 da a conocer comprimidos de tres capas recubiertas con liberación inmediata/prolongada que comprenden hemitartrato de zolpidem. La patente estadounidense nº 6.087.386 da a conocer un comprimido de tres capas con una capa de enalapril, una capa de losartán potásico y una segunda capa de maleato de enalapril o una capa de excipiente. La patente estadounidense nº 5.213.807 da a conocer un comprimido oral de tres capas con un núcleo que comprende un fármaco antiinflamatorio no esteroideo (AINE), ibuprofeno y sales de ibuprofeno y un revestimiento intermedio que comprende un material sustancialmente impenetrable/impermeable al paso del ibuprofeno. La patente estadounidense nº 6.926.907 da a conocer un comprimido de tres capas que separa la famotidina contenida en una película de revestimiento de un núcleo que comprende naproxeno de liberación controlada usando excipientes que controlan la liberación del fármaco. La película de revestimiento es un revestimiento entérico configurado para demorar la liberación de naproxeno hasta que la forma posológica alcanza un entorno en el que el pH está por encima de cuatro.
Resumen
Una realización proporciona una formulación farmacéutica en capas que comprende dos o más capas farmacéuticas y una capa intermedia dispuesta entre al menos dos de las dos o más capas farmacéuticas. En algunas realizaciones, la capa intermedia está configurada para disolverse in vivo para dejar con ello sustancialmente intactas, pero físicamente separadas, las dos o más capas farmacéuticas, formando esencialmente dos comprimidos diferenciados. En algunas realizaciones, la velocidad de disolución de una de las dos o más capas farmacéuticas separadas es sustancialmente similar a la de un comprimido simple que comprenda la misma composición farmacéutica que la de la capa farmacéutica.
El uso de un primer compuesto y de un segundo compuesto en la preparación de un medicamento para lograr la pérdida de peso, para la supresión del apetito y/o para tratar una afección relacionada con la obesidad, en el que el medicamento comprende formulaciones farmacéuticas de la presente invención en capas.
Breve descripción de los dibujos
Otros aspectos de la revelación serán inmediatamente evidentes a partir de la descripción que sigue y de los dibujos adjuntos, en los que números de referencia semejantes se refieren a partes similares de principio a fin, que están concebidos para ilustrar y no para limitar la revelación, y en los cuales:
La Figura 1A ilustra una realización de una formulación farmacéutica en capas.
Las Figuras 1B y 1C ilustran la formulación farmacéutica en capas de la Figura 1A en etapas progresivas a medida que se disuelve la capa intermedia.
La Figura 2A ilustra una segunda realización de una formulación farmacéutica en capas.
La Figura 2B ilustra la segunda realización de la Figura 2A después de que se disuelva una capa intermedia.
La Figura 3 ilustra una tercera realización de una formulación farmacéutica en capas.
La Figura 4 ilustra una cuarta realización de una formulación farmacéutica en capas.
La Figura 5 ilustra una quinta realización de una formulación farmacéutica en capas con múltiples capas intermedias.
La Figura 6 ilustra una sexta realización de una formulación farmacéutica en capas con capas de forma lenticular.
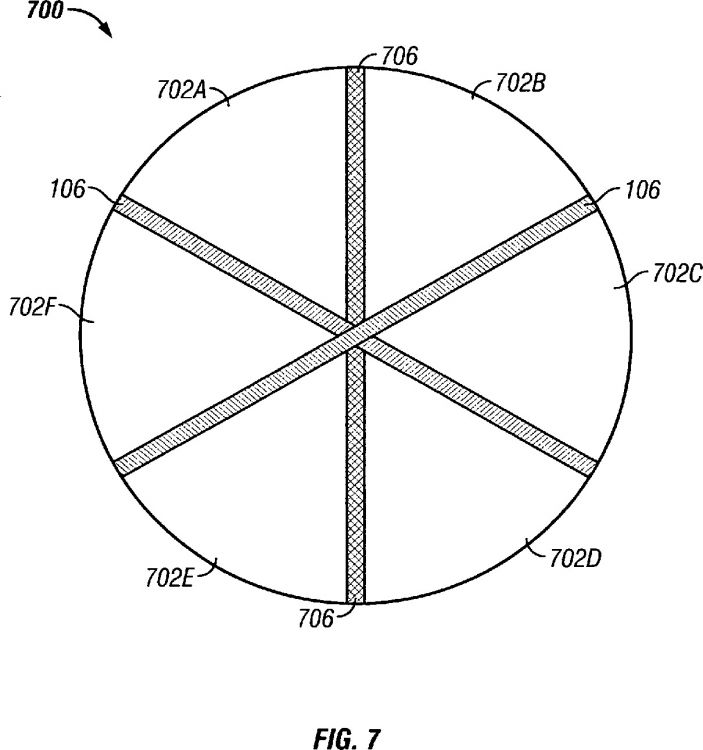
La Figura 7 ilustra una séptima realización de una formulación farmacéutica en capas.
Descripción detallada de la realización preferida
Las realizaciones de la presente revelación proporcionan mejoras significativas a la tecnología de los comprimidos de capas múltiples. En una realización, una formulación farmacéutica en capas comprende dos o más capas farmacéuticas y al menos una capa intermedia dispuesta entre al menos dos de las dos o más capas farmacéuticas. La al menos una capa intermedia está configurada para disolverse in vivo y, con ello, dejar sustancialmente intactas las dos o más capas farmacéuticas. En algunas realizaciones, la velocidad de disolución de una de las dos o más capas farmacéuticas separadas es sustancialmente similar a la de un comprimido simple que comprenda la misma composición farmacéutica que la de la capa farmacéutica. Así, la capa farmacéutica separada tiene un perfil de disolución independiente y previsible.
Un perfil de disolución para un fármaco comprende la velocidad conocida de disolución y características particulares de disolución del fármaco. Un perfil previsible de disolución para un fármaco específico permite un tratamiento más preciso de un síntoma dado. Los perfiles previsibles de disolución para fármacos diferentes dentro de un comprimido de múltiples capas permiten un tratamiento coordinado de múltiples síntomas con una sola formulación farmacéutica.
En general, las formulaciones farmacéuticas de múltiples capas presentan retos para mantener perfiles previsibles de disolución. Por ejemplo, las condiciones in vivo perturban a menudo lo que sería, si no, un perfil previsible de disolución de la formulación farmacéutica de múltiples capas. Un comprimido de múltiples capas puede fabricarse con fármacos con perfiles de disolución conocidos. Sin embargo, una vez que un paciente ingiere un comprimido de múltiples capas, no hay garantía alguna de que cada fármaco se disolverá tal como predice su perfil de disolución individual. La configuración del fármaco dentro de un comprimido, la forma del comprimido, los excipientes y los materiales de carga en el comprimido, los revestimientos del comprimido y las condiciones in vivo pueden todos afectar los perfiles de disolución. Además, la interacción entre diferentes fármacos dentro de un comprimido de múltiples capas puede provocar un cambio en el perfil de disolución para una o más composiciones...
Reivindicaciones:
1. Una formulación farmacéutica en capas para la administración de dos o más ingredientes farmacéuticos activos que comprende:
2. La formulación farmacéutica en capas de la Reivindicación 1 en la que dicha primera capa farmacéutica comprende un perfil de disolución similar a la de un comprimido simple de composición similar y en la que dicha segunda capa farmacéutica comprende un perfil de disolución similar a la de un comprimido simple de composición similar.
3. La formulación farmacéutica en capas de las Reivindicaciones 1 o 2 en la que dicha primera capa farmacéutica comprende una composición farmacéutica diferente de la de dicha segunda capa farmacéutica.
4. La formulación farmacéutica en capas de cualquiera de las Reivindicaciones 1-3 en la que dicha primera capa farmacéutica comprende un ingrediente farmacéutico activo diferente del de dicha segunda capa farmacéutica.
5. La formulación farmacéutica en capas de cualquiera de las Reivindicaciones 1-3 en la que dicha primera capa farmacéutica y dicha segunda capa farmacéutica comprenden el mismo ingrediente farmacéutico activo.
6. La formulación farmacéutica en capas de una cualquiera de las Reivindicaciones 1 a 5 en la que al menos una de dichas capas farmacéuticas primera y segunda comprende bupropiona.
7. La formulación farmacéutica en capas de una cualquiera de las Reivindicaciones 1 a 6 en la que al menos una de dichas capas farmacéuticas primera y segunda comprende zonisamida.
8. La formulación farmacéutica en capas de una cualquiera de las Reivindicaciones 1 a 6 en la que al menos una de dichas capas farmacéuticas primera y segunda comprende naltrexona.
9. La formulación farmacéutica en capas de una cualquiera de las Reivindicaciones 1 a 4 en la que dicha primera capa farmacéutica comprende zonisamida y dicha segunda capa farmacéutica comprende bupropiona.
10. La formulación farmacéutica en capas de una cualquiera de las Reivindicaciones 1 a 4 en la que dicha primera capa farmacéutica comprende naltrexona y dicha segunda capa farmacéutica comprende bupropiona.
11. La formulación farmacéutica en capas de una cualquiera de las Reivindicaciones 1 a 10 en la que al menos una de dichas capas primera y segunda comprende una formulación de liberación sostenida.
12. La formulación farmacéutica en capas de una cualquiera de las Reivindicaciones 1 a 11 en la que dicha capa intermedia de liberación rápida comprende al menos uno de un azúcar monosacárido, un azúcar disacárido o un almidón.
13. La formulación farmacéutica en capas de la Reivindicación 12 en la que dicha capa intermedia de liberación rápida comprende lactosa.
14. Una formulación farmacéutica en capas según una cualquiera de las Reivindicaciones 1-13 para ser usada como medicamento.
15. Una formulación farmacéutica en capas según una cualquiera de las Reivindicaciones 1-13 para ser usada para lograr la pérdida de peso, para la supresión del apetito o para el tratamiento de una afección relacionada con la obesidad.
16. El uso de un primer compuesto y de un segundo compuesto en la preparación de un medicamento para lograr la pérdida de peso, para la supresión del apetito o para el tratamiento de una afección relacionada con la obesidad en el que dicho medicamento comprende las formulaciones farmacéuticas en capas de una cualquier de las Reivindicaciones 1-13.
Patentes similares o relacionadas:
Regímenes de dosificación de buprenorfina, del 1 de Julio de 2020, de Indivior UK Limited: Buprenorfina para su uso en un método para tratar el trastorno por uso de opioides en un ser humano que lo necesite, que comprende las etapas […]
 Forma de dosificación llena de líquido, disuasoria del abuso y de liberación inmediata, del 24 de Junio de 2020, de Pharmaceutical Manufacturing Research Services, Inc: Una cápsula disuasoria del abuso de liberación inmediata, que comprende:
(a) un principio activo susceptible de abuso;
(b) un primer polietilenglicol (PEG) […]
Forma de dosificación llena de líquido, disuasoria del abuso y de liberación inmediata, del 24 de Junio de 2020, de Pharmaceutical Manufacturing Research Services, Inc: Una cápsula disuasoria del abuso de liberación inmediata, que comprende:
(a) un principio activo susceptible de abuso;
(b) un primer polietilenglicol (PEG) […]
Gránulos de dispersión rápida, comprimidos de desintegración oral y métodos, del 3 de Junio de 2020, de Adare Pharmaceuticals, Inc: Microgránulos de dispersión rápida, farmacéuticamente aceptables, que tienen una mediana del tamaño de partícula en el rango de 100 μm a 300 […]
Dispositivos de administración transdérmica resistentes al abuso y composiciones que comprenden un agonista de opioides y un derivado N-óxido no administrado por vía transdérmica de un antagonista de opioide para el tratamiento del dolor, del 22 de Abril de 2020, de EURO-CELTIQUE S.A.: Un dispositivo de administración transdérmica que comprende una composición farmacéutica, en el que dicha composición comprende un derivado […]
Pulverizador de buprenorfina sublingual, del 22 de Abril de 2020, de Fresh Cut Development, LLC: Una formulación de pulverización sublingual que comprende una cantidad efectiva de buprenorfina, o una sal farmacéuticamente aceptable de la misma, […]
Formulación farmacéutica a base de ibuprofeno y codeína que tiene estabilidad mejorada, del 15 de Abril de 2020, de FARMASIERRA MANUFACTURING S.L: Formulación farmacéutica a base de ibuprofeno y codeínade estabilidad mejorada. La invención consiste en una nueva formulación farmacéuticaen forma […]
Parche transdérmico de oximorfona, del 8 de Abril de 2020, de Buzzz Pharmaceuticals Limited: Un parche transdérmico que tiene una capa que contiene el fármaco que comprende oximorfona o una sal farmacéuticamente aceptable de la misma, […]
Composiciones de buprenorfina y antagonistas del receptor de opioides mu, del 1 de Abril de 2020, de Alkermes Pharma Ireland Limited: Una composición que comprende buprenorfina y un antagonista del receptor opioide μ, en donde la composición está caracterizada por un Índice […]