PROCEDIMIENTO PARA DETERMINAR LA PUREZA POLIMORFICA DE LA MINIDIPINA DICLORHIDRATO.
Procedimiento para determinar la pureza polimórfica de la manidipina diclorhidrato.
Se describe un procedimiento para determinar la pureza polimórfica de la manidipina diclorhidrato polimorfo {be} en un comprimido farmacéutico utilizando informaciones obtenidas con espectros Raman, que comprende las siguientes etapas:
i) preparar una serie de muestras conocidas, cada una de las cuales comprende una cantidad de polimorfo {be} y una cantidad de polimorfo {al}, donde en cada una de las muestras conocidas, la cantidad total de los compuestos se mantiene igual, mientras que su proporción varía;
ii) obtener los espectros Raman de las diversas muestras conocidas;
iii) seleccionar una o más señales para cada forma de longitud de onda, de manera que las diferencias en los espectros de cada una de las muestras conocidas sean más apreciables, y de manera que las señales de los excipientes no interfieran;
iv) efectuar un análisis estadístico de los datos de los espectros de las series de lasmuestras conocidas;
v) recoger los datos de los espectros de una muestra que comprenda manidipina diclorhidrato polimorfo {be} con una pureza polimórfica desconocida; y
vi) calcular la pureza polimórfica del polimorfo {be}
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200703284.
Solicitante: CHIESI FARMACEUTICI S.P.A..
Nacionalidad solicitante: Italia.
Dirección: VIA PALERMO 26/A,PARMA.
Inventor/es: PEVERI,TIZIANA, LIPRERI,MILCO, DAGLI ALBERI,MASSIMILIANO.
Fecha de Solicitud: 12 de Diciembre de 2007.
Fecha de Publicación: .
Fecha de Concesión: 12 de Julio de 2010.
Clasificación Internacional de Patentes:
- A61K31/496 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Piperazinas no condensadas conteniendo otros heterociclos, p. ej. rifampicina, tiotixeno.
- A61K9/20 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Píldoras, pastillas o comprimidos.
- C07D401/12 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 401/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, siendo al menos un ciclo de seis miembros con solamente un átomo de nitrógeno. › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
- G01N21/65 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 21/00 Investigación o análisis de los materiales por la utilización de medios ópticos, es decir, utilizando rayos infrarrojos, visibles o ultravioletas (G01N 3/00 - G01N 19/00 tienen prioridad). › Difusión de Raman.
Clasificación PCT:
- A61K31/496 A61K 31/00 […] › Piperazinas no condensadas conteniendo otros heterociclos, p. ej. rifampicina, tiotixeno.
- A61K9/20 A61K 9/00 […] › Píldoras, pastillas o comprimidos.
- C07D401/12 C07D 401/00 […] › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
- G01N21/65 G01N 21/00 […] › Difusión de Raman.
Fragmento de la descripción:
Procedimiento para determinar la pureza polimórfica de la manidipina diclorhidrato.
Campo de la invención
La presente invención, en general, se refiere a un procedimiento para determinar la pureza polimórfica.
Más específicamente, la presente invención se refiere a un procedimiento para determinar la pureza polimórfica de la manidipina diclorhidrato polimorfo ß en una forma farmacéutica con dosificación sólida utilizando informaciones de espectroscopia Raman.
Antecedentes de la invención
La capacidad de hallarse en distintas estructuras cristalinas se conoce como polimorfismo y se sabe que se ha comprobado en muchos compuestos orgánicos. Estas distintas formas cristalinas se conocen como "modificaciones polimórficas" o "polimorfos" y aparecen en su estado cristalino. Si bien las modificaciones polimórficas tienen la misma composición química, difieren en el aspecto, en la disposición geométrica y en otras propiedades descriptivas del estado sólido cristalino.
El polimorfismo es un importante fenómeno a considerar en el desarrollo farmacéutico, ya que distintos polimorfos tienen distintas propiedades físicas en el estado sólido que, a su vez, pueden influir sobre la estabilidad física, las propiedades de disolución y, por tanto, la biodisponibilidad de los fármacos. Por consiguiente, es esencial estimar el polimorfismo para poder seleccionar la forma cristalina de un fármaco más adecuada en relación con su estabilidad y biodisponibilidad.
Además, es bien sabido que durante los procedimientos de preparación tales como la desecación, trituración y compresión de formas de dosificación sólidas, como los comprimidos, pueden observarse transformaciones polimórficas (también conocidas como transiciones), con formación de cantidades significativas de la forma cristalina indesea- ble.
Tales transiciones pueden ser responsables de fenómenos tales como el endurecimiento posterior a la compresión de los comprimidos y, dado que distintos polimorfos pueden también tener distintas solubilidades y distintas velocidades de hidrólisis, pueden influir espectacularmente tanto sobre las propiedades de disolución como sobre la estabilidad química del fármaco.
A la luz de todas estas consideraciones, es muy importante evaluar si la pureza polimórfica de la forma cristalina del fármaco previamente escogida se mantiene en la forma de dosificación sólida final.
La manidipina diclorhidrato {éster 2-[4-(difenilmetil)-1-piperazinil]etil metílico del ácido (
La manidipina existe en dos formas polimórficas conocidas como forma a y forma ß.
Ésta última, cuya preparación se describe en el documento JP 1284729, se utilizada para la fabricación de los comprimidos actualmente en el mercado, dado que la forma a es menos estable.
Con el fin de distinguir las dos formas cristalinas, las técnicas analíticas más ampliamente usadas son la espectroscopia IR, la difractometría de polvos de rayos X (XRD) y la calorimetría diferencial de barrido (DSC).
Sin embargo, dichas técnicas no pueden usarse para la determinación cuantitativa de la pureza polimórfica del polimorfo ß de manidipina diclorhidrato en las formas de dosificación sólidas, dado que sus señales y/o su pico de fusión están cubiertos por los de excipientes generalmente usados para la preparación de los comprimidos.
Por consiguiente, existe la necesidad de un procedimiento para determinar la pureza polimórfica de la manidipina diclorhidrato polimorfo ß en una forma de dosificación oral sólida como un comprimido.
En particular, sería sumamente ventajoso proporcionar un procedimiento rápido, específico y preciso, y un correspondiente aparato para identificar la presencia del polimorfo cristalino a indeseable en una cantidad inferior o igual al 15% en los comprimidos que contienen manidipina diclorhidrato cristalino polimorfo ß.
Breve descripción de la invención
La invención se refiere a un procedimiento para determinar la pureza polimórfica de la manidipina diclorhidrato polimorfo ß en un comprimido farmacéutico utilizando informaciones de espectros Raman, que comprende las siguientes etapas:
i) preparar una serie de muestras conocidas, cada una de las cuales comprende una cantidad de polimorfo ß y una cantidad de polimorfo a, donde, en cada una de las muestras conocidas, la cantidad total de los compuestos se mantiene igual, mientras que su proporción varía;
ii) registrar los espectros Raman de las diversas muestras conocidas;
iii) seleccionar una o más señales para cada forma de longitud de onda, de manera que las diferencias en los espectros generadas en cada una de las muestras conocidas sean más apreciables y que las señales de los excipientes no interfieran;
iv) efectuar un análisis de regresión parcial de mínimos cuadrados de los datos de los espectros de las series de las muestras conocidas;
v) recoger los datos de los espectros de una muestra que comprenda manidipina diclorhidrato polimorfo ß con una pureza polimórfica desconocida; y
vi) calcular la pureza polimórfica del polimorfo ß.
La invención también se refiere a un procedimiento para la fabricación de comprimidos farmacéuticos que comprenden manidipina diclorhidrato polimorfo ß como ingrediente activo con una pureza polimórfica igual o superior al 85%, sobre la base de la cantidad total del ingrediente activo, en el que dicho procedimiento comprende las etapas de:
La invención se refiere también a comprimidos farmacéuticos que comprenden manidipina diclorhidrato polimorfo ß como ingrediente activo con una pureza polimórfica igual o superior al 85%, sobre la base de la cantidad total del ingrediente activo, donde la pureza polimórfica del ingrediente activo se ha determinado con el procedimiento descrito aquí anteriormente.
Breve descripción de las figuras
La figura 1 muestra el típico espectro Raman de la manidipina diclorhidrato forma ß como material de partida.
La figura 2 muestra el típico espectro Raman de la manidipina diclorhidrato forma a como material de partida.
La figura 3 muestra el espectro Raman de un comprimido que comprende 10 mg de manidipina diclorhidrato forma ß como ingrediente activo y los siguientes excipientes: lactosa 200 mesh, almidón, Klucel LF, L-HPC-LH 11, riboflavina y estearato de magnesio (comprimidos Iperten®).
La figura 4 muestra el espectro Raman de un comprimido que comprende 10 mg de manidipina diclorhidrato forma a como ingrediente activo y los siguientes excipientes: lactosa 200 mesh, almidón, Klucel LF, L-HPC-LH 11, riboflavina estearato de magnesio.
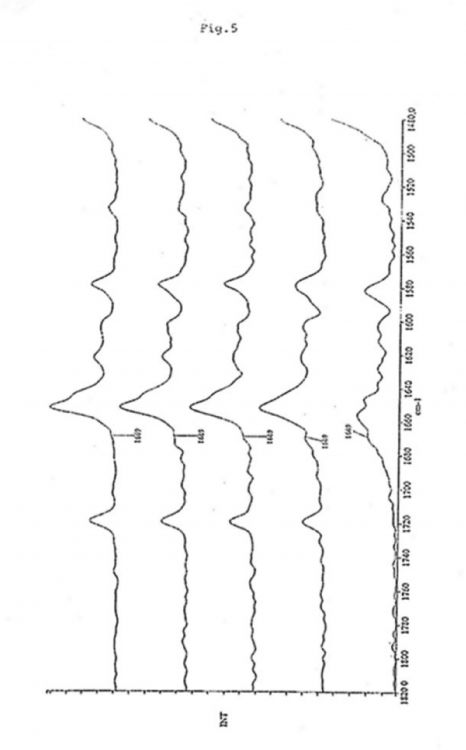
La figura 5 muestra los espectros Raman obtenidos en la región espectral de 1800-1400 cm-1 para una serie de muestras en forma de comprimidos que comprenden cantidades fijas de manidipina diclorhidrato forma ß y forma a en distintas proporciones, y los siguientes excipientes: lactosa 200 mesh, almidón, Klucel LF, L-HPC-LH 11, riboflavina y estearato de magnesio.
Descripción detallada de la invención
La presente invención se refiere a un procedimiento para determinar la pureza polimórfica en un comprimido farmacéutico que comprende manidipina diclorhidrato polimorfo, cuya pureza polimórfica se desconoce.
El procedimiento utiliza informaciones...
Reivindicaciones:
1. Un procedimiento para determinar la pureza polimórfica de la manidipina diclorhidrato polimorfo ß en un comprimido farmacéutico utilizando informaciones des espectros Raman, caracterizado porque comprende las siguientes etapas:
2. El procedimiento según la reivindicación 1, caracterizado porque la muestra que comprende la manidipina diclorhidrato polimorfo ß con una pureza polimórfica desconocida está en forma de comprimido.
3. El procedimiento según la reivindicación 1, caracterizado porque el comprimido comprende manidipina diclorhidrato polimorfo ß en una cantidad de dosificación entre 5 y 40 mg.
4. El procedimiento según la reivindicación 3, caracterizado porque el comprimido comprende manidipina diclorhidrato polimorfo ß en una cantidad de dosificación de 10 mg.
5. El procedimiento según la reivindicación 3, caracterizado porque el comprimido comprende manidipina diclorhidrato polimorfo ß en una cantidad de dosificación de 20 mg.
6. El procedimiento según una cualquiera de las reivindicaciones 3 a 5, caracterizado porque el comprimido comprende uno o más excipientes convencionales farmacéuticamente aceptables, tales como lactosa, almidón y estearato de magnesio.
7. El procedimiento según la reivindicación 6, caracterizado porque el comprimido comprende los siguientes excipientes: lactosa 200 mesh, almidón, Klucel LF, L-HPC-LH 11, riboflavina y estearato de magnesio.
8. El procedimiento según la reivindicación 7, caracterizado porque los excipientes están en proporción de peso de 74, 6: 10, 7: 3, 5: 10,7: 0,02: 0,48, respectivamente.
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Métodos y composiciones para la administración oral de proteínas, del 22 de Julio de 2020, de Entera Bio Ltd: Una única composición farmacéutica oral que comprende una proteína que tiene un peso molecular de hasta 100.000 Daltons, siendo dicha proteína PTH; […]
Formulación de vitamina D de liberación modificada estabilizada y método de administración de la misma, del 22 de Julio de 2020, de EirGen Pharma Ltd: Una formulacion oral de liberacion controlada de un compuesto de vitamina D que comprende uno o ambos de 25- hidroxivitamina D2 y 25-hidroxivitamina D3, la formulacion […]
Composición farmacéutica que comprende un agente antipsicótico atípico y método para su preparación, del 15 de Julio de 2020, de PHARMATHEN S.A.: Comprimido de liberación controlada de Paliperidona en forma de comprimido de varias capas que comprende: a) un núcleo de matriz que comprende […]
Composiciones y métodos para tratar el virus de la hepatitis C, del 15 de Julio de 2020, de Gilead Pharmasset LLC: Una composición farmacéutica que comprende: a) de aproximadamente el 25% a aproximadamente el 35% p/p de GS-7977 cristalino que tiene la estructura **(Ver […]
Macrogols para aplicación a la mucosa, y sus usos terapéuticos, del 15 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Composición farmacéutica en forma sólida que comprende, por unidad de dosificación, entre 5 y 400 mg de un PEG con un grado de 3000 o más, para uso en el tratamiento […]
Granulados secos de polvos de sílice mesoporosa, del 1 de Julio de 2020, de FORMAC PHARMACEUTICALS N.V: Un granulado seco que comprende desde el 50% al 100% p/p de sílice mesoporosa ordenada que tiene una organización bidimensional hexagonalmente […]
Composición farmacéutica novedosa, del 1 de Julio de 2020, de NOVARTIS AG: Un comprimido farmaceutico que comprende: a) un farmaco que es el solvato con sulfoxido de dimetilo de N-{3-[3-ciclopropil-5-(2-fluoro-4-5 yodofenilamino)-6,8- dimetil-2,4,7-trioxo-3,4,6,7-tetrahidro-2H-pirido[4,3-d]pirimidin-1-il]fenil}acetamida […]