DERIVADOS DE DIAZEPAN-ACETAMIDA COMO INHIBIDORES SELECTIVOS DE 11-HSD1.
Compuesto de la fórmula I
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/008664.
Solicitante: MERK PATENT GMBH.
Nacionalidad solicitante: Alemania.
Dirección: FRANKFURTER STRASSE 250,64293 DARMSTADT.
Inventor/es: DOARE, LILIANE, ROCHE, DIDIER, CARNIATO, DENIS, LERICHE,CAROLINE, CHARON,CHRISTINE.
Fecha de Publicación: .
Fecha Concesión Europea: 12 de Mayo de 2010.
Clasificación Internacional de Patentes:
- C07D243/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 243/00 Compuestos heterocíclicos que contienen ciclos de siete miembros que tienen dos átomos de nitrógeno como únicos heteroátomos del ciclo. › no condensados con otros ciclos.
Clasificación PCT:
- A61K31/551 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo dos átomos de nitrógeno como heteroátomos de un ciclo, p. ej. clozapina, dilazep.
- A61P3/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00).
- C07D243/08 C07D 243/00 […] › no condensados con otros ciclos.
Fragmento de la descripción:
Derivados de diazepan-acetamida como inhibidores selectivos de 11-HSD1.
Campo de la invención
La presente invención se refiere a derivados de diazepanoacetamida como inhibidores selectivos de la enzima 11-beta-hidroxiesteroide deshidrogenasa de tipo 1 (11ß-HSD-1) y el uso de dichos compuestos para el tratamiento y prevención del síndrome metabólico, diabetes, resistencia a la insulina, obesidad, trastornos lipídicos, glaucoma, osteoporosis, trastornos cognitivos, ansiedad, depresión, trastornos inmunitarios, hipertensión y otras enfermedades y afecciones.
Antecedentes de la invención
Las hidroxiesteroide deshidrogenasas (HSD) regulan la ocupación y activación de los receptores de hormonas esteroideas convirtiendo a las hormonas esteroides en sus metabolitos inactivos. Para una revisión reciente, véase Nobel y col., Eur. J. Biochem. 2001, 268: 4113-4125.
Se conocen muchas clases de HSD. Las 11-beta-hidroxiesteroide deshidrogenasas (11ß-HSD) catalizan la interconversión de glucocorticoides activos (como cortisol y corticosterona) y sus formas inertes (como cortisona y 11-deshidrocorticosterona). La isoforma 11-beta-hidroxiesteroide deshidrogenasa de tipo 1 (11ß-HSD1) se expresa ampliamente en hígado, tejido adiposo, cerebro, pulmón y otros tejidos glucocorticoides, mientras que la expresión de la isoforma 2 (11ß-HSD2) se limita a tejidos que expresan el receptor mineralocorticoide, como riñón, intestino y placenta. Por tanto, la inhibición de la 11ß-HSD2 se asocia con efectos adversos graves, como hipertensión.
El exceso de cortisol se asocia con numerosos trastornos, como diabetes, obesidad, dislipidemia, resistencia a insulina e hipertensión. La administración de inhibidores de la 11ß-HSD1 disminuye el nivel de cortisol y otros 11ß-hidroxiesteroides en los tejidos diana, reduciendo de este modo los efectos de cantidades excesivas de cortisol y de otros 11ß-hidroxiesteroides. De este modo, 11ß-HSD1 es una posible diana para el tratamiento asociado con diversos trastornos que pueden mejorar reduciendo la acción glucocorticoide. Por tanto, la inhibición de 11ß-HSD1 puede usarse para prevenir, tratar o controlar enfermedades mediadas por niveles anormalmente altos de cortisol y otros 11ß-hidroesteroides, como diabetes, obesidad, hipertensión o dislipidemia. La inhibición de la actividad 11ß-HSD1 en el cerebro, por ejemplo, la reducción de los niveles de cortisol, también puede ser útil para tratar o reducir la ansiedad, la depresión, el deterioro cognitivo o la disfunción cognitiva relacionada con la edad (Seckl, y col., Endocrinology, 2001, 142: 1371-1376).
El cortisol es una hormona antiinflamatoria importante y muy conocida que también actúa como antagonista a la acción de la insulina en el hígado, con lo que se reduce la sensibilidad a la insulina, dando lugar a un aumento de la gluconeogénesis y a niveles elevados de glucosa en el hígado. Los pacientes que ya presentan intolerancia a la glucosa tienen mayor probabilidad de desarrollar diabetes de tipo 2 en presencia de niveles anormalmente altos de cortisol (Long y col., J. Exp. Med. 1936, 63: 465-490; Houssay, Endocrinology 1942, 30: 884-892). Además, se ha demostrado suficientemente que 11ß-HSD1 tiene una función importante en la regulación del efecto glucocorticoide local y de producción de glucosa en el hígado (Jamieson y col., J. Endocrinol. 2000, 165: 685-692). En la publicación de Walker y col., J. Clin. Endocrinol. Metab. 1995, 80: 3155-3159, se describió que la administración de carbenoxolona, un inhibidor inespecífico de la 11ß-HSD1, daba lugar a la mejora de la sensibilidad hepática a la insulina en humanos.
Adicionalmente, el hipotético mecanismo de acción de la 11ß-HSD1 en el tratamiento de la diabetes ha sido apoyado por diversos experimentos realizados en ratones y ratas. Estos estudios mostraron que los niveles de ARNm y las actividades de dos enzimas clave en la producción hepática de glucosa, la fosfoenolpiruvato carboxicinasa (PEPCK) y la glucosa-6-fosfatasa (G6Pasa), se reducían tras la administración de inhibidores de la 11ß-HSD1. Además, se demostró que los niveles de glucemia y la producción hepática de glucosa se reducían en ratones que no expresan 11ß-HSD1. Datos adicionales recopilados usando este modelo de ratones que no expresan el gen correspondiente también confirmaron que la inhibición de 11ß-HSD1 no causará hipoglucemia, ya que los niveles basales de PEPCK y G6Pasa se regulaban independientemente de los glucocorticoides (Kotelevtsev y col., Proc. Natl. Acad. Sci. USA 1997, 94: 14924-14929).
Por tanto, la administración de una cantidad terapéuticamente eficaz de un inhibidor de la 11ß-HSD1 es eficaz para el tratamiento, control y mejora de los síntomas de la diabetes, especialmente diabetes no dependiente de insulina (DMNDI, diabetes mellitus de tipo 2) y la administración regular de una cantidad terapéuticamente eficaz de un inhibidor de la 11ß-HSD1 retrasa o previene la aparición de diabetes, especialmente en humanos.
El efecto de niveles elevados de cortisol también se ha observado en pacientes que presentaban síndrome de Cushing, que es una enfermedad metabólica caracterizada por niveles elevados de cortisol en el torrente sanguíneo. Los pacientes con síndrome de Cushing desarrollan a menudo DMNDI.
Niveles excesivos de cortisol se han asociado con la obesidad, quizás debido a un aumento de la gluconeogénesis hepática. La obesidad abdominal se asocia estrechamente con la intolerancia a la glucosa, diabetes, hiperinsulinemia, hipertrigliceridemia y otros factores del síndrome metabólico, como hipertensión arterial, VLDL elevadas y HDL reducidas (Montague y col., Diabetes, 2000, 49: 883-888). También se ha publicado que la inhibición de la 11ß-HSD1 en preadipocitos (células estromales) daba lugar a una disminución de su velocidad de diferenciación en adipocitos. Se prevé que esto tenga como resultado la disminución de la expansión (posiblemente reducción) de los depósitos de grasa epiploica, lo que puede inducir una reducción de la obesidad central (Bujalska, y col., Lancet 1997, 349: 1210-1213).
Por tanto, la administración de una cantidad eficaz de un inhibidor de la 11ß-HSD1 es útil para el tratamiento o control de la obesidad. El tratamiento prolongado con un inhibidor de la 11ß-HSD1 también es útil para el retraso o prevención de la aparición de obesidad, especialmente si el paciente utiliza un inhibidor de 11ß-HSD1 en combinación con dieta controlada y ejercicio.
Reduciendo la resistencia a la insulina y manteniendo la glucemia a concentraciones normales, los compuestos de la presente invención también son útiles para el tratamiento y prevención de las afecciones que acompañan a la diabetes de tipo 2 y de la resistencia a la insulina, como el síndrome metabólico, obesidad, hipoglucemia reactiva y dislipidemia diabética.
Se prevé que la inhibición de la 11ß-HSD1 en adipocitos maduros atenué la secreción del inhibidor del activador del plasminógeno 1 (PAI-1, por sus siglas en inglés), que es un factor de riesgo cardiovascular independiente, como se recoge en Halleux y col., J. Clin. Endocrinol. Metab. 1999, 84: 4097-4105. Además, se ha encontrado que existe una correlación entre la actividad glucocorticoide y determinados factores de riesgo cardiovascular. Esto sugiere que una reducción de los efectos glucocorticoides podría ser beneficiosa para el tratamiento o prevención de determinadas enfermedades cardiovasculares (Walker y col., Hypertension 1998, 31: 891-895 y Fraser y col., Hypertension 1999, 33: 1364-1368).
Puesto que la hipertensión y la dislipidemia contribuyen al desarrollo de la aterosclerosis, y la inhibición de la actividad 11ß-HSD1 y la reducción de la cantidad de cortisol son beneficiosas para el tratamiento o control de la hipertensión, la administración de una cantidad terapéuticamente eficaz de un inhibidor de la 11ß-HSD1 de la presente invención también puede ser especialmente beneficioso para tratar, controlar, retrasar o prevenir la aparición de la aterosclerosis.
La enzima 11ß-HSD1 también ha sido implicada en el proceso de control del apetito y, por tanto, se considera que tiene una función adicional en los trastornos relacionados con el peso. Es sabido que la adrenalectomía atenúa el efecto del ayuno tanto sobre el aumento de la ingesta de alimento como sobre la expresión del neuropéptido Y hipotalámico. Esto sugiere que los glucocorticoides actúan estimulando la ingesta de alimentos y que la inhibición de la 11ß-HSD1 en el cerebro puede aumentar la sensación de saciedad dando lugar, por tanto,...
Reivindicaciones:
1. Compuesto de la fórmula I
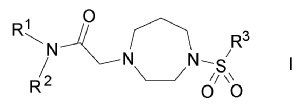
donde
R1 y R2 son independientemente entre sí alquilos, seleccionados entre el grupo compuesto por metilo, etilo, propilo, isopropilo, butilo, sec- y tert-butilo, pentilo, hexilo, heptilo, octilo y nonilo, o cicloalquilo C3-10, y combinaciones de alquilo como se define anteriormente con cicloalquilo C3-10, donde el grupo cicloalquilo esta opcionalmente sustituido por un grupo seleccionado entre alquilo según se definió anteriormente o hidroxilo, o R1, R2 y el nitrógeno al que se unen forman un anillo mono o bicíclico saturado que contiene 6-10 átomos, conteniendo opcionalmente un heteroátomo adicional seleccionado entre N, S u O y opcionalmente sustituido por un grupo seleccionado entre Hal, a partir de alquilo, según se definió anteriormente, hidroxilo, =O (oxígeno carbonílico), arilo o heteroarilo, seleccionado entre el grupo compuesto por pirrolilo, isoxazolilo, isotiazolilo, pirazolilo, piridilo, oxazolilo, oxadiazolilo, tiadiazolilo, tiazolilo, imidazolilo, triazolilo, tetrazolilo, furanilo, triazinilo, tienilo, pirimidilo, benzisoxazolilo, benzoxazolilo, benzotiazolilo, benzotiadiazolilo, dihidrobenzofuranilo, indolinilo, piridazinilo, indazolilo, isoxazolilo, isoindolilo, dihidrobenzotienilo, indolizinilo, cinnolinilo, ftalazinilo, quinazolinilo, naftiridinilo, carbazolilo, benzdioxinilo, benzodioxolilo, quinoxalinilo, purinilo, furazanilo, tiofenilo, isobenzilfuranilo, benzimidazolilo, benzofuranilo, benzotienilo, quinolilo, indolilo, isoquinolilo, dibenzofuranilo,
R4 y R5 son independientemente entre sí alquilo C1-4 o cicloalquilo C4-8,
y las sales, derivados y solvatos de los mismos fisiológicamente aceptables, incluyendo mezclas de los mismos en todas las proporciones.
2. Compuestos según la reivindicación 1, en los que
R1, R2 y el nitrógeno al cual se unen forman decahidroquinolina, opcionalmente sustituida por un grupo seleccionado entre Hal, alquilo, hidroxilo, =O (oxígeno carbonílico),
y las sales, derivados y solvatos de los mismos fisiológicamente aceptables, incluyendo mezclas de los mismos en todas las proporciones.
3. Compuestos según la reivindicación 1, en los que
R1, R2 y el nitrógeno al cual se unen forman piperidina, opcionalmente sustituida por un grupo seleccionado entre alquilo, arilo, heteroarilo, hidroxilo,
y las sales, derivados y solvatos de los mismos fisiológicamente aceptables, incluyendo mezclas de los mismos en todas las proporciones.
4. Compuestos según una de las reivindicaciones 1 a 3, en los que
y las sales, derivados y solvatos de los mismos fisiológicamente aceptables, incluyendo mezclas de los mismos en todas las proporciones.
5. Compuestos según la fórmula I, en los que
las sales, derivados y solvatos de los mismos fisiológicamente aceptables, incluyendo mezclas de los mismos en todas las proporciones.
6. Compuestos según la fórmula I, en los que
y las sales, derivados y solvatos de los mismos fisiológicamente aceptables, incluyendo mezclas de los mismos en todas las proporciones.
7. Compuesto seleccionado entre el grupo compuesto por:
y las sales, derivados y solvatos de los mismos fisiológicamente aceptables, incluyendo mezclas de los mismos en todas las proporciones.
8. Método para la preparación de un compuesto según una de las reivindicaciones 1 a 7, caracterizado porque
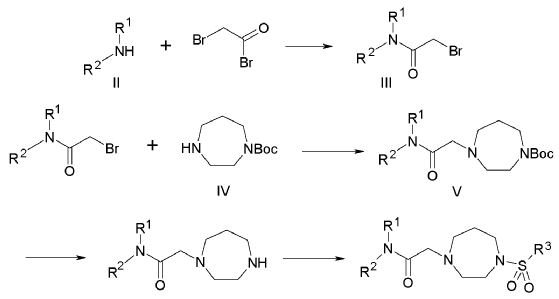
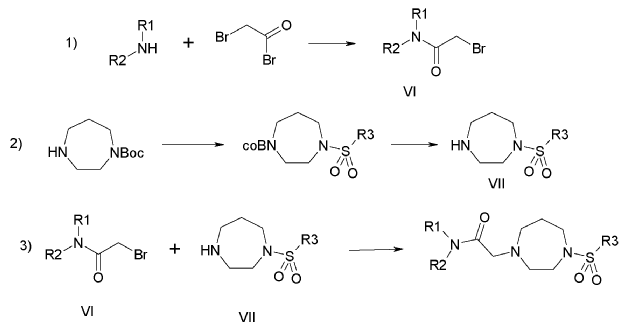
9. Uso de un compuesto según una de las reivindicaciones 1 a 7 para la preparación de un medicamento.
10. Uso de un compuesto según una de las reivindicaciones 1 a 7 para la preparación de un medicamento para el tratamiento y/o prevención de enfermedades que estén causadas, mediadas y/o se propaguen por niveles altos de cortisol.
11. Uso de un compuesto según una de las reivindicaciones 1 a 7 para la preparación de un medicamento para el tratamiento y/o prevención de una o más enfermedades o afecciones seleccionadas entre el grupo compuesto por síndrome metabólico, diabetes, especialmente diabetes mellitus no dependiente de insulina, prediabetes, resistencia a la insulina, baja tolerancia a la glucosa, hiperglucemia, obesidad y trastornos relacionados con el peso, trastornos lipídicos como dislipidemia, hiperlipidemia, hipertrigliceridemia, hipercolesterolemia, niveles bajos de HDL o niveles altos de LDL, glaucoma, osteoporosis, efectos mediados por glucocorticoides sobre la función neuronal, como deterioro cognitivo, ansiedad o depresión, enfermedad neurodegenerativa, trastornos inmunitarios como tuberculosis, lepra o psoriasis, hipertensión, aterosclerosis y sus secuelas, reestenosis vascular, enfermedades cardiovasculares, pancreatitis, retinopatía, neuropatía y nefropatía.
12. Composición farmacéutica, caracterizada porque contiene una cantidad terapéuticamente eficaz de uno o más compuestos según una de las reivindicaciones 1 a 7 que tiene como resultado la mejora del tratamiento, curación, prevención o mejoría de una enfermedad, trastorno o efecto adverso, una disminución de la velocidad de progresión de una enfermedad o trastorno, o eficaz para potenciar una función fisiológica normal.
13. Composición farmacéutica según la reivindicación 13, caracterizada porque contiene uno o más compuestos adicionales, seleccionados entre el grupo compuesto por excipientes, auxiliares, adyuvantes, diluyentes, vehículos fisiológicamente aceptables y principios activos farmacéuticamente aceptables distintos a los compuestos según una de las reivindicaciones 1 a 7.
14. Conjunto (kit) compuesto por envases separados de
15. Proceso para la fabricación de una composición farmacéutica, caracterizado porque uno o más compuestos según una de las reivindicaciones 1 a 7 y uno o más compuestos seleccionados entre el grupo compuesto por excipientes, auxiliares, adyuvantes, diluyentes, vehículos y principios farmacéuticamente activos sólidos, líquidos o semilíquidos distintos a los compuestos según las reivindicaciones 1 a 7, se convierten en una forma de dosificación adecuada.
Patentes similares o relacionadas:
Azina orbital-fumarato, hidrato, forma cristalina y método de preparación de los mismos, del 3 de Junio de 2020, de SHENZHEN ZHENXING MEDICAL TECHNOLOGY CO., LTD: Una forma cristalina de un azina orbital-hidrato de fumarato, en donde, el azina orbital-hidrato de fumarato tiene una estructura como se muestra […]
Compuestos heterocíclicos y métodos para su uso, del 25 de Marzo de 2020, de NOVARTIS AG: Un compuesto de formula (I): **(Ver fórmula)** donde X es -CHR4-, -CH2CHR4- o -C(=O)-; R1 es -C(=O)CH(fenil)(fenilo), -C(=O)CH(fenil)(ciclohexilo), […]
Compuestos terapéuticamente activos para su uso en el tratamiento de cáncer caracterizados por tener una mutación de IDH, del 2 de Agosto de 2017, de Agios Pharmaceuticals, Inc: Uso de un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo: **Fórmula** en la que: W, X, Y y Z se seleccionan cada uno independientemente de CH […]
Derivados de quinolina-8-sulfonamida que tienen una actividad anticancerosa, del 19 de Abril de 2017, de Agios Pharmaceuticals, Inc: Un compuesto de fórmula (II) o una sal farmacéuticamente aceptable del mismo, en donde:**Fórmula** W, X, Y y Z se seleccionan cada uno independientemente entre CH […]
Derivados de diamina como inhibidores de leucotrieno A4 hidrolasa, del 21 de Diciembre de 2016, de Celtaxsys, Inc: Un compuesto que tiene la fórmula (I-1) siguiente:**Fórmula** en la que: R es el grupo**Fórmula** en el que r es 0 a 4, R1a, R1b, […]
Amidas como inhibidores de 11-ß-hidroxiesteroide deshidrogenasa, del 16 de Noviembre de 2016, de JANSSEN PHARMACEUTICA NV: Un compuesto que tiene la fórmula**Fórmula** una sal por adición farmacéuticamente aceptable o una forma estereoquímicamente isómera del mismo, en donde n representa un número […]
Ligandos de unión de opsinas, composiciones y métodos de uso, del 10 de Agosto de 2016, de Bikam Pharmaceuticals, Inc: Un compuesto con la estructura de la Fórmula I A-B-Q-V**Fórmula** donde A es:**Fórmula** B es -CH≥CH-, -CH2-N(R22)- or -CH2-CH2-, […]
Compuesto de guanidina, del 27 de Abril de 2016, de ASTELLAS PHARMA INC.: Un compuesto representado por la fórmula (I) o una sal del mismo:**Fórmula** donde A es**Fórmula** Q1 es N, Q2 es CRQ22, Q4 es CRQ42, Q5 es N, RQ22 y RQ42 son H, […]