ANTICUERPOS HUMANIZADOS QUE RECONOCEN EL PEPTIDO BETA AMILOIDE.
Una inmunoglobulina humanizada para uso en terapia, que comprende una región de cadena pesada variable como se expone en los restos 1-119 de la SEC ID Nº:
12 y una región de cadena ligera variable como se expone en los restos 1-112 de la SEC ID Nº: 11, comprendiendo la inmunoglobulina una región Fc que comprende una modificación de aminoácidos en el resto de aminoácido 234, 235, 236 ó 237, con respecto a la IgG1 3D6 humanizada, de tal forma que la modificación reduce la unión a un receptor FcγRI
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/007503.
Solicitante: JANSSEN ALZHEIMER IMMUNOTHERAPY
WYETH LLC.
Nacionalidad solicitante: Irlanda.
Dirección: LITTLE ISLAND INDUSTRIAL ESTATE LITTLE ISLAND, COUNTY CORK IRLANDA.
Inventor/es: BASI,GURIQ, SALDANHA,JOSE W.
Fecha de Publicación: .
Fecha Solicitud PCT: 12 de Marzo de 2004.
Fecha Concesión Europea: 1 de Septiembre de 2010.
Clasificación Internacional de Patentes:
- C07K16/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
Clasificación PCT:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61K39/40 A61K 39/00 […] › bacterianos.
- A61K39/42 A61K 39/00 […] › virales.
- A61P25/28 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
- C07K16/00 C07K […] › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
- C07K16/18 C07K 16/00 […] › contra materiales animales o humanos.
- C07K16/46 C07K 16/00 […] › Inmoglobulinas híbridas (híbridos de una inmunoglobulina con un péptido distinto de una inmunoglobulina C07K 19/00).
- C12N15/13 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Inmunoglobulinas.
- C12N15/85 C12N 15/00 […] › para células animales.
- C12N5/10 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células modificadas por introducción de material genético extraño, p. ej. células transformadas por virus.
Clasificación antigua:
- A61K39/395 A61K 39/00 […] › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61K39/40 A61K 39/00 […] › bacterianos.
- A61K39/42 A61K 39/00 […] › virales.
- C07K16/00 C07K […] › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
Antecedentes de la Invención
La enfermedad de Alzheimer (AD) es una enfermedad progresiva que produce demencia senil. Véase, en general, Selkoe, TINS 16: 403 (1993); Hardy y col., documento WO 92/13069; Selkoe, J. Neuropathol. Exp. Neurol. 53: 438 (1994); Duff y col., Nature 373: 476 (1995); Games y col., Nature 373:523 (1995). En términos generales, la enfermedad se divide en dos categorías: de inicio tardío, que aparece a edad avanzada (más de 65 años), y de inicio temprano, que se desarrolla antes del período senil, es decir, entre los 35 y los 60 años. En los dos tipos de enfermedad la patología es igual, pero las anomalías tienen a ser más severas y generalizadas en casos que empiezan a una edad más temprana. La enfermedad se caracteriza por al menos dos tipos de lesiones en el cerebro, ovillos neurofibrilares y placas seniles. Los ovillos neurofibrilares son depósitos intracelulares de proteína tau asociada a microtúbulos que consisten en dos filamentos retorcidos más o menos entre sí en parejas. Las placas seniles (es decir, placas de amiloide) son áreas de neurópilo desorganizado de hasta 150 µm de anchura con depósitos amiloides extracelulares en el centro que son visibles por análisis microscópico de secciones de tejido cerebral. La acumulación de placas de amiloide dentro del cerebro también está asociada con el síndrome de Down y otros trastornos cognitivos.
El constituyente principal de las placas es un péptido denominado péptido Aβ o βamiloide. El péptido Aβ es un fragmento interno de 4 kDa de 39-43 aminoácidos de una glicoproteína transmembrana de mayor tamaño denominada proteína precursora de amiloide (APP). Como resultado del procesamiento proteolítico de la APP por diferentes enzimas secretasas, el Aβ se encuentra principalmente tanto en una forma corta, de 40 aminoácidos de longitud, como en una forma larga, que varía de 42-43 aminoácidos de longitud. Parte del dominio transmembrana hidrófobo de la APP se encuentra en el extremo carboxi de Aβ y puede justificar la capacidad de Aβ de agregarse en placas, particularmente en el caso de la forma larga. La acumulación de placas de amiloide en el cerebro finalmente conduce a la muerte de células neuronales. Los síntomas físicos asociados con este tipo de deterioro neural caracterizan la enfermedad de Alzheimer.
Varias mutaciones dentro de la proteína APP se han correlacionado con la presencia de enfermedad de Alzheimer. Véase, por ejemplo, Goate y col., Nature 349: 704) (1991) (valina717 a isoleucina); Chartier Harlan y col. Nature 353: 844 (1991)) (valina717 a glicina); Murrell y col., Science 254: 97 (1991) (valina717 a fenilalanina); Mullan y col., Nature Genet. 1: 345 (1992) (una doble mutación que cambia lisina595-metionina596 por asparagina595-leucina596). Se cree que estas mutaciones producen la enfermedad de Alzheimer por un aumento o alteración del procesamiento de APP para dar Aβ, particularmente el procesamiento de APP para dar mayores cantidades de la forma larga de Aβ (es decir, Aβ1-42 y Aβ1-43). Se cree que mutaciones en otros genes, tales como los genes de presenilina, PS1 y PS2, afectan indirectamente al procesamiento de APP para generar mayores cantidades de forma larga de Aβ (véase Hardy, TINS 20: 154 (1997)).
Se han usado modelos de ratón satisfactoriamente para determinar el significado de placas de amiloide en la enfermedad de Alzheimer (Games y col., supra, Johnson-Wood y col., Proc. Natl. Acad. Sci. USA 94: 1550 (1997)). En particular, cuando en ratones transgénicos PDAPP (que expresan una forma mutante de APP humana y desarrollan enfermedad de Alzheimer a una edad joven) se inyecta la forma larga de Aβ, presentan tanto una reducción en la progresión de la enfermedad de Alzheimer como un aumento en los títulos de anticuerpo contra el péptido Aβ (Schenk y col., Nature 400, 173 (1999)). Las observaciones analizadas anteriormente indican que Aβ, particularmente en su forma larga, es un elemento causante de la enfermedad de Alzheimer.
McMichael, documento EP 526.511, propone la administración de dosificaciones homeopáticas (menores o iguales a 10-2 mg/día) de Aβ a pacientes con AD preestablecida. En un ser humano típico con aproximadamente 5 litros de plasma, sería de esperar que incluso el límite superior de esta dosificación generara una concentración no mayor de 2 pg/ml. La concentración normal de Aβ en plasma humano típicamente está en el intervalo de 50-200 pg/ml (Seubert y col., Nature 359: 325 (1992)). Como la dosificación propuesta en el documento EP 526.511 apenas alteraría el nivel de Aβ circulante endógeno y como el documento EP 526.511 no recomienda el uso de un adyuvante como inmunoestimulante, parece inverosímil que se obtuviera algún efecto terapéutico beneficioso.
El documento WO 02/46237 proporciona agentes y procedimientos mejorados para enfermedades asociadas con depósitos amiloides de beta amiloide en el cerebro de un paciente. Los agentes preferidos incluyen ciertas variantes humanizadas y quiméricas del anticuerpo anti-beta amiloide 3D6 que comprende una región Fc de IgG1 humana de tipo silvestre.
Sin embargo, existe la necesidad de nuevas terapias y reactivos para el tratamiento de la enfermedad de Alzheimer, en particular, de terapias y reactivos capaces de realizar un efecto terapéutico beneficioso a dosis fisiológicas (por ejemplo, no tóxicas). Sumario de la Invención
La presente invención se ocupa de nuevos reactivos de anticuerpos terapéuticos como se menciona en las reivindicaciones para la prevención y tratamiento de enfermedades amiloidogénicas (por ejemplo, la enfermedad de Alzheimer). Se describe la identificación y caracterización de un anticuerpo monoclonal que se une específicamente al péptido Aβ y es eficaz para reducir la carga de placas y/o reducir la distrofia neurítica asociada con trastornos amiloidogénicos. El análisis estructural y funcional de este anticuerpo conduce al diseño de diversos anticuerpos humanizados para uso profiláctico y/o terapéutico. En particular, se describe la humanización de las regiones variables de estos anticuerpos y cadenas de inmunoglobulina o anticuerpo humanizadas, inmunoglobulinas o anticuerpos humanizados y fragmentos funcionales de inmunoglobulina o anticuerpo, en particular, fragmentos de unión a antígeno de los anticuerpos presentados.
Se desvela el uso de los anticuerpos en el tratamiento de enfermedades o trastornos amiloidogénicos (por ejemplo, enfermedad de Alzheimer), así como composiciones farmacéuticas y kits para uso en estas aplicaciones.
También se ocupa de procedimientos para identificar restos dentro de los anticuerpos monoclonales presentados que son importantes para una función inmunológica apropiada y para identificar restos que son susceptibles de sustitución en el diseño de anticuerpos humanizados que tienen mejores afinidades de unión y/o menor inmunogenicidad, cuando se usan como reactivos terapéuticos.
Los anticuerpos (por ejemplo, anticuerpos humanizados) de la invención tienen funciones efectoras alteradas y usos terapéuticos. Breve Descripción de los Dibujos
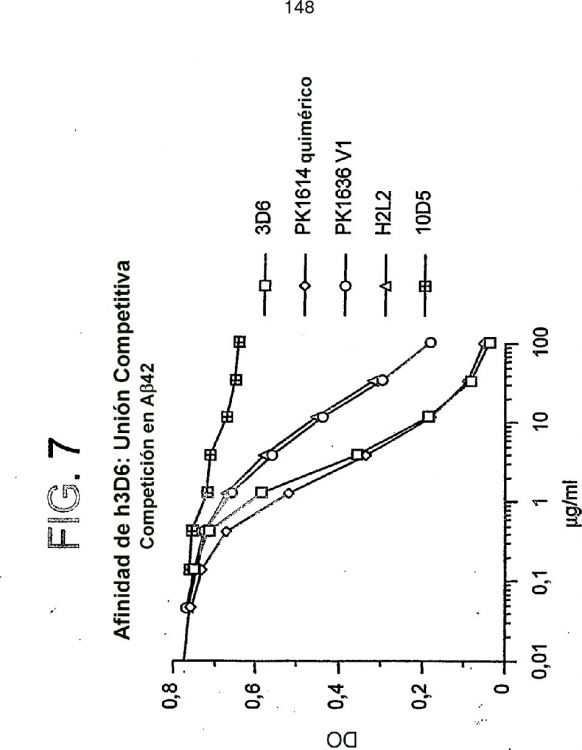
La Figura 1 representa un alineamiento de las secuencias de aminoácidos de la cadena ligera de anticuerpos 3D6 de ratón, 3D6 humanizado, Kabat ID 109230 y A19 de línea germinal. Las regiones CDR se indican por flechas. Las letras en negrita y en cursiva indican restos murinos raros. Las letras en negrita indican restos de empaquetamiento (VH+VL). El relleno sólido indica restos de interacción canónicos/CDR. Los asteriscos indican restos seleccionados para retromutación en 3D6 humanizado, versión 1. La Figura 2 representa un alineamiento de las secuencias de aminoácidos de la cadena pesada de anticuerpos 3D6 de ratón, 3D6 humanizado, Kabat ID 045919 y VH3-23 de línea germinal. La anotación es igual que en el caso de la Figura 1. La Figura 3 representa gráficamente las propiedades de unión a Aβ de 3D6, 3D6 quimérico y 10D5. La Figura 3A es un gráfico que representa la unión a Aβ a 3D6 quimérico (PK1614) en comparación con 3D6 murino. La Figura 3B es un gráfico que representa la competición de 3D6 biotinilado frente a 3D6 no marcado, PK1614 y 10D5 con respecto a la unión a Aβ. La Figura 4 representa un modelo de homología de VH y VL de 3D6, que muestra el trazo del esqueleto de α-carbono. VH se muestra como una línea punteada, y VL se muestra como una línea continua. Las regiones CDR se indican en forma de cinta. La Figura 5 representa gráficamente las propiedades de unión a Aβ de 3D6 quimérico y 3D6 humanizado....
Reivindicaciones:
1. Una inmunoglobulina humanizada para uso en terapia, que comprende una región de cadena pesada variable como se expone en los restos 1-119 de la SEC ID Nº: 12 y una región de cadena ligera variable como se expone en los restos 1-112 de la SEC ID Nº: 11, comprendiendo la inmunoglobulina una región Fc que comprende una modificación de aminoácidos en el resto de aminoácido 234, 235, 236 ó 237, con respecto a la IgG1 3D6 humanizada, de tal forma que la modificación reduce la unión a un receptor FcγRI.
2. La inmunoglobulina humanizada de la reivindicación 1, que es de isotipo IgG1 humano.
3. Una inmunoglobulina quimérica para uso en terapia que comprende las secuencias de región variable de inmunoglobulina 3D6 expuestas como restos 1 a 112 de la SEC ID Nº: 2 y restos 1 a 119 de la SEC ID Nº:4, y secuencias de región constante de cadena pesada y ligera humana, en la que la secuencia de la región constante de cadena pesada humana comprende una región Fc que comprende una modificación de aminoácidos en el resto de aminoácido 234, 235, 236 ó 237 con respecto a la IgG1 3D6 quimérica, de tal forma que la inmunoglobulina modificada tiene menor unión a un receptor FcγRI.
4. La inmunoglobulina humanizada de la reivindicación 1 o la reivindicación 2, para uso en la prevención o tratamiento de una enfermedad amiloidogénica.
5. La inmunoglobulina humanizada de la reivindicación 4, en la que la enfermedad amiloidogénica es la enfermedad de Alzheimer.
6. La inmunoglobulina humanizada de la reivindicación 4 o la reivindicación 5, en la que la dosificación eficaz es de 1 mg/kg o 10 mg/kg de peso corporal.
7. Una composición farmacéutica que comprende la inmunoglobulina humanizada de la reivindicación 1 o la reivindicación 2 y un vehículo farmacéutico.
8. Una molécula o moléculas de ácido nucleico aisladas que codifican la cadena pesada y la cadena ligera de la inmunoglobulina de cualquiera de las reivindicaciones anteriores.
9. Un vector que comprende la molécula de ácido nucleico de la reivindicación 8.
9. Una célula huésped que comprende la molécula de ácido nucleico de la reivindicación
8.
10. Un procedimiento para producir un anticuerpo, que comprende cultivar la célula huésped de la reivindicación 10 en condiciones tales que se produzca el anticuerpo y aislar dicho anticuerpo de la célula huésped o el cultivo.
Patentes similares o relacionadas:
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Terapia basada en anticuerpos de la amiloidosis por transtiretina (TTR) y anticuerpos de origen humano para ese propósito, del 22 de Julio de 2020, de Neurimmune Holding AG: Un anticuerpo anti-transtiretina (TTR) de origen humano o un fragmento de unión a antígeno del mismo, que es capaz de unirse a especies de TTR mutadas, mal plegadas, […]
Polipéptidos biparatópicos antagonistas de la señalización WNT en células tumorales, del 15 de Julio de 2020, de Boehringer Ingelheim International GmbH & Co. KG: Un polipéptido que se une específicamente a LRP5 o LRP6, que comprende - un primer dominio variable individual de inmunoglobulina seleccionado del grupo de dominios […]
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Redirectores de células T específicas de antígenos, del 1 de Julio de 2020, de THE JOHNS HOPKINS UNIVERSITY: Una nanoparticula que comprende en su superficie: (A) un anticuerpo que se une especificamente a un antigeno de celula diana o epitopo del mismo; y (B) un resto […]
Anticuerpos scFv que pasan las capas epitelial y/o endotelial, del 1 de Julio de 2020, de ESBATech, an Alcon Biomedical Research Unit LLC: Un anticuerpo monocatenario (scFv) que comprende: (a) un dominio variable de la cadena ligera (VL) que tiene tres regiones CDR de VL no […]
Un antígeno asociado con artritis reumatoide, del 24 de Junio de 2020, de PHILOGEN S.P.A.: Un conjugado de anticuerpo para su uso en un procedimiento de tratamiento de la artritis reumatoide en un paciente, en el que el conjugado de anticuerpo comprende […]
Moléculas de unión con cadena J modificada, del 24 de Junio de 2020, de IGM BIOSCIENCES, INC: Una molécula de unión que comprende un anticuerpo de IgM, IgA, IgG/IgM o IgG/IgA con una cadena J modificada, donde la cadena J modificada comprende una cadena […]