Formulación de dispersión sólida de curcuminoides.
Una formulación de curcuminoide, que comprende un producto de dispersión sólida procesado por fusión que comprende
a) uno o más curcuminoides,
b) un polímero termoplástico nutricionalmente aceptable, y
c) un fosfátido.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2011/067901.
Solicitante: ABBOTT GMBH & CO. KG.
Nacionalidad solicitante: Alemania.
Dirección: MAX-PLANCK-RING 2 65205 WIESBADEN ALEMANIA.
Inventor/es: BREITENBACH, JORG, DAS,TAPAS, KESSLER,THOMAS K, SCHNEIDER,KATRIN, SATHYA,SHREERAM, CHUAH,AI MEY, PATEL,GAURAV C.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A23L1/015
- A23L1/29
- A23L1/30
- A61K31/12 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Cetonas.
PDF original: ES-2511145_T3.pdf





Fragmento de la descripción:
Formulación de dispersión sólida de curcuminoides Campo de la invención
La curcumina es el curcuminoide principal de la especia India popular cúrcuma, la cual es un miembro de la familia del jengibre (Zingiberaceae). Otros curcuminoides de origen natural son la desmetoxicurcumina y la bis- desmetoxicurcumina. Los curcuminoides son polifenoles y son responsables del color amarillo de la cúrcuma. Los curcuminoides pueden existir en al menos dos formas tautoméricas, ceto y enol. La forma enol es más estable energéticamente en la fase sólida y en solución. La curcumina es prácticamente insoluble en agua a pH ácido y neutro, y se descompone rápidamente a pH alcalino. La curcumina es estable bajo condiciones de sequedad y también relativamente estable al calor.
La curcumina es un antioxidante muy poderoso. Su efecto antioxidante ha sido reportado como ocho veces más poderoso que el de la vitamina E. Un cierto número de estudios proveen evidencia acerca de las propiedades terapéuticas de los curcuminoides de origen natural y los derivados curcuminoides sintéticos, en particular en cuanto a su actividad anticáncer (por ejemplo, Pisano et al., Mol Cáncer. 21, 3;9( 1): 137; Bisht et al., J Nanobiotechnology. 27, 5:3). También hay reportes sobre otras actividades farmacológicas de la curcumina incluyendo efectos antimicrobianos y antiinflamatorios (Begum et al., J Pharmacol Exp Ther. 28, 326(1): 196-28).
Aunque se han sugerido los curcuminoides para una variedad de aplicaciones terapéuticas y profilácticas, un impedimento principal en este desarrollo es la muy baja biodisponibilidad de la curcumina administrada oralmente. Por ejemplo, se ha reportado que los niveles en suero en humanos después de una dosis oral de 2 g de curcumina sola fueron bien indetectables o muy bajos. Las razones que contribuyen a este efecto son la baja estabilidad y pobre absorción de la curcumina en el tracto digestivo así como su rápido metabolismo, en particular en el hígado, y la eliminación sistémica rápida. Así, los niveles de curcumina en suero suficientes para provocar los efectos beneficiosos deseados de este compuesto no pueden ser logrados por el solo consumo de cúrcuma con los alimentos. La administración concomitante de la piperina, un inhibidor de las enzimas involucradas en el metabolismo de los fármacos, ha demostrado incrementar la absorción de curcumina y así la concentración en suero de curcumina. Sin embargo, es una ventaja significativa de esta metodología que el hecho de que la piperina induce la inhibición del metabolismo de fármacos puede llevar a efectos indeseados, en particular cuando se toman otras medicaciones. (Anand et al., Mol Pharm 27 4(6):87-18; Shoba et al., Planta Med 1998 64(4):353:6).
Se han desarrollado diferentes formulaciones de curcumina para obviar la pobre solubilidad acuosa y/o biodisponibilidad oral de la curcumina. En 27, una formulación encapsulada en nanopartículas poliméricas de curcumina ("nanocurcumina") con menos de 1 nm de tamaño de partícula ha sido reportada por Bisht et al., (J Nanobiotechnology. 27, 5:3) para ser dispensable fácilmente en medio acuoso y por mostrar una eficacia comparable con la de la curcumina libre en modelos de línea celulares de cáncer humano. Una formulación de curcumina "en lípidos" ha sido descrita por Begum et al., (J Pharmacol Exp Ther. 28, 326(1): 196-28) para dar como resultado niveles de curcumina en plasma 11 veces más altos y niveles 4 veces más altos en el cerebro en comparación con dosis iguales de polvo de curcumina o de extractos de curcumina-piperina después de administración oral. En la WO 21/1431 se describen formulaciones de curcumina líquidas y semisólidas autoemulsificante con base en un sistema de vehículo lipídico de ésteres de ácidos grasos PEG las cuales demuestran una biodisponibilidad mejorada en comparación con una suspensión acuosa de curcumina después de la administración oral a ratas. Las nanopartículas de curcumina y la curcumina enlazada a nanopartículas de quitosano fueron descritas por proveer biodisponibilidad oral mejorada de la curcumina en ratones en comparación con la curcumina administrada oralmente en aceite de oliva (WO 21/13224. Paradkar et al., (Int J'Pharm. 24, 271(1-2):281-6) describe dispersiones sólidas de curcumina-PVP obtenidas por secado por aspersión que mostraron ratas de disolución incrementada en comparación con curcumina pura o mezclas físicas de curcumina. Las formulaciones de curcumina que incluyen una dispersión sólida de nanocristales en hidroxipropil celulosa, una dispersión sólida amorfa en hidroxipropilmetil celulosa y una nanoemulsión en una mezcla de solventes que comprende PEG4 ha sido descrita por Onoue et al. (J Pharm Sci. 21, 99(4): 1871-81). Se ha reportado que cada una de estas tres formulaciones de curcumina mostró solubilidad mejorada en agua así como concentraciones de curcumina en plasma más altas en ratas después de administración oral en comparación con la curcumina cristalina pura.
La US 26/67998 A se relaciona con un sistema de administración de fármacos coloidales, en donde la curcumina o un análogo respectivo es encapsulada en un lípido que forma una vesícula y en donde el sistema de administración de fármacos coloidal está presente en un vehículo farmacéuticamente aceptable, por ejemplo, solución salina.
La WO 27/13435 A se relaciona con una composición curcuminoide que tiene una biodisponibilidad mejorada y comprende un curcuminoide, un antioxidante y un vehículo solubilizante en agua, farmacéuticamente aceptable y adicionalmente de manera opcional un inhibidor de la glucuronidación.
La CN 11361713 se relaciona con una preparación nanocristalina que comprende curcumina y un agente con actividad superficial, en donde el agente con actividad superficial se disuelve primero en agua y luego la curcumina se dispersa dentro de dicha solución.
A pesar de las diversas metodologías descritas aquí existe aún una tremenda necesidad para proveer formulaciones de curcumina que permitan una biodisponibilidad óptima de la curcumina cuando se administra oralmente.
Resumen de la invención
Así, esta invención provee una formulación de curcuminoides, que comprende un producto de dispersión sólida procesado por fusión que comprende
a) uno o más curcuminoides,
b) un polímero termoplástico nutricionalmente aceptable, y
c) un fosfátido.
El producto de dispersión sólida comprende una matriz del polímero termoplástico nutricionalmente aceptable y la fosfatida en donde los curcuminoides están distribuidos homogéneamente. Además del producto de dispersión sólida, la formulación de curcuminoide puede comprender uno o más otros ingredientes, por ejemplo, aditivos u otros ingredientes nutricionalmente deseables.
La invención provee adicionalmente un método para producir la formulación de curcuminoide descrita aquí, que comprende:
a) mezclar uno o más curcuminoides, un polímero termoplástico nutricionalmente aceptable, y un fosfátido;
b) calentar la mezcla para obtener una fusión homogénea;
c) forzar la fusión así obtenida a través de una o más boquillas;
d) permitir que la fusión se solidifique para obtener un producto de dispersión sólida.
La invención también provee un producto nutricional fortificado con una formulación de curcuminoide tal como se describe aquí así como la formulación de curcuminoide descrita aquí para uso en el tratamiento o profilaxis de enfermedades y condiciones tales como cáncer, condiciones que involucran una reacción inflamatoria, trastornos neurológicos, enfermedad cardiovascular, enfermedad pulmonar, la formación de cálculos de colesterol e infestación por parásitos.
Breve resumen de las figuras
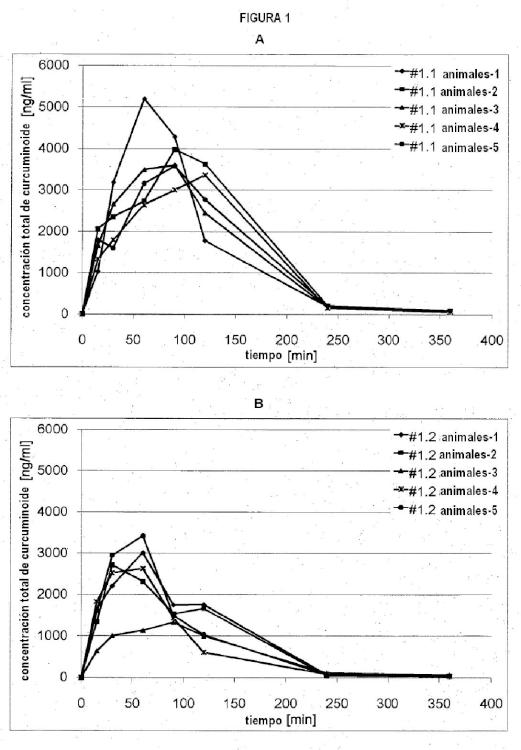
La figura 1 A-J muestra gráficas que ilustran las concentraciones de curcuminoide en plasma de ratas después de administración oral de curcuminoides. 4 a 5 ratas recibieron administración oral con una cantidad de formulación de curcuminoide # 1.1, # 1.2, # 2.1, # 2.2, # 3.1, # 3.2, # 3.3; # 4.1 o # 4.2 que comprende 2 mg de curcuminoides (Figura 1 A-I). Los sujetos de control recibieron la administración de 2 mg de curcuminoides cristalinos no formulados (Figura 1 J).
Descripción detallada de la invención
El término "curcuminoide", tal como se utiliza aquí, se refiere a curcumina y derivados de la misma y análogos de la misma. Estos incluyen derivados naturales y sintéticos de la curcumina, y cualquier combinación de más de un curcuminoide.
En particular, para los propósitos presentes, el término "curcuminoide" debe entenderse por abarcar compuestos que tengan un esqueleto 1,7-bis (4-hidroxifenil)-1,6-heptadien-3,5-diona o 1,7-bis(4-hidroxifenil)hept-4-en-3... [Seguir leyendo]
Reivindicaciones:
1. Una formulación de curcuminoide, que comprende un producto de dispersión sólida procesado por fusión que comprende
a) uno o más curcuminoides,
b) un polímero termoplástico nutricionalmente aceptable, y
c) un fosfátido.
2. La formulación curcuminoide de la reivindicación 1, en donde el producto de dispersión solida comprende adicionalmente un poliol normalmente sólido.
3. La formulación curcuminoide de la reivindicación 1 o 2, en donde los curcuminoides están presentes en un estado esencialmente no cristalino.
4. La formulación curcuminoide de cualquiera de las reivindicaciones 1 a 3, en donde el producto de dispersión sólida procesada por fusión comprende
a) de.1 a 5% en peso de los curcuminoides,
b) de 2 a 95% en peso del polímero termoplástico nutricionalmente aceptable,
c) de 5 a 5% en peso de fosfátido, y
d) de a 5% en peso del poliol normalmente sólido.
5. La formulación curcuminoide de cualquiera de las reivindicaciones 1 a 4, en donde el polímero termoplástico nutricionalmente aceptable es seleccionado del grupo consistente de homopolímeros y copolímeros de N-vinil lactamas, derivados de celulosa, óxidos de polialquileno de alto peso molecular, copolímeros de injerto de alcohol polivinílico-polietilenglicol, copolímeros de injerto que comprenden un esqueleto poli (alquilen glicol) y un copolímero de injerto de acetato de vinilo/N-vinil caprolactama sobre el esqueleto, poliacrilatos y polimetacrilatos, poliacrilamidas, polímeros de acetato de vinilo, alcohol polivinílico, oligo y polisacáridos, polihidroxialcanoatos, poliaminoácidos, proteínas y polipéptidos y mezclas de los anteriores.
6. La formulación curcuminoide de la reivindicación 5, en donde el polímero termoplástico nutricionalmente aceptable es seleccionado de derivados de celulosa.
7. La formulación de curcuminoide de la reivindicación 6, en donde el polímero termoplástico nutricionalmente aceptable es hidroxipropilmetilcelulosa.
8. La formulación de curcuminoide de cualquiera de las reivindicaciones 2 a 7, en donde el poliol normalmente sólido es un azúcar alcohol.
9. La formulación de curcuminoide de la reivindicación 8, en donde el poliol normalmente sólido es isomaltol.
1. La formulación de curcuminoide de cualquiera de las reivindicaciones 1 a 9, en donde el fosfátido es lecitina.
11. La formulación de curcuminoide de una cualquiera de las reivindicaciones 1 a 1, en donde la cantidad de curcuminoide en la sangre de una rata sujeto determinada como AUCo_6h después de una administración oral sencilla de una dosis de la formulación correspondiente a 2 mg de curcuminoide a dicho sujeto es al menos 2 veces más alta que después de la administración oral de la misma cantidad de curcuminoide cristalino no formulado.
12. Un producto nutricional fortificado con una formulación de curcuminoide de cualquiera de las reivindicaciones 1 a 11.
13. La formulación de curcuminoide de cualquiera de las reivindicaciones 1 a 11 para uso en el tratamiento o profilaxis de cáncer, condiciones que involucran una reacción inflamatoria, trastornos neurológicos, enfermedad cardiovascular, enfermedad pulmonar, la formación de cálculos de colesterol e infestación con parásitos.
14. Un método para producir la formulación de curcuminoide de cualquiera de las reivindicaciones 1 a 11, que comprende:
a) mezclar uno o más curcuminoides, un polímero termoplástico aceptable, y un fosfátido;
b) calentar la mezcla para obtener una fusión homogénea;
c) forzar la fusión así obtenida a través de una o más boquillas;
d) permitir que la fusión se solidifique para obtener un producto de dispersión sólida.
15. El método de la reivindicación 14, en donde la etapa b) se lleva a cabo en un extrusor y la mezcla es sometida a 5 una acción de mezclado en una sección de mezcla del extrusor.
Patentes similares o relacionadas:
Procedimiento para la producción de aceituna en polvo, del 17 de Agosto de 2016, de TUBITAK: Procedimiento para la obtención de la aceituna en polvo, caracterizado porque se muelen aceitunas enteras deshuesadas y secas en presencia de […]
Materiales de unión a fosfato y sus usos, del 13 de Julio de 2016, de MEDICAL RESEARCH COUNCIL: Una composicion de hierro ferrico para uso en un metodo de tratamiento de hiperfosfatemia, en donde la composicion de hierro ferrico es un […]
Alimento para bebés y lactantes que contiene aceitunas enteras, del 12 de Febrero de 2016, de TUBITAK: Alimento para bebés o lactantes que contiene aceitunas libres de sal y no químicamente tratadas que cubre las siguientes etapas de procesamiento: a. las aceitunas se ponen […]
Aparato y procedimiento de desaceitado para la fabricación de chips de patata con bajo contenido en aceite, del 1 de Julio de 2015, de Frito-Lay Trading Company GmbH (100.0%): Aparato para desaceitar rodajas de patata, comprendiendo dicho aparato un transportador longitudinal alargado provisto de un extremo aguas arriba y […]
Composiciones ingeribles que contienen un aceite odorífero, del 8 de Abril de 2015, de R.P. SCHERER TECHNOLOGIES, LLC: Una cápsula de gel blando para la administración de un aceite odorífero y que tiene un olor reducido tras la ingestión, conteniendo dicha cápsula […]
 Sistema mejorado de obtención de la anchoa para su consumo, del 29 de Enero de 2015, de MADRIGAL BALLESTER, Guillermo: El sistema mejorado de obtención de la anchoa para su consumo, se desarrolla en fases sucesivas hasta obtener una anchoa apta para su consumo, sin sal y baja en sal.
Para […]
Sistema mejorado de obtención de la anchoa para su consumo, del 29 de Enero de 2015, de MADRIGAL BALLESTER, Guillermo: El sistema mejorado de obtención de la anchoa para su consumo, se desarrolla en fases sucesivas hasta obtener una anchoa apta para su consumo, sin sal y baja en sal.
Para […]
Método de preparación de un producto tratado con calor, del 14 de Enero de 2015, de NOVOZYMES A/S: Método para preparar un producto tratado con calor, que comprende las fases secuenciales de: a) proveer una materia prima que comprende hidrato […]
 PROCEDIMIENTO PARA REDUCIR EL AMARGOR Y PICOR DE UN ACEITE DE OLIVA, del 29 de Septiembre de 2014, de ASOCIACIÓN EMPRESARIAL DE INVESTIGACIÓN CENTRO TECNOLÓGICO NACIONAL AGROALIMENTARIO "EXTREMADURA" (CTAEX): La invención es un procedimiento para reducir los atributos de "amargor" y "picante" en un aceite de oliva, que comprende introducir oxígeno en dicho […]
PROCEDIMIENTO PARA REDUCIR EL AMARGOR Y PICOR DE UN ACEITE DE OLIVA, del 29 de Septiembre de 2014, de ASOCIACIÓN EMPRESARIAL DE INVESTIGACIÓN CENTRO TECNOLÓGICO NACIONAL AGROALIMENTARIO "EXTREMADURA" (CTAEX): La invención es un procedimiento para reducir los atributos de "amargor" y "picante" en un aceite de oliva, que comprende introducir oxígeno en dicho […]