Compuesto inmunizante y método para inducir una respuesta inmune contra el sitio de escisión de la beta-secretasa de la proteína precursora de amiloide.
Un compuesto inmunizante que comprende una cantidad de efecto inmunizante de un producto antigénico queinduce una respuesta inmunitaria contra un epítopo que recubre el sitio de escisión de la l3-secretasa de la proteínaprecursora de amiloide (AI3PP),
que bloquea la escisión de la AI3PP por la l3-secretasa, y un soporte, un diluyente,un excipiente, un adyuvante o un agente auxiliar farmacéuticamente aceptables.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/006388.
Solicitante: RAMOT AT TEL AVIV UNIVERSITY LTD..
Nacionalidad solicitante: Israel.
Dirección: P.O. Box 39296 61392 Tel Aviv ISRAEL.
Inventor/es: SOLOMON,BEKA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K38/04 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen hasta 20 aminoácidos en una secuencia totalmente determinada; Sus derivados (gastrinas A61K 38/16, somatostatinas A61K 38/31, melanotropinas A61K 38/34).
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61K39/40 A61K 39/00 […] › bacterianos.
- A61K39/42 A61K 39/00 […] › virales.
- C07K16/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Inmunoglobulinas, p. ej. anticuerpos mono o policlonales.
PDF original: ES-2392247_T3.pdf
Fragmento de la descripción:
Compuesto inmunizante y método para inducir una respuesta inmune contra el sitio de escisión de la ¡3-secretasa de la proteína precursora de amiloide.
Sector de la técnica
La presente invención hace referencia a compuesto inmunizante y a un método para inducir una respuesta inmune contra el sitio de escisión de la ¡3-secretasa de la proteína precursora de amiloide. La presente invención también hace referencia a anticuerpos cultivados o generados contra el sitio de escisión de la ¡3-secretasa de la proteína precursora de amiloide y los anticuerpos a ser utilizados en inmunización pasiva.
Estado de la técnica
Proteína Precursora de Ami/oide y {3-Secretasa:
Se considera que la deposición extracelular de péptidos amiloides cortos en los cerebros de pacientes es un acontecimiento fundamental en la patogénesis de la enfermedad de Alzheimer. Las pruebas de que los amiloides pueden desempeñar un papel importante en la patogénesis inicial de la EA proceden principalmente de estudios realizados en individuos afectados por la forma familiar de Alzheimer (EFA) o por el síndrome de Down. La generación de péptidos ¡3-amiloides (A¡3) se produce a través de una cascada regulada de escisiones en su proteína precursora, A¡3PP (proteína precursora de amiloide) . Al menos tres enzimas son responsables de la proteólisis de la A¡3PP y han sido provisionalmente denominadas a, 13, y y secretasa. La reciente identificación de varias de estas secretasas es un salto importante en la comprensión de cómo regulan estas secretasas la formación de péptidos de 25 amiloide. Una de las principales metas terapéuticas es la inhibición de secretasas que producen A¡3 a partir de la gran proteína precursora. La especificidad teórica y tratabilidad de las proteasas hacen pensar que debería ser posible generar inhibidores de proteasa específicos de la secretasa que penetren en la barrera sanguínea cerebral. Ya se están realizando muchos estudios que utilizan los nuevos conocimientos de la capacidad de la enzima 13secretasa (BACE) para identificar inhibidores mediante métodos de cribado o de diseño racional (Patente U.S. Nos. 5, 744, 346; 5, 942, 400; 6, 221, 645 B1; 6, 313, 268 B1; Y solicitudes PCT publicadas WO 00/47618, WO 98/21589, y WO 96/40885) . En este momento, no existen pruebas de funciones adicionales del A¡3, por lo que no existen preocupaciones serias por la reducción de este metabolito. Tanto la 13-y la y-secretasas están presentes en muchas células diferentes del cuerpo yes razonable suponer que tienen substratos además de la A¡3PP. Por consiguiente, la completa inhibición de una de estas enzimas puede tener como resultado problemas de toxicidad, en particular en
las condiciones de tratamiento crónico que presumiblemente serían necesarias. A nivel del mRNA, la BACE se expresa ampliamente en el cerebro humano. La expresión es también elevada en el páncreas, aunque la actividad enzimática en este tejido es baja. Aparte de la escisión de la A¡3PP, no se conoce si BACE posee otra actividad y por lo tanto es demasiado pronto para predecir qué toxicidad pueden tener los inhibido res de ¡3-secretasa.
El procesado proteolítico de la proteína precursora de amiloide (A¡3PP) genera el péptido ¡3-amiloide (A¡3) que está considerado ser la causa de la patología y subsiguiente declive cognitivo en la enfermedad de Alzheimer. Para comenzar la formación de A¡3, la ¡3-secretasa escinde la A¡3PP en el N-terminal de A¡3 para liberar APPs¡3, un fragmento N-terminal aproximadamente de 100-kD soluble, y C99, un fragmento C-terminal 12-kD que permanece unido a la membrana. El sitio exacto de la escisión de la ¡3-secretasa ha sido determinado (Fig. 1) . La placa de
45 amiloides A¡3 comienza en Aspl y este sitio de escisión es por lo tanto del mayor interés. La escisión por ¡3-secretasa en el término amino de la secuencia del péptido ¡3-amiloide, entre los residuos 671 y 672 de A::JPP, conduce a la generación y liberación extracelular de la A¡3PP soluble ¡3-escindida, y su correspondiente fragmento carboxi-terminal asociado a células.
WO 99/27944; Morgan et al (en "A¡3 peptide vaccination prevents memor y loss in an animal model of Alzheimer's disease", Nature, vol. 408, 28 Diciembre 2000, páginas 982 -985) ; Y DeMattos et al (en "Peripheral antiA¡3 antibody alters CNS and plasma A¡3 clearance and decreases brain A¡3 burden in a mouse model of Alzheimer's disease", Proc. Natl. Acad. ScL USA, vol. 98, no. 15, 17 Julio 2001, páginas 8850-8855) describen la inmunización con el péptido j3-amiloide (Aj3) , o partes del mismo, a fin de reducir la deposición de amiloides.
55 [0005] La Patente US 5, 229, 490 describe múltiples sistemas de péptidos de antígenos que proporcionan una elevada concentración de antígenos en un bajo volumen molecular.
Se demostró que una de las familias de la EA familiar tiene una mutación de la A¡3PP que coincidía con el sitio de escisión previsto de la ¡3-secretasa. Esta doble mutación, identificada por primera vez en un linaje sueco, resultó producir también un exceso de péptidos ¡3-amiloides con relación a la secuencia salvaje cuando fue transfeccionada en células, haciendo pensar que era un mejor sustrato para la enzima j3-secretasa. Esta predicción ha sido recientemente considerada verdadera. La sustitución de metionina por leucina en la posición PI de APP, encontrada en la mutación de la EA familiar "sueca" que provoca una aparición temprana de la EA, mejora 65 espectacularmente la escisión de ¡3-secretasa, pero muchas otras sustituciones (por ejemplo, Metionina por Valina) reducen la escisión de j3-secretasa. Estos hallazgos demostraron la presencia de una actividad de ¡3-secretasa
responsable de una escisión que liberaba el N-terminal de péptido AJ3 y mostraron que el proceso era secretor en lugar de lisosómico, la hipótesis sostenida en aquel momento.
Barrera cerebral sanguínea:
La barrera cerebral sanguínea (BBB) (Johansson, 1992; Ermisch, 1992; Schlosshauer, 1993) está formada por una monocapa de células endoteliales microvasculares estrechamente conectadas con ~argas aniónicas. Esta capa separa dos compartimentos que contienen fluidos: el plasma sanguíneo (BP) y el fluido extracelular (ECF) del parénquima cerebral, y está rodeado por células astrogliales del cerebro. Una de las principales funciones de la BBB es regular la transferencia de componentes entre el BP y el ECF. La BBB limita el libre paso de moléculas de agentes de la sangre a las células cerebrales.
En general, las grandes moléculas de elevada polaridad, como péptidos, proteínas, (por ejemplo, enzimas, factores de crecimiento y sus conjugados, oligonucleótidos, vectores genéticos y otros) no cruzan la BBB. Por lo 15 tanto, el deficiente suministro de agentes al Sistema Nervioso Central limita la aplicabilidad de dichas macro moléculas para el tratamiento de trastornos neurodegenerativos y enfermedades neurolÓgicas.
Varios métodos de suministro de agentes terapéuticos al cerebro evitan el SNC. Dichos métodos utilizan inyecciones intratecales, implantes quirúrgicos (Ommaya, 1984 y Patente U.S. No. 5, 222, 982) e infusión intersticial (Bobo et al., 1994) . Estas estrategias suministran un agente al SNC por administración directa al fluido cerebroespinal (CSF) o al parénquima cerebral (ECF) .
El suministro de medicamentos al sistema nervioso central a través del fluido cerebroespinal se consigue por medio de un dispositivo implantable subduralmente que lleva el nombre de su inventor, el "depósito de Ommaya". El
depósito se utiliza fundamentalmente para el suministro localizado postop..., eratorio de agentes quimioterapéuticos en cánceres. El medicamento se inyecta en el dispositivo y se va liberando posteriormente al fluido cerebroespinal que rodea el cerebro. Puede ser dirigido hacia zonas específicas del tejido cerebral expuesto que luego absorbe el medicamento. Esta absorción es limitada ya que el medicamento no se desplaza libremente. Un dispositivo modificado desarrollado por Ayub Ommaya, en el que el depósito es implantado en la cavidad abdominal y el medicamento inyectado es transportado por fluido cerebroespinal (tomado de y devuelto a la espina dorsal) por todo el espacio ventricular del cerebro, es utilizado para la administración de agentes.
La difusión de macromoléculas a diversas aéreas del cerebro por liberación mejorada por convección es otro método... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto inmunizante que comprende una cantidad de efecto inmunizante de un producto antigénico que induce una respuesta inmunitaria contra un epítopo que recubre el sitio de escisión de la l3-secretasa de la proteína
precursora de amiloide (AI3PP) , que bloquea la escisión de la AI3PP por la l3-secretasa, y un soporte, un diluyente, un excipiente, un adyuvante o un agente auxiliar farmacéuticamente aceptables.
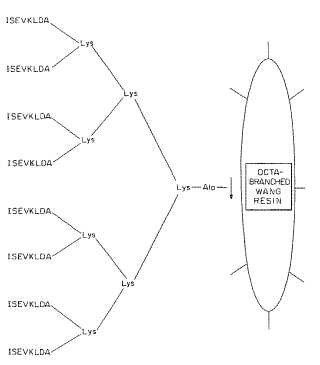
2. El compuesto inmunizante de la reivindicación 1, en el que dicho producto antigénico comprende un polímero dendrítico, construido sobre una molécula de núcleo, que es al menos disfuncional para suministrar una ramificación, Y que contiene hasta 16 grupos funcionales terminales a los que está conectado por enlaces covalentes un péptido antigénico que comprende un epítopo de la AI3PP que recubre el sitio de escisión de la l3-secretasa.
3. El compuesto inmunizante de la reivindicación 2, donde dicho polímetro dendrítico contiene ocho grupos
funcionales terminales a los que está conectado un péptido antigénico. 15
4. El compuesto inmunizante de la reivindicación 1 o 2, donde dicho epítopo de la AI3PP que recubre el sitio de escisión de la l3-secretasa comprende residuos 1 a 8 de SEO ID NO: 1.
5. El compuesto inmunizante de la reivindicación 1 . o 2, donde dicho epítopo de la AI3PP que recubre el sitio de escisión de la l3-secretasa comprende la SEO ID NO: 5.
6. El compuesto inmunizante de la reivindicación 2, donde dicha molécula nuclear es lisina.
7. El compuesto inmunizante de la reivindicación 2, que comprende además una molécula que tiene propiedades 25 adyuvantes unida a dicho polímero dendrítico.
8. El compuesto inmunizante de la reivindicación 2, donde dicho producto antigénico está encapsulado en un liposoma.
9. El compuesto inmunizante de la reivindicación 1, donde dicho producto antigénico comprende un vehículo de exposición viral que muestra en su superficie epítopo de la AI3PP que recubre el sitio de escisión de la l3-secretasa de laAI3PP.
10. El compuesto inmunizante de la reivindicación 9, donde dicho vehículo de exposición viral es un bacteriófago 35 filamentoso.
11. El compuesto inmunizante de la reivindicación 9, donde dicho epítopo de la AI3PP que recubre el sitio de escisión de la l3-secretasa de la AI3PP comprende los residuos 1 a 8 of SEO ID NO: 1.
12. El compuesto inmunizante de la reivindicación 9, donde dicho epítopo de la AI3PP que recubre el sitio de escisión de la j3-secretasa de la Aj3PP comprende la SEO ID NO: 5.
13. El compuesto inmunizante de cualquiera de las reivindicaciones 1-12, donde el sitio de escisión está rodeado por SEO ID NO: 1, Y la escisión tiene lugar entre Xaa y Asp (D) .
14. El compuesto inmunizante de la reivindicación 1 para su uso como medicamento.
15. Uso del compuesto inmunizante de la reivindicación 1 para la fabricación de un medicamento para el tratamiento de la enfermedad de Alzheimer.
16. El compuesto inmunizante de la reivindicación 1 para su uso en el tratamiento de la enfermedad de Alzheimer.
17. Una molécula que bloquea la escisión de la Aj3PP por la l3-secretasa y que comprende la parte de unión al
antígeno de un anticuerpo contra un epítopo que recubre el sitio de escisión de la j3-secretasa de la Aj3PP. 55
18. La molécula de la reivindicación 17, donde el sitio de escisión está rodeado por SEO ID NO: 1, Y la escisión tiene lugar entre Xaa y Asp (D) .
19. La molécula de la reivindicación 17 que es un anticuerpo monoclonal.
20. La molécula de la reivindicación 17 que es un anticuerpo monocatenario.
21. Vehículo de exposición bacteriófago filamentoso que expone la molécula de la reivindicación 20 en su superficie.
65 22. Un compuesto farmacéutico, que comprende el vehículo de exposición bacteriófago filamentoso de la reivindicación 21 y un soporte, un diluyente, un excipiente, un adyuvante o un agente auxiliar farmacéuticamente 26
aceptable.
23. El vehículo de exposición bacteriófago filamentoso de la reivindicación 21 para su uso como medicamento.
24. Uso del vehículo de exposición bacteriófago filamentoso de la reivindicación 21 para la fabricación de un medicamento para el tratamiento de la enfermedad de Alzheimer.
25. El vehículo de exposición bacteriófago filamentoso de la reivindicación 21 para su uso el tratamiento de la enfermedad de Alzheimer.
26. La molécula de la reivindicación 17 para su uso como medicamento.
27. Uso de la molécula de la reivindicación 17 para la fabricación de un medicamento para el tratamiento de la
enfermedad de Alzheimer. 15
28. La molécula de la reivindicación 17 para su utilización en el tratamiento de la enfermedad de Alzheimer.
Patentes similares o relacionadas:
Uso del péptido qbp1 para la prevención o el tratamiento del trastorno del estrés postraumático, el síndrome de estrés agudo y/o el síndrome de adaptación general, del 8 de Abril de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS: Una composición que comprende un péptido que consiste en una secuencia de aminoácidos con al menos un 70% de identidad con la SEQ ID NO: 1, o que […]
Péptidos capaces de reactivar mutantes de p53, del 18 de Marzo de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Un péptido recombinante o sintético que comprende una secuencia de aminoácidos expuesta en la SEQ ID NO: 314, en donde dicho péptido reactiva […]
Péptidos de diseño corto que poseen acciones selectivas contra bacterias y células cancerosas, del 26 de Febrero de 2020, de THE UNIVERSITY OF MANCHESTER: Un péptido con la fórmula I o II que se muestra a continuación **(Ver fórmula)** en donde: A1v se selecciona de G, GKI o GIK […]
Compuestos para su uso en el tratamiento y/o prevención de una infección de mycoplasma sp., del 31 de Enero de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Compuestos para su uso en el tratamiento y/o prevención de una infección de mycoplasma sp. La presente invención hace referencia a compuestos con […]
Composiciones para unir módulos de dedos de cinc, del 15 de Enero de 2020, de Sangamo Therapeutics, Inc: Una proteína de dedos de cinc de múltiples dedos que se une específicamente a un sitio diana, comprendiendo la proteína de dedos de cinc de […]
Análogos de compstatina de acción prolongada y composiciones y métodos relacionados, del 8 de Enero de 2020, de Apellis Pharmaceuticals, Inc: Un análogo de compstatina de acción prolongada que comprende un resto reductor de la eliminación unido con dos restos análogos de compstatina, en donde cada resto […]
Péptidos, dispositivos y procedimientos para la detección de anticuerpos de Anaplasma, del 20 de Noviembre de 2019, de Abaxis, Inc: Una composición que comprende una población de péptidos aislados, comprendiendo dicha población tres o más péptidos diferentes, en la que cada péptido en la población […]
Terapias de antibióticos peptídicos derivados del búfalo de agua, del 20 de Noviembre de 2019, de Centaur, Inc: Una composición antibiótica que comprende un péptido antibiótico, en donde el péptido comprende una secuencia aminoacídica sintética que tiene la […]