Sistema optofluídico para reacciones biocatalíticas con cristales de enzimas entrecruzados.
Sistema optofluídico para reacciones biocatalíticas con cristales de enzimas entrecruzados.
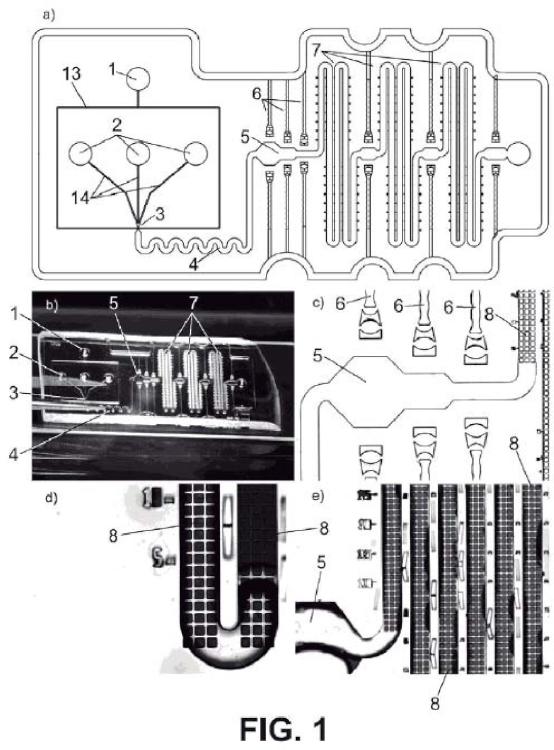
Permite cristalización y entrecruzamiento de cristales (12) enzimáticos in situ y comprende: a) cámara de mezcla con: i) primera entrada (2) para alimentar una disolución reactante, ii) segunda entrada (1) para la alimentación de un fluido de transporte, inmiscible con la disolución reactante, iii) zona de mezcla (3) para mezclar disolución reactante y fluido de transporte, y iv) canales de unión (13, 14) entre cada entrada (1, 2) de alimentación y la zona de mezcla (3); b) zona de detección con al menos un par de canales de interrogación (6) óptica para sensores de UV-VIS, que constan de elementos para confinar, colimar y/o propagar la luz dentro del sistema; c) un reactor de flujo microfluídico entre la zona de mezcla (3) y la zona de detección; y d) zona de almacenamiento de gotas, con sistemas individuales de atrapamiento de gotas.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201430058.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Nacionalidad solicitante: España.
Inventor/es: GARCIA RUIZ,JUAN MANUEL, LLOBERA ADAN,ANDREU, RODRÍGUEZ RUIZ,Isaac, GAVIRA GALLARDO,José Antonio, GÓMEZ MORALES,Jaime.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12M1/34 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12M EQUIPOS PARA ENZIMOLOGIA O MICROBIOLOGIA (instalaciones para la fermentación de estiércoles A01C 3/02; conservación de partes vivas de cuerpos humanos o animales A01N 1/02; aparatos de cervecería C12C; equipos para la fermentación del vino C12G; aparatos para preparar el vinagre C12J 1/10). › C12M 1/00 Equipos para enzimología o microbiología. › Medida o ensayo de detección de las condiciones del medio, p. ej. por contadores de colonias.
- G01N21/01 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 21/00 Investigación o análisis de los materiales por la utilización de medios ópticos, es decir, utilizando rayos infrarrojos, visibles o ultravioletas (G01N 3/00 - G01N 19/00 tienen prioridad). › Dispositivos o aparatos para facilitar la investigación óptica.
Fragmento de la descripción:
SISTEMA OPTOFLUÍDICO PARA REACCIONES BIOCATALÍTICAS CON CRISTALES DE ENZIMAS ENTRECRUZADOS
DESCRIPCION
SECTOR Y OBJETO DE LA INVENCION
La presente invención se refiere a un sistema optofluídico (OFS) que comprende al menos 5 un reactor de flujo microfluídico, sensores ópticos y medios para el almacenamiento de gotas de fluido. En particular, esta solicitud de patente describe un sistema optofluídico de bajo coste de fabricación, especialmente diseñado para su utilización en procesos de cristalización y entrecruzamiento de enzimas, así como en reacciones catalizadas por los cristales enzimáticos entrecruzados. 10
ESTADO DE LA TÉCNICA
La biocatálisis, mediante el uso de enzimas aisladas, permite la formación selectiva y controlada de productos químicos y bioquímicos. En comparación con los métodos tradicionales de síntesis química, la biocatálisis presenta unas ventajas excelentes en 15 términos de selectividad química, de localización molecular y estereoselectividad, mientras que, en términos medioambientales tiene un impacto menos nocivo que la química convencional. El uso de enzimas está muy extendido en gran variedad de industrias, tales como la alimentaria (tanto para humanos como para animales) , como en la farmacéutica, en el tratamiento de materiales y de residuos, o incluso en la producción de biocombustibles. A 20 un nivel similar de desarrollo tecnológico, las enzimas también se aplican actualmente como biosensores. Sin embargo, en el uso de enzimas en reacciones catalíticas también existen inconvenientes. Pueden presentar una conversión baja, ser inestables en las condiciones prácticas de operación, pueden tener una durabilidad corta en almacenaje, los tratamientos secundarios requeridos pueden ser complicados, el escalado de los procesos enzimáticos 25 es complejo con frecuencia y el abastecimiento de proteínas en cantidades industriales es también limitado habitualmente. A la vista de todo esto, el desarrollo de un biocatalizador estable, robusto, y preferentemente insoluble, se presenta como un gran reto para los biocatalizadores industriales. Todas estas características pueden ser logradas mediante la inmovilización de las enzimas. 30
La inmovilización de las enzimas mejora los procesos biocatalíticos, debido a la capacidad de mantener, incluso de aumentar, la actividad enzimática; permite la recuperación de la enzima tras su utilización y aumenta su estabilidad (ante la temperatura, la naturaleza de los solventes utilizados, etc) , entre otros beneficios. A pesar de ello, se estima que solo un 20% de los procesos biocatalíticos existentes hacen uso de enzimas inmovilizadas. 5 Tradicionalmente existen tres métodos para la inmovilización de enzimas: unión a un soporte, encapsulación, y entrecruzamiento.
En los dos primeros métodos, la unión al encapsulante o al soporte puede ser de naturaleza física, iónica, o covalente. Sin embargo, la unión física generalmente es demasiado débil para mantener a la enzima fijada al soporte en condiciones de operación industriales, con 10 elevadas concentraciones de reactivo y producto, así como en un medio con elevada fuerza iónica. En estos casos, la enzima se inmoviliza o se encapsula con la ayuda de polímeros (basados en siliconas, típicamente alquilsilano o polisiloxano, epóxidos, etc.) o una combinación de ambos métodos [Brady D, Jordaan J. Advances in enzyme immobilisation; Biotechnol Lett. (2009) 31 (11) :1639-50]. El uso de un soporte causa inevitablemente la 15 dilución de la actividad en términos de volumen y especificidad, dado que dichos soportes pueden comprender desde el 90% a más del 99% del peso o volumen de catalizador, dando lugar a menores rendimientos y productividades.
Un segundo tipo de metodologías, basadas en la producción de enzimas con una gran concentración de actividad, esto es, concentración de enzima, y una alta estabilidad, 20 consiste en entrecruzamiento de precipitados enzimáticos (agregados o cristalinos) , de forma que no es necesario el uso de un soporte. El entrecruzamiento se lleva a cabo mediante procesos químicos, usando típicamente ligandos bidentados, tales como el glutaraldehído, aldehído-dextrano, hexametilendiisocianato, etc. para producir cristales de enzima entrecruzados (CLECs, del inglés "Cross-Linked Enzime Cr y stals") o agregados de 25 enzima entrecruzados (CLEAs, del inglés "Cross-Linked Enzime Aggregates") [ St. Clair NL, Navia MA. Cross-linked enzyme cr y stals as robust biocatalysts; Journal of the American Chemical Society. (1992) 114 (18) :7314-6.].
El entrecruzado químico de los cristales de proteína fue desarrollado por primera vez en los años sesenta, con el propósito de estabilizar cristales de proteína para facilitar su 30 manipulación y la recogida de datos cristalográficos con rayos-X. Sin embargo, pronto se descubrió que las enzimas entrecruzadas en estado cristalino siguen siendo catalíticamente activas. Los CLECs se crean mediante una primera cristalización de la proteína, seguida por un entrecruzamiento químico, que bloquea el estado cristalino de las mismas, independientemente de las condiciones de cristalización externas. Por ello los CLECs pueden proporcionar material proteico microporoso activo, insoluble y mecánicamente robusto bajo condiciones de entrecruzamiento determinadas. Tanto los CLECs como los CLEAs se han usado hasta la fecha en distintos procesos de producción enzimáticos, como matrices de separación, como biosensores, y como vehículo para transporte de fármacos 5 [Illanes, A., et al., Recent trends in biocatalysis engineering. Bioresource Technology; 115 (2012) 48-57].
En consecuencia, y bajo el punto de vista de los biocatalizadores, los CLECs y CLEAs presentan numerosas ventajas en comparación con las enzimas unidas a soporte o libres: tienen de 10 a 1000 veces más actividad volumétrica (U/g) , una estabilidad superior en 10 condiciones no naturales (alta temperatura, solventes orgánicos, etc.) y, en casos particulares, una mayor selectividad. Aunque los CLEAs son la forma más económica y fácil de producir estos materiales tan activos, los agregados amorfos presentan dos principales desventajas en comparación con los CLECs: su distribución de tamaño de partícula no es controlable, y no tienen resistencia mecánica. 15
Por otro lado, el proceso de cristalización es un factor limitante para la producción de CLECs [Brady, D., et al., Spherezymes: A novel structured self-immobilisation enzyme technology; BMC Biotechnology 2008, 8:8]. En este contexto, el principal objetivo de esta invención es proporcionar una plataforma única para dos procesos consecutivos: primero, la producción y la inmovilización de cristales de proteína (enzimas) , que pueden ser entrecruzados in situ; y 20 segundo, el uso del mismo dispositivo en el que las enzimas han sido cristalizadas y entrecruzadas como un reactor catalítico para distintas aplicaciones biotecnológicas. En este contexto, la implementación de un sistema de detección óptica/fotónica en el reactor de microfluídica (optofluídica) permite la monitorización de la reacción via espectroscopía UV-Vis. 25
Se señalan a continuación algunos documentos que reflejan el estado de la técnica:
- El documento de patente WO2004038363 se refiere a un método microfluidico en el que se pueden llevar a cabo reacciones en contacto con un sustrato. Dicho método consiste en introducir en un primer canal, formado por dicho sustrato, un fluido de transporte (carrier-fluid) y al menos dos fluidos con los que se lleva a cabo una reacción o una precipitación, y 30 que son inmiscibles con el fluido de transporte. Mediante una zona de mezcla, se generan volúmenes discretos de fluido ("plugs") separados por el mencionado "carrier-fluid". Con dicho método puede llevarse a cabo una gran variedad de reacciones tales como polimerización, cristalización (de pequeñas moléculas y proteínas) , síntesis de nanopartículas, reacciones catalizadas por enzimas, uniones de proteínas etc. Más concretamente se ha llevado a cabo la cristalización de proteínas (lisozima) dentro de "plugs" almacenados en pocillos, fabricados en el mismo sustrato.
Además, pueden llevarse a cabo reacciones de co-cristalizacion. Por otro lado, los canales de dicho dispositivo pueden estar hechos de PDMS (polidimetilsiloxano) y por último se 5 pueden añadir aditivos que afecten a la cristalización, alterando la morfología de los cristales o la fase/polimorfo que cristaliza; entre estos aditivos se encuentran también los agentes de entrecruzamiento/reticulado que permiten la estabilización de los cristales.
- El documento US2006094119 trata sobre un sistema microfluidico que es capaz de llevar a cabo un gran número de reacciones en paralelo,...
Reivindicaciones:
1. Sistema optofluídico para reacciones biocatalíticas con cristales de enzimas entrecruzados que comprende:
a) una cámara de mezcla que a su vez comprende: 5
i) al menos una primera entrada (2) para la alimentación de una disolución reactante,
ii) al menos una segunda entrada (1) para la alimentación de un fluido de transporte, inmiscible con la disolución reactante,
iii) una zona de mezcla (3) de la disolución reactante y el fluido de transporte, y iv) canales de unión (13, 14) entre cada entrada (1, 2) de alimentación y la zona de 10 mezcla,
b) al menos una zona de detección que comprende al menos un par de canales de interrogación (6) óptica para sensores de UV-VIS, que constan de elementos para confinar, colimar y/o propagar la luz dentro del sistema.
c) un reactor de flujo microfluídico entre la zona de mezcla (3) y la zona de detección; 15
caracterizado por incluir una zona de almacenamiento de gotas en la que se encuentran ubicados sistemas individuales de atrapamiento de gotas.
2. Sistema optofluídico según la reivindicación 1, caracterizado por que en la zona de mezcla (3) se combinan el fluido de transporte y más de una disolución reactante. 20
3. Sistema optofluídico según las reivindaciones 1 o 2, caracterizado por que
tras la zona de mezcla (3) y previo a la zona de detección y reactor de flujo, se implementa un mezclador pasivo (4) que permite una rápida homogeneización de la mezcla de reactivos.
4. Sistema optofluídico según una cualquiera de las reivindicaciones 1 a 3, caracterizado por que los elementos para confinar, colimar y/o propagar la luz, ubicados en la zona de detección, consisten en: canales de alineación para inserción de fibras ópticas (9) , y al menos un par de microlentes (11) .
5. Sistema optofluídico según una cualquiera de las reivindicaciones 1 a 4, caracterizado por que la zona de detección comprende una zona de camino óptico (5) variable con un mínimo de 3 caminos ópticos distintos, colocados de forma consecutiva.
6. Sistema optofluídico según la reivindicación 5, caracterizado por que cada zona de camino óptico (5) distinto incluye un canal de interrogación (6) óptica, que consta de elementos para confinar, colimar y/o propagar la luz dentro del sistema permitiendo la determinación de la absorptividad molar de un compuesto mediante el ajuste de las medidas obtenidas a una recta de calibración. 5
7. Sistema optofluídico según una cualquiera de las reivindicaciones 1 a 6, caracterizado por que la zona de almacenamiento de gotas comprende un canal principal en forma de serpentín (7) , así como los sistemas individuales de atrapamiento de gotas comprenden una red de micropocillos (8) construidos sobre el serpentín (7) , a una altura diferente. 10
8. Sistema optofluídico según una cualquiera de las reivindicaciones 1 a 7, caracterizado por que comprende varios reactores de flujo microfluidico separados entre ellos por diferentes zonas de detección, formando todo el conjunto parte de un mismo canal microfluidico. 15
9. Uso del sistema optofluídico tal como se describe en cualquiera de las reivindicaciones 1 a 8 como biosensor.
10. Uso del sistema optofluídico tal como se describe en cualquiera de las reivindicaciones 20 1 a 8 en síntesis de productos de interés farmacéutico.
Patentes similares o relacionadas:
Sistema biométrico, del 13 de Mayo de 2020, de Tascom Co., Ltd: Un cartucho de medición para un sistema biométrico, que comprende: un recipiente de reactivo configurado para acomodar un reactivo líquido […]
APARATO DE CAPTACIÓN DE IMÁGENES HIPERESPECTRALES PARA LA EXPLORACIÓN DEL SUBSUELO, del 29 de Abril de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): 1. Aparato de captación de imágenes hiperespectrales para la exploración del subsuelo, caracterizado por que comprende: - un cabestrante con un instrumento […]
DISPOSITIVO INALAMBRICO PARA EL ANALISIS DE ALIMENTOS, del 27 de Febrero de 2020, de UNIVERSIDAD TÉCNICA PARTICULAR DE LOJA: La presente invención describe un dispositivo inalámbrico para la detección e identificación de compuestos agroquímicos, microorganismos y metales […]
Módulo de fuente de luz y procedimiento para modificar un instrumento analítico para analizar una muestra, del 8 de Enero de 2020, de F. HOFFMANN-LA ROCHE AG: Un módulo de fuente de luz para su uso en un instrumento analítico para analizar al menos una muestra , comprendiendo el […]
Sondas ópticas de escaneo directo, patrones de escaneo circulares, fibras desplazadas, del 13 de Noviembre de 2019, de ALCON, INC: Una sonda óptica de escaneo de luz, que comprende: un mango , conformado para que sea sujetado por el usuario; una cánula , que sobresale […]
Elemento receptor de muestras, kit de análisis y procedimiento para analizar un líquido, especialmente una emulsión lubricante refrigerante, del 4 de Septiembre de 2019, de Fuchs Petrolub SE: Elemento receptor de muestras para una muestra líquida para el análisis simultáneo de tres o más parámetros físico-químicos del líquido […]
Método y aparato para medidas de quimioluminiscencia y/o fluorescencia, del 6 de Marzo de 2019, de Technogenetics Holdings S.R.L: Aparato configurado para la medición de quimioluminiscencia y/o fluorescencia, comprendiendo un dispositivo fotomultiplicador configurado para recibir […]
Aparato de tratamiento de una superficie, del 6 de Marzo de 2019, de VORWERK & CO. INTERHOLDING GMBH: Aparato de tratamiento de una superficie , especialmente robot de limpieza, que presenta un dispositivo de detección para reconocer la naturaleza […]