Anticuerpo monoclonal para la detección de IgM totales y específicas de antígenos en pez cebra.
Anticuerpo monoclonal para la detección de IgM totales y específicas de antígenos en pez cebra.
En la presente invención se describe un anticuerpo monoclonal para la detección de IgM totales e IgM específicas en Danio rerio, así como sus usos y métodos que los utilizan para detección y/o cuantificación de dichas IgM, diagnóstico o cribado en pez cebra. También se refiere al antisuero, composición y kit que lo comprende así como a sus usos.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201530830.
Solicitante: INSTITUTO NACIONAL DE INVESTIGACION Y TECNOLOGIA AGRARIA Y ALIMENTARIA (INIA).
Nacionalidad solicitante: España.
Inventor/es: COLL MORALES,JULIO, GÓMEZ-CASADO,Eduardo, CHINCHILLA RODRÍGUEZ,Blanca.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/42 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra inmunoglobulinas (anticuerpos anti-idiotípicos).
- G01N33/577 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que interviene anticuerpos monoclonados.
PDF original: ES-2544358_A1.pdf


Fragmento de la descripción:
La presente invención se refiere a un anticuerpo monoclonal para la detección en pez cebra de IgM totales y específicas frente a antígenos, así como sus usos y aplicaciones. Por lo tanto, la presente invención se puede encuadrar en el campo de la medicina.
ESTADO DE LA TÉCNICA
El pez cebra (Danio rerío) se ha convertido en una excelente herramienta para el estudio del desarrollo embrionario, de la ontogenia del sistema inmune, y del estudio de la respuesta inmune frente a patologías como infecciones y cáncer. En particular, el pez cebra es un modelo animal muy versátil para el estudio de enfermedades propias de peces que cursan en aguas calientes y frías, debido a su gran capacidad de adaptación al medio. Por otro lado, el pez cebra es la especie cuyo genoma se encuentra secuenciado en mayor proporción (80%) [1], respecto a otras especies de interés como la trucha.
Sin embargo, y al contrario que en otras especies de peces, no existe hasta la fecha la posibilidad de determinar/cuantificar los anticuerpos del tipo IgM que el pez cebra (Zf) genera frente a un antígeno nativo conformacional en el desarrollo de la respuesta inmune mediada por anticuerpos. Se han producido anticuerpos que reconocen la cadena pesada IgM de Zf (IgM-Zf), pero siempre que ésta se encuentre desnaturalizada, es decir, en conformación casi lineal, cuando pierde la conformación adecuada para reconocer el antígeno en su conformación natural. Este hecho limita la detección de gran cantidad de anticuerpos específicos frente a antígenos de estudio en modelos de enfermedades humanas y animales. Cabe destacar las enfermedades causadas por virus o bacterias que conllevan infecciones con grandes pérdidas económicas en peces de piscifactoría [2], Una de ellas es la enfermedad causada por un rhabdovirus (novirhabdovirus) que causa infecciones en múltiples especies con grandes pérdidas económicas en peces salvajes y de piscifactoría: el virus de la septicemia hemorrágica viral (VHSV).
Se hace por lo tanto necesario obtener un anticuerpo frente a IgM-Zf que reconozca anticuerpos de Zf generados frente a antígenos conformacionales. La capacidad de determinar de forma cualitativa y cuantitativa los anticuerpos IgM-Zf que produce el pez cebra en respuesta a antígenos concretos, permitirá desarrollar nuevas estrategias de vacunación basadas en este modelo de pez, frente a patógenos que afectan a humanos y a otros organismos.
DESCRIPCIÓN DE LA INVENCIÓN
En la presente invención se demuestra el uso de un anticuerpo monoclonal que reconoce específicamente la secuencia SEQ ID NO: 1, para la detección de la cadena pesada de la IgM de pez cebra. Además, se han caracterizado por primera vez anticuerpos frente a IgM-Zf específicos de la proteína G del virus VHSV, que confieren protección frente a la infección por VHSV, y de la proteína flagelina de Marinobacter algicola, como ejemplos de uso de los anticuerpos de la presente invención.
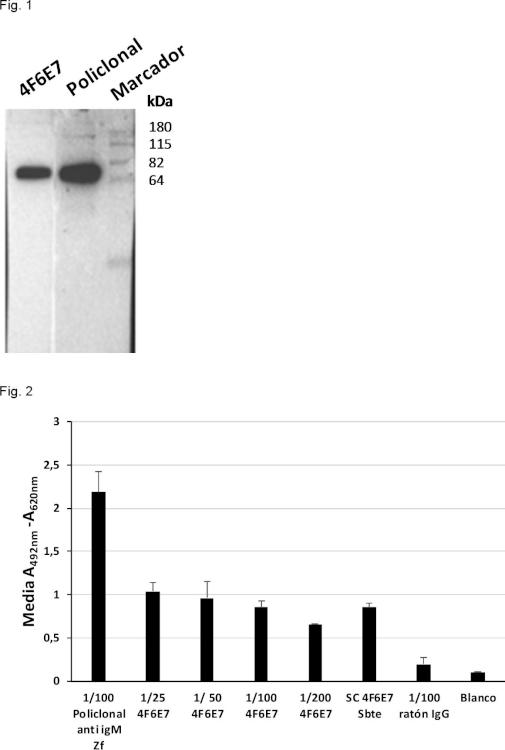
A partir del plasma de un solo pez cebra, las IgM-Zf específicas se pueden determinar por técnicas conocidas por el experto en la materia, por ejemplo serológicas (ELISA), inmunoquímicas (Western-blot), de inmunofluorescencia y de citometría de flujo (FACS).
El anticuerpo monoclonal de la presente invención también puede usarse "in vivo" mediante técnicas de imagen por fluorescencia.
En un primer aspecto la invención se refiere a un anticuerpo monoclonal que reconoce específicamente la secuencia SEQ ID NO: 1. En adelante nos referiremos a él como al "anticuerpo de la invención".
El término "anticuerpo", tal como aquí se utiliza en la presente invención, se refiere a moléculas de inmunoglobulinas y porciones (o fragmentos) inmunológicamente activas de moléculas de inmunoglobulinas. Es decir, moléculas que se unen específicamente (inmunorreaccionan) con un antígeno, tal como, por ejemplo, un péptido o una proteína (un inmunógeno o epítopo). El término "anticuerpo" comprende anticuerpos monoclonales y anticuerpos policlonales, en la presente invención el anticuerpo es monoclonal, y se refiere a un anticuerpo intacto o a fragmentos inmunológicamente activos de él, e incluye anticuerpos humanos, humanizados y de origen no humano,
recombinantes, quiméricos y sintéticos. En el contexto de esta invención el término anticuerpo se refiere a la inmunoglobulina que el animal o una célula híbrida ha sintetizado de forma específica frente a la secuencia SEQ ID NO: 1.
Ejemplos de porciones o fragmentos de ¡nmunoglobulínas inmunológicamente activas incluyen fragmentos F(ab) y F(ab)2, los cuales pueden ser generados tratando el anticuerpo con una enzima, por ejemplo pepsina.
Los "anticuerpos monoclonales" son poblaciones homogéneas de anticuerpos idénticos, producidos por un hibridoma, es decir, una célula híbrida producto de la fusión de un clon de linfocitos B descendiente de una sola y única célula madre y una célula plasmática tumoral, que están dirigidos contra un único sitio o determinante antigénico. El procedimiento de obtención de los anticuerpos monoclonales de la invención puede realizarse según métodos convencionales, conocidos en el estado de la técnica. Opcionalmente, dichos anticuerpos pueden purificarse por medios convencionales, tales como cromatografía de afinidad, proteína A-Sepharosa, cromatografía con hidroxiapatito, electroforesis en gel o diálisis.
Tal y como es conocido por el experto en la materia, hay cinco isotipos o clases principales de inmunoglobulinas: inmunoglobulina M (IgM), inmunoglobulina D (IgD), inmunoglobulina G (IgG), inmunoglobulina A (IgA) e inmunoglobulina E (IgE).
En una realización preferida del primer aspecto de la invención el anticuerpo es de tipo IgG, preferiblemente lgG1, lgG2, lgG3 o lgG4; más preferiblemente es lgG1.
Una realización más preferida del primer aspecto de la invención se refiere al anticuerpo donde dicho anticuerpo está expresado a partir de la línea celular (hibridoma) depositada en la autoridad internacional Leibniz-lnstitut DSMZ-Deutsche Sammlung vori Mikroorganismen und Zellkulturen GmbH (DSMZ) bajo la designación DSM ACC3243, en la presente invención también se denomina hibridoma 4F6E7 y genera el anticuerpo 4F6E7 (o también denominado 4F6E7 anti-IgM-zf). El depósito tuvo lugar el 5 de junio de 2014 en esta autoridad de depósito en Braunschweig, Alemania.
En una realización particular el anticuerpo puede comprender una etiqueta detectable. Una realización aún más preferida del primer aspecto de la invención se refiere al
anticuerpo donde dicho anticuerpo está conjugado con un fluorocromo, una enzima, una partícula de oro, una nanopartícula, un péptido u otra proteína de interés, por ejemplo una proteína o péptido ligando de un receptor.
El término "etiqueta detectable" o "mareaje" en la presente invención hace referencia a una etiqueta molecular que permite la detección, localización y/o identificación de la molécula a la que está unido, mediante procedimientos y equipamiento adecuados para la detección, bien mediante medios espectroscópicos, fotoquímicos, bioquímicos, inmunoquímicos o químicos. Ejemplos de etiquetas detectables para el mareaje de compuestos incluyen, aunque no se limitan a isótopos radiactivos, sustratos enzimáticos, co-factores, ligandos, agentes quimioluminiscentes, fluoróforos, enzimas (por ejemplo peroxidasa), receptores y combinaciones de éstos. En una realización particular el anticuerpo está marcado con biotina, avidina, estreptoavidina, fosfatasa alcalina o peroxidasa de rábano (HRP). Métodos para el mareaje y guía para la elección de mareajes adecuados para diferentes propósitos son conocidos por el experto en la materia.
El anticuerpo monoclonal puede ser alterado bioquímicamente, por manipulación genética o puede ser sintético, puede también carecer de porciones que confieran ventajas.
El anticuerpo de la invención también puede reconocer específicamente variantes de la secuencia SEQ ID NO: 1. Las variantes pueden tener al menos un 70% de identidad (un 70, 71, 72, 73, 74, 75, 76, 77, 78, 79, 80, 81, 82, 83, 84, 85, 86, 87, 88, 89, 90, 91, 92, 93, 94, 95, 96, 97, 98, 99 o 100% de identidad). El anticuerpo también puede reconocer fragmentos de la secuencia SEQ ID NO: 1 o de sus variantes.
El término "identidad", tal y como se utiliza en esta memoria, hace referencia a la proporción de aminoácidos idénticos entre dos péptidos o proteínas que se comparan. Los métodos de comparación de secuencias son conocidos en el estado de la técnica, e incluyen, aunque sin limitarse a ellos, el programa BLASTP o BLASTN, ClustalW y FASTA. Podemos considerar, que péptidos o proteínas con porcentajes de identidad de, al menos, un 70% mantendrán... [Seguir leyendo]
Reivindicaciones:
1. Anticuerpo monoclonal que reconoce específicamente la secuencia SEQ ID NO: 1.
2. Anticuerpo según la reivindicación 1 donde el anticuerpo es de tipo lgG1.
3. Anticuerpo según cualquiera de las reivindicaciones 1 a 2 donde dicho anticuerpo está expresado a partir de la línea celular de designación DSM ACC3243.
4. Anticuerpo según cualquiera de las reivindicaciones 1 a 3 donde dicho anticuerpo está conjugado con un fluorocromo, una enzima, un péptido o una proteína.
5. Antisuero que comprende el anticuerpo según cualquiera de las reivindicaciones 1 a 4.
6. Composición que comprende el anticuerpo monoclonal según cualquiera de las reivindicaciones 1 a 4.
7. Célula que expresa el anticuerpo según cualquiera de las reivindicaciones 1 a 4.
8. Célula según la reivindicación 7 donde dicha célula es la denominada DSM ACC3243.
9. Uso in vitro del anticuerpo según cualquiera de las reivindicaciones 1 a 4 o del antisuero según la reivindicación 5 para la detección y/o cuantificación de anticuerpos IgM de Danio rerio.
10. Uso según la reivindicación 9 donde los anticuerpos IgM de Danio rerio reconocen la proteína G del VHSV.
11. Uso in vitro del anticuerpo según cualquiera de las reivindicaciones 1 a 4 o del antisuero según la reivindicación 5 para el diagnóstico de enfermedades que cursan con variación en el número de anticuerpos IgM de Danio rerio.
12. Uso in vitro del anticuerpo según cualquiera de las reivindicaciones 1 a 4 o del antisuero según la reivindicación 5 para el diagnóstico del virus de la septicemia hemorrágica vírica (VHSV).
13. Uso in vitro del anticuerpo según cualquiera de las reivindicaciones 1 a 4 o del antisuero según la reivindicación 5 para el cribado de fármacos que varían el número de anticuerpos IgM de Danio rerio.
14. Uso in vitro del anticuerpo según cualquiera de las reivindicaciones 1 a 4 o del antisuero según la reivindicación 5 para el cribado de antígenos reconocidos por anticuerpos IgM de Danio rerio.
15. Uso según cualquiera de las reivindicaciones 9 a 14 donde la detección y/o cuantificacíón, el diagnóstico o el cribado se realiza mediante ELISA, western blot, inmunoquímica, inmunohistoquímica, inmunofluorescencia o citometría de flujo.
16. Método in vitro para la detección y/o cuantificacíón de anticuerpos IgM de Danio rerio que comprende las siguientes etapas:
a. poner en contacto una muestra biológica de Danio rerio con el anticuerpo según cualquiera de las reivindicaciones 1 a 4 o el antisuero según la reivindicación 5; y
b. detectar y/o cuantificar la unión específica.
17. Método in vitro para el diagnóstico de enfermedades que cursan con variación en el número de anticuerpos IgM de Danio rerio que comprende las siguientes etapas:
a. poner en contacto una muestra biológica de Danio rerio con el anticuerpo según cualquiera de las reivindicaciones 1 a 4 o el antisuero según la reivindicación 5; y
b. detectar y/o cuantificar la unión específica del anticuerpo o del antisuero del paso (a);
c. comparar la concentración de los anticuerpos IgM de pez cebra con un control;
d. atribuir una diferencia significativa a la enfermedad.
18. Método in vitro para el diagnóstico del virus de la septicemia hemorrágica vírica (VHSV) que comprende las siguientes etapas:
a. poner en contacto una muestra biológica de Danio rerio con el anticuerpo según cualquiera de las reivindicaciones 1 a 4 o el antisuero según la reivindicación 5; y
b. detectar y/o cuantificar la unión específica a anticuerpos IgM específicos del VHSV.
19. Método in vitro para evaluar la protección frente al VHSV en Danio rerio que comprende las siguientes etapas:
a. poner en contacto una muestra biológica de Danio rerio con el anticuerpo según cualquiera de las reivindicaciones 1 a 4 o el antisuero según la reivindicación 5; y
b. detectar y/o cuantificar la unión específica a las IgM de Danio rerio que reconocen la proteína G del VHSV.
20. Método in vitro para para el cribado de fármacos que varían el número de anticuerpos IgM de Danio rerio que comprende las siguientes etapas:
a. poner en contacto una muestra biológica de Danio rerio con el anticuerpo según cualquiera de las reivindicaciones 1 a 4 o el antisuero según la reivindicación 5; y
b. detectar y/o cuantificar la unión específica.
21. Método in vitro para para el cribado de antígenos reconocidos por anticuerpos IgM de Danio rerio que comprende las siguientes etapas:
a. poner en contacto una muestra biológica de Danio rerio con el anticuerpo según cualquiera de las reivindicaciones 1 a 4 o el antisuero según la reivindicación 5; y
b. detectar y/o cuantificar la unión específica.
22. Método según cualquiera de las reivindicaciones 16 a 21 donde la detección y/o cuantificación se realiza mediante ELISA, western blot, inmunoquímica, inmunohistoquímica, inmunofluorescencia o citometría de flujo.
23. Método de obtención de un anticuerpo monoclonal que reconoce la cadena pesada del anticuerpo IgM de Danio rerio que comprende:
a. obtener el suero previamente extraído de un animal no-humano inmunizado con una proteína recombinante que comprende el péptido de secuencia SEQ ID NO: 1,
b. obtener un hibridoma a partir del suero que genere anticuerpos 5 monoclonales frente a la cadena pesada de los anticuerpos IgM de Danio
rerio.
24. Método según la reivindicación 23, que comprende además una etapa (c) de aislamiento del anticuerpo monoclonal a partir del hibridoma generado en la etapa
(b).
25. Método según cualquiera de las reivindicaciones 23 o 24, donde el animal no- humano es un mamífero que se selecciona de la lista que consiste en cerdo, chimpancé, ratón, rata, conejo y cobaya.
26. Kit o dispositivo que comprende el anticuerpo según cualquiera de las reivindicaciones 1 a 4, el antisuero según la reivindicación 5, la composición según la reivindicación 6 o la célula según cualquiera de las reivindicaciones 7 u 8.
27. Uso del kit o dispositivo según la reivindicación 26 para llevar a cabo el método
descrito en cualquiera de las reivindicaciones 16 a 22.
Patentes similares o relacionadas:
Anticuerpo biespecífico o mezcla de anticuerpos con cadenas ligeras comunes, del 15 de Julio de 2020, de Jiangsu Alphamab Biopharmaceuticals Co., Ltd: Anticuerpo biespecífico o parte de unión a antígeno del mismo, en el que el anticuerpo biespecífico o la parte de unión a antígeno del mismo tiene una cadena […]
Antígeno de superficie de células de cáncer de próstata para el diagnóstico, del 25 de Marzo de 2020, de Minomic International Ltd: Un método in vitro para detectar cáncer de próstata en un paciente, el método comprende medir el nivel de glipicano-1 soluble en una muestra de fluido corporal […]
ANTICUERPO MONOCLONAL ESPECÍFICO CONTRA EL ANTÍGENO N DEL VIRUS RESPIRATORIO SINCICIAL HUMANO (VRSH), ÚTILES PARA EL TRATAMIENTO DE LA INFECCIÓN, SU DETECCIÓN Y DIAGNÓSTICO, del 12 de Marzo de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención se refiere a un anticuerpo monoclonal o fragmento del mismo, que reconoce la proteína N (nucleocápside) del virus respiratorio sincicial humano (VRS), […]
ANTICUERPO MONOCLONAL 14F5F6 O FRAGMENTO DEL MISMO, QUE RECONOCE ESPECÍFICAMENTE VIRUS HERPES SIMPLE 1 Y 2, del 5 de Marzo de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La presente invención se refiere a un nuevo anticuerpo monoclonal o fragmento del mismo, denominado 14F5F6, que reconoce específicamente virus herpes […]
ANTICUERPO MONOCLONAL 11B2C7 O FRAGMENTO DEL MISMO, QUE RECONOCE ESPECÍFICAMENTE VIRUS HERPES SIMPLE 1 Y 2, del 5 de Marzo de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La presente invención se refiere a un nuevo anticuerpo monoclonal o fragmento del mismo, denominado 11B2C7, que reconoce específicamente virus herpes simple […]
Método para detectar cáncer, del 20 de Noviembre de 2019, de TORAY INDUSTRIES, INC.: Un método para detectar un cáncer, que comprende medir el nivel de expresión de CAPRINA-1 en una muestra biológica a través de una reacción de antígeno-anticuerpo […]
Anticuerpos anti péptido Beta Amiloide N3pGlu y usos de los mismos, del 13 de Noviembre de 2019, de ELI LILLY AND COMPANY: Un anticuerpo anti Aß N3pGlu que comprende una región variable de cadena ligera (LCVR) y una región variable de cadena pesada (HCVR), en el que LCDR1 es KSX1X2SLLYSRX3KTYLN […]
Inmunoensayo para la detección de cromogramina A, del 16 de Octubre de 2019, de CEZANNE S.A.S: Un método de inmunoensayo para la detección de cromogranina A o un fragmento de la misma que comprende las etapas de: a) poner en contacto […]