Terapia anticancerígena enzimática.
Una adenosina desaminasa conjugada a un polímero sustancialmente no antigénico para uso en el tratamiento de un tumor.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/060733.
Solicitante: Sigma-Tau Rare Diseases S.A.
Nacionalidad solicitante: Portugal.
Dirección: Rua dos Ferreiros no. 260 9000-082 Funchal PORTUGAL.
Inventor/es: SAPRA,PUJA, FILPULA,DAVID R.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12Q1/68 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
PDF original: ES-2507508_T3.pdf
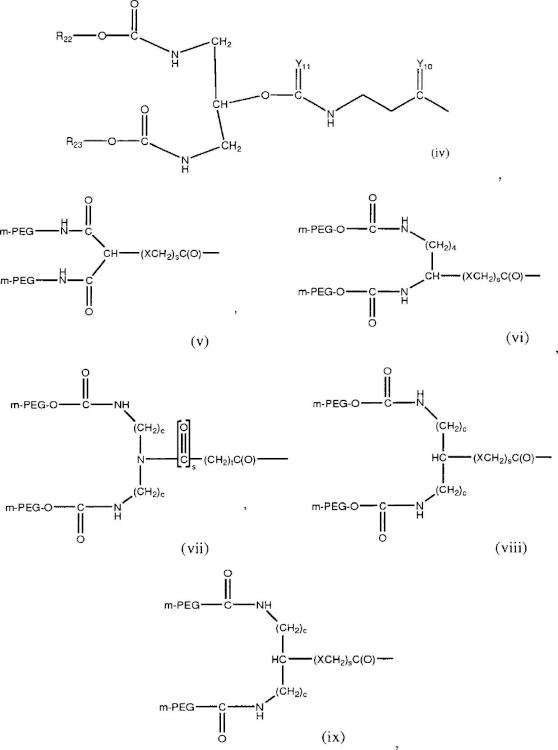
Fragmento de la descripción:
Terapia anticancerígena enzimática Campo de la invención La invención se refiere a adenosina desaminasa para uso en el tratamiento de tumores, especialmente de tumores malignos. En particular, dicho uso implica la reducción de los niveles en tejido de adenosina y desoxiadenosina. 5
Antecedentes de la invención Un tumor es un crecimiento anormal benigno o maligno de células o tejidos que surge de una proliferación celular descontrolada. Un tumor maligno es aquel que se extiende desde su sitio de origen, y en la técnica también se conoce como cáncer. Por tanto, los tumores y los cánceres son una familia de enfermedades que comparten la propiedad común de un crecimiento celular descontrolado o inapropiado. De forma general, los tumores malignos 10 son tumores derivados de la sangre, tales como la leucemia, o tumores sólidos. Los tumores malignos derivados de sangre generalmente circulan en la sangre, mientras que los tumores malignos sólidos se extienden a través del organismo desde un tumor primario. Las células tumorales distribuidas presentan entonces el potencial de desarrollarse en múltiples tumores secundarios, en un proceso de metástasis. Para que un tumor sólido se vea sometido a una extensión metastásica, las células del tumor sólido deben escapar del tumor primario u original, 15 entrar en la corriente sanguínea o el sistema linfático y a partir de ahí invadir el tejido de otros órganos, donde se multiplican y forman nuevos tumores. La metástasis es un proceso multi-etapa complejo que implica cambios en la adhesión y la movilidad de las células tumorales, la secreción de enzimas proteolíticas, quimioatractores y proteoglicanos, y otros factores. Adicionalmente, la angiogénesis, o la formación de nuevos vasos sanguíneos, también es una etapa vital en el proceso metastásico (Folkman, 1995, Nature Medicine 1: 27-31) . 20
También se ha demostrado que el sistema inmune inhibe la metástasis de dichas células tumorales malignas, y se ha publicado que la adenosina, a su vez, puede inhibir dichas reacciones protectoras inmunes. Por ejemplo, Loshkin et al., (2006, Cancer Res. 66: 7758-7765) han publicado que la adenosina inhibe la activación y la producción de citocinas en la producción de células T asesinas. La adenosina influye negativamente en otras funciones inmunes, que incluyen elementos celulares y funciones inflamatorias (véanse, p.ej., las revisiones de Spychala, 2000, 25 Pharmacology & Therapeutics 87: 161-173 y de Sitkovesky et al., 2005 Nature Reviews Immunology 5: 713-721) . Sitkovesky et al., en la solicitud de patente WO 03/050241, publicada el 19 de junio de 2003, también describieron métodos para aumentar la respuesta inmune a un antígeno y para tratar tumores, mediante la administración de un antagonista de receptor de adenosina, que puede incluir adenosina desaminasa.
También se ha demostrado que la adenosina promueve la migración de células tumorales y la angiogénesis (Barcz 30 et al., 2000, Oncol. Rep. 7 (6) : 1285-91; Adair, 2005, Am J Physiol Regul Integr Comp Physiol 289: R283-R296) y que la adenosina estimula la proliferación de células de cáncer de colon (Mujoomdar et al. 2003, Biochemical Pharmacology 66 1737-1747) . Asmar et al., 1966, Proc. Am. Assoc. Cancer Res. (Resumen nº 73) también han publicado que el crecimiento de determinadas células tumorales se vio inhibido por la inyección de ADA en más de un 50% en un modelo de ascitis de ratón. Se trataba de las leucemias linfáticas L1210 y L4946, el linfosarcoma 35 6C3HED, el adenocarcinoma mamario TA3 y el carcinoma de Ehrlich E2. En el mismo Resumen, se publicó que un adenocarcinoma 755 era el doble de resistente y un sarcoma 180 fue completamente resistente al efecto. La solicitud de patente WO03050241A2 describe los efectos de un inhibidor de receptores de adenosina sobre células de melanoma B16. Aunque el documento WO03050241A2 menciona ADA como inhibidor de adenosina, no se incluye ninguna descripción específica para aplicar ADA al tratamiento de cánceres específicos, y particularmente 40 cáncer de ovario y cáncer de próstata.
Por tanto, parece que para algunos tumores, la presencia de adenosina proporciona una señal de "arranque" para la proliferación tumoral y para la angiogénesis tumoral, y una señal de "parada" para las células T asesinas que normalmente matarían a estos tumores.
En contraposición a los descubrimientos discutidos anteriormente, Lind, et al. (Patente de EE.UU. nº 6.579.857) han 45 publicado que la adenosina, en combinación con un inhibidor de la enzima adenosina desaminasa, y/o en combinación con un agente anticancerígeno tal como la coformicina, es útil en un método para potenciar la muerte celular en células neoplásicas de origen epitelial. Por tanto, esta referencia sugiere que el papel de la adenosina en el cáncer es más complejo y no está establecido.
Tal como se ha indicado anteriormente, la enzima adenosina desaminasa es un agente para reducir los niveles de 50 adenosina endógena. La adenosina desaminasa ("ADA") , designada EC 3.5.4.4, es una enzima importante en la ruta de rescate de purina. La ADA convierte adenosina o desoxiadenosina, en presencia de agua, en inosina o desoxinosina y amoníaco. Es conocido que los individuos que albergan mutaciones perjudiciales en el gen de ADA pueden desarrollar grados variables de un trastorno de inmunodeficiencia, desde suave a severo, es decir trastorno de inmunodeficiencia combinada severa ("SCID") . Se ha confirmado que el SCID es el resultado de la acumulación 55 tóxica de los sustratos enzimáticos, adenosina y desoxiadenosina, en células linfoides inmaduras. El inicio del trastorno puede oscilar entre la infancia temprana y la edad adulta, dependiendo de las mutaciones heredadas. Las deficiencias en ADA son una de las causas principales del SCID, en niños, y es una de las dianas principales para las estrategias de terapia génica (R. Parkman et al., 2000, "Gene therapy for adenosine deaminase deficiency", Ann. Rev. Med., 51: 33-47) .
La ADA ha sido aislada comercialmente previamente a partir de fuentes bovinas y ha sido empleada en el tratamiento de una serie de trastornos, incluyendo el SCID, en la forma de una ADA bovina conjugada a polímero de polietilen glicol ("PEG") . La ADA PEGilada para uso médico se encuentra disponible comercialmente en Enzon 5 Pharmaceuticals, Inc. como ADAGEN®, PEGylated ADA. La conjugación de una función PEG con ADA permite que la enzima alcance su efecto terapéutico completo aumentando la vida en circulación y haciendo que la ADA sea sustancialmente no antigénica, a fin de minimizar el potencial de reacciones inmunogénicas. También es posible producir enzimas ADA recombinantes humanas o bovinas para uso en una forma conjugada, tal como se describe en la Solicitud de Patente de EE.UU. compartida con nº de serie 11/738.012, titulada "Stabilized Proteins", y en la 10 Solicitud de Patente de EE.UU. compartida nº 8.071.741, titulada "Stable Recombinant Adenosine Deaminase", presentada en una fecha uniforme con la presente y que reivindica beneficio de prioridad de la Solicitud de Patente de EE.UU. con nº de serie 60/913.009.
Por tanto, existe una necesidad antigua en la técnica de moléculas nuevas y mejoradas para uso en el tratamiento o en la inhibición del crecimiento, la extensión y el desarrollo de cánceres. 15
Compendio de la invención Por consiguiente, la invención se refiere a ADA para uso en el tratamiento de un tumor en un paciente que lo necesite. Una cantidad efectiva es aquella que se determina fácilmente por parte del especialista en la técnica para reducir los niveles en tejido de adenosina o desoxiadenosina en el paciente, y donde se inhibe el crecimiento o la extensión del tumor mediante niveles en tejido sustancialmente reducidos de adenosina en el paciente. La ruta de 20 administración es una ruta tal como subcutánea, intravenosa, intramuscular, intratecal, intraperitoneal, inhalación y transuretral.
El tumor puede ser maligno o no maligno, y preferiblemente es un tumor sólido, p.ej., un tumor tal como un tumor de próstata, un cáncer de ovario y/o un cáncer colorrectal.
La adenosina desaminasa se conjuga preferiblemente con un polímero sustancialmente no antigénico, tal como 25 polióxido de alquileno (PAO) . El PAO preferiblemente oscila en tamaño entre aproximadamente 4.000 y aproximadamente 45.000 Daltons. Preferiblemente el PAO es un polietilen glicol ("PEG") . La relación molar de ADA a polímero puede ser de 1:1, o puede ser de dos o más moléculas por polímero, o más preferiblemente, proporciona entre aproximadamente 1 y aproximadamente 20 moléculas de polímero (es decir, cadenas de PEG de 11-18 unidades) por cada molécula de ADA. 30
La dosis de ADA conjugada a polímero... [Seguir leyendo]
Reivindicaciones:
1. Una adenosina desaminasa conjugada a un polímero sustancialmente no antigénico para uso en el tratamiento de un tumor.
2. La adenosina desaminasa para uso de la reivindicación 1, para uso para reducir sustancialmente los niveles en tejido de adenosina o desoxiadenosina, y donde el crecimiento o la extensión del tumor son inhibidos por los niveles 5 reducidos de adenosina.
3. La adenosina desaminasa para uso de la reivindicación 1, donde el tumor es un tumor sólido.
4. La adenosina desaminasa para uso de la reivindicación 1, donde el tumor se selecciona del grupo que consiste en tumor de próstata, cáncer de ovario y cáncer colorrectal.
5. La adenosina desaminasa para uso de la reivindicación 4, donde el tumor se selecciona del grupo que consiste en 10 tumor de próstata y cáncer de ovario.
6. La adenosina desaminasa para uso de la reivindicación 1, donde el polímero sustancialmente no antigénico es un polióxido de alquileno.
7. La adenosina desaminasa para uso de la reivindicación 6, donde el polióxido de alquileno es polietilen glicol.
8. La adenosina desaminasa para uso de la reivindicación 6, donde el polímero sustancialmente no antigénico oscila 15 en tamaño entre aproximadamente 4.000 y aproximadamente 45.000 Daltons.
9. La adenosina desaminasa para uso de la reivindicación 1, donde la dosis de adenosina desaminasa conjugada oscila entre aproximadamente 10U y aproximadamente 30U por kg.
10. La adenosina desaminasa para uso de la reivindicación 1, donde el uso de adenosina desaminasa es para un periodo de tiempo que oscila entre 1 y aproximadamente 20 días. 20
11. La adenosina desaminasa para uso de la reivindicación 1, donde el conjugado comprende dos o más moléculas de adenosina desaminasa por polímero sustancialmente no antigénico.
12. La adenosina desaminasa para uso de la reivindicación 1, donde la adenosina desaminasa comprende entre aproximadamente 11 y aproximadamente 18 cadenas de polietilen glicol unidas a grupos amino épsilon de uno o más residuos de Lys de la adenosina desaminasa. 25
13. La adenosina desaminasa para uso de la reivindicación 6 ó 12, donde la adenosina desaminasa está conjugada al polietilen glicol vía un enlace de uretano.
14. La adenosina desaminasa para uso de la reivindicación 1, donde la adenosina desaminasa es una adenosina desaminasa purificada a partir de una fuente bovina o es una adenosina desaminasa recombinante.
15. La adenosina desaminasa para uso de la reivindicación 14, donde la adenosina desaminasa recombinante se 30 selecciona del grupo que consiste en adenosina desaminasa recombinante que comprende la SEQ ID NO: 1, adenosina desaminasa humana recombinante que comprende la SEQ ID NO: 3 y una adenosina desaminasa recombinante bovina que comprende la SEQ ID NO.
5.
16. La adenosina desaminasa para uso de la reivindicación 1 ó 15, donde la adenosina desaminasa recombinante es adenosina desaminasa recombinante bovina que comprende la SEQ ID NO: 1. 35
17. La adenosina desaminasa para uso de la reivindicación 1 ó 15, donde la adenosina desaminasa recombinante es adenosina desaminasa recombinante bovina que comprende la SEQ ID NO: 5.
18. La adenosina desaminasa para uso de cualquiera de las reivindicaciones 15-17, donde la adenosina desaminasa bovina recombinante que comprende la SEQ ID NO: 5 comprende una Cys74 que está tapada para prevenir la oxidación en un medio acuoso. 40
19. La adenosina desaminasa para uso de cualquiera de las reivindicaciones 15-17, donde la adenosina desaminasa recombinante es según la SEQ ID NO: 1 ó la SEQ ID NO: 5, con una sustitución de aminoácido seleccionada del grupo que consiste en Gln en lugar de Lys198; Ala en lugar de Thr245; Arg en lugar de Gly351, y combinaciones de las mismas.
Patentes similares o relacionadas:
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]
MÉTODOS PARA EL DIAGNÓSTICO DE ENFERMOS ATÓPICOS SENSIBLES A COMPONENTES ALERGÉNICOS DEL POLEN DE OLEA EUROPAEA (OLIVO), del 23 de Julio de 2020, de SERVICIO ANDALUZ DE SALUD: Biomarcadores y método para el diagnostico, estratificación, seguimiento y pronostico de la evolución de la enfermedad alérgica a polen del olivo, kit […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Secuenciación dirigida y filtrado de UID, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento para generar una biblioteca de polinucleótidos que comprende: (a) generar una primera secuencia del complemento (CS) de un polinucleótido diana a partir […]
Métodos para la recopilación, estabilización y conservación de muestras, del 8 de Julio de 2020, de Drawbridge Health, Inc: Un método para estabilizar uno o más componentes biológicos de una muestra biológica de un sujeto, comprendiendo el método obtener un […]
Evento de maíz DP-004114-3 y métodos para la detección del mismo, del 1 de Julio de 2020, de PIONEER HI-BRED INTERNATIONAL, INC.: Un amplicón que consiste en la secuencia de ácido nucleico de la SEQ ID NO: 32 o el complemento de longitud completa del mismo.
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Aislamiento de ácidos nucleicos, del 24 de Junio de 2020, de REVOLUGEN LIMITED: Un método de aislamiento de ácidos nucleicos que comprenden ADN de material biológico, comprendiendo el método las etapas que consisten en: (i) efectuar un lisado […]