Línea celular, sistema y procedimiento para el control óptico de mensajeros secundarios.
Ácido nucleico que codifica una proteína de membrana quimérica de base rodopsina sensible a la luz con una o más subunidades de receptor heterólogo que responde a un estímulo óptico desencadenando la liberación de un mensajero secundario en el interior de dicha célula,
en el que dicha una o más subunidades de receptor heterólogo incluye un receptor adrenérgico,
para utilizar en un procedimiento de tratamiento de un mamífero, en el que dicho tratamiento comprende dirigir genéticamente dicho ácido nucleico a una célula y estimular ópticamente la célula.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E13160448.
Solicitante: THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1705 EL CAMINO REAL PALO ALTO, CA 94306-1106 ESTADOS UNIDOS DE AMERICA.
Inventor/es: AIRAN,RAAG D, DEISSEROTH,KARL.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12P21/04 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Péptidos o polipéptidos cíclicos o puenteados, p. ej. bacitracina.
- C12P21/06 C12P 21/00 […] › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
PDF original: ES-2532235_T3.pdf
Fragmento de la descripción:
Línea celular, sistema y procedimiento para el control óptico de mensajeros secundarios 5 Documento de patente relacionado Campo de la Invención
[0001] La presente Invención se refiere generalmente a sistemas y estrategias para generar mensajeros 10 secundarios en respuesta al estímulo óptico y, más particularmente, a líneas celulares, secuencias nucleotídicas,
proteínas quiméricas y usos de las mismas, cada una relacionada con la producción de mensajeros secundarios en respuesta a la luz.
Antecedentes
[0002] Se cree que las proteínas de unión a nucleótidos de guanina (proteínas G) alternan entre un estado de difosfato de guanosina (GDP) Inactivo y un estado unido a trifosfato de guanosina (GTP) activo. Estos dos estados se han vinculado a la liberación de un mensajero secundario dentro de una célula. El mensajero secundario liberado puede funcionar para regular los procesos celulares cascada abajo.
[0003] Los mensajeros secundarios incluyen moléculas de señalización que se generan/liberan rápidamente. Estas moléculas producen respuestas celulares al activar las proteínas efectoras dentro de la célula. Los sistemas de señalización celulares ejemplares incluyen el sistema de fosfoinositol, el sistema de monofosfato de adenosina cíclico (cAMP) y el sistema de ácido araquidónico.
[0004] Los cambios entre los diferentes estados de las proteínas G se pueden desencadenar como un resultado de proteínas denominadas receptores acoplados a proteína G (GPCR), receptores unidos a proteína G (GPLR), receptores de siete dominios de transmembrana (receptores 7TM) o receptores heptahelicoidales. Esta familia de proteínas incluye una diversidad de receptores transmembrana. Estos receptores responden a los
estímulos externos (por ejemplo, luz, neurotransmisores, olores u hormonas) activando las rutas de transducción de señal internas a la célula. Específicamente, los ligandos unen y activan las rutas de transducción causando en consecuencia que las proteínas G alternen los estados. La actividad relacionada con GPCR se asocia con muchas enfermedades y, de esta manera, los GPCR son el objetivo de muchos productos farmacéuticos y tratamientos.
[0005] Se cree que más del 30% de todos los fármacos en el mercado se dirigen a los receptores acoplados a la proteína G (GPCR) y que muchos de esos fármacos se relacionan con la producción o inhibición del mensajero secundario cAMP. Existe una abundancia de procesos patológicos que implican directamente el cAMP, incluyendo enfermedades neurofisiológicas, endocrinológicas, cardiacas, metabólicas e inmunes. En el estudio de comportamientos de mamífero complejos, las limitaciones tecnológicas han impedido un control espacio- 40 temporalmente preciso sobre los procesos de señalización intracelular. Los procedimientos basados en productos químicos actuales para modular los niveles de mensajeros secundarios, tales como niveles de cAMP, operan relativamente de manera lenta y presentan problemas para estudiar la actividad en las escalas de tiempo rápido que el cuerpo usa en conexión con cierto tejido, tal como en el tejido nervioso cardiaco. Estos procedimientos químicos carecen frecuentemente de la velocidad para sondear estas escalas de tiempo rápido (por ejemplo, mientras que se 45 clasifican para productos terapéuticos novedosos).
[0006] L¡ y col., (Proc. Nati. Acad. Sci., USA (2005), 102; 17816-17821) describe una activación e inhibición rápida no invasiva de la actividad neural y de red por la rodopsina de vertebrados y la rodopsina-canal de algas verdes.
Descripción resumida de la Invención
[0007] La presente invención se dirige a superar los retos que se han mencionado anteriormente y otros relacionados con la generación de mensajeros secundarios y dispositivos de formación de imágenes relacionados y
sus implementaciones. La presente invención se define en las reivindicaciones que se acompañan y se ilustra en varias implementaciones y aplicaciones, algunas de las cuales se resumen a continuación.
[0008] En concordancia con una realización de la presente invención, se implementa un procedimiento para generar mensajeros secundarios en una célula. Se modifica una secuencia nucleotídica para expresar una proteína
de membrana quimérica sensible a la luz (por ejemplo, rodopslna) con una o más subunldades de receptor adrenérgico {por ejemplo, alfal, Beta2}. La proteína de membrana sensible a la luz se expresa en una célula para producir un mensajero secundario en respuesta a la luz.
[0009] En concordancia con una realización de la presente invención, se implementa un procedimiento para evaluar la eficacia de un posible régimen de tratamiento (por ejemplo, un fármaco o estimulo eléctrico o cualquiera que funcione a través de estos mensajeros secundarios) en relación con mensajeros intracelulares. Se modifica una secuencia nucleotídica para expresar una proteína de membrana quimérica sensible a la luz (rodopsina) con una o más subunidades de receptor adrenérgico {por ejemplo, alfal, Beta2}. La proteína de membrana sensible a la luz se 10 expresa en una célula para producir un mensajero secundario en respuesta a la luz. La proteína se expone a la luz. Se evalúan los efectos del tratamiento.
[0010] Una realización de la presente memoria se dirige a una célula que expresa una proteína de membrana quimérica sensible a luz (rodopsina) con una o más subunidades de receptor adrenérgico {por ejemplo, alfal,
Beta2}.
[0011] Una realización de la presente memoria se dirige a una secuencia nucleotídica para expresar una proteína de membrana quimérica sensible a la luz (rodopsina) con una o más subunidades de receptor adrenérgico {por ejemplo, alfal, Beta2}.
[0012] El resumen anterior de la presente invención no pretende describir cada realización ilustrada o cada implementación de la presente invención. Las figuras y la descripción detallada que se indican a continuación ejemplifican más particularmente estas realizaciones.
Breve Descripción de los Dibujos
[0013] La invención se puede entender más completamente en consideración de la descripción detallada de diversas realizaciones de la invención que se indican a continuación junto con los dibujos adjuntos, en los que:
la figura 1A muestra una representación esquemática que muestra optoGs y optoGq, consistentes con las 30 realizaciones ejemplares de la presente invención;
la figura 1B muestra el Ensayo Inmunoabsorbente Ligando a Enzimas (ELISA) de cAMP, cGMP e IP1 de células transfectadas con ya sea nada, optoGs u optoGq, consistentes con las realizaciones ejemplares de la presente
invención;
la figura 1C muestra la formación de imágenes de Ca de células transfectadas con proteínas de fusión mCherry de 35 optoGs y optoGq, consistentes con las realizaciones ejemplares de la presente invención;
la figura 2 la formación de imágenes de Ca de células transfectadas con las proteínas de fusión mCherry de optoGs y optoGq, consistentes con las realizaciones ejemplares de la presente invención;
la figura 3A muestra los niveles de cAMP, IPi e IP3 para las células HEK que expresan diversas construcciones, consistentes con las realizaciones ejemplares de la presente invención;
la figura 3B muestra un vector de expresión lentívíral, inmunotinción GAD de células que expresan opto-atAR y la activación pCREB observada en células que expresan optoXR (mCherry+) después de 10 min de estimulación óptica, consistentes con las realizaciones ejemplares de la presente invención;
la figura 4A muestra el objetivo de optrodo de accumbens traducidos, formas de onda pico y velocidad de disparo de línea basal para construcciones indicadas, consistentes con las realizaciones ejemplares de la presente invención;
la figura 4B muestra registros de optrodos in vivo con estimulación de luz, consistentes con las realizaciones ejemplares de la presente invención;
la figura 4C muestra el cambio en la frecuencia pico con la luz frente a la línea basal, consistentes con las realizaciones ejemplares de la presente invención;
la figura 4D muestra la cinética de cambio de velocidad de disparo, consistente con las realizaciones ejemplares de
la presente invención;
la figura 5A muestra el objetivo estereotáctico de una región transducida, un ratón que se mueve libremente con fibras ópticas implantadas, una representación esquemática del lugar del aparato de preferencia y prueba y un rastro de un ratón que se mueve libremente, consistente con las realizaciones ejemplares de la presente invención; la figura 5B muestra preferencias para el control y opto-ouAR, consistentes con las realizaciones... [Seguir leyendo]
Reivindicaciones:
I. Ácido nucleico que codifica una proteína de membrana quimérica de base rodopsina sensible a la luz con una o más subunidades de receptor heterólogo que responde a un estímulo óptico desencadenando la liberación de un
mensajero secundario en el interior de dicha célula, en el que dicha una o más subunidades de receptor heterólogo incluye un receptor adrenérgico,
para utilizar en un procedimiento de tratamiento de un mamífero, en el que dicho tratamiento comprende dirigir genéticamente dicho ácido nucleico a una célula y estimular ópticamente la célula.
2. Ácido nucleico para utilizar, según la reivindicación 1, en el que dicho ácido nucleico comprende además un promotor específico de célula expresado en una célula de mamífero.
3. Ácido nucleico para utilizar, según la reivindicación 1 ó 2, en el que dicho ácido nucleico se expresa en una célula de mamífero.
4. Ácido nucleico para utilizar, según cualquiera de las reivindicaciones anteriores, en el que dicha célula está modificada para expresar un canal catiónico dirigido al mensajero secundario que es sensible al segundo mensajero.
5. Ácido nucleico para utilizar, según cualquiera de las reivindicaciones anteriores, en el que el receptor adrenérgico 20 es un receptor adrenérgico alfal o un receptor adrenérgico beta2.
6. Ácido nucleico para utilizar, según cualquiera de las reivindicaciones anteriores, en el que la proteína de membrana quimérica de base rodopsina sensible a la luz es una proteína de siete dominios transmembrana.
7. Ácido nucleico para utilizar, según cualquiera de las reivindicaciones anteriores, en el que el mensajero secundario es uno entre cAMP, guanosín monofosfato cíclico (cGMP), trifosfato de inositol/1,4,5-trifosfato de inositol/trifosfoinositol (IP3) y ácido araquidónico.
8. Ácido nucleico para utilizar, según cualquiera de las reivindicaciones anteriores, en el que la proteína de 30 membrana quimérica de base rodopsina sensible a la luz comprende una secuencia de aminoácidos que tiene al
menos un 90% de homología en la secuencia de aminoácidos con la secuencia de aminoácidos según la SEQ ID
NO: 2 o la SEQ ID NO: 4.
9. Mamífero transgénico no humano que comprende una célula que expresa una proteína de membrana quimérica 35 de base rodopsina sensible a la luz con una o más subunidades de receptor heterólogo que responde a un estímulo
óptico desencadenando la liberación de un mensajero secundario en el interior de dicha célula, en el que dicha una o más subunidades de receptor heterólogo incluye un receptor adrenérgico,
10. Mamífero transgénico no humano, según la reivindicación 9, en el que dicho ácido nucleico comprende además 40 un promotor específico de célula expresado en una célula de mamífero.
II. Mamífero transgénico no humano, según la reivindicación 9, en el que dicha célula está modificada para expresar un canal catiónico dirigido al mensajero secundario que es sensible al segundo mensajero.
12. Mamífero transgénico no humano, según la reivindicación 9, 10 u 11, en el que el receptor adrenérgico es un receptor adrenérgico alfal o un receptor adrenérgico beta2.
13. Mamífero transgénico no humano, según la reivindicación 9, 10 u 11, en el que la proteína de membrana quimérica de base rodopsina sensible a la luz es una proteína de siete dominios transmembrana.
14. Mamífero transgénico no humano, según cualquiera de las reivindicaciones 9 a 13, en el que el mensajero secundario es uno entre cAMP, guanosín monofosfato cíclico (cGMP), trifosfato de inositol/1,4,5-trifosfato de inositol/trifosfoinositol (IP3) y ácido araquidónico.
15. Mamífero transgénico no humano, según cualquiera de las reivindicaciones 9 a 14, en el que la proteína de membrana quimérica de base rodopsina sensible a la luz comprende una secuencia de aminoácidos que tiene al menos un 90% de homología en la secuencia de aminoácidos con la secuencia de aminoácidos según la SEQ ID NO: 2 o la SEQ ID NO: 4.
16. Mamífero transgénico no humano, según cualquiera de las reivindicaciones 9 a 15, que es un ratón.
17. Procedimiento para evaluar la eficacia de un posible régimen de tratamiento relacionado con mensajeros intracelulares, comprendiendo el procedimiento:
proporcionar el animal transgénico no humano, según cualquiera de las reivindicaciones 9 a 16, que tiene una proteína de membrana de base rodopsina sensible a la luz; estimular ópticamente dicha proteína sensible a la luz; y evaluar los efectos del tratamiento cuando la proteína se expone a la luz.
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Composiciones y métodos para inmunomodulación en un organismo, del 19 de Febrero de 2020, de UNIVERSITY OF CONNECTICUT: Una composicion para su uso en un metodo de (i) tratamiento de cancer en un ser humano; (ii) mejora de la vacunacion en un ser humano; (iii) aumento de las respuestas […]
CD33 soluble para tratar síndromes mielodisplásicos (MDS), del 8 de Enero de 2020, de H. Lee Moffitt Cancer Center And Research Institute, Inc: Una proteína de fusión recombinante quimérica, que comprende: (a) una combinación de al menos dos fracciones de unión a S100A9 seleccionados de entre el grupo que […]
Métodos para la diferenciación y transducción in vitro de células b de memoria con vectores virales pseudotipados vsv-g, del 1 de Enero de 2020, de Immusoft Corporation: Un método in vitro para expresar un ácido nucleico de interés en una célula B, que comprende (a) poner en contacto células B de memoria con una composición que comprende […]
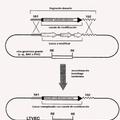 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Intercambio de casetes de la región variable de la inmunoglobulina, del 12 de Junio de 2019, de Humanigen, Inc: Un método de modificación genética de un anticuerpo que retiene la especificidad de unión de un anticuerpo de referencia con un antígeno diana, comprendiendo el método: […]
Procedimiento de modificar células eucariotas, del 3 de Abril de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento de reemplazar in situ, en parte, en una célula madre embrionaria (ES) de ratón, un locus génico endógeno de región variable de […]
Diacuerpos covalentes y usos de los mismos, del 2 de Abril de 2019, de MACROGENICS, INC: Una molécula de diacuerpo que comprende una primera cadena polipeptídica y una segunda cadena polipeptídica, en la que: (a) dicha primera cadena […]