Alérgeno producido de manera recombinante.
Un alérgeno Can f 4 producido de manera recombinante que tiene una secuencia de aminoácidos de acuerdo con el SEQ ID NO: 2.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/SE2010/050623.
Solicitante: PHADIA AB.
Nacionalidad solicitante: Suecia.
Dirección: BOX 6460 751 37 UPPSALA SUECIA.
Inventor/es: LIDHOLM,JONAS, LUNDGREN,THOMAS, MATTSSON,LARS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/35 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Alergenos.
- A61P11/06 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 11/00 Medicamentos para el tratamiento de trastornos del aparato respiratorio. › Antiasmáticos.
- A61P37/08 A61P […] › A61P 37/00 Medicamentos para el tratamiento de problemas inmunológicos o alérgicos. › Agentes antialérgicos (agentes antiasmáticos A61P 11/06; antialérgicos oftálmicos A61P 27/14).
- C07K14/47 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de mamíferos.
- C12N15/63 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Introducción de material genético extraño utilizando vectores; Vectores; Utilización de huéspedes para ello; Regulación de la expresión.
- C12N15/86 C12N 15/00 […] › Vectores virales.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/68 G01N 33/00 […] › en los que intervienen proteínas, péptidos o aminoácidos.
PDF original: ES-2505245_T3.pdf



Fragmento de la descripción:
Alérgeno producido de manera recombinante Campo de la invención La presente invención se refiere al campo de la alergia. Más específicamente, la invención se refiere a la identificación de nuevos alérgenos de mamíferos y al diagnóstico y tratamiento de la alergia a mamíferos.
Antecedentes La caspa de perro es una causa común de alergia de interiores con síntomas que incluyen rinitis, conjuntivitis, inflamación bronquial y asma. Los alérgenos de perro se pueden detectar no sólo en las viviendas donde los perros son mantenidos como mascotas, sino también en otros lugares, como escuelas y centros de día donde los perros no están presentes de forma regular [1].
La alergia al perro se acompaña y depende de la sensibilización a las proteínas liberadas por pelos y caspa de perro. En los casos de sospecha de alergia a perros, la investigación clínica incluye la evaluación de la sensibilización por el pinchazo de la piel o la medición de anticuerpos IgE específicos utilizando extracto de pelo y/o caspa de perro. Un inmunoanálisis de laboratorio para IgE específica, tal como Phadia ImmunoCAP™, puede detectar la mayoría de los casos de sensibilización a perro utilizando extracto natural de caspa de perro, debido a las favorables condiciones de análisis y a una gran fase sólida disponible para el anclaje del alérgeno.
Los extractos de pelo y caspa de perro contienen una complejidad de proteínas alergénicas y no alergénicas [2, 3]. Hasta ahora se han identificado y estudiado en detalle cuatro alérgenos de perro: Can f 1, Can f 2, Can f 3 y Can f 5 [4-6]. Los dos primeros son ambos miembros de la familia de proteínas de lipocalina y se han purificado y expresado como proteínas recombinantes [4, 7]. Can f 3, albúmina de suero perro, es una proteína relativamente conservada que muestra considerable reactividad cruzada con otras albúminas de mamíferos [8]. Can f 5, calicreína prostática de perro, se ha descrito recientemente como un alérgeno principal de perro y muestra reacción cruzada con el antígeno específico de próstata humano (PSA) [5].
De los alérgenos de caspa de perro conocidos hasta la fecha, Can f 1 y Can f 5 parecen ser los más importantes, uniéndose a anticuerpos IgE de aproximadamente 50% y 70% de los sujetos alérgicos al perro, respectivamente [5, 9]. Aunque aproximadamente 20-40% de los individuos adultos alérgicos al perro presenta unión del anticuerpos IgE a Can f 2 o Can f 3, pocos parecen reaccionar exclusivamente o incluso predominantemente a cualquiera de estos alérgenos [5, 9]. En un estudio recientemente referido, se encontró que una pequeña proporción de pacientes alérgicos al perro no presentaba unión del anticuerpo IgE a ninguno de Can f 1, Can f 2, Can f 3 y Can f 5, a pesar de estar sensibilizados a extracto de caspa natural de perro [5].
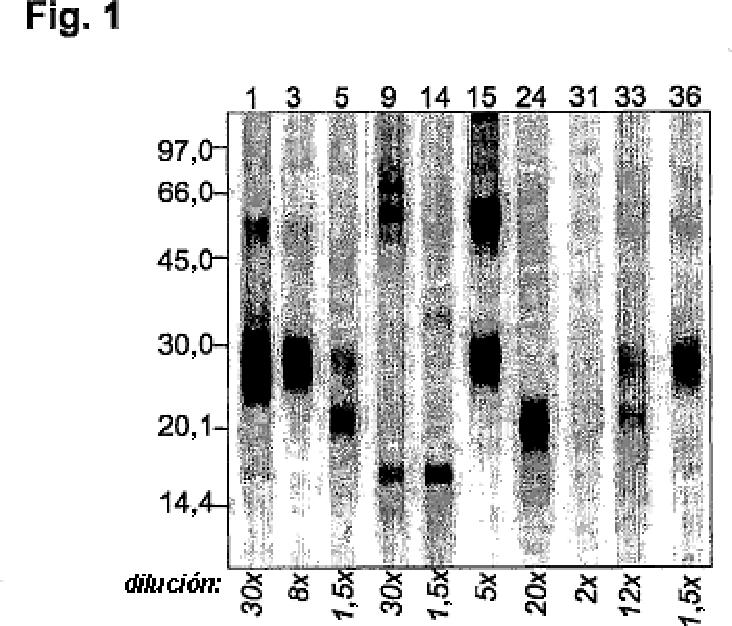
Además de los alérgenos mencionados anteriormente, se ha informado sobre una proteína de tipo lipocalina de 18 kDa, reactiva con IgE, distinta de Can f 1 y Can f 2, y se ha denominado Can f 4 [9]. Se informó de que 15 de 25 (60%) pacientes alérgicos al perro presentaban reactividad de IgE en suero con esta banda de 18 kDa en la inmunotransferencia, haciendo de ésta un componente potencialmente importante de alérgeno perro. Sin embargo, el alérgeno sólo se ha caracterizado como una secuencia N-terminal de 13 de aminoácidos a partir de un gel de SDS PAGE, una secuencia que no produce emparejamientos con ninguna otra secuencia de proteína conocida de perro. La secuencia de proteína completa es por tanto desconocida, y no se ha llevado a cabo la clonación de una proteína recombinante. Tampoco se ha purificado la proteína nativa, y no se ha proporcionado ninguna sugerencia en cuanto a cómo se podría completar la clonación de Can f 4.
En un resumen de Saarelainen et al. publicado en Abstract Book of 3rd International Symposium on Molecular Allegology en Salzburgo, de 18 a 20 de Abril de 2008, se establece que un mAb específico de Can f 4 reconocía una proteína de 20 kDa en un extracto de caspa de vaca.
En una edición especial de la revista científica Allergy que publica los resúmenes del XXVIII Congress of the European Academy of Allergy and Clinical Immunology (EAACI) en Varsovia de 6 a 10 de Junio de 2009, existe un resumen que describe que se ha clonado un ADNc que codifica Can f 4 completo [Allergy 64 (Supl. 90) : 179-538) . Sin embargo no se indica sobre cómo se podría lograr esta clonación y no se proporciona ninguna secuencia de ácido nucleico o de aminoácidos.
El registro de la base de datos de NCBI Protein XP_581277, introducido el 30 de Septiembre 2005, contiene una proteína de tipo proteína de unión a odorante pronosticada de 172 aminoácidos. La secuencia se proporciona en esta solicitud como SEQ ID NO: 4.
Compendio de la invención Los autores de la presente invención han identificado la necesidad en la técnica de una caracterización y validación adicionales de la trascendencia del alérgeno Can f 4.
Como se ha establecido anteriormente, un inmunoanálisis de laboratorio para la IgE específica puede detectar la mayoría de los casos de sensibilización a perros utilizando extracto natural caspa de perro, debido a las condiciones de análisis favorables y a una gran fase sólida disponible para el anclaje del alérgeno. Sin embargo, en un inmunoanálisis miniaturizado o no de laboratorio, tal como una micromatriz de alérgeno o una prueba de consultorio médico, se ha encontrado que la combinación de condiciones de análisis menos favorables, menor capacidad de unión al anticuerpo del reactivo alérgeno y un extracto de alérgeno natural de potencia limitada, causan una sensibilidad insuficiente del diagnóstico. Una situación similar puede existir también para inmunoanálisis para IgE específica para otros epitelios de animales. De este modo, existe la necesidad en algunos casos de utilizar proteínas alergénicas puras para conseguir suficiente sensibilidad en los ensayos de diagnóstico para IgE específica. Otra necesidad para el uso de componentes de alérgenos recombinantes está dada por el concepto de diagnóstico resuelto por componentes [24]. De acuerdo con este concepto, el análisis de la respuesta de IgE a componentes de alérgenos individuales en lugar de extractos de alérgenos completos permite una mejor distinción entre las sensibilizaciones cruzadas de los alérgenos y las sensibilizaciones originales los alérgenos. De este modo, existe la necesidad de identificar y producir como proteína recombinante todos los componentes potenciales de alérgenos a partir de una fuente de alérgeno concreta.
Los presentes autores de la presente invención experimentaron problemas cuando trataron de secuenciar y clonar Can f 4 mediante el uso de métodos convencionales conocidos en la técnica. Los problemas solo se resolvieron mediante el uso de métodos no convencionales, como se describe a continuación en la sección Resultados. La presente invención se basa en el hallazgo inesperado de la unión del anticuerpo IgE a extracto de caspa tanto de perro como de vaca, y la comprensión de que a fin de identificar la secuencia de ácido nucleico y para completar la clonación de Can f 4, los autores de la presente invención tuvieron que correlacionar Can f 4 con una proteína de otro organismo.
En un aspecto, la invención se refiere a un alérgeno Can f 4 producido de manera recombinante que tiene una secuencia de aminoácidos de acuerdo con el SEQ ID NO: 2.
En otro aspecto, la invención se refiere a un ácido nucleico que codifica dicho alérgeno Can f 4 producido de manera recombinante.
En otros aspectos, la invención se refiere a un vector que comprende dicho ácido nucleico, y a una célula anfitriona que comprende dicho vector.
En otro aspecto más, la invención se refiere al uso de un alérgeno Can f 4 producido de manera recombinante en un diagnóstico in vitro de alergia de tipo I.
Otro aspecto de la invención se refiere a un método para producir una composición de alérgeno, que comprende la etapa de añadir un alérgeno Can f 4 producido de manera recombinante a una composición que comprende un extracto de alérgeno y/o al menos un componente de alérgeno purificado.
En otro aspecto más, la invención se refiere a un método de diagnóstico in vitro para diagnosticar una alergia de tipo I en un paciente, en donde una muestra de fluido corporal tal como una muestra de sangre o suero del paciente se pone en contacto con un alérgeno Can f 4 producido de manera recombinante, y se detecta si la muestra del paciente contiene o no anticuerpos IgE que se unen específicamente al alérgeno Can f 4 producido de manera recombinante, en donde la presencia de tales anticuerpos IgE que se unen específicamente... [Seguir leyendo]
Reivindicaciones:
1. Un alérgeno Can f 4 producido de manera recombinante que tiene una secuencia de aminoácidos de acuerdo con el SEQ ID NO: 2.
2. Una molécula de ácido nucleico que codifica el alérgeno Can f 4 de acuerdo con la reivindicación 1.
3. La molécula de ácido nucleico de acuerdo con la reivindicación 2, que tiene la secuencia de acuerdo con el SEQ ID NO: 1.
4. Un vector que comprende la molécula de ácido nucleico de acuerdo con la reivindicación 2 o 3.
5. Una célula anfitriona que comprende el vector de acuerdo con la reivindicación 4.
6. Un alérgeno Can f 4 producido de manera recombinante que tiene una secuencia de aminoácidos de acuerdo con los residuos de aminoácido 17-174 del SEQ ID NO: 2.
7. El uso del alérgeno Can f 4 producido de manera recombinante de acuerdo con la reivindicación 1, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con dicho alérgeno Can f 4, en un diagnóstico in vitro de alergia de tipo I.
8. Un método para el diagnóstico in vitro de alergia tipo I que comprende las etapas
-Poner en contacto una muestra de fluido corporal de un paciente que se sospecha que tiene alergia de tipo I con el alérgeno Can f 4 producido de manera recombinante de acuerdo con la reivindicación 1, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con el alérgeno Can f 4; y
-Detectar la presencia, en la muestra, de anticuerpos IgE que se unen específicamente a dicho alérgeno Can f 4, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con el alérgeno Can f 4,
en donde la presencia de tales anticuerpos IgE que se unen específicamente a dicho alérgeno Can f 4, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con el alérgeno Can f 4, es indicativa de una alergia de tipo I.
9. Un kit de diagnóstico para realizar el método de acuerdo con la reivindicación 8, que comprende el alérgeno Can f 4 producido de manera recombinante de acuerdo con la reivindicación 1, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con el alérgeno Can f 4.
10. Un alérgeno Can f 4 producido de manera recombinante de acuerdo con la reivindicación 1, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con el alérgeno Can f 4, para su uso en un método para el tratamiento de una alergia de tipo I a un mamífero, preferiblemente en donde el mamífero es canino.
11. El uso de un alérgeno Bos d 23k producido de manera recombinante que tiene una secuencia de aminoácidos de acuerdo con el SEQ ID NO: 4, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con el alérgeno Bos d 23k, en un diagnóstico in vitro de alergia de Tipo I.
12. Método para el diagnóstico in vitro de alergia de tipo I que comprende las etapas
-Poner en contacto una muestra de fluido corporal de un paciente que se sospecha que tiene alergia de tipo I con un alérgeno Bos d 23k producido de manera recombinante que tiene una secuencia de aminoácidos de acuerdo con el SEQ ID NO: 4, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con el alérgeno Bos d 23k ; y
-Detectar la presencia, en la muestra, de anticuerpos IgE que se unen específicamente a dicho alérgeno Bos d 23k, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con el alérgeno Bos d 23k,
en donde la presencia de tales anticuerpos IgE que se unen específicamente a dicho alérgeno Bos d 23k, o un fragmento del mismo que comparte epítopos para los anticuerpos IgE con el alérgeno Bos d 23k, es indicativa de una alergia de tipo I.
13. Un alérgeno Bos d 23k producido de manera recombinante que tiene una secuencia de aminoácidos de acuerdo con el SEQ ID NO: 4, o un fragmento del mismo que comparte epítopos para anticuerpos IgE con el alérgeno Can f 4, para su uso en un método para el tratamiento de una alergia de tipo I a un mamífero, preferiblemente en donde el mamífero es bovino.
Patentes similares o relacionadas:
Método y medios para purificar vectores retrovíricos, del 29 de Julio de 2020, de Autolus Limited: Una célula productora de retrovirus que expresa una proteína de marcaje en la superficie celular, de tal manera que los vectores retrovíricos producidos por la célula se […]
 CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
CD52 soluble para su uso en el tratamiento o la prevención de la esclerosis múltiple o de la artritis reumatoide, del 29 de Julio de 2020, de THE WALTER AND ELIZA HALL INSTITUTE OF MEDICAL RESEARCH: Uno cualquiera o más de:
i) glucoproteína CD52 soluble, ii) una proteína de fusión que comprende la glucoproteína CD52 soluble como una primera proteína, y una segunda proteína;
[…]
Arenavirus trisegmentados como vectores de vacunas, del 22 de Julio de 2020, de UNIVERSITE DE GENEVE: Una partícula de arenavirus trisegmentada infecciosa y competente para la replicación que comprende un segmento L y dos segmentos S, en donde uno de los dos segmentos […]
Promotor híbrido y usos del mismo, del 15 de Julio de 2020, de Just Biotherapeutics, Inc: Un promotor híbrido, que comprende: (i) una secuencia potenciadora de citomegalovirus murino (mCMV), que comprende un elemento potenciador de mCMV (mCMV-E) y una […]
Señal para el empaquetamiento de vectores del virus de la gripe, del 24 de Junio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Un vector del virus de la gripe para la expresión y empaquetamiento de ARNv recombinante, en el que el vector comprende: secuencias correspondientes […]
Métodos y composiciones para la producción de virus vaccina, del 10 de Junio de 2020, de SillaJen Biotherapeutics, Inc: Un metodo para producir un virus vaccinia de la cepa Wyeth o Western Reserve que comprende: (a) infectar las celulas HeLa adheridas a una superficie […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]
Terapia génica basada en VAA para la esclerosis múltiple, del 3 de Junio de 2020, de UNIVERSITY OF FLORIDA RESEARCH FOUNDATION, INC.: Un vector de ácido nucleico vírico adenoasociado recombinante (VAAr) con el serotipo VAA8 que comprende: un polinucleótido que incluye un segmento de ácido […]