PROCEDIMIENTO PARA ESTIMAR LA CANTIDAD DE TIPOS CELULARES DE NEUTROFILOS ESPECIFICOS.
Un procedimiento para estimar in vitro la cantidad de células específicas en una muestra de un paciente,
en el que se usan moléculas con especificidad celular para calcular el número de células específicas, que comprende
a) extraer una alícuota de dicha muestra; y
b) medir la concentración de dos moléculas con especificidad celular en dicha muestra extraída por medio de un ensayo inmunológico y determinar la relación entre las concentraciones de dichas moléculas,
en el que las moléculas con especificidad celular son proteínas de neutrófilos
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/SE02/01214.
Solicitante: PHADIA AB.
Nacionalidad solicitante: Suecia.
Dirección: BOX 6460,751 37 UPPSALA.
Inventor/es: VENGE, PER.
Fecha de Publicación: .
Fecha Concesión Europea: 17 de Febrero de 2010.
Clasificación Internacional de Patentes:
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
- G01N33/50D6
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/566 G01N 33/00 […] › utilizando un soporte específico o proteínas receptoras como reactivos para la formación de uniones por ligando.
- G01N33/569H2
Clasificación PCT:
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Clasificación antigua:
- G01N33/53 G01N 33/00 […] › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
Fragmento de la descripción:
Procedimiento para estimar la cantidad de tipos celulares de neutrófilos específicos.
Campo de la invención
La presente invención se refiere a la estimación de la cantidad de subtipos de células específicas, por ejemplo el número de ciertos subtipos de leucocitos, por medio de mediciones de proteínas únicas en extractos de sangre y otro material biológico. El conocimiento del número o cantidad de subtipos específicos de glóbulos blancos es importante en el diagnóstico clínico y la vigilancia de sujetos con enfermedades inflamatorias entre las que se incluyen enfermedad infecciosa, cáncer, alergia/asma, etc.
Antecedentes de la invención
La estimación del número de diversos leucocitos en la sangre y en otros fluidos corporales es una de las herramientas usadas más ampliamente en medicina. La forma tradicional de obtener esta información es el recuento y diferenciación de las células con un microscopio óptico. Esta técnica se complementa por el recuento automático en contadores de células basados en el principio de recuento del número de partículas en el fluido y la medición de diversos parámetros físicos tales como el tamaño y la dispersión hacia delante y lateral, pero también por tinción histoquímica de células. Una extensión de estas técnicas es el principio del citómetro de flujo en el que se usan anticuerpos para identificar células individuales basándose en sus antígenos de la superficie celular o por medio de su contenido de antígenos intracelulares después de la permeabilización de las células.
En el documento WO 00/58726 se describe un procedimiento para cuantificar la cantidad de leucocitos en sangre entera. Sin embargo, este procedimiento no cuantifica diferentes subtipos específicos de leucocitos respecto al número o relación.
Sumario de la invención
Existe la necesidad de ensayos fáciles de usar, baratos y fiables para estimar el número de diversos glóbulos blancos tales como neutrófilos y eosinófilos, en la sangre y en otros fluidos corporales, aplicables en el sitio de atención, ayudando de esta manera al médico en su toma de decisiones inmediata.
El presente inventor ha descubierto que la extracción de sangre entera con, por ejemplo, detergentes tales como CTAB (bromuro de N-cetil-N,N,N-trimetilamonio) y la posterior medición por inmunoensayos específicos de las proteínas de neutrófilos MPO (micloperoxidasa), HNL (lipocalina de neutrófilos humanos) o lactoferrina, o las mediciones específicas de proteínas de eosinófilos tales como EPX (proteína x de eosinófilos) o EPO (peroxidasa de eosinófilos) identificarán de forma precisa el número de eosinófilos presentes en la sangre. La estimación del número de neutrófilos es útil en el diagnóstico y monitorización de sujetos con enfermedades inflamatorias tales como infecciones o enfermedades reumatoides, pero también junto con el tratamiento médico, en particular el tratamiento citostático, en el que puede producirse una reducción de la producción de neutrófilos, es decir, neutropenia como efecto adverso grave del tratamiento. La estimación del número de eosinófilos es útil en pacientes con enfermedad alérgica, enfermedades inflamatorias crónicas, enfermedades parasitarias y ciertos cánceres tales como la enfermedad de Hodking, pero también como un indicador general de enfermedad, ya que pueden aparecer números elevados de eosinófilos en varias enfermedades por razones desconocidas.
La invención se refiere a la estimación de poblaciones en diversas fases de maduración de células mieloides, ya que algunas proteínas intracelulares se producen principalmente por células inmaduras y otras proteínas principalmente por células más maduras.
De esta manera, la invención se refiere a un procedimiento para estimar in vitro la cantidad, refiriéndose la cantidad al número o relación de subtipos de células específicas en una muestra de un paciente, que comprende
en el que las moléculas con especificidad celular son proteínas de neutrófilos.
La muestra preferentemente es sangre u otro fluido corporal. Se extrae una cantidad muy pequeña de muestra, tal como 1-10 µl de muestra, pero podrían considerarse volúmenes mayores.
La extracción preferentemente se realiza con detergentes catiónicos. El tiempo de extracción es muy corto, por ejemplo, 1 minuto. Preferentemente, el detergente es CTAB.
Preferentemente, la medición en la etapa b) es por medio de un inmunoensayo, tal como ELISA, EIA, FEIA o RIA.
La molécula o moléculas con especificidad celular son proteínas de neutrófilos tales como MPO (mieloperoxidasa), HNL (lipocaína de neutrófilos humanos) o lactoferrina para medir neutrófilos.
Descripción detallada de la invención
La presente invención se describirá con más detalle a continuación en asociación con los dibujos adjuntos en los que
la Fig. 1 muestra una correlación entre el número de neutrófilos sanguíneos y la concentración de proteína MPO en sangre entera extraída con detergente.
La Fig. 2 muestra la relación entre MPO y lactoferrina en sangre entera extraída con detergente.
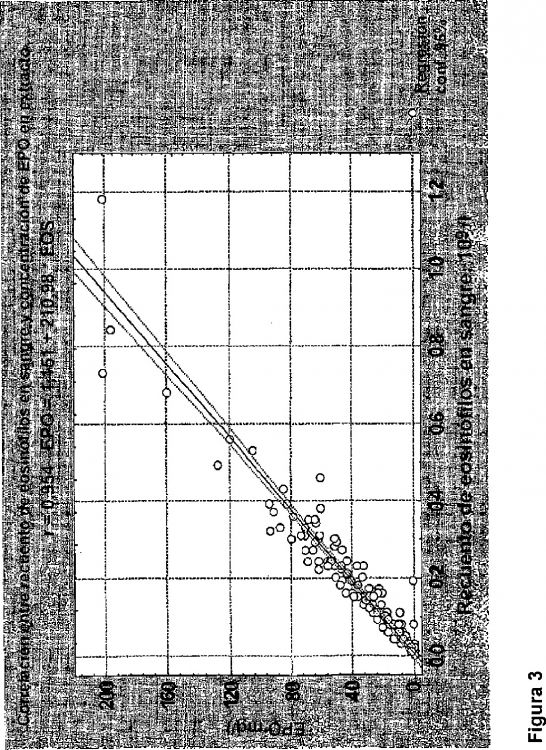
La Fig. 3 muestra una correlación entre el número de eosinófilos y la concentración de proteína EPO en sangre entera extraída con detergente.
Sección experimental
Aislamiento y purificación de proteínas de gránulos de eosinófilos y neutrófilos humanos
Se prepararon gránulos a partir de la capa leucocitaria de granulocitos obtenidos de donantes de sangre sanos usando una modificación del procedimiento descrito por Peterson y col. (Eur. J. Haematol. 40 (1988) 415-423). En resumen, los glóbulos rojos se dejaron sedimentar usando Dextrano T-500 antes de recoger el plasma rico en leucocitos. Los leucocitos se lavaron dos veces en Sacarosa 0,34 M y se suspendieron en 5 volúmenes de Sacarosa 0,34 M. Los leucocitos se cavitaron usando N2 a una presión de 750 psi (5,17 MPa) durante 30 min a +4ºC (Klempner y col., J. Cell. Biol. 86 (1980) 21-28; y Borregaard y col., J. Cell. Biol. 97 (1983) 52-61). El cavitado se suspendió en Sacarosa 0,34 M y NaCl 0,17 M y se centrifugó durante 20 min a 450 xg a +4ºC.
Es sobrenadante se centrifugó durante 20 min a 10.000 xg a +4ºC para sedimentar los gránulos. A partir de los extractos de gránulos se purificó mieloperoxidasa (MPO) de acuerdo con Olsson y col. (Scand. J. Haematol. 9 (1972) 483-491) y Cooray y col. (Vet. Immunol. Immunopathol. 38 (1993) 261-272). La preparación final fue completamente homogénea de acuerdo con la relación de absorbancia A430 nm/A280 nm, que fue 0,80 (Agner Acta. Chem. Scand. 12 (1958) 89-94).
Se purificó lipocalina de neutrófilos humanos (HNL) como se describe (Xu y col., Scand J Clin Lab Invest 54 (1994) 365-376). La HNL se purificó hasta la homogeneidad de acuerdo con la electroforesis en SDS-PAGE y tinción con plata y el antígeno no reaccionaba con anticuerpos contra las otras proteínas de neutrófilos, MPO; Lactoferrina, Catepsina G, Elastasa y Lisozima. La Lactoferrina se purificó como se describe (Reiter Int. J. Tissue React. 5 (1983) 87-96). La Peroxidasa de Eosinófilos (EPO) se purificó como se describe (Carlson y col. J. Immunol. 134 (1985) 1875-1879) y la preparación final fue homogénea de acuerdo con la relación de absorbancia A415 nm/A280 nm, que fue 1,15. La proteína de eosinófilos (EPX) se purificó hasta la homogeneidad como se describe (Peterson y col., Immunol. 50 (1983) 19-26). La preparación final aparecía como una banda en la electroforesis SDS-PAGE y no reaccionaba con anticuerpos contra la proteína catiónica de eosinófilos (ECP), elastasa, catepsina G, MPO y EPO.
Producción de anticuerpos
Anticuerpos policlonales
Se indujeron anticuerpos contra MPO, HNL, EPO y EPX en conejos mediante inyecciones intracutáneas en múltiples sitios en conejos de 50-100 µg en total de las proteínas purificadas suspendidas en adyuvante completo e incompleto de Freund. La especificidad de los anticuerpos se evaluó por inmunodifusión doble (Ouchterlony Acta Pathol. Microbiol. Scand 26 (1949) 507-) en agarosa y se ensayó frente a extractos de gránulos de neutrófilos y eosinófilos y las siguientes...
Reivindicaciones:
1. Un procedimiento para estimar in vitro la cantidad de células específicas en una muestra de un paciente, en el que se usan moléculas con especificidad celular para calcular el número de células específicas, que comprende
en el que las moléculas con especificidad celular son proteínas de neutrófilos.
2. Un procedimiento de acuerdo con la reivindicación 1, en el que la extracción se realiza con un detergente catiónico.
3. Un procedimiento de acuerdo con la reivindicación 2, en el que el detergente es CTAB (bromuro de N-cetil-N,N,N-trimetilamonio).
4. Un procedimiento de acuerdo con cualquiera de las reivindicaciones anteriores, en el que la muestra del paciente es sangre entera.
5. Un procedimiento de acuerdo con cualquiera de las reivindicaciones anteriores, en el que las moléculas con especificidad celular son MPO (mieloperoxidasa), HNL (lipocalina de neutrófilos humanos) o lactoferrina.
Patentes similares o relacionadas:
Dispositivos modulares para puntos de atención y usos de los mismos, del 29 de Julio de 2020, de Labrador Diagnostics LLC: Un sistema para la detección automatizada de un analito a partir de una muestra de fluido corporal, que comprende: un dispositivo de fluidos que comprende: […]
Anticuerpos del OPGL, del 15 de Julio de 2020, de AMGEN FREMONT INC.: Un anticuerpo, que comprende una cadena pesada y una cadena ligera, donde: a) la cadena pesada comprende: 1) una secuencia de aminoácidos recogida […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
ANTICUERPO MONOCLONAL O UNA PORCIÓN DE UNIÓN A ANTÍGENO DEL MISMO QUE SE UNE A LA PROTEÍNA L DEL VIRUS PARAINFLUENZA HUMANO (PIV); MÉTODO Y KIT PARA DETECTAR AL VIRUS PIV, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína L del virus parainfluenza humano (PIV), donde dichos […]
ANTICUERPOS MONOCLONALES ESPECÍFICOS PARA EL ANTÍGENO PB2 DEL VIRUS DE LA INFLUENZA HUMANA (FLU), SECUENCIAS NUCLEOTÍDICAS; MÉTODO Y KIT DE DIAGNÓSTICO DE INFECCIÓN PRODUCIDA POR FLU, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína PB2 del virus de la influenza humana (Flu), […]
Dispositivo para la detección de analitos, del 1 de Julio de 2020, de TECHLAB, INC.: Un dispositivo para detectar por lo menos una sustancia de interés en una muestra líquida, comprendiendo el dispositivo: (a) una unidad que […]
Un ensayo de la respuesta inmunológica mediada por células, del 17 de Junio de 2020, de Cellestis Limited: Un método para medir una actividad de respuesta inmunológica mediada por células, comprendiendo dicho método: (a) proporcionar una composición de incubación […]
Método de deducción de un valor de positividad de biomarcador en porcentaje para células seleccionadas presentes en un campo de visión, del 10 de Junio de 2020, de NOVARTIS AG: Método de deducción de un valor para el % de positividad de biomarcador (PBP) para todas las células u, opcionalmente, uno o más subconjuntos de las […]