Tratamiento y prevención de la enfermedad intestinal inflamatoria que implica IL-13 y células NKT.
Una sustancia que inhibe la unión de la IL-13 a los receptores de IL-13 sobre células NKT para usar en eltratamiento o la prevención de la respuesta inflamatoria en la enfermedad intestinal inflamatoria,
en donde laenfermedad intestinal inflamatoria comprende enfermedad de Crohn o colitis ulcerosa, o en donde la enfermedadintestinal inflamatoria produce fibrosis en un sujeto, en donde la sustancia comprende una IL-13 mutante o unácido nucleico aislado que codifica una IL-13 mutante, en donde la una IL-13 mutante comprende una mutaciónque consiste en la sustitución de un residuo de ácido glutámico en la posición 13 de la IL-13 por un residuo deaminoácido cargado positivamente o neutro, y en donde la IL-13 mutante está unida a una molécula efectora, endonde la molécula efectora es una citotoxica o un radionúclido.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/014393.
Solicitante: THE GOVERNMENT OF THE UNITED STATES OF AMERICA, AS REPRESENTED BY THE SECRETARY OF HEALTH AND HUMAN SERVICES.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: Office of Technology Transfer, 6011 Executive Boulevard, Suite 325 Bethesda, MD 20852-3804 ESTADOS UNIDOS DE AMERICA.
Inventor/es: STROBER, WARREN, FUSS, IVAN, MANNON,PETER, PREISS,JAN, PURI,RAJ, KAWAKAMI,KOJI, FICHTNER-FEIGL,STEFAN, KITANI,ATSUSHI.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/17 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- A61K38/20 A61K 38/00 […] › Interleuquinas.
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P1/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 1/00 Medicamentos para el tratamiento de trastornos del tracto alimentario o del aparato digestivo. › para úlceras, gastritis o reflujo esofágico p.ej. antiácidos, inhibidores de la secreción ácida, protectores de la mucosa.
- C07K14/54 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Interleuquinas (IL).
- C12N15/62 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Secuencias de ADN que codifican proteínas de fusión.
PDF original: ES-2412005_T3.pdf
Fragmento de la descripción:
Tratamiento y prevención de la enfermedad intestinal inflamatoria que implica IL-13 y células NKT
Antecedentes de la invención La enfermedad intestinal inflamatoria (EII) incluye la enfermedad de Crohn y la colitis ulcerosa. La colitis ulcerosa es una enfermedad del colon o del intestino grueso. La enfermedad está marcada por inflamación y ulceración de la mucosa del colon, en revestimiento más interno. La inflamación suele comenzar en el recto y la parte inferior del colon, pero también puede afectar a todo el colon, extendiéndose hacia arriba del colon de un modo continuo. Por el contrario, la enfermedad de Crohn puede afectar a cualquier zona del tracto gastrointestinal, incluido el intestino delgado y el colon, generalmente no es continua y puede afectar a todo el espesor de la pared intestinal.
Se cree que tanto la enfermedad de Crohn como la colitis ulcerosa se deben a una sensibilidad anómala de los linfocitos T en la mucosa frente a los antígenos bacterianos en la luz intestinal ( (Sartor, 1995) . En personas con EII, el sistema inmunitario reacciona de forma inadecuada, confundiendo alimentos, bacterias y otros materiales del intestino con sustancias extrañas o invasoras. En el proceso, el cuerpo envía glóbulos blancos al revestimiento de los intestinos, donde producen inflamación crónica, Estas células generan productos dañinos que en última instancia conducen a úlceras y lesión intestinal. Cuando esto sucede, el paciente experimenta los síntomas de EII.
Se estima que ya un millón de americanos tiene EII, con una cifra que se reparte de forma uniforme entre la enfermedad de Crohn y la colitis ulcerosa. Actualmente no existe una curación médica para la EII, no obstante los tratamientos médicos actuales están dirigidos a suprimir la inflamación anómala en el revestimiento del colon y, de este modo, a controlar los síntomas. Las principales clases de medicación que se usan actualmente para tratar la EII incluyen aminosalicilatos, corticosteroides y medicamentos inmunomoduladores. No obstante, los aminosalicilatos son eficaces únicamente en el tratamiento de episodios leves o moderados de colitis ulcerosa, no se recomienda el uso prolongado de esteroides debido a los efectos secundarios y las actuales medicaciones inmunomoduladoras (p. ej., azatioprina, 6-mercaptopurina y metotrexato) pueden necesitar hasta tres meses antes de que comiencen a producir efectos beneficiosos. Por tanto, se necesitan nuevos y mejores tratamientos para tratar y prevenir los síntomas de la EII.
Sumario de la invención En el presente documento se proporciona una sustancia que inhibe la unión de la IL-13 a los receptores de IL-13 sobre las células NKT para usar en el tratamiento o prevención de la respuesta inflamatoria en la enfermedad intestinal inflamatoria, en el que la enfermedad intestinal inflamatoria comprende enfermedad de Crohn o colitis ulcerosa, o en el que la enfermedad intestinal inflamatoria produce fibrosis en un sujeto, en el que la sustancia comprende una IL-13 mutante o un ácido nucleico aislado que codifica una IL-13 mutante, en el que la una IL-13 mutante comprende una mutación que consiste en la sustitución de un residuo de ácido glutámico en la posición 14 de la IL-13 por un residuo de aminoácido cargado positivamente o neutro, y en el que la IL-13 mutante está unida a una molécula efectora, en la que la molécula efectora es una citotoxina o un radionúclido.
También se proporciona el uso de una sustancia que inhibe la unión de la IL-13 a los receptores de IL-13 sobre las células NKT para preparar un medicamento para el tratamiento o la prevención de la respuesta inflamatoria en la enfermedad intestinal inflamatoria, en el que la enfermedad intestinal inflamatoria comprende enfermedad de Crohn o colitis ulcerosa, o en el que la enfermedad intestinal inflamatoria produce fibrosis en un sujeto, en el que el compuesto comprende una IL-13 mutante o un ácido nucleico aislado que codifica una IL-13 mutante, en el que la una IL-13 mutante comprende una mutación que consiste en la sustitución de un residuo de ácido glutámico en la posición 14 de la IL-13 por un residuo de aminoácido cargado positivamente o neutro, y en el que la IL-13 mutante está unida a una molécula efectora, en la que la molécula efectora es una citotoxina o un radionúclido.
Breve descripción de las figuras
Las figuras adjuntas, que se incorporan y constituyen una parte de esta memoria, ilustran varias formas de realización de la invención y, junto con la descripción, sirven para explicar los principios de la invención.
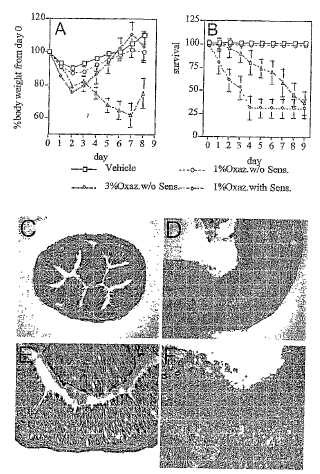
Las Figuras 1A -F muestran que la sensibilización previa antes de la exposición intrarrectal a oxazolona conduce a una colitis progresiva crónica. Las Figuras 1A y 1B muestran la pérdida de peso y la mortalidad, respectivamente, de los ratones después de la sensibilización previa con vehículo (etanol) o con oxazolona y la exposición intrarrectal con vehículo o diferentes dosis de oxazolona. Las Figuras C y E muestran aumentos por 5 y por 10, respectivamente, de secciones transversales teñidas con H-E de colon de ratones 7 días después de la sensibilización previa con etanol y la exposición. Las Figuras 1D y 1F muestran los efectos tras la sensibilización previa con oxazolona y la reexposición a un 1 % de oxazolona por vía intrarrectal.
Las Figuras 2A -B muestran la producción de citocina por los linfocitos de ratones con colitis por oxazolona. (A) Células mononucleares de la lámina propia (LPMC) , Células mononucleares hepáticas (HMNC) , células de los ganglios linfáticos mesentéricos (MLNC) y esplenocitos (SPC) se aislaron el día 5 tras la inducción de colitis por oxazolona (gris) o colitis por TNBS aguda (negro) y se estimularon in vitro durante 48 horas con anti-CD3 y anti-CD28 unidos a la placa. Las concentraciones de las citocinas se midieron en los sobrenadantes mediante ELISA. (B)
LPMC se aislaron los días 2, 5 u 8 tras la inducción de colitis por oxazolona. Las LPMC se estimularon como se ha indicado anteriormente y se midieron las concentraciones de IL-4 (abiertos) e IL-13 (rayados) en los sobrenadantes. Las LPMC, MLNC, o SPC producen una cantidad muy pequeña de IL-13 en el modelo agudo de colitis inducida por TMBS. No obstante, como se ha descrito anteriormente se observa una producción mucho mayor de IL-13 en un modelo crónico de TNBS en ratones BALB/c.
Las Figuras 3A-B muestran que la neutralización de la IL-13 previene la inducción de la colitis por oxazolona. (A) Pérdida de peso y (B) mortalidad de ratones con colitis por oxazolona tratada con IL-13Rα2-Fc (rombos) o proteína control (cuadrados) .
Las Figuras 4A-D muestran que el agotamiento de los linfocitos NK1.1 protege a los ratones de la colitis por oxazolona pero no de la colitis por TNSB. Pérdida de peso (A+C) y mortalidad (B+D) tras la inducción de colitis por oxazolona (A+B) o colitis por TNSB (C+D) o inyección de vehículo (etanol; círculos) . Se inyectó a los ratones anticuerpo control (cuadrados) o con agotamiento de células NK1.1 con PK136 (rombos) .
Las Figuras 5A-B muestran la presentación de antígenos a CD1 y que las células NKT para Jα281 son esenciales para la inducción de colitis con oxazolona. (A) Pérdida de peso de los ratones tras la inyección intrarrectal de vehículo (círculos) u oxazolona tras la inyección i.v. de anticuerpos CD1 de bloqueo (20H2; rombos) o anticuerpo control (cuadrados) . (B) Pérdida de peso de ratones CD1KO tras la inducción de colitis con oxazolona (rombos) , ratones Jα281KO (círculos) y ratones de tipo silvestre (cuadrados) .
La Figura 6 muestra la producción de citocinas en respuesta a αGalCer. LPMC (panel superior) , esplenocitos o células CD4 (panel inferior) no estimuladas (sin estim.) o estimuladas con anti-CD3 unido a la placa y anti-CD28 soluble, células L no transfectadas y vehículo (LC+Veh.) , o células L transfectadas con CD1 y 100 ng/ml de αGalCer (LCD1+aGC) .
La Figura 7 muestra un gráfico del peso de los ratones con colitis por oxazolona tratados con una toxina de IL-13 de pseudomonas (IL13PE38) .
La Figura 8 muestra una curva del peso de ratones Balb/c que recibieron administración intrarrectal de TNBS.
La Figura 9 muestra la cuantificación de colágeno en muestras de colon. La inflamación intestinal crónica se establece y se observa aumento de la cantidad de formación de colágeno. La formación de colágeno coincide con la aparición de fibrosis.
La Figura 10 muestra la medición de citocinas obtenidas según una base semanal de tejido de colon de ratones Balb/c sometidos a administración seminal de TNBS. Inicialmente se encontró una respuesta mediada por Th1 (aumento de IL-12 e IFN-gamma) . No obstante,... [Seguir leyendo]
Reivindicaciones:
1. Una sustancia que inhibe la unión de la IL-13 a los receptores de IL-13 sobre células NKT para usar en el tratamiento o la prevención de la respuesta inflamatoria en la enfermedad intestinal inflamatoria, en donde la 5 enfermedad intestinal inflamatoria comprende enfermedad de Crohn o colitis ulcerosa, o en donde la enfermedad intestinal inflamatoria produce fibrosis en un sujeto, en donde la sustancia comprende una IL-13 mutante o un ácido nucleico aislado que codifica una IL-13 mutante, en donde la una IL-13 mutante comprende una mutación que consiste en la sustitución de un residuo de ácido glutámico en la posición 13 de la IL-13 por un residuo de aminoácido cargado positivamente o neutro, y en donde la IL-13 mutante está unida a una molécula efectora, en donde la molécula efectora es una citotoxica o un radionúclido.
2. La sustancia que inhibe la unión de IL-13 a los receptores de IL-13 en células NKT para usar de acuerdo con la reivindicación 1, en la que la IL-13 mutante es una IL-13 humana mutante que se une al receptor de IL-13 pero que tiene una capacidad reducida para activar la señalización en dicho receptor
3. La sustancia que inhibe la unión de IL-13 a los receptores de IL-13 en células NKT para usar de acuerdo con la 15 reivindicación 2, en la que la IL-13 mutante tiene una mayor afinidad por el receptor de IL-13 que la IL-13 humana.
4. La sustancia que inhibe la unión de IL-13 a los receptores de IL-13 en células NKT para usar de acuerdo con la reivindicación 1, en la que el residuo cargado negativamente en la posición 13 de la IL-13 está sustituido por un residuo seleccionado de lisina y arginina.
5. La sustancia que inhibe la unión de IL-13 a los receptores de IL-13 en células NKT para usar de acuerdo con la 20 reivindicación 1, en la que la IL-13 mutante comprende la mutación hIL-13E13K de la SEC ID Nº 8.
6. La sustancia que inhibe la unión de IL-13 a los receptores de IL-13 en células NKT para usar de acuerdo con la reivindicación 1, en la que la IL-13 unida a una molécula efectora es una proteína de fusión.
7. La sustancia que inhibe la unión de IL-13 a los receptores de IL-13 en células NKT para usar de acuerdo con la reivindicación 1, en la que la molécula efectora está conjugada con la IL-13 mutante.
8. La sustancia que inhibe la unión de IL-13 a los receptores de IL-13 en células NKT para usar de acuerdo con la reivindicación 1, en la que la citotoxina se selecciona de exotoxina de Pseudomonas o una subunidad citotóxica o mutante de la misma, la toxina diftérica o una subunidad citotóxica o mutante de la misma, ricina, saporina, gelonina, caliqueamicina, doxorrubicina, ribotoxina, proteína inactivadora del ribosoma y abrina.
9. La sustancia que inhibe la unión de IL-13 a los receptores de IL-13 en células NKT para usar de acuerdo con la reivindicación 8, en la que la exotoxina de Pseudomonas se selecciona de PE35, PE38, PE38KDEL, PE40, PE4E y PE38QQR.
10. La sustancia que inhibe la unión de IL-13 a los receptores de IL-13 en células NKT para usar de acuerdo con la reivindicación 1, en la que el ácido nucleico es un vector.
11. Uso de una sustancia que inhibe la unión de la IL-13 a los receptores de IL-13 sobre células NKT para preparar
un medicamento para el tratamiento o la prevención de la respuesta inflamatoria en la enfermedad intestinal inflamatoria, en donde la enfermedad intestinal inflamatoria comprende enfermedad de Crohn o colitis ulcerosa, o en donde la enfermedad intestinal inflamatoria produce fibrosis en un sujeto, en donde el compuesto comprende una IL-13 mutante o un ácido nucleico aislado que codifica una IL-13 mutante, en donde la IL-13 mutante comprende una mutación que consiste en la sustitución de un residuo de ácido glutámico en la posición 13 de la IL-13 por un residuo de aminoácido cargado positivamente o neutro, y en donde la IL-13 mutante está unida a una molécula efectora, en donde la molécula efectora es una citotoxina o un radionúclido.
12. El uso de la reivindicación 11, en el que la IL-13 mutante es una IL-13 mutante humana que se une al receptor de IL-13 pero que tiene menor capacidad para activar la señalización en dicho receptor.
13. El uso de la reivindicación 11, en el que la IL-13 mutante tiene una afinidad mayor por el receptor de IL-13 que la 45 IL-13 humana.
14. El uso de la reivindicación 11, en el que el residuo cargado negativamente en la posición 13 de la IL-13 está sustituido por un residuo seleccionado de lisina y arginina.
15. El uso de la reivindicación 11, en el que la IL-13 mutante comprende la mutación hIL-13E13K de la SEC ID Nº 8.
16. El uso de la reivindicación 11, en el que la IL-13 unida a una molécula efectora es una proteína de fusión.
17. El uso de la reivindicación 11, en el que la molécula efectora está conjugada a la IL-13 mutante.
18. El uso de la reivindicación 11, en el que la citotoxina se selecciona de exotoxina de Pseudomonas o de una subunidad citotóxica o mutante de la misma, toxina diftérica o una subunidad citotóxica o mutante de la misma,
ricina, saporina, gelonina, caliqueamicina, doxorrubicina, ribotoxina, proteína inactivadora del ribosoma y abrina.
19. El uso de la reivindicación 18, en el que la exotoxina de Pseudomonas se selecciona de PE35, PE38, PE38KDEL, PE40, PE4E y PE38QQR.
20. El uso de la reivindicación 11, en el que el ácido nucleico es un vector.
21. Un procedimiento ex vivo para proporcionar específicamente una molécula efectora a una célula NKT, que comprende unir la molécula efectora a una molécula de unión al receptor de IL-13 (IL13RBM) y proporcionar a la célula una cantidad eficaz de la molécula efectora unida a IL13RBM.
22. El procedimiento de la reivindicación 21, en el que IL13RBM es una IL-13 humana mutante.
23. El procedimiento de la reivindicación 21, en el que el efector unido a IL13RBM es una proteína de fusión. 10 24. El procedimiento de la reivindicación 21, en el que la molécula efectora está conjugada a IL13RBM.
25. El procedimiento de la reivindicación 21, en el que la molécula efectora inhibe la actividad de la célula NKT.
26. El procedimiento de la reivindicación 25, en el que la molécula efectora se selecciona de una citotoxina, un marcador, un radionúclidos, un fármaco, un liposoma y un anticuerpo.
27. El procedimiento de la reivindicación 25, en el que la molécula efectora es una citotoxina.
28. El uso de la reivindicación 27, en el que la citotoxina se selecciona de exotoxinas de Pseudomonas o una subunidad citotóxica o mutante de la misma, toxina diftérica o una subunidad citotóxica o mutante de la misma, ricina, saporina, gelonina, caliqueamicina, doxorrubicina, ribotoxina, proteína inactivadora del ribosoma y abrina.
29. El procedimiento de la reivindicación 28, en el que la exotoxina de Pseudomonas se selecciona de PE35, PE38, PE38KDEL, PE40, PE4E y PE38QQR.
Patentes similares o relacionadas:
Cadena ligera de enteroquinasa modificada, del 22 de Julio de 2020, de NOVO NORDISK A/S: Un análogo de la cadena ligera de la enteroquinasa bovina que comprende una secuencia de aminoácidos establecida en la SEQ ID NO: 1, en donde dicho análogo comprende […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Métodos y composiciones para ingeniería genómica, del 3 de Junio de 2020, de Sangamo Therapeutics, Inc: Una pareja de nucleasas de dedo de zinc (ZFN) que comprende una ZFN izquierda y una ZFN derecha, comprendiendo cada ZFN un dominio de escisión […]
Métodos y composiciones para escisión dirigida y recombinación, del 20 de Mayo de 2020, de Sangamo Therapeutics, Inc: Un método in vitro para la escisión selectiva de un gen HLA clase I, un gen HLA que codifica una proteína de clase 1 del Complejo de Histocompatibilidad Mayor (MHC) […]
Antígenos de coagulasa estafilocócica y métodos para su uso, del 13 de Mayo de 2020, de UNIVERSITY OF CHICAGO: Una composición inmunógena que comprende al menos dos dominios 1-2 de coagulasa estafilocócica diferentes, en donde cada uno de los al menos dos dominios […]
Reconocimiento de unión a diana celular mediante un agente bioactivo usando transferencia de energía de resonancia de bioluminiscencia intracelular, del 6 de Mayo de 2020, de PROMEGA CORPORATION: Un sistema de ensayo que comprende: (a) una biblioteca de agentes bioactivos, cada uno de los cuales está fijado a un fluoróforo; (b) una diana celular fusionada a […]
Etiqueta de epítopo y método de detección, captura y/o purificación de polipéptidos etiquetados, del 15 de Abril de 2020, de ChromoTek GmbH: Péptido epítopo aislado que tiene de 12 a 25 aminoácidos, en donde la secuencia de aminoácidos comprende una secuencia según se define en SEQ ID NO: 32 (X1X2RX4X5AX7SX9WX11X12), […]
Utilización diagnóstica de un polipéptido de fusión que comprende una proteína vírica y un enzima MGMT, del 15 de Abril de 2020, de INSTITUT PASTEUR: Utilización in vitro de un polipéptido de fusión que comprende una proteína vírica y i) el enzima 6-metilguanina-ADN-metiltransferasa (MGMT, EC 2.1.1.63) o un homólogo […]