Señuelos de factores de transcripción.
Un método no terapéutico para reducir la viabilidad de células procariotas,
comprendiendo el método:
(a) proporcionar un polinudeótido set'iuelo que comprende un sitio de unión para un factor de transcripción diana (una secuencia señuelo);
(b) introducir el polinucle6tido señuelo en una célula procariota que comprende un sitio de unión para el factor de transcripción , unido operativamente a un gen o genes; en el que la introducción del polinucleótido set'iuelo reduce la unión del factor de transcripción diana al sitio de unión en la célula y causa una alteración en la expresión del gen o genes unidos operativa mente; y
en el que el factor de transcripción diana comprende un regulador de la expresión de un gen o genes que codifican uno o más de:
(i) una respuesta celular adaptativa;
(ii) un mecanismo celular intrlnseco de resistencia a antibióticos;
(iii) un factor celular de virulencia;
(iv) una respuesta celular a estrés; o
(v) un gen celular esencial.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2009/051301.
Solicitante: PROCARTA BIOSYSTEMS LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: Norwich Bioincubator Norwich Research Park Colney Lane Norwich, Norfolk NR4 7UH REINO UNIDO.
Inventor/es: MCARTHUR,MICHAEL, MOORE,JANE MARION.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N1/21 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 1/00 Microorganismos, p.ej. protozoos; Composiciones que los contienen (preparaciones de uso médico que contienen material de protozoos, bacterias o virus A61K 35/66, de algas A61K 36/02, de hongos A61K 36/06; preparación de composiciones de uso médico que contienen antígenos o anticuerpos bacterianos, p. ej. vacunas bacterianas, A61K 39/00 ); Procesos de cultivo o conservación de microorganismos, o de composiciones que los contienen; Procesos de preparación o aislamiento de una composición que contiene un microorganismo; Sus medios de cultivo. › modificados por la introducción de material genético extraño.
- C12N15/10 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Procedimientos para el aislamiento, la preparación o la purificación de ADN o ARN (preparación química de ADN o ARN C07H 21/00; preparación de polinucleótidos no estructurales a partir de microorganismos o con la ayuda de enzimas C12P 19/34).
- C12N15/63 C12N 15/00 […] › Introducción de material genético extraño utilizando vectores; Vectores; Utilización de huéspedes para ello; Regulación de la expresión.
- C12N15/66 C12N 15/00 […] › Métodos generales para insertar un gen en un vector para formar un vector recombinante, utilizando la escisión y la unión; Utilización de "linkers" no funcionales o de adaptadores, p. ej. "linkers" que contienen la secuencia para una endonucleasa de restricción.
- C12Q1/68 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
- C40B40/06 C […] › C40 TECNOLOGIA COMBINATORIA. › C40B QUIMICA COMBINATORIA; BIBLIOTECAS, p. ej. QUIMIOTECAS (bibliotecas combinatorias in silico de ácidos nucleicos, proteínas o péptidos G16B 35/00; química combinatoria in silico G16C 20/60). › C40B 40/00 Bibliotecas per se , p. ej. arrays, mezclas. › Bibliotecas que contienen nucleótidos o polinucleótidos, o sus derivados.
PDF original: ES-2444640_T3.pdf
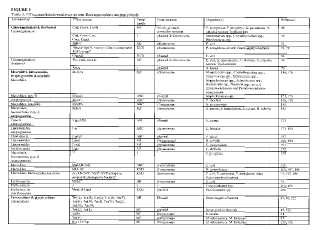
Fragmento de la descripción:
Señuelos de factores de transcripción la presente invención se refiere a métodos y composiciones para modutar fenotipos de procariotas, particutarmente bacterias patogénicas, usando secuencias señuelo de factores de transcripción.
El control del crecimiento y virulencia bacteriano plantea un problema creciente, particularmente en aplicaciones médicas y veterinarias, y puede convertirse en un reto importante para la salud pública. los antibióticos para uso frente a bacterias patogénicas son muy conocidos en la técnica. Sin embargo, el uso extenso de dichos antibióticos ha dado lugar al surgimiento de bacterias que son resistentes al menos a uno, y en algunos casos, a múltiples antibióticos (las denominadas cepas resistentes a múltiples fánnacos) . la situación se exacerba por una disminución en el número de antibióticos convencionales que se descubren y que están en desarrollo. De hecho, la resistencia a antibióticos es un reto importante para la investigación antibacteriana y amenaza la potencia de los antibióticos comercializados asi como los que todavla están en desarrollo. Consecuentemente, existe una necesidad para nuevos agentes anti-bacterianos que puedan usarse para abordar la diseminación e infección bacteriana.
Como un ejemplo, Staphylococcus aureus representa un reto importante para la salud global causando numerosas enfermedades humanas y animales, con un amplio espectro de gravedad desde infecciones en la piel hasta sepsis mortal por choque tóxico (lowy, New Engl. J. Med. (1998) 339: 520-532) . Se estima que el 20% de la población humana es portador de las bacterias en infección de tejido blando, frecuentemente con caracleristicas clinicas no perceptibles, a partir de donde las bacterias pueden penetrar en el cuerpo para infectar la sangre y posterionnente los tejidos óseo y cardiaco (Gordon y lowy, Clin. Infec!. Dis. (2008) 40 (SS) : S350-9) . Aunque en un principio se pensó que era un patógeno extracelular, está surgiendo una evidencia sustancial que sugiere que S. aureus puede evitar la acción antibacleriana o el engullimiento por macrófagos persistiendo intercelularmente (Garzoni y Kelley, Trends Microbio!. (2009) 17: 59-65) , complicando potencialmente su tratamiento. los mecanismos de resistencia también se han adquirido o se han desarrollado desde la primera exposición a antibióticos hasta tal grado que las cepas resistentes a múltiples fánnacos son ahora la nonna en la clinica (Hawkey, J. Antimicrob. Chemother. (2008) 62 (S1) : il-9) , lo que ha limitado adicionalmente las opciones de tratamiento.
Existen varias razones por las que S. aureus es un patógeno tan versátil: posee mecanismos para evadirse de la respuesta inmune del huésped (Foster, Na!. Rev. Microbio!. (2005) 3: 948-958) ; puede producir una amplio rango de detenninantes de virulencia (Novick, Mol. Micro. (2003) 48: 1429-1449) ; tiene la capacidad de catabolizar los tejidos del huésped (Vojtov et al. (2002) Proc. Nat!. Acad. Sci. USA 99: 10102-10107) y puede adaptarse fácilmente a entornos con nutrientes limitados y anóxicos encontrados en el interior del huésped (Haselbeck et al, Curr. Phann. Des. (2002) 8: 1155-1172) . Muchos de estos procesos están controlados a nivel de la transcripción y como tales actualmente no son las dianas de los antibióticos tradicionales (que actúan mayoritariamente en la sintesis de la pared celular, proteinas o ADN) .
las infecciones por Streptococcus pyogenes (Streptococcus Grupo A: GAS) pueden tratarse habitualmente con muchos antibióticos diferentes. El tratamiento temprano puede reducir el riesgo de muerte por la enfermedad invasiva streptococcal del grupo A. Sin embargo, induso el mejor cuidado médico no previene la muerte en cada caso. Para aquellos con una enfermedad muy grave, puede necesitarse el cuidado paliativo en una unidad de cuidado intensivo. Para las personas con fascitis necrosante, frecuentemente es necesaria la cirugra para eliminar el tejido dañado. Han surgido cepas de S. pyogenes resistentes a antibióticos macrólidos, sin embargo todas las cepas permanecen uniformemente sensibles a penicilina.
la resistencia de Streptococcus pneumoniae a penicilina y otras bela-Iactamas se está incrementando en todo el mundo. El mecanismo principal de resistencia implica la introducción de mutaciones en genes que codifican proteínas de unión a penicilina. Se piensa que la presión selectiva juega un papel importante y el uso de antibióticos beta-Iactama se ha implicado como un factor de riesgo para infección y colonización. streptococcus pneumoniae es responsable de neumonia, bacteremia, otitis media, meningitis, sinusitis, peritonitis y artritis.
la neumonia resistente a penicilina causada por Streptococcus pneumoniae (conocida comúnmente como pneumococcus) , se detectó por primera vez en 1967, como lo fue la gonorrea resistente a penicilina. la resistencia a sustitutos de penicilina también se conoce más allá de S. aureus. Hacia 1993 Escherichia coIi era resistente a cinco variantes de f1uoroquinolona. Myoobacterium tuben;ufosis es resistente comúnmente a isoniazida y rifampina y algunas veces resistente universalmente a los tratamientos comunes. Otros patógenos que muestran alguna resistencia incluyen Salmonelfa, Campylobacter y Streptococci.
Enterococcus faecium es otro microorganismo multirresistente encontrado en hospitales. los Enterococcus resistentes a penicilina se observaron en 1983, enterococcus resistentes a vancomicina (VRE) en 1987 y Enterococcus resistentes a linezolida (lRE) al final de la década de 1990.
Pseudomonas aeruginosa es un patógeno oportunista altamente prevalente. Una de las características más preocupantes de P. aeruginosa consiste en su baja susceptibilidad a antibióticos. Esta baja susceptibilidad es atribuible a una acción concertada de bombas de eflujo multifánnaco con genes de resistencia a antibióticos codificados cromosómicamente (por ejemplo, mexAB-oprM, mexXY etc) y la baja permeabilidad de las cubiertas celulares bacterianas. Además de la resistencia intrinseca, P. aeruginosa desarrolla fácilmente resistencia adquirida bien por mutación en genes codificados cromosómicamente o por transferencia génica horizontal de determinantes de resistencia a antibióticos. El desarrollo de resistencia a múltiples fármacos por aislados pele P. aeruginosa requiere varios eventos genéticos diferentes que incluyen la adquisición de diferentes mutaciones y/o la transferencia horizontal de genes de resistencia a antibióticos. la hipermutación favorece la selección de resistencia a antibióticos dirigida por mutación en cepas de P. aeruginosa que producen infecciones crónicas, mientras que el agrupamiento de varios genes de resistencia a antibióticos diferentes en integrones favorece la adquisición concertada de determinantes de resistencia a antibióticos. Algunos estudios recientes han mostrado que la resistencia fenollpica asociada con la formación de biopelicula o con el surgimiento de variantes de colonia pequena puede ser importante en la respuesta de poblaciones de P. aeruginosa al tratamiento con antibióticos (Comelis P. (editor) Pseudomonas: Genomics and Molecular-Biology (1-ed.) (2008) Caister Academic Press) .
C/ostridium difficile es un patógeno nosocomial que causa enfermedad diarreica en hospitales de todo el mundo. Se indicó que C. difficile resistente a clindamicina era el agente causante de grandes brotes de enfermedad diarreica en hospitales en Nueva York. Arizona. Florida y Massachusetts entre 1989 y 1992 (Johnson S. et al, New England Journal of Medicine (1999) 341 : 1645-1651) . los brotes dispersos geográficamente de cepas de C. difficile resistentes a antibióticos fluoroquinolona, tales como ciprofloxacina y levofloxacina, también se indicaron en América del Norte en 2005 (loo V. et al N. Engl. J. Med. (2005) 353 (23) : 2442-9) .
E. eoli y Salmonella provienen directamente de comida contaminada. De la carne que está contaminada con E. coli. el ochenta por ciento de las bacterias son resistentes a uno o mas fármacos preparados; causa infecciones de vejiga que son resistentes a antibióticos ("HSUS Fact Sheen. Salmonella se encontró por primera vez en los seres humanos en los años 70 y en algunos casos es resistente a tantos como nueve antibióticos diferentes rHSUS Facl Sheef) . Cuando ambas bacterias se diseminan, surgen afecciones serias para la salud. Mucha genle se hospitaliza cada ano después de haber sido infectada y como resullado algunos mueren.
El 5 de noviembre de 2004, los Centros para el Control y Prevención de Enfermedades (CDC) indicaron un número creciente de infecciones sanguineas por Acinetobacter baumannii en pacientes en instalaciones médicas militares en las que se trataron integrantes de las Fuerzas Armadas lesionados en la región Iraq/Kuwait... [Seguir leyendo]
Reivindicaciones:
1. Un método no terapéutico para reducir la viabilidad de células procariotas, comprendiendo el método:
(a) proporcionar un polinudeótido set'iuelo que comprende un sitio de unión para un factor de transcripción diana (una secuencia señuelo) ;
(b) introducir el polinucleótido señuelo en una célula procariota que comprende un sitio de unión para el factor de transcripción, unido operativamente a un gen o genes;
en el que la introducción del polinucleótido set'iuelo reduce la unión del factor de transcripción diana al sitio de unión en la célula y causa una alteración en la expresión del gen o genes unidos operativa mente;
y en el que el factor de transcripción diana comprende un regulador de la expresión de un gen o genes que codifican uno o más de:
(i) una respuesta celular adaptativa;
(ii) un mecanismo celular intrlnseco de resistencia a antibióticos;
(iii) un factor celular de virulencia;
(iv) una respuesta celular a estrés; o
(v) un gen celular esencial.
2. Un método no terapéutico para incrementar la susceptibilidad procariota a antibióticos, comprendiendo el método:
(a) proporcionar un polinucleótido sef'iuelo que comprende un sitio de unión para un factor de transcripción diana (una secuencia sef'iuelo) ;
(b) introducir el poi nucleótido senuelo en una célula procariota que comprende un sitio de unión para el factor de transcripción, unido operativamente a un gen o genes;
en el que la introducción del polinudeótido señuelo reduce la unión del factor de transcripción diana al sitio de unión en la célula y causa una alteración en la expresión del gen o genes unidos operativamente, incrementando de esta manera la susceptibilidad a antibióticos de la célula;
y en el que el factor de transcripción diana comprende un regulador de la expresión de un gen o genes que codifican uno o mas de:
(i) una respuesta celular adaptativa;
(ii) un mecanismo celular intrinseco de resistencia a antibióticos;
(iii) un factor celular de virulencia;
(iv) un gen celular esencial.
3. Un método segun la reivindicación 1 o reivindicación 2, en el que la reducción de la viabilidad comprende uno o más de:
(i) inhibir una respuesta celular adaptativa tal como una respuesta al estrés;
(ii) incrementar la susceptibilidad celular a antibióticos; (jii) inhibir la expresión de uno o más genes esenciales;
(iv) inhibir la expresión de uno o más genes de virulencia.
4. Un método segun una cualquiera de las reivindicaciones 1 a 3, en el que el factor de tranSCripción diana se selecciona de: WhiB7; FadR; YycGNycF; Sigma 54 (o SigA) ; Fur; TcdR; Vfr; NtrC; ArsR; TcaA; AgrA; WaIR; sigB; Ksig; fhu; o una variante u homólogo funcional de cualquiera de éstos.
5. Un método segun cualquiera de las reivindicaciones 1 a 4, en el que el procariota es una bacteria.
6. Un método según la reivindicación 5, en el que la bacteria es patogénica.
7. Un método segun cualquiera de las reivindicaciones anteriores en el que el sitio de unión del factor de transcripción en el polinucleótido señuelo no está unido operativamente a un gen.
8. Un polinucleótido señuelo como se define en cualquiera de las reivindicaciones 1 a 7 para uso en el tratamiento de infección bacteriana.
9. Un pOlinucleótido señuelo según la reivindicación 8 para uso en el tratamiento de infección bacteriana, en el que
el tratamiento de la infección bacteriana comprende el uso de uno o más antibióticos y/o otro (s) agente (s) 5 antibacteriano (s) .
10. Un polinucleótido señuelo según la reivindicación 8 o reivindicación 9 para uso en el tratamiento de infección bacteriana, en el que el tratamiento de la infección bacteriana comprende tratar una afección seleccionada de: neumonia, bacteremia, tosferina, enfermedad de Iyme, brucelosis, enteritis aguda, septicemia, tularemia, gripe, úlceras pépticas, enfermedad del legionario, gonorrea, infecciones nosocomiales, sepsis, rickettsiosis, tifus,
disentería, cólera, peste, ántrax, colitis pseudomembranosa, difteria, listerosis, tuberculosis, septicemia, meningitis.
11. Un método ex vivo para matar bacterias, inhibir el crecimiento bacteriano, o reducir la virulencia bacteriana, comprendiendo el método aplicar un polfnucleótido señuelo como se define en cualquiera de las reivindicaciones 1 a 10, opcionalmente en combinaciÓn con uno o más antibióticos y/o agentes antibacterianos.
12. Uso de señuelos de factores de transcripción (TFD) para reducir la viabilidad de células procariotas ex vWo. 15 13. Uso de señuelos de factores de transcripción (TFD) para reducir la virulencia de células procariotas ex vivo.
Patentes similares o relacionadas:
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]
MÉTODOS PARA EL DIAGNÓSTICO DE ENFERMOS ATÓPICOS SENSIBLES A COMPONENTES ALERGÉNICOS DEL POLEN DE OLEA EUROPAEA (OLIVO), del 23 de Julio de 2020, de SERVICIO ANDALUZ DE SALUD: Biomarcadores y método para el diagnostico, estratificación, seguimiento y pronostico de la evolución de la enfermedad alérgica a polen del olivo, kit […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Secuenciación dirigida y filtrado de UID, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento para generar una biblioteca de polinucleótidos que comprende: (a) generar una primera secuencia del complemento (CS) de un polinucleótido diana a partir […]
Métodos para la recopilación, estabilización y conservación de muestras, del 8 de Julio de 2020, de Drawbridge Health, Inc: Un método para estabilizar uno o más componentes biológicos de una muestra biológica de un sujeto, comprendiendo el método obtener un […]
Evento de maíz DP-004114-3 y métodos para la detección del mismo, del 1 de Julio de 2020, de PIONEER HI-BRED INTERNATIONAL, INC.: Un amplicón que consiste en la secuencia de ácido nucleico de la SEQ ID NO: 32 o el complemento de longitud completa del mismo.
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Aislamiento de ácidos nucleicos, del 24 de Junio de 2020, de REVOLUGEN LIMITED: Un método de aislamiento de ácidos nucleicos que comprenden ADN de material biológico, comprendiendo el método las etapas que consisten en: (i) efectuar un lisado […]