Metodo para el tratamiento y la profilaxis de enfermedades relacionadas con la deposicion de amiloide utilizando igm.
Preparación de inmunoglobulina producida a partir de muestras combinadas de plasma humano como material departida,
en la que la preparación de inmunoglobulina está enriquecida en inmunoglobulina M (IgM), para suutilización en un método de tratamiento o prevención de una enfermedad neurodegenerativa asociada con amiloide,en la que la preparación de inmunoglobulina comprende anticuerpos IgM que se unen específicamente a Aß 1-42.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/061269.
Solicitante: Grifols Therapeutics Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 4101 Research Commons, 79 T.W. Alexander Drive Research Triangle Park, NC 27709 ESTADOS UNIDOS DE AMERICA.
Inventor/es: SCUDERI,JR. PHILIP, SAFAVI,AFSHIN, LANGEVIN,MATTHEW G.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
PDF original: ES-2409844_T3.pdf
Fragmento de la descripción:
Método para el tratamiento y la profilaxis de enfermedades relacionadas con la deposición de amiloide utilizando IgM
Antecedentes de la invención Se cree que el péptido amiloide º (Aº) 1-42 es uno de los factores clave en el desarrollo y la progresión de la enfermedad de Alzheimer. Aunque todavía no se ha determinado de forma definitiva el papel patogénico preciso del péptido amiloide º en dicha enfermedad, cada vez más indicios apoyan la hipótesis de que la producción de péptido amiloide º y su deposición en el cerebro es un acontecimiento causal de la misma. Por consiguiente, el problema de la producción, acumulación y eliminación del péptido amiloide º en el cerebro se ha erigido como uno de los posibles enfoques razonables para el tratamiento de la enfermedad de Alzheimer.
Recientemente se ha descubierto que las preparaciones de IgG intravenosas contienen anticuerpos específicos del péptido amiloide Aº 1-42. Además, en dos pequeños ensayos en humanos, se ha descubierto que la IgG intravenosa ralentiza la progresión de la enfermedad de Alzheimer (Dodel, R y otros, “Intravenous Immunoglobulins containing antibodies against b-amyloid for the treatment of Alzheimer’s disease”, J. Neurol. Neurosurg. Psychiatr y , 75:1472-1474 (2004) ; y Dodel, R y otros, “Human antibodies against amyloid beta peptide: A potential treatment for Alzheimer’s disease”, Ann. Neurol, 52:253-256 (2002) ) . Aunque queda por esclarecer el mecanismo de acción de la IgG en esta indicación, los autores han planteado la hipótesis de que la simple eliminación sistémica del péptido Aº 1-42 problemático podría ser la razón de la eficacia de la IgG intravenosa.
El documento WO 03/097093 da a conocer la administración de IgM policlonal humana a pacientes que padecen enfermedades inmunitarias, como asma, inmunodeficiencia común variable, artritis reumatoide, lupus eritematoso sistémico, enfermedad del suero y vasculitis.
En Levy y otros, 2003, se menciona el tratamiento con pentaglobina de un paciente con síndrome de Sjögren.
El documento EP 1 172 378 describe la utilización de anticuerpo IgG humano en el tratamiento de la enfermedad de Alzheimer.
Los documentos FR 2 824 568, DE 93 27 112 y EP 0 835 880 describen diversos métodos para obtener preparaciones de IgM derivadas de plasma humano.
La inmunoglobulina M (IgM) es la tercera inmunoglobulina por orden de mayor a menor concentración que se encuentra en el suero de la mayoría de animales (aproximadamente un 6-10% del conjunto total de inmunoglobulinas) . Las concentraciones plasmáticas normales de IgM en humanos están comprendidas entre aproximadamente 0, 6 y aproximadamente 2, 5 mg/ml en los hombres y entre aproximadamente 0, 7 y aproximadamente 2, 8 mg/ml en las mujeres.
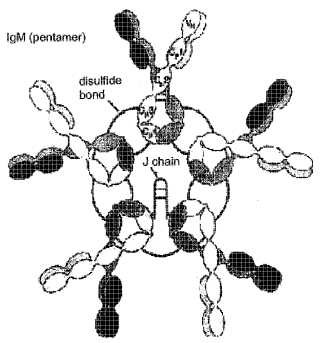
La IgM es una molécula 19S con un peso molecular de 950 kDa y está compuesta por cinco subunidades idénticas de 180 kDa. Cada una de estas subunidades es estructuralmente parecida al monómero de IgG, excepto porque poseen cuatro dominios CH en lugar de tres. Los monómeros de IgM están unidos por enlaces disulfuro en una disposición circular que forma una estrella, y un pequeño polipéptido rico en cisteína llamado cadena J (20 kDa) une dos de las unidades (véase la figura 1) . Las moléculas de IgM son secretadas intactas por las células plasmáticas, y por consiguiente la cadena J se debe considerar una parte integral de las mismas. La semivida plasmática de la IgM es de aproximadamente 5, 1 días.
La IgM es el principal isotipo de inmunoglobulina que se produce en una respuesta inmunitaria primaria. También se produce en una respuesta secundaria, pero este hecho se ve a menudo enmascarado por el predominio de la IgG. Aunque se produce en una cantidad relativamente pequeña, debido a su estructura pentamérica la IgM es considerablemente más eficiente (en términos molares) que la IgG en la activación del complemento, la opsonización, la neutralización de virus y la aglutinación. La mayoría de isoaglutininas presentes en el suero humano, que reconocen los antígenos sanguíneos de tipo A y B, son de la clase IgM. Por consiguiente, pueden adoptarse algunas medidas especiales durante la purificación a fin de eliminar las isoaglutininas y hacer que la preparación sea más compatible con los tipos sanguíneos A y B.
La inmunización pasiva utilizando preparaciones de inmunoglobulina que contienen IgM puede proporcionar ventajas en el tratamiento y/o prevención de trastornos o enfermedades asociados con los péptidos amiloides.
Características de la invención La presente invención se refiere a una preparación para su utilización en métodos de tratamiento o prevención (incluidas cualquier disminución clínicamente significativa de los síntomas o la ralentización de la progresión de la enfermedad, respectivamente) de enfermedades neurodegenerativas asociadas con el amiloide o de la amiloidosis. La presente invención también se refiere a preparaciones de inmunoglobulina útiles en dichos métodos.
Así, en un aspecto, la presente invención se refiere a una preparación para su utilización en un método de tratamiento o prevención de una enfermedad asociada con los polipéptidos de amiloide que comprende la administración de una preparación de inmunoglobulina obtenida a partir de muestras combinadas de plasma humano como material de partida, en la que la preparación de inmunoglobulina está enriquecida en inmunoglobulina M (IgM) . La preparación de inmunoglobulina puede comprender, como mínimo, aproximadamente el 80% de IgM o, como mínimo, aproximadamente el 90% de IgM. La preparación de inmunoglobulina comprende anticuerpos IgM que se unen específicamente a A 1-42. La enfermedad asociada con los polipéptidos de amiloide puede ser una enfermedad neurodegenerativa asociada con amiloide. Dicha enfermedad puede ser la enfermedad de Alzheimer.
En algunas realizaciones, la preparación de inmunoglobulina se puede administrar en una dosis de inmunoglobulina comprendida entre aproximadamente 0, 1 Ig por kg de peso corporal y aproximadamente 1.000 mg por kg de peso corporal. La preparación de inmunoglobulina también se puede administrar en una dosis comprendida entre aproximadamente 0, 5 Ig por kg de peso corporal y aproximadamente 500 mg por kg de peso corporal; entre aproximadamente 0, 5 Ig por kg de peso corporal y aproximadamente 100 mg por kg de peso corporal; o entre aproximadamente 0, 5 Ig por kg de peso corporal y aproximadamente 50 mg por kg de peso corporal.
En otro aspecto, la presente invención se refiere a una composición farmacéutica que comprende IgM, una parte de la cual, como mínimo, se une específicamente a A 1-42, en la que la IgM se puede preparar a partir de material de partida que comprende inmunoglobulinas y otras sustancias del siguiente modo: ajustando el pH del material de partida a fin de obtener una solución intermedia que comprende inmunoglobulinas disueltas, ajustando la solución intermedia de la etapa a) a unas condiciones de pH, temperatura y concentración de caprilato que hacen que se forme un primer precipitado y un primer sobrenadante que comprende inmunoglobulinas, separando el primer sobrenadante del primer precipitado, incubando el primer sobrenadante en unas condiciones de tiempo, pH, temperatura y concentración de caprilato que hacen que se forme un segundo precipitado y un segundo sobrenadante que comprende inmunoglobulinas, separando el segundo sobrenadante del segundo precipitado, poniendo en contacto el segundo sobrenadante con una primera resina de intercambio aniónico en unas condiciones de pH y fuerza iónica que hacen que sustancialmente ninguna cantidad de la inmunoglobulina G o la inmunoglobulina M se una a la primera resina, mientras que la inmunoglobulina A y otras sustancias se unan a la misma, separando una fracción que contiene sustancialmente toda la inmunoglobulina G y la inmunoglobulina M a partir del resultado de la etapa anterior, poniendo en contacto las inmunoglobulinas G y M con una segunda resina de intercambio aniónico en unas condiciones de pH y fuerza iónica que hacen que sustancialmente ninguna cantidad de la inmunoglobulina G se una a la segunda resina, mientras que la inmunoglobulina M y otras sustancias se unan a la misma, eluyendo la IgM a partir de la segunda columna de resina de intercambio iónico con una solución tamponada que tiene una conductividad parecida a la que presenta una solución de cloruro de sodio con una concentración, como mínimo, de 100 mM, aplicando la IgM a una resina de filtración en gel y recuperando la IgM, aplicando la IgM a una resina de afinidad que comprende antígenos A y B inmovilizados y recuperar la IgM. El material de partida se puede obtener a partir de hemoderivados humanos combinados.... [Seguir leyendo]
Reivindicaciones:
1. Preparación de inmunoglobulina producida a partir de muestras combinadas de plasma humano como material de partida, en la que la preparación de inmunoglobulina está enriquecida en inmunoglobulina M (IgM) , para su utilización en un método de tratamiento o prevención de una enfermedad neurodegenerativa asociada con amiloide, en la que la preparación de inmunoglobulina comprende anticuerpos IgM que se unen específicamente a A 1-42.
2. Utilización de muestras combinadas de plasma humano como material de partida en la fabricación de una preparación de inmunoglobulina enriquecida en inmunoglobulina M (IgM) , para el tratamiento o prevención de una enfermedad neurodegenerativa asociada con amiloide, en la que la preparación de inmunoglobulina comprende anticuerpos IgM que se unen específicamente a A 1-42.
3. Preparación para su utilización según la reivindicación 1, o utilización según la reivindicación 2, en la que la
preparación de inmunoglobulina comprende, como mínimo, aproximadamente el 80% de IgM o, como mínimo, 15 aproximadamente el 90% de IgM.
4. Preparación para su utilización según las reivindicaciones 1 ó 3, o utilización según cualquiera de las reivindicaciones 2 ó 3, en la que la enfermedad es la enfermedad de Alzheimer.
5. Preparación para su utilización según cualquiera de las reivindicaciones 1, 3 ó 4, o utilización según cualquiera de las reivindicaciones 2, 3 ó 4, en la que la preparación de inmunoglobulina se administra en una dosis de inmunoglobulina comprendida entre aproximadamente 0, 1 Ig por kg de peso corporal y aproximadamente 1.000 mg por kg de peso corporal.
6. Preparación para su utilización según cualquiera de las reivindicaciones 1, 3, 4 ó 5, o utilización según cualquiera de las reivindicaciones 2, 3, 4 ó 5, en la que la preparación de inmunoglobulina se administra en una dosis comprendida entre aproximadamente 0, 5 Ig por kg de peso corporal y aproximadamente 500 mg por kg de peso corporal; entre aproximadamente 0, 5 Ig por kg de peso corporal y aproximadamente 100 mg por kg de peso corporal; o entre aproximadamente 0, 5 Ig por kg de peso corporal y aproximadamente 50 mg por kg de peso corporal.
7. Composición farmacéutica, que comprende moléculas de inmunoglobulina M (IgM) que se unen específicamente a A 1-42, para su utilización en un método de tratamiento o prevención de una enfermedad neurodegenerativa asociada con amiloide, en la que la IgM se puede obtener a partir de material de partida, que comprende inmunoglobulinas y otras sustancias, del siguiente modo:
a) ajustando el pH del material de partida a fin de obtener una solución intermedia que comprende inmunoglobulinas disueltas,
b) ajustando la solución intermedia de la etapa a) a unas condiciones de pH, temperatura y concentración de caprilato que hacen que se forme un primer precipitado y un primer sobrenadante que comprende inmunoglobulinas,
c) separando el primer sobrenadante del primer precipitado,
d) incubando el primer sobrenadante en unas condiciones de tiempo, pH, temperatura y concentración de caprilato que hacen que se forme un segundo precipitado y un segundo sobrenadante que comprende inmunoglobulinas,
e) separando el segundo sobrenadante del segundo precipitado,
f) poniendo en contacto el segundo sobrenadante con una primera resina de intercambio aniónico en unas condiciones de pH y fuerza iónica que hacen que sustancialmente nada de la inmunoglobulina G o la inmunoglobulina M se una a la primera resina, mientras que la inmunoglobulina A y otras sustancias se unan a 55 la misma,
g) separando una fracción que contiene sustancialmente toda la inmunoglobulina G y la inmunoglobulina M a partir del resultado de la etapa anterior,
h) poniendo en contacto las inmunoglobulinas G y M con una segunda resina de intercambio aniónico en unas condiciones de pH y fuerza iónica que hacen que sustancialmente nada de la inmunoglobulina G se una a la segunda resina, mientras que la inmunoglobulina M y otras sustancias se unan a la misma,
i) eluyendo la IgM a partir de la segunda columna de resina de intercambio iónico con una solución tamponada 65 que tiene una conductividad parecida a la que presenta una solución de cloruro de sodio con una concentración, como mínimo, de 100 mM,
j) aplicando la IgM a una resina de filtración en gel y recuperar la IgM,
k) aplicando la IgM a una resina de afinidad que comprende antígenos A y B inmovilizados, y 5 l) recuperando la IgM.
8. Composición farmacéutica para su utilización según la reivindicación 7, en la que el material de partida se obtiene a partir de hemoderivados humanos combinados. 10
9. Composición farmacéutica para su utilización según la reivindicación 7 u 8, en la que los hemoderivados humanos combinados se obtienen de donantes que no han sido seleccionados para determinar su título de inmunoglobulina anti-A .
Patentes similares o relacionadas:
Eliminación de impurezas de cultivos celulares residuales, del 29 de Julio de 2020, de NOVARTIS AG: Un método para eliminar la Proteína Nuclear (NP) de la Gripe de una preparación que comprende proteínas del virus de la gripe de interés que incluyen hemaglutinina […]
 Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Cepas de Bordetella vivas atenuadas como vacuna de dosis única contra la tos ferina, del 29 de Julio de 2020, de INSTITUT PASTEUR DE LILLE: Una vacuna que comprende una cepa viva, atenuada y mutada de Bordetella pertussis que comprende al menos una mutación del gen (ptx) de la toxina […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Composición de vacuna que contiene un adyuvante sintético, del 22 de Julio de 2020, de INFECTIOUS DISEASE RESEARCH INSTITUTE: Una composición farmacéutica que comprende: un adyuvante lípido de glucopiranosilo (GLA), que tiene la fórmula: **(Ver fórmula)** en la que: […]
Arenavirus trisegmentados como vectores de vacunas, del 22 de Julio de 2020, de UNIVERSITE DE GENEVE: Una partícula de arenavirus trisegmentada infecciosa y competente para la replicación que comprende un segmento L y dos segmentos S, en donde uno de los dos segmentos […]
Composiciones para inducir la diferenciación de células supresoras derivadas mieloides para tratar el cáncer y las enfermedades infecciosas, del 15 de Julio de 2020, de OSE Immunotherapeutics: Un compuesto seleccionado del grupo que consiste en un anticuerpo y un fragmento de unión a antígeno del mismo que se une específicamente a la proteína […]
Polipéptidos biparatópicos antagonistas de la señalización WNT en células tumorales, del 15 de Julio de 2020, de Boehringer Ingelheim International GmbH & Co. KG: Un polipéptido que se une específicamente a LRP5 o LRP6, que comprende - un primer dominio variable individual de inmunoglobulina seleccionado del grupo de dominios […]