MÉTODO DE DIAGNÓSTICO DIFERENCIAL DE LA ENFERMEDAD DE CHAGAS.
Método de diagnóstico diferencial de la enfermedad de Chagas.
La presente invención se refiere a un péptido y al método de obtención de datos útiles para el diagnóstico diferencial de la enfermedad de Chagas que permite diferenciar pacientes con Chagas crónico de individuos sanos y de aquellos con otras enfermedades infecciosas afines,
basado en la detección anticuerpos frente a dicho péptido. Además, este método permite diferenciar pacientes con la enfermedad de Chagas en forma clínica indeterminada de aquellos pacientes de Chagas con patologías cardíaca y digestiva. También permite diferenciar pacientes con cadiopatía chagásica de aquellos con alteraciones cardíacas no chagásicas (miocarditis, cardiopatías idiopáticas, infarto de miocardio, etc.). La presente invención permite también evaluar la respuesta al tratamiento de dicha enfermedad en enfermos de Chagas en fase crónica, especialmente con alteraciones cardíacas. La presente invención se refiere también a un kit para llevar a cabo dicho método de diagnóstico diferencial.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201031097.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Nacionalidad solicitante: España.
Inventor/es: LOPEZ LOPEZ,MANUEL CARLOS, THOMAS CARAZO,Mari Carmen, MARAÑÓN LIZANA,Concepción, FERNÁNDEZ VILLEGAS,Ana Isabel, SEGOVIA HERNÁNDEZ,Manuel.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K7/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 12 a 20 aminoácidos.
- G01N33/569 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para microorganismos, p. ej. protozoarios, bacterias, virus.
PDF original: ES-2373262_A1.pdf
Fragmento de la descripción:
Método de diagnóstico diferencial de la enfermedad de Chagas.
La presente invención se encuentra dentro de la medicina, la biología molecular, la inmunología y la parasitología, y se refiere a un método de obtención de datos útiles para el diagnóstico diferencial de la enfermedad de Chagas, permitiendo diferenciar pacientes en fase indeterminada de pacientes crónicos con patologías cardíaca y digestiva, así como para evaluar la respuesta al tratamiento de dicha enfermedad en enfermos de Chagas en fase crónica cardíaca.
Estado de la técnica anterior
La enfermedad de Chagas (enfermedad de Chagas-Mazza, mal de Chagas o tripanosomiasis americana), es una enfermedad parasitaria tropical principalmente del Centro y Sudamérica, generalmente crónica y cuyo agente etiológico es el protozoo Trypanosoma cruzi (T. cruzi). Se estima que da lugar a unas 21.000 muertes cada año (WHO, 2002, 2005), con aproximadamente 50.000-200.000 nuevos casos diagnosticados por año (Tarleton RL, 2007. PLoS Med 4(12): e332). Aunque tradicionalmente la enfermedad se ha visto confinada a la América Latina, actualmente se encuentra en expansión a zonas no endémicas como consecuencia de los procesos migratorios, por lo que ha sido necesaria la implantación de pruebas diagnósticas en bancos de sangre y centros de salud en aquellos países con una alta tasa de población inmigrante proveniente de zonas endémicas. Así, la incidencia de la enfermedad en dicha población inmigrante es del 16 por 1.000 en Australia, 9 por 1.000 en Canadá, 25 por 1.000 en España y 8-50 por 1.000 en EEUU (Schmunis GA et al, 2007. Mem Inst Oswaldo Cruz. 102 Suppl 1:75-85).
T. cruzi es un protozoo parásito flagelado que pertenece al Orden Kinetoplástida y presenta una fase obligada de multiplicación intracelular en el hospedador vertebrado, en el cual es capaz de infectar los diferentes tipos de células. La forma infectiva del parásito o tripomastigote metacíclico se encuentra en el tracto gastrointestinal del hospedador invertebrado o insecto trasmisor de la enfermedad y es transmitido al hospedador vertebrado tras la picadura del insecto, el cual, además, defeca en el momento de la picadura favoreciéndose la entrada del parásito por el rascado provocado por el carácter irritante de las heces. El tripomastigote metacíclico es visible en la sangre como un tripomastigote fusiforme, con forma de "C" o de "S", de 20 μm de largo por 1 μm de ancho y no tiene capacidad replicativa. Cuando el parásito infecta en el hospedador vertebrado las células de distintos tejidos, principalmente del músculo cardíaco estriado, del músculo esquelético y del músculo liso, se acorta el flagelo y se transforma en un amastigote redondo de 2 a 5 μm de diámetro. El amastigote se multiplica por medio de fisión binaria formando "racimos" o "nidos" que se acumulan en la célula huésped hasta que esta se rompe. Los parásitos liberados de la célula se transforman a la forma de tripomastigote sanguíneo y son liberados al torrente sanguíneo. Los mismos tienen un tamaño que varía entre 15 y 20 μm, tienen flagelo libre gracias al cual pueden moverse, un cinetoplasto voluminoso, terminal o subterminal, y un núcleo oval. Estos tripomastigotes pueden infectar otras células para repetir el ciclo, pero no son capaces de multiplicarse en la sangre, ya que la única forma replicativa en el vertebrado es la forma amastigote intracelular.
Los hospedadores invertebrados son hematófogos y adquieren el parásito al alimentarse del hombre o de los animales domésticos o silvestres infectados. Los tripomastigotes migran al intestino medio del insecto, donde se transforman en epimastigotes, flagelados anchos, muy móviles, con el cinetoplasto entre el núcleo y el flagelo libre. Allí se dividen un gran número de veces, quedando el insecto infectado de por vida. Los epimastigotes migran al intestino posterior donde, debido a la acidez de la zona, se transforman a tripomastigotes metacíclicos siendo excretados con las heces en el momento de la picadura.
En el caso de la infección causada por T. cruzi en el hombre, la enfermedad presenta dos estados severos. La fase aguda, tiene lugar tras la picadura del insecto y, aunque suele pasar desapercibida, a ella se asocia aproximadamente el 10% de mortalidad. La fase crónica, que puede desarrollarse incluso pasados más de diez años, se caracteriza por la aparición de cardiomegalia, anormalidades electrocardiográficas, arritmias (Chagas crónico con afectación cardiaca), aperistalsis, megaesófago y megacolon (Chagas crónico con afectación digestiva), pudiendo llegar a causar la muerte. La fase aguda tiene una duración de dos a tres meses, aproximadamente, progresando para dar lugar a una fase crónica asintomática, actualmente llamada fase indeterminada, la cual se caracteriza por la persistencia de la infección sin presentar problemas clínicos aparentes. Cerca del 40% de los casos serológicamente positivos se encuentran en fase indeterminada, la cual evoluciona frecuentemente a una fase crónica sintomática varios años más tarde.
La enfermedad de Chagas es diagnosticada de forma rutinaria mediante diversos métodos serológicos comerciales como las técnicas de ELISA, inmunofluorescencia indirecta (IFI) o hemaglutinación, para las cuales se utilizan extractos completos o semipurificados de proteínas de las formas epimastigotes del parásito T. cruzi, mezclas de proteínas recombinantes o péptidos sintéticos correspondientes a antígenos o fragmentos antigénicos del parásito (Umezawa et al., 1996. J. Clin Microbiol. 34:2143-2147; da Silveira et al., 2001. Trend Parasitol. 17:286-291). Otro método de diagnóstico serológico desarrollado es el denominado ID-PaGIA-Chagas (Rabello et al., 1999. Mem Inst Oswaldo Cruz 94 (1): 77-82), basado en una reacción de aglutinación en gel usando tres péptidos sintéticos derivados de sendos antígenos de T. cruzi, o el llamado INNO-LIA (Saez-Alquezar et al., 2000. J. Clin Microbiol. 38:851-854), basado en la reactividad frente a siete proteínas recombinantes fijadas sobre un soporte de nylon. El kit inmunocromátográfico Stat-Pack utiliza seis proteínas recombinantes y presenta altos niveles de sensibilidad y especificidad (Ponce et al., 2005. J Clin Microbiol 43(10): 5065-5068). Estos métodos han sido especialmente propuestos para la obtención de resultados rápidos de seropositividad en screenings en bancos de sangre, emergencias médicas y en transplantes de órganos. Sin embargo, sólo permiten obtener un resultado cualitativo (positivo/negativo) y, por tanto, son de baja utilidad para evaluar la evolución del paciente chagásico. Recientemente, se ha evaluado la eficacia de nueve diferentes sistemas de diagnóstico serológico de la enfermedad de Chagas, siete de ellos comerciales (Caballero et al., 2007. Clinical and Vaccine Immunology. 14(8):1045-1049), mostrando porcentajes de sensibilidad y especificidad que van desde el 75% al 100%, usando como referencia un ensayo de Western blot (inmunoblot) con antígenos secretores-excretores de formas tripomastigotes de T. cruzi. Sin embargo, ninguno de los métodos descritos permite el diagnóstico diferencial entre las distintas formas clínicas de la fase crónica de la enfermedad de Chagas.
En general, los sistemas de diagnóstico serológico permiten detectar anticuerpos en sueros de pacientes crónicos, pero resultan poco útiles para evaluar la evolución de los pacientes bajo tratamiento, ya que los niveles de anticuerpos persisten, de forma estable, durante mucho tiempo. Probablemente, el tratamiento si bien al disminuir la carga parasitaria pueda influir en la reducción del nivel de anticuerpos, al destruir el parásito puede conducir a la exposición al sistema inmune de nuevos componentes parasitarios, con la consiguiente posible generación de anticuerpos con otras especificidades. Estos dos efectos conjugados (aumento del título de algunos anticuerpos y disminución de otros) dan lugar a una aparente estabilidad del título medido frente a proteínas de lisados totales del parásito o combinaciones de antígenos. Por tanto, estos kits comerciales no permiten detectar la dinámica de respuesta después del tratamiento ni, por tanto, reconocer los casos en que la terapia no es efectiva.
Los dos únicos medicamentos disponibles para el tratamiento de la enfermedad de Chagas son Nifurtimox, desarrollado en 1960 por Bayer, y Benznidazol, desarrollado en 1974 por Roche. La ventaja terapéutica de estos fármacos en las fases crónicas de la enfermedad... [Seguir leyendo]
Reivindicaciones:
1. Un péptido de secuencia aminoacídica:
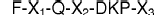
Donde: X1 representa un aminoácido que se selecciona de entre G y A; donde X2 es un grupo de 4 aminoácidos que se seleccionan de entre A, E y G; donde X3 es un grupo de 2 aminoácidos que se seleccionan de entre S, L, P y A.
2. El péptido según la reivindicación anterior, donde X1 es G.
3. El péptido según cualquiera de las dos reivindicaciones anteriores, donde X1 es A.
4. El péptido según cualquiera de las tres reivindicaciones anteriores, donde X2 es AAX4 y X4 es un grupo de dos aminoácidos que se seleccionan de entre A, E y G.
5. El péptido según la reivindicación anterior, donde X4 es AA, AG o EG.
6. El péptido según cualquiera de las cinco reivindicaciones anteriores, donde X3 es SL, PP, AP o AA.
7. El péptido según cualquiera de las seis reivindicaciones anteriores, donde la secuencia aminoacídica del péptido es SEQ ID NO: 1, SEQ ID NO: 2, SEQ ID NO: 3, SEQ ID NO: 4, SEQ ID NO: 5, SEQ ID NO: 6, SEQ ID NO: 7 o SEQ ID NO: 8.
8. El péptido según cualquiera de las siete reivindicaciones anteriores, donde la secuencia aminoacídica del péptido es SEQ ID NO: 1.
9. Un péptido caracterizado porque su secuencia aminoacídica comprende la secuencia aminoacídica del péptido según cualquiera de las ocho reivindicaciones anteriores.
10. El péptido según la reivindicación anterior caracterizado porque su secuencia está repetida al menos dos veces.
11. Un uso del péptido según cualquiera de las diez reivindicaciones anteriores como marcador para el diagnóstico diferencial, pronóstico o seguimiento del estadio de la enfermedad de Chagas en una muestra biológica aislada.
12. Un método de obtención de datos útiles para el diagnóstico y seguimiento de la enfermedad de Chagas, que comprende:
13. El método según la reivindicación anterior, que además comprende:
14. El método según cualquiera de las dos reivindicaciones anteriores para el diagnóstico o seguimiento de la enfermedad de Chagas, que además comprende:
15. Un método para el diagnóstico diferencial de la enfermedad de Chagas que comprende los pasos (a) y (b) según cualquiera de las reivindicaciones 12 y 13, que además comprende:
16. El método de seguimiento de la evolución de la enfermedad de Chagas en individuos chagásicos crónicos con cardiopatías que comprende realizar al menos dos veces la secuencia de pasos (a) y (b) según cualquiera de las reivindicaciones 12 y 13, en muestras biológicas procedentes de un mismo individuo, y aisladas en momentos diferentes.
17. El método de seguimiento según la reivindicación anterior, donde el seguimiento se realiza post-tratamiento.
18. El método de seguimiento según la reivindicación anterior, que además comprende comparar la cantidad de anticuerpos cuantificados en el paso (a) antes del inicio del tratamiento, con la cantidad de anticuerpos cuantificados en el paso (a) en distintos momentos tras el inicio del tratamiento.
19. El método según cualquiera de las siete reivindicaciones anteriores, donde la cuantificación de los anticuerpos se realiza mediante un ELISA.
20. El método según la reivindicación anterior, donde el ELISA es un ELISA indirecto.
21. Un kit que comprende el péptido según cualquiera de las reivindicaciones 1 a 10 para cuantificar los anticuerpos frente a dicho péptido en una muestra biológica aislada.
22. El kit según la reivindicación anterior donde el péptido está inmovilizado en una fase sólida.
23. Uso del kit según cualquiera de las dos reivindicaciones anteriores para el diagnóstico de la enfermedad de Chagas.
24. Uso del kit según cualquiera de las reivindicaciones 21 y 22 para el diagnóstico diferencial del estadio de la enfermedad de Chagas.
25. Uso del kit según cualquiera de las reivindicaciones 21 y 22 para el seguimiento de la enfermedad de Chagas tras el inicio del tratamiento.
Patentes similares o relacionadas:
Método de determinación de la presencia y/o cantidad de moléculas diana, del 22 de Julio de 2020, de Canopy Biosciences, LLC: Método para el análisis de células individuales en una muestra de sangre mediante la determinación de la presencia y/o cantidad de una o más moléculas […]
Ensayo de toxina botulínica con sensibilidad mejorada, del 1 de Julio de 2020, de BioMadison, Inc: Un método para aumentar la sensibilidad de la detección basada en células de una toxina botulínica, que comprende: (i) proporcionar una célula […]
Bebidas energéticas y otras ayudas nutricionales derivadas de licores a base de agave, del 1 de Julio de 2020, de Roar Holding, LLC: Una composición que comprende compuestos inhibidores de monoamino oxidasa (MAO), cuya composición se prepara mediante la eliminación de etanol de una bebida […]
Evaluación asistida del pronóstico en la enfermedad inflamatoria, del 24 de Junio de 2020, de KINGS COLLEGE LONDON: Un método in vitro de recopilación de información útil para predecir el resultado clínico en un sujeto, en donde el sujeto tiene o se sospecha que tiene una enfermedad […]
Vacunas y diagnóstico de torque teno virus porcino, del 18 de Junio de 2020, de VIRGINIA TECH INTELLECTUAL PROPERTIES, INC.: Composición inmunogénica que comprende una proteína según SEQ ID NO. 16.
Marcadores celulares para el diagnóstico de la enfermedad de Alzheimer y para la progresión de la enfermedad de Alzheimer, del 17 de Junio de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Un método para el diagnóstico de la probabilidad de la enfermedad de Alzheimer (EA) en un individuo examinado, que comprende: (i) medir los […]
Biomarcadores de TB, del 22 de Abril de 2020, de United Kingdom Research and Innovation: Un método para el diagnóstico de TB en un sujeto, comprendiendo el método: (a) proporcionar una muestra de dicho sujeto, siendo dicha muestra seleccionada […]
Procedimiento para detectar bacterias coliformes contenidas en la leche, del 15 de Abril de 2020, de ASAHI KASEI KABUSHIKI KAISHA: Procedimiento para lisar bacterias coliformes contenidas en la leche, que comprende la etapa de mezclar un agente de lisis que contiene lisozima, un surfactante aniónico […]