Forma cristalina delta de la sal de arginina de perindopril, procedimiento para su preparación y composiciones farmacéuticas que la contienen.
Forma cristalina delta de la sal de L-arginina de perindopril,
de fórmula (I):**Fórmula**
caracterizada por los siguientes picos de difracción RX en polvo, medidos en un difractómetro de anticátodode cobre y expresados en términos de ángulo de Bragg 2 theta (º): 4,3, 11,0, 11,1, 13,2, 14,6, 16,0 y 21,9.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E13150296.
Solicitante: LES LABORATOIRES SERVIER.
Nacionalidad solicitante: Francia.
Dirección: 35, RUE DE VERDUN 92284 SURESNES CEDEX FRANCIA.
Inventor/es: LAURENT, STEPHANE, Linol,Julie, GRENIER,Arnaud, MATHIEU,SEBASTIEN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/403 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › condensados con carbociclos, p. ej. carbazol.
- C07D209/42 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 209/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros, condensados con otros ciclos, con solamente un átomo de nitrógeno como heteroátomo. › Atomos de carbono que tienen tres enlaces a heteroátomos con a lo más un enlace a halógeno, p. ej. radicales éster o nitrilo.
PDF original: ES-2439871_T3.pdf
Fragmento de la descripción:
Forma cristalina delta de la sal de arginina de perindopril, procedimiento para su preparación y composiciones farmacéuticas que la contienen La presente invención se refiere a la forma cristalina delta de la sal de L-arginina de perindopril de fórmula (I) :
a su procedimiento de preparación y a las composiciones farmacéuticas que la contienen.
El perindopril, así como sus sales farmacéuticamente aceptables, y más particularmente su sal de arginina, tienen propiedades farmacológicas interesantes. Su propiedad principal es inhibir la enzima de conversión de la angiotensina I (o quininasa II) , lo que por una parte permite impedir la transformación del decapéptido angiotensina I en el octapéptido angiotensina II (vasoconstrictor)
y, por otra parte, prevenir la degradación de la bradiquinina (vasodilatador) a un péptido inactivo. Estas dos acciones contribuyen a los efectos beneficiosos del perindopril en las enfermedades cardiovasculares, más particularmente en la hipertensión arterial, la insuficiencia cardíaca y la enfermedad coronaria estable.
En la patente europea EP 0 049 658 se describe el perindopril, su preparación y su utilización terapéutica. 15 En la patente europea EP 1 354 873 se describe por primera vez la sal de arginina de perindopril.
En las patentes europeas EP 1 989 182 y EP 2 016 051 se describen las formas cristalinas alfa y beta de la sal de arginina de perindopril. En la solicitud de patente WO 2009/157018 se describe la forma cristalina gamma de la sal de arginina de perindopril. 20 En la patente SI 23001 se describe un procedimiento de obtención de perindopril arginina.
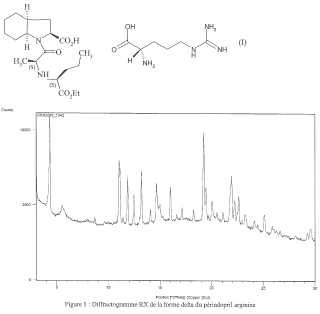
Teniendo en cuenta el interés farmacéutico del perindopril arginina, era primordial obtenerlo con una excelente estabilidad. Más específicamente, la presente invención se refiere a la forma cristalina delta del compuesto de fórmula (I) . La forma cristalina delta del perindopril arginina según la invención se puede caracterizar mediante su difractograma
RX según la figura 1 y/o mediante su espectro RMN en sólido de la figura 3. En ausencia de excipientes e impurezas, la forma cristalina delta del perindopril arginina según la invención se puede caracterizar mediante el siguiente diagrama de difracción X en polvo, medido en difractómetro de anticátodo de cobre y expresado en términos de distancia interreticular d, ángulo de Bragg 2 theta e intensidad relativa, expresada en porcentaje con respecto a la línea más intensa:
Ángulo 2 theta (º) Distancia interreticular d[Å] Intensidad relativa [%]
4, 34 20, 37 66, 2
5, 57 15, 86 5, 2
11, 04 8, 02 57, 5
11, 15 7, 94 47, 5
Ángulo 2 theta (º) Distancia interreticular d[Å] Intensidad relativa [%]
11, 87 7, 454 35, 0
12, 47 7, 09 17, 9
13, 21 6, 70 33, 6
14, 06 6, 30 6, 6
14, 64 6, 05 31, 8
16, 03 5, 53 17, 5
17, 11 5, 18 5, 6
18, 27 4, 85 4, 1
19, 23 4, 61 100
19, 44 4, 57 17, 8
20, 04 4, 43 13, 6
21, 11 4, 21 3, 7
21, 93 4, 05 23, 0
22, 20 4, 00 16, 9
22, 61 3, 93 21, 2
23, 21 3, 83 4, 5
24, 30 3, 66 2, 3
25, 09 3, 55 9, 4
25, 95 3, 43 1, 7
29, 54 3, 02 4, 2
Se considera que cada línea tiene una precisión de ±0, 2º en 2-theta.
Las intensidades relativas se dan a título indicativo.
El espectro de difracción X en polvo se mide bajo las siguientes condiciones experimentales:
• Difractómetro Panalytical X'Pert Pro.
• Detector X'Celerator.
• Anticátodo de cobre, tensión 40 KV, intensidad 30 mA.
• Montaje en transmisión; muestra fija.
• Temperatura: ambiente. 10 • Campo de medición: 3º a 40º.
• Incremento entre cada medición: 0, 017º.
• Tiempo de medición por paso: 49 s.
• Sin referencia interna.
• Datos experimentales tratados con el software X'Pert Highscore (versión 2.2a) .
En presencia de impurezas o excipientes, en particular en presencia de lactosa, determinados picos de difracción RX de la forma delta del perindopril arginina según la invención pueden estar enmascarados.
En este caso, dependiendo de la naturaleza de los excipientes o impurezas, la forma cristalina delta del perindopril arginina según la invención podrá estar caracterizada por los siguientes picos de difracción RX en polvo, medidos en difractómetro de anticátodo de cobre y expresados en términos de ángulo 2-theta (º) : 4, 3, 11, 0, 11, 1, 13, 2, 14, 6, 16, 0 y 21, 9; o 4, 3, 11, 0, 11, 1, 11, 9, 13, 2, 14, 6, 19, 2, 21, 9 y 22, 6; o 4, 3, 11, 0, 11, 1, 11, 9, 12, 5, 13, 2, 14, 6, 16, 0, 19, 2, 19, 4, 21, 9, 22, 2 y 22, 6.
La forma cristalina delta de la sal de arginina de perindopril también ha sido caracterizada mediante espectroscopia RMN en estado sólido.
El espectro 13C-RMN en estado sólido se registra a temperatura ambiente con ayuda de un espectrómetro Bruker SB Avance con una sonda de tipo 4 mm CP/MAS SB VTN bajo las siguientes condiciones:
- Frecuencia: 125, 76 MHz.
- Anchura espectral: 40 kHz.
- Velocidad de rotación de la muestra en ángulo mágico (Magic Angle Spinning Rate) : 10 kHz.
- Secuencia de impulsión CP (Cross Polarizaton) con desacoplamiento SPINAL64 (potencia de desacoplamiento de 80 kHz) .
- Plazo de repeticiones: 10 s.
- Tiempo de adquisición: 47 ms.
- Tiempo de contacto: 4 ms.
- Número de barridos: 4096. Antes de una transformación de Fourier se aplica un ensanchamiento de las líneas de 5 Hz. El espectro así obtenido está referido con respecto a una muestra de adamantano (pico de alta frecuencia del
adamantano fijado a 38, 48 ppm) . Los picos observados se reúnen en la siguiente tabla (expresados en ppm ± 0, 2 ppm) :
Pico nº Desplazamiento químico (ppm) Pico nº Desplazamiento químico (ppm)
1 2 3 4 5 6 7 8 9 181, 2 180, 5 180, 1 174, 0 173, 7 172, 7 172, 0 39, 3 38, 8 10 11 12 13 14 38, 4 15, 6 15, 2 15, 0 14, 5
La invención también se refiere a un procedimiento para la preparación de la forma cristalina delta de la sal de arginina de perindopril, por cristalización o recristalización de la sal de arginina de perindopril en una mezcla binaria de acetonitrilo, acetato de etilo o metil terc-butil éter y de sulfóxido de dimetilo o en una mezcla ternaria de acetonitrilo, sulfóxido de dimetilo y tolueno, a una temperatura superior a 20ºC.
En caso de un procedimiento por cristalización, la sal de arginina de perindopril se puede obtener a partir de otra sal de perindopril, por ejemplo la sal de terc-butilamina, que se somete a reacción con un ácido para obtener el perindopril en forma de ácido libre, el cual se salifica con arginina en una mezcla binaria de acetonitrilo, acetato de etilo o metil terc-butil éter y sulfóxido de dimetilo o en una mezcla ternaria de acetonitrilo, sulfóxido de dimetilo y tolueno.
En caso de un procedimiento por recristalización, la sal de arginina de perindopril utilizada como materia prima puede estar en forma anhidra o en forma hidratada, en forma amoría o en cualquier tipo de forma cristalina.
Cuando se utiliza una mezcla binaria de acetonitrilo, acetato de etilo o metil terc-butil éter y sulfóxido de dimetilo, la proporción acetonitrilo/sulfóxido de dimetilo, acetato de etilo/sulfóxido de dimetilo o metil terc-butil éter/sulfóxido de dimetilo oscila preferentemente entre 90/10 m/m y 10/90 m/m, ambos inclusive.
La temperatura del medio durante la cristalización o recristalización oscila preferentemente entre 25ºC y 80ºC, ambos inclusive, en particular entre 60ºC y 80ºC, ambos inclusive.
Ventajosamente, la mezcla se puede sembrar durante la etapa de enfriamiento (modo "con siembra") .
Cuando la mezcla no se siembra (modo "sin siembra") , el tiempo de puesta en contacto con la mezcla de disolventes preferiblemente es superior a 6 horas.
La invención se refiere también a las composiciones farmacéuticas que contienen como principio activo la forma cristalina delta del compuesto de fórmula (I) junto con uno o varios excipientes inertes, no tóxicos y apropiados. Entre las composiciones farmacéuticas según la invención se pueden citar, más en particular, aquellas que son adecuadas para la administración vía oral, parenteral (intravenosa o subcutánea) , nasal, los comprimidos simples o en grageas, los comprimidos sublinguales, grageas, tabletas, supositorios, cremas, pomadas, geles dérmicos, preparaciones inyectables, suspensiones bebibles.
La composición farmacéutica en forma de comprimido se prepara preferentemente por compresión directa.
La posología... [Seguir leyendo]
Reivindicaciones:
1. Forma cristalina delta de la sal de L-arginina de perindopril, de fórmula (I) :
caracterizada por los siguientes picos de difracción RX en polvo, medidos en un difractómetro de anticátodo de cobre y expresados en términos de ángulo de Bragg 2 theta (º) : 4, 3, 11, 0, 11, 1, 13, 2, 14, 6, 16, 0 y 21, 9.
2. Forma cristalina delta del compuesto de fórmula (I) según la reivindicación 1, caracterizada por los siguientes picos de difracción RX en polvo, medidos en un difractómetro de anticátodo de cobre y expresados en términos de ángulo de Bragg 2 theta (º) : 4, 3, 11, 0, 11, 1, 11, 9, 12, 5, 13, 2, 14, 6, 16, 0, 19, 2,
19, 4, 20, 0, 21, 9, 22, 2 y 22, 6.
3. Forma cristalina delta del compuesto de fórmula (I) según la reivindicación 1, caracterizada por el siguiente diagrama de difracción X en polvo, medido en un difractómetro de anticátodo de cobre y expresado en términos de distancia interreticular d, ángulo de Bragg 2 theta e intensidad relativa, expresada en porcentaje con respecto a la línea más intensa:
4. Forma cristalina delta del compuesto de fórmula (I) según la reivindicación 1, caracterizada por un espectro RMN en estado sólid.
13. CPMAS que presenta los siguientes picos, expresados en ppm:
Ángulo 2 theta (º) Distancia interreticular d[Å] Intensidad relativa [%]
4, 34 20, 37 66, 2
5, 57 15, 86 5, 2
11, 04 8, 02 57, 5
11, 15 7, 94 47, 5
11, 87 7, 454 35, 0
12, 47 7, 09 17, 9
13, 21 6, 70 33, 6
14, 06 6, 30 6, 6
14, 64 6, 05 31, 8
16, 03 5, 53 17, 5
17, 11 5, 18 5, 6
18, 27 4, 85 4, 1
19, 23 4, 61 100
19, 44 4, 57 17, 8
20, 04 4, 43 13, 6
21, 11 4, 21 3, 7
21, 93 4, 05 23, 0
Ángulo 2 theta (º) Distancia interreticular d[Å] Intensidad relativa [%]
22, 20 4, 00 16, 9
22, 61 3, 93 21, 2
23, 21 3, 83 4, 5
24, 30 3, 66 2, 3
25, 09 3, 55 9, 4
25, 95 3, 43 1, 7
29, 54 3, 02 4, 2
Pico nº Desplazamiento Pico nº Desplazamiento
químico (ppm) químico (ppm)
1 181, 2 10 38, 4
2 180, 5 11 15, 6
3 180, 1 12 15, 2
4 174, 0 13 15, 0
5 173, 7 14 14, 5
6 172, 7
7 172, 0
8 39, 3
9 38, 8
5. Procedimiento de preparación de la forma cristalina delta del compuesto de fórmula (I) según cualquiera de las reivindicaciones 1 a 4, por cristalización o recristalización en una mezcla binaria de acetonitrilo, acetato de etilo o metil terc-butil éter y sulfóxido de dimetilo o en una mezcla ternaria de acetonitrilo, sulfóxido de dimetilo y tolueno, a una temperatura superior a 20ºC.
6. Procedimiento según la reivindicación 5, caracterizado porque la mezcla binaria de acetonitrilo, acetato de etilo o metil terc-butil éter y sulfóxido de dimetilo presenta una proporción acetonitrilo/sulfóxido de dimetilo, acetato de etilo/sulfóxido de dimetilo o metil terc-butil éter/sulfóxido de dimetilo que oscila entre 90/10 m/m y 10/90 m/m.
7. Procedimiento según cualquiera de las reivindicaciones 5 o 6, caracterizado porque la temperatura del medio oscila entre 25ºC y 80ºC, ambos inclusive.
8. Procedimiento según la reivindicación 7, caracterizado porque el medio se calienta a una temperatura de 60 a 80ºC.
9. Procedimiento según cualquiera de las reivindicaciones 5 a 8, caracterizado porque el medio se siembra con la forma cristalina delta.
10. Composición farmacéutica que contiene como principio activo el compuesto según cualquiera de las
reivindicaciones 1 a 4, en combinación con uno o más vehículos inertes, no tóxicos y farmacéuticamente aceptables.
11. Composición farmacéutica según la reivindicación 10, caracterizada porque además contiene un diurético, un antagonista del calcio o un inhibidor de la corriente If.
12. Composición farmacéutica según la reivindicación 11, caracterizada porque el diurético es indapamida.
13. Composición farmacéutica según la reivindicación 11, caracterizada porque el antagonista del calcio es 5 amlodipino.
14. Composición farmacéutica según la reivindicación 11, caracterizada porque el inhibidor de la corriente If es ivabradina.
15. Compuesto según cualquiera de las reivindicaciones 1 a 4, para su utilización en el tratamiento de enfermedades cardiovasculares.
16. Compuesto según cualquiera de las reivindicaciones 1 a 4, para su utilización en el tratamiento de hipertensión arterial, insuficiencia cardíaca o enfermedad coronaria estable.
Patentes similares o relacionadas:
Compuestos de tienopirrol y usos de los mismos como inhibidores de luciferasas procedentes de Oplophorus, del 6 de Mayo de 2020, de PROMEGA CORPORATION: Un compuesto de fórmula (I), o una sal del mismo: **(Ver fórmula)** en la que: la línea discontinua representa la presencia o ausencia de un enlace; X es […]
Compuestos heterocíclicos y métodos para su uso, del 8 de Abril de 2020, de NOVARTIS AG: Un compuesto de formula (I): **(Ver fórmula)** donde: X esta ausente e Y es -CHR3CH2-, -CH2CHR3-, -CHR3CHR4CH2-, -CH2CHR3CHR4-, -CH2CH2CHR3-, -CR3=CHCH2-, […]
Modificaciones de proteínas quimioenzimáticas específicas para lisina utilizando transglutaminasa microbiana, del 21 de Agosto de 2019, de NOVARTIS AG: Un método para modificar una proteína, que comprende: proporcionar una proteína diana que tiene al menos un residuo de lisina; poner […]
Derivados de indol mono- o disustituidos como inhibidores de la replicación del virus del dengue, del 27 de Mayo de 2019, de Janssen Pharmaceuticals, Inc: Un compuesto de fórmula (I)**Fórmula** una forma estereoisomérica, una sal, un solvato o un polimorfo farmacéuticamente aceptables de estos, […]
Indoles mono o disustituidos como inhibidores de la replicación del virus del dengue, del 30 de Abril de 2019, de Janssen Pharmaceuticals, Inc: Un compuesto de fórmula (I)**Fórmula** una forma estereoisomérica, una sal, un solvato o un polimorfo farmacéuticamente aceptables de este, que comprende un grupo indol […]
Agentes de obtención de imágenes de carga equilibrada, del 4 de Octubre de 2018, de BETH ISRAEL DEACONESS MEDICAL CENTER, INC.: Un método para obtener imágenes de tejido o células, comprendiendo el método: (a) poner en contacto el tejido o las células con un agente de obtención de […]
Un proceso mejorado para la preparación de perindoprilo intermedio, del 14 de Marzo de 2018, de Piramal Enterprises Limited: Un proceso para la preparación de un compuesto de fórmula II,**Fórmula** comprendiendo, hacer reaccionar el compuesto de fórmula III,**Fórmula** con […]
Derivados de indolcarboxamida y usos de los mismos, del 22 de Noviembre de 2017, de NOVARTIS AG: Un compuesto de Fórmula (I)**Fórmula** en donde R1 es H; R2 es H, metilo, trifluorometilo, cloro, bromo, fluoro, o ciano; R3 es H; R4 es […]