Anticuerpos monoclonales que reconocen selectivamente Metanfetamina y compuestos similares a Metanfetamina.
Un anticuerpo monoclonal que reconoce cada compuesto del grupo que consiste en (+)anfetamina,
(+)metanfetamina y (+)3,4-metilendioximetanfetamina, obtenible usando un agente inmunizante que comprende lafórmula **Fórmula**
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/071354.
Solicitante: THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ARKANSAS.
Inventor/es: CARROLL, IVY F., OWENS,MICHAEL S, GUNNELL,MELINDA, CHI,YINGNI, HENRY,RALPH, PETERSON,ERIC.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07K16/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
PDF original: ES-2415655_T3.pdf
Fragmento de la descripción:
Anticuerpos monoclonales que reconocen selectivamente Metanfetamina y compuestos similares a Metanfetamina Derechos gubernamentales
Campo de la invención [0001] La invención proporciona anticuerpos monoclonales que reconocen (+) metanfetamina, (+) anfetamina y (+) 3, 4-metilendioximetanfetamina ( (+) MDMA) , pero no reconocen (-) metanfetamina, (-) anfetamina o (-) MDMA.
Antecedentes de la invención [0002] El abuso de (+) metanfetamina ( (+) METH) se ha convertido en la amenaza de drogas número uno de América (NACO, 2005) . Todas las estrategias conocidas para combatir el uso de las drogas de (+) metanfetamina tienen inconvenientes. Las presentes farmacoterapias para controlar el sistema cardiovascular agudo, sistema nervioso central y efectos tóxicos son habitualmente auxiliares (Sato, 1992; Albertson y col., 1999; Richards y col., 1999) ; y no hacen nada para eliminar la droga de sus sitios de acción en el cerebro. También faltan medicaciones que puedan reducir o tratar los efectos médicamente incapacitantes de la adicción a (+) METH. Los anticuerpos proporcionan una posible medicación atractiva que puede elegir como diana la droga en lugar del sitio de acción (Kosten y Owens, 2005) . Estas medicaciones basadas en proteínas de alta afinidad actúan de los llamados antagonistas farmacocinéticos, secuestrando la droga en la circulación sanguínea de tejidos médicamente vulnerables como el cerebro y corazón.
A diferencia de la nicotina y la cocaína en las que los efectos se producen por un único compuesto específico, drogas como los opiáceos (por ejemplo, morfina) , arilciclohexilaminas (por ejemplo, fenciclidina) y anfetaminas (por ejemplo, (+) METH) son estructuras de partida a partir de las cuales pueden sintetizarse muchos compuestos farmacológicamente similares. Estas llamadas “drogas de diseño” pueden modificarse químicamente para alterar sus efectos. Así, para que un anticuerpo tenga la aplicabilidad médica más amplia debe tener alta afinidad y especificidad por más de un miembro médicamente importante de esta clase de drogas (es decir, (+) METH, (+) anfetamina ( (+) AMP) y (+) MDMA) .
Hay otros asuntos del diseño de medicaciones que adicionalmente complican el desarrollo de tratamientos eficaces para estimulantes similares a (+) METH. Primero, la (+) METH es una de las varias drogas estimulantes con efectos similares o solapantes. En particular, la (+) AMP es tanto un metabolito farmacológicamente activo de (+) METH como una droga frecuentemente usada que podría sustituirse por (+) METH. A continuación, la (+/-) 3, 4metilendioximetanfetamina es la mezcla racémica comúnmente denominada MDMA o éxtasis. El isómero positivo ( (+) MDMA) tiene predominantemente actividad dopaminérgica similar a estimulante con efectos solapantes con (+) METH, mientras que la (-) MDMA tiene efectos predominantemente serotonérgicos (Cho y Segal, 1994) . (+) METH, (+) AMP y (+) MDMA pueden producir efectos potencialmente mortales a altas dosis (Cho y Segal, 1994; Farre y col., 2004) . Adicionalmente, todas estas drogas son estereoisómeros positivos, teniendo los isómeros negativos un perfil farmacológico de efectos significativamente diferente, algunos de los cuales pueden ser beneficiosos. Por ejemplo, la (-) metanfetamina se usa comúnmente como broncodilatador en medicaciones de venta sin receta. Los isómeros negativos de estas drogas podrían ser posiblemente intencionadamente tomados por drogadictos para neutralizar medicaciones de mAb con alta afinidad de unión por tanto estereoisómeros positivos como negativos. De una forma relacionada, hay muchos compuestos estructuralmente similares como efedrina y pseudoefedrina que podrían usarse para reducir la eficacia de anticuerpos si el anticuerpo no es altamente específico por estructuras similares a (+) METH.
Hay una necesidad en la materia de anticuerpos específicos que reconozcan al menos una o más de (+) metanfetamina, (+) anfetamina o (+) MDMA, y que no reaccionan sustancialmente de forma cruzada con () metanfetamina, (-) anfetamina o (-) MDMA. En particular, existe la necesidad de anticuerpos monoclonales específicos que reconozcan cada compuesto del grupo que consiste en (+) metanfetamina, (+) anfetamina y (+) MDMA, y que no reaccionen sustancialmente de forma cruzada con (-) metanfetamina, (-) anfetamina o (-) MDMA.
Referencia a las figuras en color
El archivo de la solicitud contiene al menos una fotografía realizada en color. Copias de la presente publicación de solicitud de patente con fotografías en color serán proporcionadas por la oficina a petición y pago de la tasa necesaria.
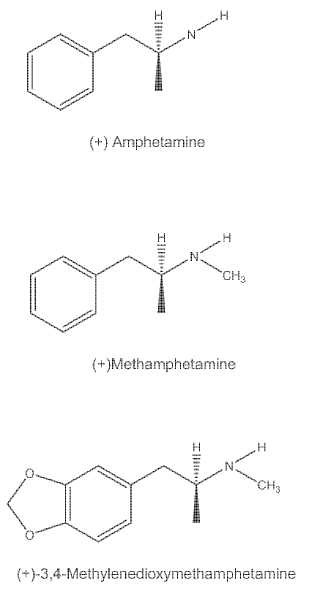
Breve descripción de las figuras [0007] La Fig. 1 representa las estructuras químicas de (+) metanfetamina, (+) anfetamina y (+) 3, 4metilendioximetanfetamina ( (+) MDMA) .
La Fig. 2 presenta los alineamientos de secuencias de aminoácidos de las regiones variables de cinco mAb anti- (+) METH y anti- (+) METH/ (+) AMP, y anti- (+) METH/ (+) AMP/ (+) MDMA de afinidad moderada a alta (en la presente memoria, mAb se refiere a anticuerpos monoclonales, tanto en singular como en plural) . El Panel A presenta las secuencias de aminoácidos de las cadenas pesadas. El Panel B presenta las secuencias de aminoácidos de las cadenas ligeras. Las secuencias se presentan en la notación de aminoácidos de una sola letra y se numeran según Kabat y Wu (1991 J Immunol 147:1709-1719) . Se indica la localización de los residuos de la región estructural (FR) y región determinante de la complementariedad (CDR) para las cadenas pesadas y las cadenas ligeras.
La Fig. 3 presenta modelos moleculares de tres mAb anti- (+) METH. Panel superior: Estereovista de modelos moleculares superpuestos de mAb anti- (+) METH. Se modelaron las regiones variables de los tres mAb, se alinearon estructuralmente y se representaron en formato de dibujo. Los residuos de la región estructural se representan en azul. Las CDR están coloreadas según mAb: mAb6H4, azul; mAb6H8, rojo; mAb4G9, verde. Están marcadas la cadena pesada, la cadena ligera y CDR. Panel inferior: Desviaciones de la raíz cuadrada media (RMSD) (A) de CDR de la conformación de cadena principal de mAb6H4.
La Fig. 4 ilustra estructuras modeladas de las cadenas variables de mAb anti- (+) METH. En este modelo, METH (magenta) se ha acoplado molecularmente informáticamente en un bolsillo en la superficie de separación de las cadenas VH y VL con el software FlexX. Paneles izquierdos: Representación de superficie tridimensional del bolsillo profundo en mAb6H4 y mAb4G9. El dominio de la cadena VL está a la izquierda en azul y el dominio de la cadena VH está a la derecha en verde. Paneles derechos: Representación de varillas de mAb6H4 y mAb4G9. Sólo se muestran cadenas laterales dentro de 8 angstroms de la molécula de METH por claridad. La vista está orientada en un “vista desde arriba” con el mismo esquema de color que en el panel izquierdo. Las cadenas laterales están marcadas y numeradas en el esquema de Kabat como en la Figura 2.
La Fig. 5 presenta una gráfica que representa concentración en suero de (+) METH con el tiempo. Concentraciones de (+) METH antes (símbolo D con “M” dentro) y después del tratamiento (símbolos blancos) con cinco mAb anti- (+) METH diferentes (n=3 ratas/momento de tiempo) y concentraciones de (+) AMP antes (símbolo D con “A” dentro) y después del tratamiento (círculos rellenos) con mAb4G9. Las concentraciones de (+) AMP (círculos rellenos) se muestran sólo para mAb4G9 debido a que los otro cuatro mAb no produjeron aumentos a largo plazo en las concentraciones de (+) AMP. La recta de ajuste óptimo se determinó usando un modelo farmacocinético de dos compartimentos ponderado.
La Fig. 6 presenta gráficas que representan el efecto de mAb4G9 sobre la discriminación de METH (Panel A) y la auto-administración de AMP (Panel B) en ratas. (A) Se entrenaron ratas para discriminar cocaína y METH y luego se les administró mAb4G9. Entonces se determinaron las curvas de respuesta a dosis de discriminación de droga para METH. (B) Auto-administración de (+) AMP antes y después del tratamiento con mAb4G9 (3-4 ratas/momento de tiempo) . Se usan líneas discontinuas para mostrar los agrupamientos de respondedores a (+) AMP antes y después de mAb. *P<0, 05 en comparación con el grupo de control antes del anticuerpo (círculos blancos) .
La Fig. 7 representa dos gráficas que muestran el efecto de mAb6H4 (Panel A) y mAb4G9 (Panel B) sobre concentraciones de METH (círculos rellenos) y AMP (círculos blancos) en suero de rata. METH se infundió usando una minibomba osmótica subcutánea y, una vez se alcanzaron las concentraciones en estado estacionario, se administró mAb anti-METH. Las ratas... [Seguir leyendo]
Reivindicaciones:
1. Un anticuerpo monoclonal que reconoce cada compuesto del grupo que consiste en (+) anfetamina,
(+) metanfetamina y (+) 3, 4-metilendioximetanfetamina, obtenible usando un agente inmunizante que comprende la 5 fórmula 2. El anticuerpo monoclonal de la reivindicación 1, en el cual el anticuerpo tiene una relación de CI50 de inferior al 15% para cada compuesto del grupo que consiste en (-) anfetamina, (-) metanfetamina y (-) 3, 4metilendioximetanfetamina en el cual la relación de CI50 es la relación de CI50 para (+) metanfetamina en presencia de (+) metanfetamina marcada con respecto a CI50 para un ligando de prueba en presencia de (+) metanfetamina marcada.
3. El anticuerpo monoclonal de la reivindicación 1 ó 2, en el cual el anticuerpo tiene una relación de CI50 superior al 20% para cada compuesto del grupo que consiste en (+) anfetamina, (+) metanfetamina y (+) 3, 4
metilendioximetanfetamina, en el cual la relación de CI50 es la relación de CI50 para (+) metanfetamina en presencia de (+) metanfetamina marcada con respecto a CI50 para un ligando de prueba en presencia de (+) metanfetamina marcada.
4. El anticuerpo monoclonal de cualquier reivindicación precedente, en el cual el anticuerpo tiene una relación de CI50 inferior al 12% para cada compuesto del grupo que consiste en (-) anfetamina, (-) metanfetamina y (-) 3, 4metilendioximetanfetamina, en el cual la relación de CI50 es la relación de CI50 para (+) metanfetamina en presencia de (+) metanfetamina marcada con respecto a CI50 para un ligando de prueba en presencia de (+) metanfetamina marcada.
5. El anticuerpo monoclonal de cualquier reivindicación precedente, en el cual el anticuerpo tiene una relación de CI50 superior al 25% para cada compuesto del grupo que consiste en (+) anfetamina, (+) metanfetamina y (+) 3, 4metilendioximetanfetamina, en el cual la relación de CI50 es la relación de CI50 para (+) metanfetamina en presencia de (+) metanfetamina marcada con respecto a CI50 para un ligando de prueba en presencia de (+) metanfetamina marcada.
6. El anticuerpo monoclonal de cualquier reivindicación precedente, en el cual la cadena pesada del anticuerpo comprende la secuencia de aminoácidos de SEC ID Nº: 25 y la cadena ligera del anticuerpo comprende la secuencia de aminoácidos de SEC ID Nº: 26.
7. El anticuerpo monoclonal de cualquiera de las reivindicaciones 1-5, en el cual la cadena pesada del anticuerpo comprende la secuencia de aminoácidos de SEC ID Nº: 19 y la cadena ligera del anticuerpo comprende la secuencia de aminoácidos de SEC ID Nº: 21.
8. El anticuerpo monoclonal de cualquier reivindicación precedente, en el cual el anticuerpo está seleccionado del
grupo que consiste en un anticuerpo murino, un anticuerpo humano, un anticuerpo humanizado, un anticuerpo quimérico, un anticuerpo recombinante y un fragmento de anticuerpo.
9. Un anticuerpo monoclonal según cualquier reivindicación precedente para su uso en terapia.
10. Un anticuerpo monoclonal según cualquier reivindicación precedente para su uso en un procedimiento de tratamiento del uso de drogas en un sujeto, en el cual el anticuerpo monoclonal disminuye la concentración de (+) anfetamina, (+) metanfetamina y (+) 3, 4-metilendioximetanfetamina en el cerebro del sujeto.
11. El anticuerpo monoclonal de la reivindicación 10, en el cual el sujeto está seleccionado del grupo que comprende 50 un roedor, un primate no humano y un ser humano.
12. Un ensayo para detectar la presencia de al menos un compuesto en una muestra seleccionada del grupo de compuestos que consiste en (+) metanfetamina, (+) anfetamina y (+) 3, 4-metilendioximetanfetamina, comprendiendo el ensayo poner en contacto la muestra con un anticuerpo monoclonal de la reivindicación 1 y detectar la asociación 55 del anticuerpo monoclonal en la muestra con al menos un compuesto seleccionado del grupo que consiste en (+) metanfetamina, (+) anfetamina y (+) 3, 4-metilendioximetanfetamina.
13. El ensayo de la reivindicación 12, en el cual la muestra es una muestra biológica o una muestra química.
14. El ensayo de la reivindicación 12 ó 13, en el cual la asociación se detecta por un medio seleccionado del grupo que consiste en ELISA, ensayo inmunocromatográfico y ensayo de inmunoprecipitación.
15. Un kit, en el cual el kit comprende un anticuerpo monoclonal según cualquiera de las reivindicaciones 1 a 11.
REFERENCIAS CITADAS EN LA DESCRIPCIÓN
Esta lista de referencias citadas por el solicitante es únicamente para la comodidad del lector. No forma parte del documento de la patente europea. A pesar del cuidado tenido en la recopilación de las referencias, no se pueden excluir errores u omisiones y la EPO niega toda responsabilidad en este sentido.
Documentos de patentes citados en la descripción Literatura diferente de patentes citadas en la descripción
Patentes similares o relacionadas:
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Terapia basada en anticuerpos de la amiloidosis por transtiretina (TTR) y anticuerpos de origen humano para ese propósito, del 22 de Julio de 2020, de Neurimmune Holding AG: Un anticuerpo anti-transtiretina (TTR) de origen humano o un fragmento de unión a antígeno del mismo, que es capaz de unirse a especies de TTR mutadas, mal plegadas, […]
Polipéptidos biparatópicos antagonistas de la señalización WNT en células tumorales, del 15 de Julio de 2020, de Boehringer Ingelheim International GmbH & Co. KG: Un polipéptido que se une específicamente a LRP5 o LRP6, que comprende - un primer dominio variable individual de inmunoglobulina seleccionado del grupo de dominios […]
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Redirectores de células T específicas de antígenos, del 1 de Julio de 2020, de THE JOHNS HOPKINS UNIVERSITY: Una nanoparticula que comprende en su superficie: (A) un anticuerpo que se une especificamente a un antigeno de celula diana o epitopo del mismo; y (B) un resto […]
Anticuerpos scFv que pasan las capas epitelial y/o endotelial, del 1 de Julio de 2020, de ESBATech, an Alcon Biomedical Research Unit LLC: Un anticuerpo monocatenario (scFv) que comprende: (a) un dominio variable de la cadena ligera (VL) que tiene tres regiones CDR de VL no […]
Un antígeno asociado con artritis reumatoide, del 24 de Junio de 2020, de PHILOGEN S.P.A.: Un conjugado de anticuerpo para su uso en un procedimiento de tratamiento de la artritis reumatoide en un paciente, en el que el conjugado de anticuerpo comprende […]
Moléculas de unión con cadena J modificada, del 24 de Junio de 2020, de IGM BIOSCIENCES, INC: Una molécula de unión que comprende un anticuerpo de IgM, IgA, IgG/IgM o IgG/IgA con una cadena J modificada, donde la cadena J modificada comprende una cadena […]