Análogos de CAP de ARNm.
Uno o más de los siguientes compuestos, o un estereoisómero de uno o más de los siguientes compuestos,
omezclas de estereoisómeros de uno o más de los siguientes compuestos, o una sal o sales de cualquiera de ellos:**Fórmula**
1donde Y1, Y2, Y3 y Y4 se seleccionan del grupo que consiste en O, BH3 y Se; los diversos grupos Yi pueden seriguales o diferentes, donde i es 1, 2, 3 ó 4; y al menos un Yi es BH3 o Se;
n es 0 ó 1;
R se selecciona del grupo que consiste en:**Fórmula**
R3 y R4 se seleccionan del grupo que consiste en H, OH, OCH3 y OCH2CH3; y R3 y R4 pueden ser iguales odiferentes.
W se selecciona del grupo que consiste en: **Fórmula**
R1 y R2 se seleccionan del grupo que consiste en H, OH, OCH3 u OCH2CH3; y R1 y R2 pueden ser iguales odiferentes; y
X se selecciona del grupo que consiste en metilo, etilo, propilo, butilo, bencilo, bencilo sustituido, metilennaftilo ymetilennaftilo sustituido.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/046249.
Solicitante: UNIWERSYTET WARSZAWSKI.
Nacionalidad solicitante: Polonia.
Dirección: Ul. Krakowskie Przedmiescie 26/28 00-927 Warszawa POLONIA.
Inventor/es: KOWALSKA,JOANNA, JEMIELITY,JACEK, DARZYNKIEWICZ,EDWARD, RHOADS,ROBERT E, LUKASZEWICZ,MACIEJ, ZUBEREK,JOANNA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07H21/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos.
- C07H21/02 C07H […] › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con ribosilo como radical sacárido.
PDF original: ES-2425781_T3.pdf
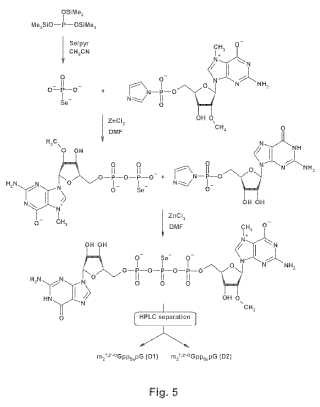
Fragmento de la descripción:
El desarrollo de esta invención fue subvencionado parcialmente por el gobierno de los Estados Unidos de América bajo el subsidio número R01GM20818 otorgado por el Instituto Nacional de Ciencias Médicas Generales de los Institutos Nacionales de la Salud (National Institute of General Medical Sciences of the National lnstitutes of Health) . El gobierno de los Estados Unidos de América posee determinados derechos sobre esta invención.
El desarrollo de esta invención fue subvencionado parcialmente por el gobierno de Polonia bajo el subsidio número PBZ-MNiSW-07/1/2007 otorgado por el Proyecto Nacional de Apoyo a las Ciencias 2008-2010.
Campo técnico Esta invención se refiere a los nuevos análogos de caperuza de dinucleótidos y sus usos, las moléculas de ARN que contienen estos análogos, el uso de estos análogos en la síntesis de ARN, el uso de estos análogos en la síntesis de péptidos y proteínas, el uso de estos análogos para inhibir la traducción y otros usos.
Antecedentes El ácido ribonucleico (ARN) es un polímero lineal de cadena sencilla de nucleótidos. Cada unidad de nucleótido contiene una base nitrogenada, un azúcar de ribosa y un grupo fosfato. Existen diferentes tipos de moléculas de ARN. Las moléculas de ARN mensajero (ARNm) son aquellas cuya secuencia de nucleótidos determina la composición aminoácida de las proteínas. En eucariotes, los extremos 5' de la mayoría de los ARNm están bloqueados, o "encaperuzados" con un nucleótido modificado de guanina. La caperuza contiene un enlace 5'-5' de trifosfato entre dos nucleósidos y un grupo 7-metilo en un anillo de guanina distal a la cadena polimérica de ARN. Otras formas del ARN también llevan caperuza, por ejemplo, los pequeños ARNnucleares (ARNpn) . El uso de caperuzas en el ARN regula las actividades moleculares intracelulares, incluidas la estabilidad del ARN y la eficiencia de la traducción.
La capacidad de sintetizar in vitro moléculas de ARN con caperuza es útil porque permite la preparación de moléculas de ARN que funcionarán correctamente en una variedad de aplicaciones biológicas. Estas aplicaciones incluyen tanto aplicaciones en la investigación como en la producción comercial de polipéptidos, por ejemplo la producción de polipéptidos en un sistema acelular de traducción que contiene un aminoácido "no natural" en un lugar específico, o la producción de polipéptidos en células cultivadas que requieren la modificación posttraduccional de la actividad o estabilidad. Debido a que las moléculas con caperuza de ARN son más estables y se enlazan más fácilmente a la maquinaria celular traduccional, la traducción de los ARN con caperuza continúa durante un período considerablemente más largo que en el caso de los ARN sin caperuza, lo que tiene como resultado una producción mayor de proteínas.
El método usado con mayor frecuencia para la preparación in vitro de ARN con caperuza es la transcripción de una plantilla de ADN con una polimerasa de ARN bacteriano o bacteriófago en presencia de los cuatro trifosfatos de ribonucleósido y un dinucleótido bloqueado como m7G (5') ppp (5') G (también conocido como m7GpppG) . La polimerasa de ARN inicia la transcripción con un ataque nucleofílico por el 3'-OH del grupo Guo de m7GpppG sobre el a-fosfato del siguiente trifosfato de nucleósido en la plantilla, produciendo el producto intermedio m7GpppGpN. La formación del producto competidor iniciado por GTP pppGpN se suprime al definir el cociente molar entre m7GpppG y GTP como de 5 a 10 en la mezcla de reacción de transcripción. Los ARNm con caperuza en 5' producidos con m7GpppG pueden adoptar una de las siguientes dos formas: una que contiene el análogo con caperuza incorporado en la orientación correcta hacia el frente [m7G (5') ppp (5') GpNp...] y otra que contiene el análogo en la posición inversa [G (5') ppp (5') m7GpNp...]. La maquinaria traduccional de la célula no reconoce a éste último como un ARNm con caperuza y disminuye la eficiencia de traducción de las preparaciones sintéticas de ARNm. Este problema puede evitarse mediante el uso de análogos de caperuza que poseen modificaciones O-metilo o desoxi en la posición C2' ó C3' de m7GuO. Véase J. Stepinski et al., "Synthesis and properties of mRNAs containing the novel "anti-reverse" cap analogues 7-methyl (3'-O-methyl) GpppG y 7-methyl (3'-deoxy) GpppG", RNA, vol. 7, págs. 1.486
1.495 (2001) ; y J. Jemielity et al., "Novel "anti-reverse" cap analogues with superior translational properties", RNA, vol. 9, págs. 1108-1122 (2003) . Estos análogos de caperuza se incorporan a los transcriptos de ARN exclusivamente en la orientación hacia el frente y por lo tanto se conocen como "análogos de caperuza anti-inversos" (ARCA, por sus siglas en inglés) . En un lisado de reticulocito de conejo (LRC) , los ARNm con caperuza de ARCA poseen eficiencias traduccionales que son dos veces más altas que las de los transcriptos con caperuza de m7GpppG (Stepinski et al., 2001) . En células mamíferas cultivadas, los ARNm con caperuza de ARCA se traducen entre 2 y 2, 5 veces más eficientemente que los que llevan caperuza de m7GpppG. Véase E. Grudzien et al., "Differential inhibition of mRNA degradation pathways by novel cap analogs", J. Biol. Chem., vol. 281, págs. 1.857-1.867 (2006) .
La cantidad de proteína producida a partir de ARNm sintéticos introducidos a células mamíferas cultivadas está limitada por la degradación natural del ARNm. Una ruta in viva para la degradación del ARNm se inicia con la
eliminación del bloqueo del ARNm. Esta eliminación está catalizada por una pirofosfatasa heterodimérica, que contiene una subunidad reguladora (Dcp1) y una subunidad catalítica (Dcp2) . La subunidad catalítica se escinde entre los grupos fosfato a y º del puente trifosfato.
E. Grudzien et al. (2006) describieron un análogo de caperuza, m27, 3'-OGppCH2pG, en donde el átomo de oxígeno fue reemplazado con un grupo metileno entre los grupos a y 13 de fosfato. Los ARNm con caperuza de este análogo fueron resistentes a la hidrólisis con Dcp2 recombinante humano in vitro. Cuando se introducen a células cultivadas, los ARNm con caperuza del análogo m27, 3'-OGppCH2pG fueron más estables que los que llevan caperuza de m27, 3'-OGpppG. Sin embargo, el ARNm con caperuza de m27, 3'-OGppCH2pG posee una eficiencia traduccional general más baja, posiblemente debido a que m27, 3'-OGppCH2pG tiene una afinidad de enlace más baja por elF4E que la del m27, 3'-OGpppG. El factor de iniciación de la traducción eucariótica elF4E participa en llevar el ARNm con caperuza al ribosoma para la traducción.
J. Kowalska et al., "Synthesis and characterization of mRNA cap analogs containing phosphorothioate substitutions that bind tightly to elF4E and are resistant to the decapping pyrophosphatase DcpS", RNA, vol. 14, págs. 1.119-1.131 (2008) , describió las síntesis de tres ARCA en donde uno de los tres átomos de O no enlazantes en la cadena de trifosfato se reemplazó con un átomo de S. Cada uno de estos análogos de fosforotioato (también conocidos como S-ARCA) se sintetizó como una mezcla de diaestereoisómeros que pueden separarse cromatográficamente para producir diaestereoisómeros puros. La afinidad de enlace de los análogos de caperuza de fosforotioato al elF4E fue igual o, en algunos casos, superior a la del m7GpppG.
E. Grudzien et al., "Phosphorothioate cap analogs stabilize mRNA and increase translational efficiency in mammalian cells", RNA, vol. 13, págs. 1.745-1.755 (2007) , demostraron que los ARNm bloqueados con S-ARCA modificados en el º-fosfato fueron resistentes a la hidrólisis con Dcp2 recombinante humano in vitro. Asimismo, el ARNm bloqueado con un diaesteroisómero º S-ARCA tiene una vida media más larga cuando se introduce a células mamíferas que la del ARNm correspondiente bloqueado con ARCA, y además presenta una mayor eficiencia traduccional en las células. Probablemente, la primera de estas propiedades se debe a la resistencia del º S-ARCA a la hidrólisis por Dcp2, y probablemente la segunda propiedad se debe la mayor afinidad de º-S-ARCA por elF4E.
Otro uso de los análogos sintéticos de caperuza de ARNm es inhibir la traducción dependiente de la caperuza mediante la competencia con el ARNm con caperuza por enlace a elF4E. Véase A. Cai et al., "Quantitative assessment of mRNA cap analogues as inhibitors of in vitro translation", Biochemistr y , vol. 38, págs. 8.538-8.547 (1999) ; y E. Grudzien et al., "Novel cap analogs for in vitro synthesis of mRNAs with high translational efficiency", RNA, vol. 10, págs. 1.479-1.487 (2004) .
La capacidad de los análogos de caperuza de inhibir la traducción posee una importancia terapéutica potencial. Muchos tipos de células de cáncer sobreexpresan... [Seguir leyendo]
Reivindicaciones:
1. Uno o más de los siguientes compuestos, o un estereoisómero de uno o más de los siguientes compuestos, o mezclas de estereoisómeros de uno o más de los siguientes compuestos, o una sal o sales de cualquiera de ellos:
donde Y1, Y2, Y3 y Y4 se seleccionan del grupo que consiste en O, BH3 y Se; los diversos grupos Yi pueden ser iguales o diferentes, donde i es 1, 2, 3 ó 4; y al menos un Yi es BH3 o Se; n es 0 ó 1; 15 R se selecciona del grupo que consiste en:
R3 y R4 se seleccionan del grupo que consiste en H, OH, OCH3 y OCH2CH3; y R3 y R4 pueden ser iguales o diferentes.
W se selecciona del grupo que consiste en:
R1 y R2 se seleccionan del grupo que consiste en H, OH, OCH3 u OCH2CH3; y R1 y R2 pueden ser iguales o diferentes; y
X se selecciona del grupo que consiste en metilo, etilo, propilo, butilo, bencilo, bencilo sustituido, metilennaftilo y metilennaftilo sustituido.
2. Un compuesto como el indicado en la reivindicación 1; donde Y1, Y2, Y3 y Y4 se seleccionan del grupo que consiste en O, Se y BH3; los diversos grupos Y, pueden ser iguales o diferentes, donde i es 1, 2, 3, ó 4; y al menos un Yi es BH3 o Se;
3. Un compuesto como el indicado en la reivindicación 2, donde R se selecciona del grupo que consiste en:
4. Un compuesto como el indicado en la reivindicación 2, donde W es:
R2 es OH; R1 es H u OCH3; X es metilo, yn = 0; y sólo uno entre Y1, Y2 y Y3 es BH3 o Se.
5. Un compuesto como el indicado en la reivindicación 2, donde, si n = 0, entonces Y2 o Y3 es BH, o Se, y donde, si n = 1, entonces Y2, Y3 o Y4 es BH 3 o Se.
6. Una molécula de ARN cuyo extremo 5' incorpora un compuesto como el indicado en la reivindicación 2.
7. Una molécula de ARN cuyo extremo 5' incorpora un compuesto como el indicado en la reivindicación 5.
8. Una molécula de ARN como la indicada en la reivindicación 7, donde R se selecciona del grupo que consiste en:
9. Un método de síntesis, in vitro o in vivo, de una molécula de ARN como la indicada en la reivindicación 6, donde
dicho método comprende la reacción de ATP, CTP, UTP y GTP, una composición como la indicada, y una plantilla de polinucleótido en presencia de ARN polimerasa, bajo condiciones que conduzcan a la transcripción por el ARN polimerasa de la plantilla de polinucleótido en una copia del ARN; por lo cual algunas de las copias de ARN incorporarán el compuesto para formar una molécula de ARN como la indicada en la reivindicación 6.
10. Un método de síntesis de una proteína o péptido in vitro, donde dicho método comprende la traducción de una molécula de ARN como la indicada en la reivindicación 6 en un sistema acelular de síntesis de proteína, donde la molécula de ARN comprende un marco de lectura abierto, bajo condiciones adecuadas para la traducción del marco de lectura abierto de la molécula de ARN en la proteína o péptido codificado por el marco de lectura abierto.
11. Un método de síntesis de una proteína o péptido in vivo o en células cultivadas, donde dicho método comprende la traducción de una molécula de ARN como la indicada en la reivindicación 6 in vivo o en células cultivadas, donde la molécula de ARN comprende un marco de lectura abierto, bajo condiciones adecuadas para la traducción del marco de lectura abierto de la molécula de ARN en la proteína o péptido codificado por el marco de lectura abierto.
12. Un compuesto como el indicado en la reivindicación 2 para el uso en un método de inhibición total o parcial de la traducción del ARN en una proteína o péptido en un sistema que traduce el ARN en una proteína o péptido.
13. Un compuesto como el indicado en la reivindicación 2 para el uso en un método como el indicado en la 10 reivindicación 12, donde el sistema es un sistema nativo de traducción del ARN de un organismo vivo.
14. Una composición como la indicada en la reivindicación 2; donde R1 es OCH3; R2 es OH; R3 es OH; R4 es OH; n es O; Y1 es O; Y2 es Se; Y3 es O; W es y R es
Patentes similares o relacionadas:
Proteínas de unión a interleuquina-13, del 15 de Julio de 2020, de AbbVie Bahamas Ltd: Un anticuerpo anti-IL-13 recombinante, o fragmento de unión a antígeno del mismo, en donde dicho anticuerpo anti-IL-13 recombinante, o fragmento de unión a antígeno del mismo, […]
Polinucleótidos aislados y métodos y plantas que usan los mismos para regular la acidez de las plantas, del 10 de Junio de 2020, de The State of Israel, Ministry of Agriculture and Rural Development, Agricultural Research Organization, (A.R.O.), Volcani Cent: Una célula de planta o una planta que comprende una construcción de ácido nucleico que comprende una secuencia de ácido nucleico que codifica un polipéptido […]
Métodos y composiciones para modular PD1, del 13 de Mayo de 2020, de Sangamo Therapeutics, Inc: Célula aislada que comprende una inserción o una deleción en un gen de PD1 endógeno dentro de, o entre, las secuencias mostradas en SEQ ID NO: 56 y SEQ ID NO: 60 del gen de PD1 […]
Compuesto de tioéter para la protección del grupo 2''-hidroxi en nucleósidos que van a ser utilizados en la síntesis de oligonucleótidos, del 6 de Mayo de 2020, de Bonac Corporation: Un éter representado por la siguiente fórmula química : **(Ver fórmula)** en dicha fórmula química , R4 es un grupo alquilo de cadena lineal o ramificada […]
Métodos de preparación de polinucleótidos usando composiciones de sales de catiónicas multivalentes, del 6 de Mayo de 2020, de GERON CORPORATION: Un método para preparar un polinucleótido, comprendiendo el método: a) poner en contacto una primera composición polinucleotídica con una sal catiónica […]
Nucleótidos modificados para secuenciación de polinucleótidos, del 8 de Abril de 2020, de ILLUMINA CAMBRIDGE LIMITED: Una molécula de nucleótido que tiene una unidad estructural de azúcar ribosa o desoxirribosa y una base enlazada a un marcador detectable a través de […]
Análogos de oligonucleótidos que incorporan 5-aza-citosina en los mismos, del 8 de Enero de 2020, de Astex Pharmaceuticals, Inc: Un análogo de oligonucleótido aislado o sintético, o una sal o éster del mismo, de fórmula general 5'-DpG-3' o 5'-GpD-3', en los que D es decitabina; p es un […]
Nucleótidos modificados, del 1 de Enero de 2020, de ILLUMINA CAMBRIDGE LIMITED: Un kit que comprende cuatro moléculas de nucleótido trifosfato modificadas, cada una de las cuales comprende una base de purina o pirimidina y una unidad estructural […]