MÉTODO Y KIT PARA LA DETECCIÓN DE LA ACTIVACIÓN DE INTERFERÓN Y LA RESPUESTA INFLAMATORIA INDEPENDIENTE DE INTERFERÓN.
Método y kit para la detección de la activación del interferón y la respuesta inflamatoria independiente de interferón.
La presente invención se refiere a una combinación de cebadores y un método para la detección y/o cuantificación de la activación del interferón y la respuesta inflamatoria independiente de interferón. La amplificación se realiza mediante RT-PCR multiplex (mRT-PCR) donde los cebadores empleados amplifican los genes OAS2, ISG56, IL-8 e IFN{al} o IFN{be}. Además, la presente invención incluye un kit con la combinación de los cebadores mencionados y otros componentes.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201031026.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Nacionalidad solicitante: España.
Inventor/es: BERZAL HERRANZ,ALFREDO, REYES DARIAS,Jose Antonio.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12Q1/68 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
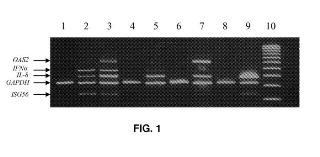
Fragmento de la descripción:
Método y kit para la detección de la activación de interferón y la respuesta inflamatoria independiente de interferón.
La presente invención se refiere a una combinación de cebadores y un método para la detección y/o cuantificación de la activación del sistema interferón y de la respuesta inflamatoria independiente de interferón producida por la liberación de citoquinas proinflamatorias. La amplificación se realiza mediante RT-PCR multiplex (mRT-PCR) donde los cebadores empleados amplifican los genes OAS2, ISG56, IL-8 e IFNα o IFNβ. Además, la presente invención se refiere a un kit con la combinación de los cebadores mencionados y otros componentes.
Estado de la técnica anterior
Los ácidos nucleicos pueden inhibir la expresión génica o actuar como agentes terapéuticos. Sin embargo, muchos de los ácidos nucleicos, incluidos los RNAs de cadena simple (ssRNA), RNAs de cadena doble (dsRNA) y oligodesoxirribonucleotidos (ODN) que contienen en su secuencia dinucleótidos CpG no metilados (CpG ODN), pueden estimular el sistema interferón o la respuesta inflamatoria independiente de interferón producida por la liberación de citoquinas proinflamatorias en los mamíferos.
Así, pequeños ssRNA pueden desencadenar una potente inducción de interferón en una variedad de líneas celulares, de la misma forma, pequeños RNA interferentes (siRNA) sintéticos o expresados a partir de plásmidos o vectores virales pueden inducir una importante respuesta mediada por interferón cuando se expresan en determinadas líneas celulares. Los CpG ODN sintéticos activan las células inmunes a través del receptor Toll-like 9 (TLR-9) estimulando el sistema interferón o la respuesta inflamatoria independiente de interferón producida por la liberación de citoquinas proinflamatorias. Estos CpG ODN se han dividido en tres clases, A, B y C, en función de su modo inmunoestimulador y su secuencia. Los CpG ODN de las clases A y C inducen altos niveles de interferón-α (IFN-α), en contraste, los CpG ODN de la clase B inducen preferentemente la producción de las citoquinas inflamatorias IL-6, IL-8 e IL-10, pero son relativamente pobres inductores del IFN-α (Vollmer J et al., 2004 J Endotoxin Res.10(6) pag. 431-438; Agrawal S y Kandimalla ER, 2007. Biochemical Society Transactions 35, 6). A diferencia de las IL-6 e IL-10, la IL-8 (citoquina proinflamatoria) es inducida en células no pertenecientes al sistema inmune, que expresan de forma estable el TLR-9 (Hemmi H et al., 2000 Nature. 7, 408(6813) pag. 740-745).
La inducción de citoquinas proinflamatorias y/o interferón (IFN) por la transfección o la administración in vivo de ácidos nucleicos pueden influir de manera significativa en las aplicaciones ex vivo o in vivo de estas estrategias de inactivación de la expresión génica o terapéuticas, debido a los efectos inespecíficos asociados con la respuesta del sistema interferón y/o a la toxicidad relacionada con la respuesta inflamatoria independiente de interferón desencadenada por la liberación de citoquinas proinflamatorias. Por ello, es recomendable, para cualquier ácido nucleico, que se esté utilizando con fines de inhibición de la expresión génica o terapéutica, mediante algún método eficaz, determinar si se produce o no la activación de la respuesta interferón y la detección de la expresión de citoquinas proinflamatorias. Esta comprobación es esencial para asignar inequívocamente a un determinado ácido nucleico un efecto inhibidor específico o terapéutico.
La activación del interferón implica la inducción de más de 300 genes estimulados por interferón (ISGs). La forma de saber si existe o no activación de la respuesta del interferón es analizando los niveles de los genes o proteínas inducidos por dicha respuesta. El desarrollo de kits comerciales proporciona un procedimiento para evaluar la existencia o no de efectos no específicos de activación de la respuesta dependiente de interferón, analizando los niveles de algunas proteínas (mediante análisis de western o Elisa) o genes (mediante PCR, del inglés Polymerase Chain Reaction) que son inducidos como consecuencia de la activación del sistema del interferón.
Actualmente sólo existe un kit en el mercado capaz de detectar mediante RT-PCR si pequeños siRNAs pueden afectar la respuesta dependiente de interferón, analizando, mediante dos pasos sucesivos, la expresión de los genes OAS1, OAS2, MX1, IFITM1 e ISGFγ (System biosciences "Interferón Response Detection Kit for validation of siRNA experiments" (Cat. #SI300A-1) User Manual).
La RT-PCR es la técnica más sensible que existe, para determinar la presencia o ausencia de un determinado RNA molde en una mezcla. La metodología usada para realizar una RT-PCR es realizar una reacción RT bajo óptimas condiciones y luego usar una fracción de la misma como molde para realizar una PCR convencional en un tubo diferente. Este procedimiento ha sido denominado RT-PCR en dos pasos o en dos tubos. Sin embargo, otra posibilidad más sencilla, es añadir todos los componentes necesarios para la RT y la PCR en un mismo tubo para realizar dichas reacciones en un solo paso y sin interrupción. Este procedimiento más simple se denomina RT-PCR en un solo paso o en un solo tubo y decrece considerablemente la probabilidad de la contaminación debida a la manipulación durante el proceso. Esta técnica monoespecífica permite la detección de un RNA diana, requiriendo, por tanto, tantas reacciones como número de RNAs queramos detectar.
Por otro lado, la mRT-PCR no sólo posee la sensibilidad de la técnica RT-PCR sino que además permite la detección y cuantificación simultánea de dos o más genes diana de una muestra de RNA en una misma reacción haciendo que el procedimiento sea mucho más rápido, de menor coste, y más reproducible debido a que exige una menor manipulación con lo que se minimizan errores y evita contaminaciones en este paso (Koch, 2004. Nat Rev Drug Discov, Vol. 3, 749-761). Sin embargo, debido a la complejidad que supone esta técnica a la hora de encontrar una combinación de cebadores específica que permita la amplificación simultánea de los genes seleccionados para la detección, actualmente sólo se dispone de un kit comercial basado en la mRT-PCR (Hemavision-7 System DNA Technology A/S, Aarhus, Denmark) de aplicación rutinaria en el diagnóstico molecular hematopatológico, el cual detecta simultáneamente las siete translocaciones más frecuente en la leucemia. Un estudio científico demostró una eficacia del 100% de este kit en el análisis de muestras de pacientes (Salto-tellez et al., 2003. Journal of Molecular Diagnostics, Vol. 5, No. 4, 231-236).
También se debe tener en cuenta que la sensibilidad de las diferentes líneas celulares a la activación de genes inducidos en respuesta a la activación del sistema del interferón puede variar significativamente. El tipo celular, las condiciones de crecimiento y el número de pases pueden afectar la susceptibilidad, nivel y extensión de la activación de la respuesta del interferón. Por tanto, cuanto mayor sea el número de genes o proteínas analizados y cuanto más sensibles sean estos genes a la estimulación, mayor será la probabilidad de asegurarnos si existe o no una activación del interferón.
A todos estos factores, hay que añadir que, además de respuestas dependientes de interferón también se pueden inducir respuestas inflamatorias que inducen la producción de citoquinas proinflamatorias como por ejemplo IL-8, independientes del sistema interferón.
En este contexto, es necesario desarrollar un método capaz de identificar de una manera reproducible, rápida y eficaz cualquier respuesta inmunológica asociada con la introducción de ácidos nucleicos y otros productos en los distintos tipos de líneas celulares usadas en tratamientos, como por ejemplo, la terapia génica.
Descripción de la invención
La presente invención se refiere a una combinación de cebadores y a un método para la detección y/o cuantificación de la activación del interferón y la respuesta inflamatoria independiente de interferón. La amplificación se realiza mediante RT-PCR (del inglés Reverse Transcription-Polymerase Chain Reaction) multiplex (mRT-PCR) donde los cebadores empleados amplifican simultáneamente los genes OAS2, ISG56, IL-8 e IFNα o IFNβ. Además, la presente invención incluye un kit con la combinación de los cebadores mencionados y otros componentes.
La presente invención proporciona, por tanto, un procedimiento...
Reivindicaciones:
1. Uso de los cebadores directos SEQ ID NO: 1; SEQ ID NO: 3; SEQ ID NO: 5 y, SEQ ID NO: 7 o SEQ ID NO: 9, y de los cebadores reversos SEQ ID NO: 2; SEQ ID NO: 4; SEQ ID NO: 6 y, SEQ ID NO: 8 o SEQ ID NO: 10, para la detección y/o cuantificación de:
a. los genes OAS2, ISG56 e IFNα o IFNβ involucrados en la activación del interferón y,
b. el gen IL-8 involucrado en la respuesta inflamatoria independiente de interferón producida por la liberación de citoquinas proinflamatorias,
en una muestra biológica aislada de un sujeto o en un cultivo celular.
2. Uso según la reivindicación 1, donde se usa además el cebador directo SEQ ID NO: 11 y el cebador reverso SEQ ID NO: 12 para la detección y/o cuantificación del gen control GAPDH.
3. Uso según cualquiera de las reivindicaciones 1 ó 2, donde la detección y/o cuantificación se realiza en un cultivo celular.
4. Uso según cualquiera de las reivindicaciones 1 ó 2 donde la muestra biológica aislada es un tejido o un fluido biológico.
5. Uso según cualquiera de las reivindicaciones 1, 2 ó 4, donde el sujeto es un mamífero.
6. Método de obtención de datos útiles para determinar la capacidad de un agente para provocar una respuesta inmune, que comprende:
a. seleccionar un cultivo celular que previamente ha sido tratado con dicho agente,
b. amplificar de forma simultánea los genes OAS2, ISG56, IL-8 e IFNα o IFNβ, utilizando los cebadores SEQ ID NO: 1/SEQ ID NO: 2; SEQ ID NO: 3/SEQ ID NO: 4; SEQ ID NO: 5/SEQ ID NO: 6 y, SEQ ID NO: 7/SEQ ID NO: 8 o SEQ ID NO: 9/SEQ ID NO: 10, y
c. detectar y/o cuantificar los genes OAS2, ISG56, IL-8 e IFNα o IFNβ, en el cultivo celular seleccionado.
7. Método de obtención de datos útiles para la detección y/o cuantificación de la activación del interferón y de la respuesta inflamatoria independiente de interferón que comprende:
a. obtener una muestra biológica aislada de un sujeto o seleccionar un cultivo celular,
b. amplificar de forma simultánea los genes OAS2, ISG56, IL-8 e IFNα o IFNβ, utilizando los cebadores SEQ ID NO: 1/SEQ ID NO: 2; SEQ ID NO: 3/SEQ ID NO: 4; SEQ ID NO: 5/SEQ ID NO: 6 y, SEQ ID NO: 7/SEQ ID NO: 8 o SEQ ID NO: 9/SEQ ID NO: 10, y
c. detectar y/o cuantificar los genes OAS2, ISG56, IL-8 e IFNα o IFNβ, en la muestra biológica aislada o en el cultivo celular seleccionado.
8. Método de obtención de datos útiles para diagnosticar respuesta inmune en un sujeto o cultivo celular, que comprende los pasos (a), (b) y (c) del método según la reivindicación 7 y además los siguientes pasos:
d. comparar los resultados obtenidos en (c) con unos valores de referencia para encontrar una desviación significativa y,
e. atribuir la desviación a la presencia de respuesta inmune en el sujeto o en el cultivo celular.
9. Método según cualquiera de las reivindicaciones 6 a 8, donde además se amplifica el gen control GAPDH utilizando los cebadores SEQ ID NO: 11/SEQ ID NO: 12.
10. Método según cualquiera de las reivindicaciones 6 a 9, donde la amplificación del paso (b) se realiza mediante mRT-PCR.
11. Método según la reivindicación 6, donde el agente es un ácido nucleico.
12. Método según la reivindicación 11, donde el ácido nucleico es un oligodesoxirribonucleótido.
13. Método según la reivindicación 11, donde el ácido nucleico es ssRNA.
14. Método según la reivindicación 11, donde el ácido nucleico es dsRNA
15. Método según la reivindicación 14, donde el dsRNA es siRNA.
16. Método según cualquiera de las reivindicaciones 7 a 10 donde la muestra biológica aislada es un tejido o un fluido biológico.
17. Método según cualquiera de las reivindicaciones 7 a 10, donde el sujeto es un mamífero.
18. Kit que comprende los cebadores directos SEQ ID NO: 1; SEQ ID NO: 3; SEQ ID NO: 5 y, SEQ ID NO: 7 o SEQ ID NO: 9, y los cebadores reversos SEQ ID NO: 2; SEQ ID NO: 4; SEQ ID NO: 6 y, SEQ ID NO: 8 o SEQ ID NO: 10.
19. Kit según la reivindicación 18 que además comprende el cebador directo SEQ ID NO: 11 y el cebador reverso SEQ ID NO: 12.
20. Uso del kit según cualquiera de las reivindicaciones 18 ó 19, para la obtención de datos útiles para la detección y/o cuantificación de la activación del interferón y de la respuesta inflamatoria independiente de interferón en una muestra biológica aislada de un sujeto o en un cultivo celular.
21. Uso del kit según la reivindicación 20, donde la detección y/o cuantificación se realiza en un cultivo celular.
22. Uso del kit según cualquiera de las reivindicaciones 18 ó 19, para determinar la capacidad de un agente para provocar una respuesta inmune en un cultivo celular que previamente ha sido tratado con dicho agente.
23. Uso según la reivindicación 22, donde el agente es un ácido nucleico.
24. Uso según la reivindicación 23, donde el ácido nucleico es un oligodesoxirribonucleótido.
25. Uso según la reivindicación 24, donde el ácido nucleico es ssRNA.
26. Uso según la reivindicación 24, donde el ácido nucleico es dsRNA
27. Uso según la reivindicación 26, donde el dsRNA es siRNA.
Patentes similares o relacionadas:
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]
MÉTODOS PARA EL DIAGNÓSTICO DE ENFERMOS ATÓPICOS SENSIBLES A COMPONENTES ALERGÉNICOS DEL POLEN DE OLEA EUROPAEA (OLIVO), del 23 de Julio de 2020, de SERVICIO ANDALUZ DE SALUD: Biomarcadores y método para el diagnostico, estratificación, seguimiento y pronostico de la evolución de la enfermedad alérgica a polen del olivo, kit […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Secuenciación dirigida y filtrado de UID, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un procedimiento para generar una biblioteca de polinucleótidos que comprende: (a) generar una primera secuencia del complemento (CS) de un polinucleótido diana a partir […]
Métodos para la recopilación, estabilización y conservación de muestras, del 8 de Julio de 2020, de Drawbridge Health, Inc: Un método para estabilizar uno o más componentes biológicos de una muestra biológica de un sujeto, comprendiendo el método obtener un […]
Evento de maíz DP-004114-3 y métodos para la detección del mismo, del 1 de Julio de 2020, de PIONEER HI-BRED INTERNATIONAL, INC.: Un amplicón que consiste en la secuencia de ácido nucleico de la SEQ ID NO: 32 o el complemento de longitud completa del mismo.
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Aislamiento de ácidos nucleicos, del 24 de Junio de 2020, de REVOLUGEN LIMITED: Un método de aislamiento de ácidos nucleicos que comprenden ADN de material biológico, comprendiendo el método las etapas que consisten en: (i) efectuar un lisado […]