Procedimiento para la purificación de un complejo factor VIII/factor von Willebrans(vWF) por cromatografía de intercambio catiónico.
La invención se refiere a un procedimiento para obtener un complejo del factor VIII/vWF,
que se caracteriza en que el complejo del factor VIII/vWF de una solución de proteínas se une con un intercambiador de cationes y el complejo de factor VIII/vWF que contiene especialmente multímeros de vWF de alto peso molecular se obtiene mediante levigación gradual. La invención también se refiere a un complejo de factor VIII/vWF que puede obtenerse mediante cromatografía de intercambio de cationes.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/AT1998/000043.
Solicitante: Baxter Innovations GmbH.
Nacionalidad solicitante: Austria.
Dirección: Industriestrasse 67 1220 Wien AUSTRIA.
Inventor/es: DORNER, FRIEDRICH, MITTERER, ARTUR, EIBL, JOHANN, FISCHER, BERNHARD, SCHONBERGER,OYVIND,L, THOMAS-URBAN,KATHRIN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K38/37 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Factores VIII.
- A61K38/43 A61K 38/00 […] › Enzimas; Proenzimas; Sus derivados.
- A61P7/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 7/00 Medicamentos para el tratamiento de trastornos de la sangre o del fluido extracelular. › Antihemorrágicos; Procoagulantes; Hemostáticos; Antifibrinolíticos.
- C07K1/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › Cromatografía de intercambio iónico.
- C07K14/755 C07K […] › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Factores VIII.
- C12P21/04 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Péptidos o polipéptidos cíclicos o puenteados, p. ej. bacitracina.
PDF original: ES-2306471_T3.pdf
Fragmento de la descripción:
Procedimiento para la purificación de un complejo factor VIII/ factor von willebrand (vWF) por cromatografía de intercambio catiónico La invención se refiere a un procedimiento para la purificación de un complejo factor VIII/vWF a partir de un material de partida biológico por cromatografía de intercambio catiónico (donde el intercambiador de cationes no es heparina) y elución gradual, así como a un complejo factor VIII/vWF purificado que, en particular, contiene multímeros de vWF de alto peso molecular.
En plasma, el factor von Willebrand circula en una concentración de 5 a 10 mg/l y, en su mayor parte, en forma de complejo con el factor VIII no ligado de modo covalente. En crioprecipitado, el complejo factor VIII/vWF está fuertemente enriquecido y puede aislarse del mismo o desde el plasma o desde fracciones de plasma mediante procedimientos de fraccionamiento conocidos.
En el caso de la hemofilia, la coagulación sanguínea se ve afectada por la falta de determinados factores plasmáticos de coagulación sanguínea. En el caso de la hemofilia A, la tendencia a la hemorragia se debe a una falta de factor VIII o de vWF (hemofilia fenotípica) . El tratamiento de la hemofilia A se realiza en primer lugar sustituyendo el factor de coagulación deficiente por concentrados de factores, por ejemplo mediante infusión de factor VIII o de complejo factor VIII/vWF.
Para la terapia de pacientes con hemofilia A, pero también del síndrome de von Willebrand, es deseable utilizar un factor VIII purificado formando un complejo con vWF (Berntorp, 1994, Haemostasis 24: 289-297) . En particular, siempre se destaca que en aquellos preparados sin o con un pequeño contenido en vWF se puede observar un mayor tiempo de hemorragia y un corto período de semidesintegración del factor VIII:C in vivo. La normalización del vWF in vivo es importante para mantener la concentración de factor VIII plasmática, tanto por reducción del porcentaje de eliminación de factor VIII como también por el refuerzo de la liberación de factor VIII endógeno (Lethagen y col., 1992, Ann. Hematol. 65: 253-259) .
La DE 3 504 385 describe la realización de una cromatografía de intercambio iónico para la purificación del complejo factor VIII/vWF en la que se liga el complejo de factor VIII sobre grupos sulfato y se eluye con un tampón citrato, cloruro cálcico y un gradiente de NaCl. Aquí se eluye del vehículo el complejo factor VIII/vWF a una concentración 0, 5M de NaCl.
La EP 0 416 983 describe la obtención del complejo factor VIII/vWF a partir de plasma humano mediante la combinación de un precipitado de cloruro de bario o de hidróxido de aluminio y una cromatografía de intercambio aniónico en fractogel DEAE.
Harrison y col. (Thrombosis Res., 1988, 50, 295-304) describe la purificación del complejo factor VIII/vWF mediante cromatografía en sefarosa-sulfato-dextrano.
La EP 0 600 480 describe un procedimiento para la purificación de complejo factor VIII/vWF a partir de plasma total por medio de una cromatografía combinada de intercambio aniónico/intercambio catiónico. Entonces se lleva a cabo la elución del complejo FVIII/vWF adsorbido en el intercambiador de cationes se realiza utilizando una sustancia tampón que contiene Ca con 0, 3M NaCl, en un rango de pH entre 6, 6 y 7, 0.
La WO 96/10584 describe un procedimiento para la obtención de vWF recombinante altamente purificado por medio de una cromatografía de afinidad combinada de intercambio aniónico/heparina y la EP 0 705 846 describe la separación en fracciones tanto de alto peso molecular como de bajo peso molecular de vWF recombinante mediante cromatografía de afinidad/heparina.
Aunque los preparados de factor VIII descritos en el estado de la técnica actual contienen en su mayor parte todo el patrón multimérico de vWF, éste varía, sin embargo, entre la parte de vWF de alto peso molecular (HMW-vWF) y vWF de bajo peso molecular (LMW-vWF) y los preparados tienen las estructuras denominadas de triplete, que indican una descomposición proteolítica, en particular de HMW-vWF. Por ello, con frecuencia se ve limitada la estabilidad de estos preparados.
Continuamente se destaca que los preparados de factor VIII/vWF que contienen esencialmente HMW-vWF posiblemente favorecen positivamente la duración de la hemorragia, ya que realizan la función primaria del vWF, la aglutinación de plaquetas, y tienen una mayor afinidad con los receptores plaquetarios de glicoproteína IB y IIb/IIIa que los multímeros vWF de bajo peso molecular.
Existe la necesidad de un complejo de factor VIII con una actividad específica suficiente de factor VIII:C- y de vWF. El problema que surge durante la obtención de un complejo tal consiste particularmente en la separación de aquellas moléculas que contienen multímeros de vWF de bajo peso molecular y en el enriquecimiento de complejos con una alta actividad específica de vWF.
Por tanto, el objetivo de la presente invención consiste en proporcionar un complejo factor VIII/vWF con una actividad específica y una estabilidad mejoradas.
Otro objetivo consiste en proporcionar un procedimiento para la obtención de tal complejo factor VIII/vWF. El procedimiento debería poder utilizarse para la purificación de complejos de factor VIII/vWF tanto recombinantes como también plasmáticos.
Según la invención este objetivo se alcanza en base a que se proporciona un procedimiento para la obtención de un complejo factor VIII/vWF en el que se liga el complejo factor VIII/vWF procedente de una solución proteica en un intercambiador de cationes -donde el intercambiador de cationes no es heparina -y, mediante una elución gradual fraccionada, se obtiene un complejo factor VIII/vWF con una mejor actividad específica de vWF. En particular, la obtención y el enriquecimiento del factor VIII/vWF con una mejor actividad y estabilidad se lleva a cabo debido a que se liga el complejo factor VIII/vWF con una concentración baja de sal , mediante un aumento gradual de la concentración de sal se separan, con una mayor concentración de sal, fracciones que contienen el complejo factor VIII/vWF con multímeros de vWF de bajo peso molecular, con una concentración media de sal productos inactivos de la descomposición del vWF y proteínas accidentales no específicas y se obtienen fracciones que contienen el complejo factor VIII/vWF conteniendo especialmente multímeros de vWF de alto peso molecular con una concentración de sal alta.
Normalmente, el complejo factor VIII/vWF se purifica gracias a su punto isoeléctrico ácido (IEP = 5, 5 a 6) y a la carga neta negativa resultante en un medio desde ligeramente ácido hasta básico sobre el intercambiador aniónico cargado positivamente. Por tanto, no podía esperarse, debido a los procedimientos hasta ahora descritos para la purificación del complejo factor VIII/vWF por el intercambiador aniónico de carga positiva, que el complejo factor VIII/vWF también se uniera a una matriz de gel cargada negativamente de un intercambiador catiónico a un pH por encima del IEP del complejo y con una concentración de sal baja y que pudiera efectuarse una elución selectiva de la misma mediante el aumento de la concentración de sal. Tampoco podía esperarse que por elución gradual con una concentración de sal de entre ≥ 250 mM y ≤ 300 mM, proteínas accidentales no específicas se pudieran eluir productos inactivos de descomposición de vWF, componentes del complejo con una reducida actividad específica, multímeros de vWF de bajo peso molecular que contienen el complejo factor VIII/vWF, factor VIII sin formar complejo de bajo peso molecular o factor VIII débilmente ligado y factor VIII libre y que a una concentración de sal ≥ 350 mM se obtuviera, especialmente, un complejo factor VIII/vWF con multímeros de vWF de alto peso molecular.
Dentro del marco de la presente invención, se observa que con el procedimiento según la invención, partiendo de un material biológico impuro se obtienen fracciones purificadas esencialmente libres de ácidos nucleicos contaminantes. Así, mediante este procedimiento se eliminan ácidos nucleicos de los preparados proteicos. Este efecto no es posible con los procedimientos tradicionales de intercambio aniónico, debido a que los ácidos nucleicos se ligan al intercambiador de aniones por su carga negativa, se desprenden de nuevo del intercambiador aniónico debido al aumento de la concentración de la sal y entran en el producto de elución.
Durante la purificación del complejo factor VIII/vWF hay que tener en cuenta, particularmente,... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la obtención de un complejo factor VIII/vWF caracterizado porque se obtiene el complejo factor VIII/vWF a partir de una solución proteica ligado a un intercambiador de cationes y, por el aumento gradual de la concentración de sal, un complejo de factor VIII/vWF que contiene en particular multímeros vWF de alto peso molecular, no siendo el intercambiador de cationes heparina.
2. Procedimiento según la reivindicación 1, caracterizado porque el complejo factor VIII/vWF queda ligado en un intercambiador de cationes con una concentración de sal desde 50mM a 250mM, y se eluye y obtiene el complejo factor VIII/vWF con multímeros vWF de bajo peso molecular y factor VIII:C libre de actividad vWF de aglutinante plaquetario con una concentración de sal entre ≥ 250 mM y ≤ 300 mM.
3. Procedimiento según la reivindicación 1 ó 2, caracterizado porque el complejo factor VIII/vWF, que contiene en particular multímeros de vWF de alto peso molecular, se obtiene por fraccionamiento gradual con una concentración de sal de ≥ 350 mM.
4. Procedimiento según la reivindicación 3, caracterizado porque se obtiene una fracción que contiene un complejo factor VIII/vWF, fracción que está especialmente libre de multímeros de vWF de bajo peso molecular, de productos de descomposición de vWF, de factor VIII sin formar complejo o débilmente ligado con vWF y de ácidos nucleicos contaminantes.
5. Procedimiento según una de las reivindicaciones 1 a 4, caracterizado porque la elución de los polipéptidos del intercambiador de cationes se realiza en un sistema tampón a un pH en el rango entre 4, 5 y 8, 5,
preferentemente ≥ 7, 1 y ≤ 8, 5.
6. Procedimiento según una de las reivindicaciones 1 a 5, caracterizado porque el intercambiador de cationes es un vehículo conjugado con grupos sulfopropilo o carboximetilo.
7. Procedimiento según una de las reivindicaciones 1 a 6, caracterizado porque se obtiene un complejo factor VIII/vWF que contiene, en particular, multímeros de vWF de alto peso molecular.
8. Procedimiento según una de las reivindicaciones 1 a 7 caracterizado porque el complejo factor VIII/vWF se obtiene a partir de plasma, de una fracción de plasma, de un crioprecipitado, de un sobrenadante libre de células o del extracto de un cultivo celular recombinante o de una fracción proteica enriquecida.
9. Complejo factor VIII/vWF que contiene especialmente multímeros de vWF de alto peso molecular que se obtiene a partir de una solución que contiene factor VIII/vWF mediante cromatografía de intercambio catiónico de acuerdo con un procedimiento según una de las reivindicaciones 1 a 8, teniendo el complejo una actividad específica de vWF mínima de 66 U/mg de proteína y una actividad específica de factor VIII mínima de 500 U/mg de proteína.
10. Complejo factor VIII/vWF según la reivindicación 9, caracterizado porque está especialmente libre de multímeros de vWF de bajo peso molecular, de productos inactivos de descomposición de vWF, de factor VIII sin formar complejo y de actividad de factor VIIIa.
11. Preparado que contiene el complejo factor VIII/vWF según la reivindicación 9 ó 10, caracterizado porque está garantizado contra virus y está libre de sustancias infecciosas.
12. Preparado según la reivindicación 11, caracterizado porque se presenta en una forma estable al almacenamiento.
13. Preparado según una de las reivindicaciones 11 ó 12, caracterizado porque se formula como un preparado farmacéutico.
14. Utilización de un preparado según una de las reivindicaciones 11 a 13 para la producción de un medicamento para el tratamiento de pacientes con hemofilia A, hemofilia fenotípica y vWD.
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Composiciones y métodos para inmunomodulación en un organismo, del 19 de Febrero de 2020, de UNIVERSITY OF CONNECTICUT: Una composicion para su uso en un metodo de (i) tratamiento de cancer en un ser humano; (ii) mejora de la vacunacion en un ser humano; (iii) aumento de las respuestas […]
CD33 soluble para tratar síndromes mielodisplásicos (MDS), del 8 de Enero de 2020, de H. Lee Moffitt Cancer Center And Research Institute, Inc: Una proteína de fusión recombinante quimérica, que comprende: (a) una combinación de al menos dos fracciones de unión a S100A9 seleccionados de entre el grupo que […]
Métodos para la diferenciación y transducción in vitro de células b de memoria con vectores virales pseudotipados vsv-g, del 1 de Enero de 2020, de Immusoft Corporation: Un método in vitro para expresar un ácido nucleico de interés en una célula B, que comprende (a) poner en contacto células B de memoria con una composición que comprende […]
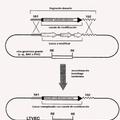 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Intercambio de casetes de la región variable de la inmunoglobulina, del 12 de Junio de 2019, de Humanigen, Inc: Un método de modificación genética de un anticuerpo que retiene la especificidad de unión de un anticuerpo de referencia con un antígeno diana, comprendiendo el método: […]
Procedimiento de modificar células eucariotas, del 3 de Abril de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento de reemplazar in situ, en parte, en una célula madre embrionaria (ES) de ratón, un locus génico endógeno de región variable de […]
Diacuerpos covalentes y usos de los mismos, del 2 de Abril de 2019, de MACROGENICS, INC: Una molécula de diacuerpo que comprende una primera cadena polipeptídica y una segunda cadena polipeptídica, en la que: (a) dicha primera cadena […]