Composiciones y métodos para la terapia y diagnosis de la influenza.
Un anticuerpo anti-ectodominio de la matriz 2 (M2e) completamente humano aislado,
en donde dicho anticuerpo comprende una región CDR1 de VH que comprende la secuencia de aminoácidos deNYYWS (SEQ ID NO: 72); una región CDR2 de VH que comprende la secuencia de aminoácidos deFIYYGGNTKYNPSLKS (SEQ ID NO: 74); una región CDR3 de VH que comprende la secuencia de aminoácidos deASCSGGYCILD (SEQ ID NO: 76); una región CDR1 de VL que comprende la secuencia de aminoácidos deRASQNIYKYLN (SEQ ID NO: 59); una región CDR2 de VL que comprende la secuencia de aminoácidos deAASGLQS (SEQ ID NO: 61); y una región CDR3 de VL que comprende la secuencia de aminoácidos QQSYSPPLT(SEQ ID NO: 63), o
en donde dicho anticuerpo comprende una región CDR1 de VH que comprende la secuencia de aminoácidos deSNYMS (SEQ ID NO: 103); una región CDR2 de VH que comprende la secuencia de aminoácidos de VIYSGGSTYYADSVK (SEQ ID NO: 105), una región CDR3 de VH que comprende la secuencia de aminoácidos deCLSRMRGYGLDV (SEQ ID NO: 107); una CDR1 de VL que comprende la secuencia de aminoácidos deRTSQSISSYLN (SEQ ID NO: 92); una región CDR2 de VL que comprende la secuencia de aminoácidos deAASSLQSGVPSRF (SEQ ID NO: 94); y una región CDR3 de VL que comprende la secuencia de aminoácidos deQQSYSMPA (SEQ ID NO: 96).
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2008/083265.
Solicitante: Theraclone Sciences, Inc.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1124 Columbia Street, Suite 300 Seattle, WA 98104 ESTADOS UNIDOS DE AMERICA.
Inventor/es: MOYLE, MATTHEW, OLSEN, OLE, GRANDEA,ANDRES G, KING,GORDON, COX,THOMAS, MITCHAM,JENNIFER.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P31/16 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › para virus de la gripe o rinovirus.
- C07K14/11 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Orthomyxoviridae, p. ej. virus de la influenza.
- C07K16/10 C07K […] › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › de virus ARN.
- G01N33/569 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para microorganismos, p. ej. protozoarios, bacterias, virus.
PDF original: ES-2395784_T3.pdf
Fragmento de la descripción:
Composiciones y métodos para la terapia y diagnosis de la influenza Campo de la Invención La presente invención se refiere generalmente a la terapia, diagnosis y control de la infección por influenza. La invención se refiere más específicamente a anticuerpos específicos de la proteína de la matriz 2 de influenza completamente humanos aislados y a su fabricación y uso. Dichos anticuerpos son útiles en composiciones farmacéuticas para la prevención y el tratamiento de la influenza, y para la diagnosis y el control de la infección por influenza.
Antecedentes de la Invención El virus de la influenza infecta a 5-20% de la población y produce 30.000-50.000 muertes cada año en los Estados Unidos. Aunque la vacuna de la influenza es el método primario de prevención de la infección, solamente se encuentran disponibles cuatro fármacos antivirales en los Estados Unidos: amantadina, rimantadina, oseltamivir y zanamivir. En Diciembre de 2005, solamente se recomienda oseltamivir (TAMIFLU™) para el tratamiento de la influenza A debido a la resistencia creciente del virus a la amantadina y la rimantidina resultante de una sustitución de aminoácidos en la proteína M2 del virus.
La enfermedad causada por las infecciones virales de influenza A está tipificada por su naturaleza cíclica. La deriva y el desplazamiento antigénicos permiten que emerjan diferentes cepas A cada año. Sumado a esto, la amenaza de cepas altamente patogénicas que se introducen en la población general ha acentuado la necesidad de terapias novedosas para las infecciones por gripe. La fracción predominante de los anticuerpos neutralizadores está dirigida a las regiones polimorías de las proteínas hemaglutinina y neuraminidasa. De este modo, dicho MAb neutralizadorelegiría presumiblemente como diana solamente una o unas pocas cepas. Últimamente el centro de atención ha sido la proteína de la matriz 2 (M2) relativamente invariable. Potencialmente, un MAb neutralizador para M2 sería una terapia adecuada para todas las cepas de influenza A.
La proteína M2 se encuentra en un homotetrámero que forma un canal iónico y se piensa que ayuda en la pérdida de la envoltura del virus tras la entrada en la célula. Tras la infección, se puede encontrar M2 en abundancia en lasuperficie de la célula. Ésta se incorpora con posterioridad a la envoltura del virión, en donde solamente comprende aproximadamente 2% de la proteína de la envoltura total. El dominio extracelular de M2 (M2e) es corto, con los aminoácidos 2-24 amino terminales desplegados fuera de la célula. Los MAb anti-M2 se han dirigido hasta la fecha hacia esta secuencia lineal. De este modo, pueden no mostrar las propiedades de unión deseadas para la M2 expresada celularmente, incluyendo determinantes conformacionales sobre la M2 nativa.
Por ejemplo, el documento WO 2006/061723 describe el anticuerpo monoclonal Z3G1 totalmente humano obtenido de ratones transgénicos que albergan regiones del gen de la inmunoglobulina humana inmunizados con el polipéptido M2. El anticuerpo Z3G1 se une a un determinante dentro de la secuencia LLTEVETPIR y es terapéuticamente eficaz contra la infección por influenza A en ratones.
Por lo tanto, existe una necesidad en la técnica, hace mucho tiempo, de nuevos anticuerpos que se unan a la M2 expresada en la célula y a los determinantes conformacionales sobre la M2 nativa.
Compendio de la Invención La presente invención proporciona anticuerpos monoclonales completamente humanos aislados dirigidos específicamente contra M2e y que tienen las secuencias CDR mostradas en la reivindicación 1. Opcionalmente, el anticuerpo se aísla de una célula B de un donante humano. Los anticuerpos monoclonales ilustrativos incluyen 8i10, 21B15 y 23K12 descritos en la presente memoria. Los anticuerpos son referidos respectivamente en la presente memoria como anticuerpos para huM2e. El anticuerpo para huM2e tiene una o más de las siguientes características: a) se une a un epítopo en el dominio extracelular del polipéptido del ectodominio de la matriz 2 (M2e) de un virus de influenza; b) se une a células infectadas con influenza A; o c) se une al virus influenza A.
El epítopo al que se une el anticuerpo para huM2e es un epítopo no lineal de un polipéptido M2. Preferiblemente, el epítopo incluye la región amino terminal del polipéptido M2e. Más preferiblemente el epítopo incluye total o parcialmente la secuencia de aminoácidos SLLTEV (SEQ ID NO: 42) . Lo más preferiblemente, el epítopo incluye el aminoácido de las posiciones 2, 5 y 6 del polipéptido M2e cuando se numera de acuerdo con el SEQ ID NO: 1. El aminoácido de la posición 2 es una serina; el de la posición 5 es una treonina; y el de la posición 6 es un ácido glutámico.
Un anticuerpo para huM2e contiene una cadena pesada variable que tiene la secuencia de aminoácidos de los SEQ ID NOS: 44 o 50 y una cadena ligera variable que tiene la secuencia de aminoácidos de los SEQ ID NOS: 46 o 52. Las tres CDR de la cadena pesada incluyen las secuencias de aminoácidos NYYWS (SEQ ID NO: 72) , FIYYGGNTKYNPSLKS (SEQ ID NO: 74) , y ASCSGGYCILD (SEQ ID NO: 76) , o SNYMS (SEQ ID NO: 103) , VIYSGGSTYYADSVK (SEQ ID NO: 105) , y CLSRMRGYGLDV (SEQ ID NO: 107) (determinadas mediante el método de Kabat) y una cadena ligera con tres CDR que incluyen las secuencias de aminoácidos RASQNIYKYLN (SEQ ID NO: 59) , AASGLQS (SEQ ID NO: 61) , y QQSYSPPLT (SEQ ID NO: 63) ; o RTSQSISSYLN (SEQ ID NO: 92) , AASSLQSGVPSRF (SEQ ID NO: 94) , QQSYSMPA (SEQ ID NO: 96) (determinadas mediante el método de Kabat) . El anticuerpo se une a M2e.
En otro aspecto la invención proporciona una composición que incluye un anticuerpo para huM2e de acuerdo con la invención. En varios aspectos la composición incluye adicionalmente un fármaco anti-viral, un inhibidor de la entrada viral o un inhibidor del anclaje viral. El fármaco anti-viral es por ejemplo un inhibidor de neuraminidasa, un inhibidor de HA, un inhibidor de ácido siálico o un inhibidor del canal iónico M2. El inhibidor del canal iónico M2 es por ejemplo amantadina o rimantadina. El inhibidor de neuraminidasa es por ejemplo zanamivir, o fosfato de oseltamivir. En un aspecto adicional la composición incluye adicionalmente un segundo anticuerpo anti-influenza A.
En un aspecto adicional los anticuerpos para huM2e de acuerdo con la invención están conectados operablemente a un agente terapéutico o una marca detectable.
También se incluye en la invención un método para determinar la presencia de una infección por el virus de la influenza en un paciente, poniendo en contacto una muestra biológica obtenida del paciente con un anticuerpo de la invención; detectando la cantidad del anticuerpo que se une a la muestra biológica; y comparando la cantidad de anticuerpo que se une a la muestra biológica con un valor de control.
La invención proporciona adicionalmente un kit de diagnóstico que comprende un anticuerpo para huM2e.
Otras características y ventajas de la invención serán evidentes a partir de la siguiente descripción detallada y las reivindicaciones y se describen por medio de las mismas.
Breve Descripción de los Dibujos La Figura 1 muestra la unión de tres anticuerpos de la presente invención y el anticuerpo de control hu14C2 a células HEK 293 transfectadas con un constructo de expresión o vector de control de M2, en presencia o ausencia de péptido M2 libre.
Las Figuras 2A y B son gráficos que muestran la unión del anticuerpo monoclonal humano a influenza A/Puerto Rico/8/32.
La Figura 3A es un diagrama que muestra secuencias de aminoácidos de dominios extracelulares de variantes de M2.
Las Figuras 3B y C son diagramas de barras que muestran la unión del anticuerpo anti-influenza monoclonal humano que se une a variantes de M2 mostradas en la Figura 3A.
Las Figuras 4A y B son diagramas de barras que muestran la unión del anticuerpo anti-influenza monoclonal humano que se une a péptidos M2 sometidos a mutagénesis de barrido con alanina.
La Figura 5 es una serie de diagramas de barras que muestran la unión de los MAb 8i10 y 23K12 a la proteína M2 que representa la secuencia A/HK/483/1997 de la cepa de influenza que fue expresada establemente en la línea de células CHO DG44.
La Figura 6A es un diagrama que muestra la unión por reactividad cruzada de anticuerpos anti-M2 a péptidos M2 variantes.
La Figura 6B es un diagrama que muestra la actividad de unión de anticuerpos para M2 a péptidos M2 truncados.
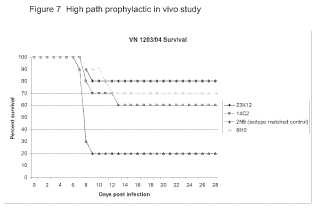
La Figura 7 es un gráfico que muestra la supervivencia de ratones infectados con influenza tratados con anticuerpos monoclonales anti-influenza humanos.
La Figura 8 es una ilustración que demuestra que los anticuerpos anti-M2... [Seguir leyendo]
Reivindicaciones:
1. Un anticuerpo anti-ectodominio de la matriz 2 (M2e) completamente humano aislado,
en donde dicho anticuerpo comprende una región CDR1 de VH que comprende la secuencia de aminoácidos de NYYWS (SEQ ID NO: 72) ; una región CDR2 de VH que comprende la secuencia de aminoácidos de FIYYGGNTKYNPSLKS (SEQ ID NO: 74) ; una región CDR3 de VH que comprende la secuencia de aminoácidos de ASCSGGYCILD (SEQ ID NO: 76) ; una región CDR1 de VL que comprende la secuencia de aminoácidos de RASQNIYKYLN (SEQ ID NO: 59) ; una región CDR2 de VL que comprende la secuencia de aminoácidos de AASGLQS (SEQ ID NO: 61) ; y una región CDR3 de VL que comprende la secuencia de aminoácidos QQSYSPPLT (SEQ ID NO: 63) , o en donde dicho anticuerpo comprende una región CDR1 de VH que comprende la secuencia de aminoácidos de SNYMS (SEQ ID NO: 103) ; una región CDR2 de VH que comprende la secuencia de aminoácidos de VIYSGGSTYY ADSVK (SEQ ID NO: 105) , una región CDR3 de VH que comprende la secuencia de aminoácidos de CLSRMRGYGLDV (SEQ ID NO: 107) ; una CDR1 de VL que comprende la secuencia de aminoácidos de RTSQSISSYLN (SEQ ID NO: 92) ; una región CDR2 de VL que comprende la secuencia de aminoácidos de AASSLQSGVPSRF (SEQ ID NO: 94) ; y una región CDR3 de VL que comprende la secuencia de aminoácidos de QQSYSMPA (SEQ ID NO: 96) .
2. El anticuerpo de acuerdo con reivindicación 1, en donde dicho anticuerpo está conectado operablemente a un agente terapéutico o una marca detectable.
3. Una composición que comprende el anticuerpo de las reivindicaciones 1 o 2, que comprende adicionalmente opcionalmente un fármaco antiviral, un inhibidor de la entrada viral o un inhibidor del anclaje viral.
4. La composición de la reivindicación 3 que comprende adicionalmente un fármaco anti-viral, en donde dicho fármaco anti-viral es un inhibidor de neuraminidasa tal como zanamivir o fosfato de oseltamivir; un inhibidor de HA; un inhibidor de ácido siálico; o un inhibidor del canal iónico de M2 tal como amantadina o rimantadina.
5. La composición de la reivindicación 3 que comprende adicionalmente un segundo anticuerpo anti-influenza A.
6. Una composición farmacéutica que comprende el anticuerpo de una cualquiera de las reivindicaciones 1-5 para su uso como medicamento.
7. Una composición farmacéutica que comprende el anticuerpo de una cualquiera de las reivindicaciones 1-5 para su uso en el tratamiento o la prevención de una infección por el virus de la influenza.
8. Un método para determinar la presencia de una infección por virus de la influenza en un paciente, que comprende las etapas de:
(a) poner en contacto una muestra biológica obtenida del paciente con el anticuerpo de acuerdo con la reivindicación 1 o 2;
(b) detectar una cantidad del anticuerpo que se une a la muestra biológica; y
(c) comparar la cantidad de anticuerpo que se une a la muestra biológica a un valor de control; y determinar de allí la presencia del virus de la influenza en el paciente.
9. Un kit diagnóstico que comprende el anticuerpo de acuerdo con reivindicación 1-2.
Patentes similares o relacionadas:
Método de determinación de la presencia y/o cantidad de moléculas diana, del 22 de Julio de 2020, de Canopy Biosciences, LLC: Método para el análisis de células individuales en una muestra de sangre mediante la determinación de la presencia y/o cantidad de una o más moléculas […]
Ensayo de toxina botulínica con sensibilidad mejorada, del 1 de Julio de 2020, de BioMadison, Inc: Un método para aumentar la sensibilidad de la detección basada en células de una toxina botulínica, que comprende: (i) proporcionar una célula […]
Bebidas energéticas y otras ayudas nutricionales derivadas de licores a base de agave, del 1 de Julio de 2020, de Roar Holding, LLC: Una composición que comprende compuestos inhibidores de monoamino oxidasa (MAO), cuya composición se prepara mediante la eliminación de etanol de una bebida […]
Evaluación asistida del pronóstico en la enfermedad inflamatoria, del 24 de Junio de 2020, de KINGS COLLEGE LONDON: Un método in vitro de recopilación de información útil para predecir el resultado clínico en un sujeto, en donde el sujeto tiene o se sospecha que tiene una enfermedad […]
Vacunas y diagnóstico de torque teno virus porcino, del 18 de Junio de 2020, de VIRGINIA TECH INTELLECTUAL PROPERTIES, INC.: Composición inmunogénica que comprende una proteína según SEQ ID NO. 16.
Marcadores celulares para el diagnóstico de la enfermedad de Alzheimer y para la progresión de la enfermedad de Alzheimer, del 17 de Junio de 2020, de YEDA RESEARCH AND DEVELOPMENT CO. LTD.: Un método para el diagnóstico de la probabilidad de la enfermedad de Alzheimer (EA) en un individuo examinado, que comprende: (i) medir los […]
Biomarcadores de TB, del 22 de Abril de 2020, de United Kingdom Research and Innovation: Un método para el diagnóstico de TB en un sujeto, comprendiendo el método: (a) proporcionar una muestra de dicho sujeto, siendo dicha muestra seleccionada […]
Procedimiento para detectar bacterias coliformes contenidas en la leche, del 15 de Abril de 2020, de ASAHI KASEI KABUSHIKI KAISHA: Procedimiento para lisar bacterias coliformes contenidas en la leche, que comprende la etapa de mezclar un agente de lisis que contiene lisozima, un surfactante aniónico […]