Composición para aumento en el tejido duro.
Uso de una composición que comprende al menos un primer y un segundo componente precursores,
caracterizado porque el primer componente precursor comprende al menos m grupos nucleofílicos y el segundo componente precursor comprende al menos n grupos electrofílicos donde m+n es al menos cinco y en donde el primer y segundo componentes precursores son seleccionados del grupo que consiste de oligómeros y son seleccionados de modo que los grupos nucleofílicos y electrofílicos formen enlaces covalentes entre sí, a temperaturas fisiológicas para la producción de un biomaterial para aumentar el tejido duro.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2003/002979.
Solicitante: Kuros Biosurgery AG.
Nacionalidad solicitante: Suiza.
Dirección: Technoparkstrasse 1 8005 Zürich.
Inventor/es: MOLENBERG, AALDERT, RENS, ZAMPARO,Enrico, FEHR,Daniel.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/131 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › acíclicas.
- A61K31/22 A61K 31/00 […] › de ácidos acíclicos, p. ej. pravastatina.
- A61K31/695 A61K 31/00 […] › Compuestos del silicio.
- A61K45/06 A61K […] › A61K 45/00 Preparaciones medicinales que contienen ingredientes activos no previstos en los grupos A61K 31/00 - A61K 41/00. › Mezclas de ingredientes activos sin caracterización química, p. ej. compuestos antiflojísticos y para el corazón.
- A61L27/00 A61 […] › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14).
- A61L27/16 A61L […] › A61L 27/00 Materiales para prótesis o para revestimiento de prótesis (prótesis dentales A61C 13/00; forma o estructura de las prótesis A61F 2/00; empleo de preparaciones para la fabricación de dientes artificiales A61K 6/80; riñones artificiales A61M 1/14). › obtenidos mediante reacciones en las que sólo participan enlaces insaturados carbono-carbono.
- A61L27/50 A61L 27/00 […] › Materiales caracterizados por su función o por sus propiedades físicas.
- A61P13/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 13/00 Medicamentos para el tratamiento del aparato urinario (diuréticos A61P 7/10). › de la vejiga.
- A61P19/00 A61P […] › Medicamentos para el tratamiento de problemas del esqueleto.
PDF original: ES-2381185_T3.pdf
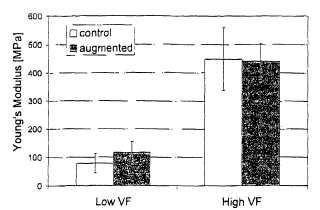
Fragmento de la descripción:
Composición para aumento en el tejido duro La presente invención se relaciona con la formación in situ de biomateriales, con componentes precursores capaces de formar esos biomateriales y con el uso de esos biomateriales del diseño de tejido en particular, como material para aumentar tejidos duros.
Una de las áreas en las cuales la tecnología ha avanzado significativamente es la cirugía reconstructiva que implica el uso de materiales sintéticos para implantarse en el cuerpo para ayudar a la reconstrucción y reparación quirúrgica. Se ha hecho mucho trabajo sobre el desarrollo de sistemas polímericos que puedan ser aplicados como líquidos y que reticulen in situ para formar biomateriales en el sitio que sean necesarios sobre y/o en el cuerpo. Los biomateriales de origen polimérico sintético son ahora ampliamente aceptados para aplicaciones relacionadas con tejidos, como matrices de regeneración de tejido, como adhesivos de tejido, como matrices de liberación de fármacos, y la prevención de adhesiones quirúrgicas, para superficies de recubrimiento o implantes sintéticos y como materiales para aumentar tejido. Dependiendo de la estructura química de los componentes precursores y su estequiometría, los biomateriales tienen propiedades físicas y químicas variables.
Cirugía Ortopédica La cirugía ortopédica ha sido históricamente la aplicación más significativa de los biomateriales. Esta resuelve problemas médicos en el sistema musculoesquelético y el tratamiento de enfermedades y perturbaciones a sus componentes, particularmente huesos, cartílagos, ligamentos y tendones. El sistema musculoesquelético produce movimiento y responde a fuerzas, por lo tanto es susceptible a lesiones y enfermedades relacionadas con el esfuerzo, las cuales pueden tener un efecto devastador sobre la movilidad. Cualquier reemplazo y refuerzo de esos tejidos tiene que efectuarse en el mismo ambiente médico, y el logro del desempeño mecánico relevante no es trivial. Además como parte del proceso de envejecimiento, los tejidos cambian su forma y consistencia. En particular, algunos tejidos pierden su forma y de este modo es deseable un aumento o restauración. Particularmente severa para un individuo es la pérdida de masa ósea y estabilidad como la osteoporosis. Numerosas otras enfermedades también perturban la función ósea y de las articulaciones, conduciendo a dolor, pérdida de movimiento, o pérdida de funciones vitales. Un ejemplo prominente es la osteoartritis, en gran medida una perturbación mecánica del cartílago y el hueso subyacente en las articulaciones.
Aumento de tejido duro Aunque un biomaterial usado para aumentar el tejido duro puede ser aplicado de diferentes maneras, una forma particularmente preferida es por cirugía mínimamente invasiva. La cirugía mínimamente invasiva es el procedimiento de elección para tratar fracturas por compresión vertebral o vértebras osteoporóticas, un tratamiento conocido bajo el término de vertebroplastia. Las fracturas por compresión son particularmente problemáticas en mujeres osteoporóticas. Antes de que fuera desarrollada la vertebroplastia, los cirujanos no trataban las fracturas por compresión debido a que la intervención en esos pacientes-casos era riesgosa y solo estaban disponibles herramientas inadecuadas. La vertebroplastia, un procedimiento en el cual el cuerpo vertebral es llenado percutáneamente con metacrilato de polimetilo (PMMA) fue desarrollada para satisfacer ese hueco en el tratamiento. El PMMA es principalmente conocido como cemento óseo y es usado en límites en esta indicación. El PMMA es un polímero duro, frágil, tolerado por tejidos y generalmente resistente a la degradación. El PMMA es usado en la vertebroplastia como un sistema pulverizado/líquido (copolímero de PMMA/metilmetacrilato monomérico) mezclado en la sala de operación hasta una pasta viscosa y jalado en una jeringa inmediatamente antes de inyectarse en la vértebra.
La vertebroplastia como tratamiento en sí es muy efectivo. Esta alivia el dolor en la mayoría de los casos debido a la prevención del micromovimiento de la estructura de tejido esponjoso dentro de la vértebra y estabilización mecánica de las microfracturas existentes (Mathis J. et al., Am. J. Neuroradiol. 22, 373-381, 2001) . El factor de riesgo y problemas en la vertebroplastia están asociados principalmente con la toxicidad del metacrilato de metilo. El metacrilato de metilo altamente tóxico puede filtrarse hacia el flujo sanguíneo antes de reticular lo suficiente haciendo que la presión sanguínea caiga y la migración de cemento óseo hacia las venas con la posibilidad de finalizar en los pulmones o causando hipotensión. Aunque este es un riesgo común a todos los usos del PMMA, este aumento en la vertebroplastia debido al hecho de que el PMMA es inyectado bajo presión en un espacio cerrado dentro de un hueso fracturado, lo cual hace el riesgo de fuga aún más pertinente. El proceso de polimerización exotérmica, una deficiencia adicional del PMMA, con frecuencia conduce a daño sustancial del tejido circundante. De este modo, el PMMA está lejos de ser el biomaterial ideal para aumentar tejido duro en general y para la aplicación en la vertebroplastia en particular.
Los problemas de manejo también pueden ser mejorados. La preparación final de la mezcla de PMMA tiene que ser efectuada en la sala de operación. Los componentes individuales tienen que ser medidos, mezclados hasta una mezcla homogénea y la mezcla tiene que ser llenada en los dispositivos apropiados para su aplicación, los cuales en el caso de la vertebroplastia son una jeringa. Este procedimiento consume tiempo, es susceptible a errores y conlleva riesgos de salud para la persona que prepare el PMMA causados por la inhalación del polvo agitado y el metacrilato de metilo volátil.
Aún después de la inyección por polimerización exitosa, el PMMA puede producir complicaciones. El PMMA es muy duro y puede producir desprendimiento por esfuerzo y/o colapsarse la vértebra adyacente a la tratada la cual puede entonces fracturarse también. (Ferguson S. et al, Transactions of the 47th Annual Meeting of the ORS, 0280, 2001) .
Por lo tanto, existe una necesidad general de biomateriales novedosos que pueden ser usados para aumentar el tejido duro. Puesto que la vertebroplastia es un tratamiento que está creciendo rápidamente también con respecto a un crecimiento de la población vieja, existe la necesidad particular del reemplazo de PMMA en la vertebroplastia.
Las composiciones que tienen que formar biomateriales en el sitio de inyección en el cuerpo humano o animal y que tienen que aumentar vértebras osteoporóticas, tienen que cumplir con varias necesidades: el tratamiento deberá disminuir o remover completamente el dolor asociado con vértebras fracturadas, de modo que el paciente pueda abandonar la cama y moverse nuevamente. En segundo lugar, las propiedades mecánicas de las vértebras osteoporóticas tienen que mejorar. Esto es evidente cuando se compara la fuerza de compresión y el módulo de Young E de una vértebra sana joven (la vértebra en su estado ideal) y una vértebra osteoporótica. La fuerza de compresión de la parte interna esponjosa de una vértebra ideal puede constituir hasta 8 veces más la de una vértebra osteoporótica; de manera similar, el módulo de Young E de la parte esponjosa de una vértebra ideal puede constituir hasta 100 veces más que el módulo de Young E de una osteoporótica. Está aceptado, que las propiedades mecánicas de una vértebra ideal pueden ser difícilmente re establecidas pero la gente que padece de osteoporosis es principalmente de edad avanzada pero no busca efectuar más esfuerzos físicos que los que requieren la presencia de la vértebra ideal. De este modo, en tanto el paciente esté libre de dolor y haya recuperado la movilidad en una parte sustancial el tratamiento es exitoso.
Los biomateriales que han sido producidos a partir de sistemas hidrofílicos poliméricos por ejemplo derivados de PEG han sido descritos en la técnica anterior como en la US 5, 626, 863, US 6, 166, 130, US 6, 051, 648, US 5, 874, 500, US 6, 258, 351 o WO 00/44808. Ellos no son adecuados para usarse para aumentar tejido duro debido a la carencia de desempeño mecánico, como resistencia y rigidez y debido al hinchamiento exhaustivo. El hinchamiento incontrolable, sin embargo, hace los biomateriales inaceptables para su aplicación en espacios limitados como en vértebras. El material se expande y puede presionar contra nervios, por ejemplo la médula espinal o proyectarse de manera incontrolable desde el lugar de inyección.
Por lo tanto un objetivo de la presente invención... [Seguir leyendo]
Reivindicaciones:
1. Uso de una composición que comprende al menos un primer y un segundo componente precursores, caracterizado porque el primer componente precursor comprende al menos m grupos nucleofílicos y el segundo componente precursor comprende al menos n grupos electrofílicos donde m+n es al menos cinco y en donde el primer y segundo componentes precursores son seleccionados del grupo que consiste de oligómeros y son seleccionados de modo que los grupos nucleofílicos y electrofílicos formen enlaces covalentes entre sí, a temperaturas fisiológicas para la producción de un biomaterial para aumentar el tejido duro.
2. El uso de una composición que comprende al menos un primer y un segundo componentes precursores, caracterizado porque el primer componente precursor comprende al menos dos grupos nucleofílicos y el segundo componente precursor comprende al menos dos grupos electrofílicos, donde el primer y segundo grupos precursores son seleccionados del grupo que consiste de oligómeros, y están seleccionados de modo que los grupos nucleofílicos y electrofílicos formen enlaces covalentes entre sí, a temperaturas fisiológicas para la producción de una composición farmacéutica o biomaterial para aumentar el tejido duro.
3. El uso de una composición según cualquiera de las reivindicaciones 1 ó 2, en donde el tejido duro es al menos una vértebra.
4. El uso de una composición según cualquiera de las reivindicaciones 1 a 3, en donde los grupos nucleofílicos del primer componente precursor y los grupos electrofílicos del segundo componente precursor son seleccionados de modo que formen enlaces covalentes por la reacción de adición de Michael.
5. El uso de una composición según cualquiera de las reivindicaciones 1 a 4, en donde los grupos nucleofílicos del primer componente precursor son seleccionados del grupo que consiste de tioles o aminas.
6. El uso de una composición según cualquiera de las reivindicaciones 1 a 5, en donde los grupos electrofílicos del segundo componente precursor comprende grupos insaturados conjugados.
7. El uso de una composición según cualquiera de las reivindicaciones 1 a 6, en donde m del primer componente precursor es tres, cuatro o cinco.
8. El uso de una composición según cualquiera de las reivindicaciones 1 a 7, en donde n del segundo componente precursor es tres o cuatro.
9. El uso de una composición según cualquiera de las reivindicaciones 1 a 8, en donde n+m es siete.
10. El uso de una composición según cualquiera de las reivindicaciones 1 a 9, en donde el primer componente precursor es seleccionado del grupo que consiste de siloxanos y derivados de los mismos.
11. El uso de una composición según la reivindicación 10, en donde el siloxano o derivado del mismo es un ciclosiloxano de la fórmula
R1 Si O R2"-X n n = 3-6, preferiblemente 4; R1= alquilo, preferiblemente alquilo de C1-C6; R2" = alquilo, preferiblemente alquilo de C2-C3; X = -SH, -NH2.
12. El uso de una composición según la reivindicación 11, en donde el ciclosiloxano es 2, 4, 6, 8-tetra (2mercaptoetil) -2, 4, 6, 8-tetrametil-ciclotetra-siloxano con n=4; R1=CH3; R2=C2H4; X=-SH.
13. El uso de una composición según cualquiera de las reivindicaciones 1 a 12, en donde el grupo insaturado conjugado comprende al menos un grupo acrilato.
14. El uso de una composición según cualquiera de las reivindicaciones 1 a 13, en donde el segundo componente precursor es seleccionado del grupo que consiste de derivados de 1, 1, 1 tris (hidroximetil) propano, pentaeritritol y triglicerol.
15. El uso de una composición según la reivindicación 13, en donde el segundo componente precursor es triacrilato de trimetilolpropano.
16. El uso de una composición según cualquiera de las reivindicaciones 1 a 15, en donde la composición además comprende bases seleccionadas del grupo de bases de alquilamina terciaria.
17. El uso de una composición según la reivindicación 16, en donde la base de alquilamina terciaria es tributilamina.
18. El uso de una composición según la reivindicación 1, en donde el primer componente comprende al menos grupos m nucleofílicos y el segundo componente precursor comprende al menos n grupos insaturados conjugados, en donde m+n es al menos cinco y en donde el primer componente comprende siloxanos o derivados del mismo, los siloxanos comprenden tioles como grupos nucleofílicos y en donde el grupo insaturado conjugado comprende acrilatos.
19. El uso de una composición según la reivindicación 12, en donde el primer componente comprende al menos dos grupos nucleofílicos y el segundo componente comprende al menos dos grupos insaturados conjugados en donde los grupos nucleofílicos están seleccionados del grupo que consiste de tioles y aminas y los grupos insaturados conjugados están seleccionados del grupo que consiste de itaconatos, acrilatos e itaconamidas.
20. El uso de una composición según la reivindicación 19, en donde el primer componente comprende siloxanos.
21. El uso de una composición según cualquiera de las reivindicaciones 18 o 20, en donde el siloxano es un ciclosiloxano de la fórmula
R1 Si O R2"-X n n = 3-6, preferiblemente 4; R1= alquilo, preferiblemente alquilo de C1-C6; R2 = alquilo, preferiblemente alquilo de C2-C3; X = -SH, -NH2.
22. El uso de una composición según la reivindicación 20 ó 21, en donde el ciclosiloxano es 2, 4, 6, 8-tetra (2mercaptoetil) -2, 4, 6, 8-tetrametilciclotetrasiloxano con n=4; R1=CH3; R2=C2H4; X=-SH.
23. El uso de una composición según cualquiera de las reivindicaciones 18 a 22, en donde el segundo componente precursor es seleccionado del grupo que consiste de derivados de 1, 1, 1-tris (hidroximetil) propano, pentaeritritol y triglicerol.
24. El uso de una composición según la reivindicación 23, en donde el segundo componente precursor es triacrilato de trimetilolpropano.
25. Un equipo de partes adecuado para formar un biomaterial curable in situ para aumentar tejido duro, caracterizado porque comprende al menos un primer y un segundo componentes precursores separados entre sí, donde el primer componente precursor comprende al menos m grupos nucleofílicos y el segundo componente precursor comprende al menos n grupos electrofílicos, siendo la suma de m+n al menos cinco y donde el primer y segundo componentes precursores son seleccionados del grupo que consiste de oligómeros y están seleccionados de modo que los grupos nucleofílicos y electrofílicos forman enlaces covalentes entre sí por una reacción de adición del tipo de Michael a temperaturas fisiológicas.
26. Un equipo de partes adecuado para formar un biomaterial curable in situ, para aumentar tejido duro, caracterizado porque comprende al menos un primer y un segundo componentes precursores separados entre sí, en donde el primer componente precursor comprende al menos dos grupos nucleofílicos y el segundo componente precursor comprende al menos dos grupos electrofílicos, en donde el primer y segundo componentes precursores son seleccionados del grupo que consiste de oligómeros, y están seleccionados de tal modo que los grupos nucleofílicos y electrofílicos forman enlaces covalentes entre sí por una reacción de adición del tipo de Michael a temperaturas fisiológicas.
27. El equipo de partes según cualquiera de las reivindicaciones 25 ó 26, caracterizado porque los grupos nucleofílicos del primer componente precursor son grupos tiol.
28. El equipo de partes según cualquiera de las reivindicaciones 25 a 27, caracterizado porque los grupos electrofílicos de los segundos componentes precursores son seleccionados del grupo de acrilatos, itaconatos o itaconamidas.
29. El equipo de partes según cualquiera de las reivindicaciones 25 a 28, caracterizado porque el primer componente precursor es seleccionado del grupo que consiste de siloxanos y derivados de los mismos.
30. El equipo de partes según la reivindicación 29, caracterizado porque el siloxano es un ciclosiloxano de fórmula
R1 Si O R2"-X n n = 3-6, preferiblemente 4; R1= alquilo, preferiblemente alquilo de C1-C6; R2" = alquilo, preferiblemente alquilo de C2-C3; X = -SH, -NH2.
31. El equipo de partes según la reivindicación 30, caracterizado porque el ciclosiloxano es 2, 4, 6, 8-tetra (2mercaptoetil) -2, 4, 6, 8-tetrametilciclotetrasiloxano con n=4; R1= CH3; R2"= C2H4; X= -SH.
32. El equipo de partes según cualquiera de las reivindicaciones 25 a 31, caracterizado porque el segundo componente precursor es seleccionado del grupo que consiste de derivados de 1, 1, 1 tris (hidroximetil) propano, pentaeritritol y triglicerol.
33. Una composición reticulable in situ adecuada para formar un biomaterial para aumentar tejido duro, la composición caracterizada porque comprende al menos un primer y un segundo componentes precursores, donde el primer y segundo componentes precursores son monómeros y dicho primer componente precursor comprende al menos m grupos nucleofílicos y el segundo componente precursor comprende al menos n grupos electrofílicos, donde m+n es al menos cinco y donde el primer o segundo componentes precursores son seleccionados de modo que los grupos nucleofílicos y electrofílicos formen enlaces covalentes entre sí a temperaturas fisiológicas.
34. Una composición reticulable in situ adecuada para formar un biomaterial para aumentar tejido duro, la composición caracterizada porque comprende al menos un primer y un segundo componentes precursores, en donde el primer y segundo componentes precursores son monómeros y el primer componente precursor comprende al menos dos grupos nucleofílicos y el segundo componente precursor comprende al menos dos grupos electrofílicos, en donde el primer y segundo componentes precursores son seleccionados de modo que los grupos nucleofílicos y electrofílicos formen enlaces covalentes entre sí a temperaturas fisiológicas.
35. La composición reticulable in situ, según la reivindicación 33 ó 34, caracterizada porque es adecuada para formar un biomaterial que tiene una resistencia a la compresión final de al menos 10 MPa después de dos días de almacenamiento bajo condiciones secas a 37º C.
36. La composición reticulable in situ, según cualquiera de las reivindicaciones 33 a 35, caracterizada porque el primer componente precursor es seleccionado del grupo que consiste de siloxanos.
37. La composición reticulable in situ, según la reivindicación 36, en donde el siloxano es un ciclosiloxano de la formula
R1
Si O
R2"X
n n = 3-6, preferiblemente 4; R1 = alquilo, preferiblemente alquilo de C1-C6; R2" = alquilo, preferiblemente alquilo de C2-C3; X = -SH, -NH2.
38. La composición reticulable in situ según la reivindicación 37, caracterizada porque el ciclosiloxano es 5 2, 4, 6, 8-tetra (2-mercaptoetil) -2, 4, 6, 8-tetrametilciclotetrasiloxano con n = 4; R1 = CH3; R2" = C2H4; X = -SH.
39. La composición reticulable in situ, según cualquiera de las reivindicaciones 33 a 38, en donde el segundo componente precursor es seleccionado del grupo que consiste de derivados de 1, 1, 1 tris (hidroximetil) propano, pentaeritritol y triglicerol.
40. La composición reticulable in situ de conformidad con la reivindicación 39, caracterizada porque el segundo 10 componente precursor es triacrilato de trimetilolpropano.
Patentes similares o relacionadas:
Formulaciones farmacéuticas de estatinas y ácidos grasos omega-3 para encapsulación, del 27 de Mayo de 2020, de Catalent Ontario Limited: Una cápsula de gelatina blanda multifase para administración oral, comprendiendo la cápsula de gelatina blanda: una forma de dosificación […]
Proteínas de unión a antígeno para proproteína convertasa subtilisina kexina tipo 9 (PCSK9), del 6 de Mayo de 2020, de AMGEN INC.: Una proteína de unión a antígeno, donde dicha proteína de unión a antígeno (i) comprende (a) un dominio variable de cadena ligera que comprende una secuencia […]
Análogos deuterados de ácido 4hidroxibutírico, del 8 de Abril de 2020, de CONCERT PHARMACEUTICALS, INC: Una composición farmacéutica que comprende un compuesto de Fórmula IV **(Ver fórmula)** en la que: A es hidrógeno, deuterio, -CH2-C(O)OR2 o -CH(R1)-C(O)OR2; […]
Composición farmacéutica para administración oral que comprende una concentración elevada de taxano, del 18 de Marzo de 2020, de Dae Hwa Pharma. Co., Ltd: Una composición farmacéutica para administración oral, que comprende (a) de un 4 a un 40 % en peso de un taxano, (b) de un 10 a un 30 % en peso de un triglicérido de cadena […]
Composiciones tópicas que comprenden fipronilo y permetrina y procedimientos de uso, del 22 de Enero de 2020, de Boehringer Ingelheim Animal Health USA Inc: Composición tópica para el tratamiento y prevención de una infestación ectoparasitaria que comprende: de 2% (p/p) a 15% (p/p) de fipronil; […]
Trastornos neurodegenerativos y métodos de tratamiento y diagnóstico de los mismos, del 8 de Enero de 2020, de THE UNIVERSITY OF QUEENSLAND: Triheptanoína para su uso en el tratamiento, prevención y/o retraso del inicio de una enfermedad de la neurona motora (MND) en un animal, en el que […]
Composición que contiene el compuesto de monoacetil diacilglicerol como principio activo para prevenir o tratar la dermatitis atópica, del 1 de Enero de 2020, de Enzychem Lifesciences Corporation: Una composición para uso en la prevención o el tratamiento de la dermatitis atópica, en donde la composición es para administración oral y en donde la composición comprende […]
Composición que contiene un compuesto de monoacetildiacilglicerol como principio activo para la prevención o tratamiento de enfermedades pulmonares obstructivas crónicas, del 1 de Enero de 2020, de Enzychem Lifesciences Corporation: Composición farmacéutica que comprende un compuesto de monoacetildiacilglicerol de Fórmula 1 como principio activo para utilizar en la prevención o el tratamiento […]