Antígenos bacterianos y usos de los mismos.
Un procedimiento de preparar una vacuna que comprende:
separar lipopolisacáridos de una bacteria de interés,
en la que la bacteria está seleccionada del grupo queconsiste en Neisseria meningitidis y Mannheimia haemolytica;
desesterificar el lipopolisacárido;
retirar al menos un ácido graso N-ligado del lipopolisacárido con una actividad amidasa aislada; yconjugar el lipopolisacárido modificado con una molécula transportadora adecuada.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/CA2006/001927.
Solicitante: NATIONAL RESEARCH COUNCIL OF CANADA.
Nacionalidad solicitante: Canadá.
Dirección: INTELLECTUAL PROPERTY SERVICES OFFICE EG06B BLDG. M-58, MONTREAL ROAD OTTAWA, ONTARIO K1A 0R6 CANADA.
Inventor/es: RICHARDS,JAMES,C, COX,ANDREW, NEELAMEGAN,DHAMODHARAN, SCHOENHOFEN,IAN, ST. MICHAEL,FRANK.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/14 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que contienen radicales sacárido; Sus derivados.
- A61K39/02 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Antígenos bacterianos.
- A61K39/095 A61K 39/00 […] › Neisseria.
- A61K39/102 A61K 39/00 […] › Pasteurella; Haemophilus.
- A61P31/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Agentes antibacterianos.
- C12N9/24 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › actúan sobre compuestos glicosílicos (3.2).
- C12P19/04 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › Polisacáridos, es decir, compuestos que contienen más de cinco radicales sacárido unidos entre ellos por enlaces glucosídicos.
PDF original: ES-2389814_T3.pdf
Fragmento de la descripción:
Antígenos bacterianos y usos de los mismos
Información de solicitudes anteriores
La presente solicitud reivindica el beneficio de la Solicitud de Patente Provisional de los EE.UU. 60/738.985, presentada el 23 de noviembre, 2005.
Antecedentes de la invención
Las bacterias gram-negativas pueden causar enfermedades de preocupación en salud pública y económica significativa en seres humanos y en otros animales. Se están persiguiendo estrategias de vacunas para combatir estas infecciones. Estas estrategias se basan en la identificación de componentes de superficie celular inmunogénicos, conservados; sin embargo, la detección de moléculas conservadas que debería conferir protección contra la gran mayoría de las cepas de una única especie ha demostrado ser problemática.
La superficie exterior de la membrana externa de todas las bacterias gram-negativas contiene una molécula de carbohidratos anfifílica llamada lipopolisacárido (LPS) que en virtud de su localización de superficie puede considerarse como un antígeno candidato de vacuna. Como su nombre sugiere esta molécula contiene una región lipídica que une a la molécula en la membrana exterior, en virtud tanto de ácidos grasos unidos a ésteres (O-ligados) como de ácidos grasos unidos a amida (N-ligados) . La región de lípidos A y específicamente los ácidos grasos son responsables de la actividad endotóxica de la bacteria gram-negativa y consisten en la mayoría de las especies de un disacárido de azúcares de glucosamina que están fosforiladas y los ácidos grasos unidos a ésteres y unidos a amidas como se muestran en las figuras 1 y 2.
El oligosacárido de núcleo se puede dividir arbitrariamente en un núcleo externo e interno y está conectado a la región de lípidos A por medio de uno o más azúcar (es) de cetosa, ácido 2-ceto-3-deoxi-octulosónico (Kdo) . Una unidad de repetición polimérica (O-antígeno) puede estar presente o ausente más allá del oligosacárido de núcleo de la molécula de LPS. El O-antígeno es un resto variable entre cepas de la misma especie y a menudo es el antígeno responsable de los esquemas de serotipado adoptados para clasificar una especie. Debido a su naturaleza variable dentro de la mayoría de las especies el O-antígeno no es un buen candidato para vacunas ya que los anticuerpos dirigidos a un O-antígeno serán específicos de serotipo y no ofrecen protección a los otros serotipos de la misma cepa. De forma similar la región de núcleo externo puede ser algo variable dentro de una especie y no es por lo tanto un buen candidato para vacunas. Sin embargo, lo que se denomina de forma arbitraria el oligosacárido de núcleo interno se ha encontrado que está conservado dentro de varias especies y es el antígeno de vacuna de elección en esta solicitud. Las regiones conservadas de moléculas de LPS se han identificado en el núcleo oligosacarídico de varias especies y los ejemplos de estructuras oligosacarídicas de núcleo se detallan en la figura 3 más adelante para LPS de las especies Neisseria meningitidis, Haemophilus influenzae y Mannheimia haemolytica. Para los propósitos de este debate, pero no restringido a justamente estas estructuras, la región de núcleo interior para Neisseria meningitidis, Haemophilus influenzae y Mannheimia haemolytica vinculada a la región de lípido A se ilustra en las figuras 3b-d. Sin embargo la tecnología descrita aquí sería igualmente aplicable a los otros antígenos de carbohidratos de LPS, oligosacárido de núcleo externo y O-antígeno.
La endotoxicidad de la región de lípido A se debe a los residuos de ácidos grasos. La eliminación de los ácidos grasos unidos a ésteres deja una especie de LPS O-deacilada que ya no es endotóxica. La eliminación de todos los ácidos grasos es decir tanto de los ácidos grasos unidos a amida como de los ácidos grasos unidos a ésteres puede llevarse a cabo químicamente, pero implica condiciones severas que pueden hacer efecto en otras regiones de la molécula de LPS. Incluso las condiciones químicas suaves empleadas para efectuar la O-deacilación pueden hacer efecto sobre residuos unidos a éster en cualquier parte en el LPS.
Las vacunas basadas en LPS requieren generalmente la retirada de ácidos grasos de la región de lípido A de la molécula para reducir la endotoxicidad. Preferentemente, esta etapa de detoxificación no modifica los epítopos de carbohidratos en la molécula de LPS, sin embargo las técnicas comúnmente disponibles no lo permiten.
Los procedimientos actuales empleados son para O-deacilar químicamente LPS produciendo una molécula de LPS O-deacilada (LPS-OH) que puede usarse bien directamente o bien tras modificación adicional para conjugar a un vehículo proteico adecuado para producir un candidato de vacuna glucoconjugado. La eliminación de los ácidos grasos N-ligados que quedan de LPS-OH mejoraría grandemente las estrategias de conjugación, ya que esto crearía una molécula completamente soluble en agua susceptible de todas las manipulaciones subsiguientes. Sin embargo, los procedimientos químicos actualmente empleados para de-N-acilar moléculas de LPS modifican también algunos residuos en el núcleo interno, alterando así la estructura de epítopos potencialmente inmunogénicos en la molécula de LPS. Por ejemplo el residuo de fosfoetanolamina (PEtn) del oligosacárido de núcleo interno de LPS de Neisseria meningitidis (fig. 3ab) , un resto inmunogénico conocido, es sensible a las condiciones químicas requeridas para retirar los ácidos grasos N-ligados, modificando así un residuo conservado en el LPS de núcleo interno y creando así una molécula que ya no es representativa de la estructura de LPS nativa.
Sumario de la invención
De acuerdo con un primer aspecto de la invención, se proporciona un procedimiento de preparar una vacuna que comprende:
separar lipopolisacáridos de una bacteria de interés;
desesterificar el lipopolisacárido;
retirar al menos un ácido graso N-ligado del lipopolisacárido con una actividad amidasa aislada; y
conjugar el lipopolisacárido modificado con una molécula transportadora adecuada. De acuerdo con un segundo aspecto de la invención, se proporciona un procedimiento de recuperar un lipopolisacárido modificado de una bacteria de interés que comprende:
separar lipopolisacáridos de la bacteria de interés;
desesterificar el lipopolisacárido;
retirar al menos un ácido graso N-ligado del lipopolisacárido con una actividad amidasa aislada; y
recuperar el LPS modificado. De acuerdo con un tercer aspecto de la invención, se proporciona una molécula de lipopolisacárido (LPS) mono-Nacilada-de-O-acilada o una molécula de LPS de-N-acilada-de-O-acilada a partir de una bacteria de interés conjugado a una proteína transportadora.
De acuerdo con un cuarto aspecto de la invención, se proporciona el uso del conjugado según se describe anteriormente para la inmunización de individuos que tienen o son sospechosos de tener o están en riesgo de desarrollar una infección por la bacteria de interés.
De acuerdo con un quinto aspecto de la invención, se proporciona el uso del conjugado como se describe anteriormente en la elaboración de un medicamento para la inmunización de individuos que tienen o son sospechosos de tener o están en riesgo de desarrollar una infección por la bacteria de interés
Breve descripción de los dibujos
La figura 1 es una representación esquemática de la región de lípido A de molécula LPS de Escherichia coli donde R es la región de oligosacárido-O-antígeno de núcleo de la molécula de LPS y los números en la parte de abajo de la figura se refieren a la longitud de cadenas de las moléculas de ácidos grasos. La fosforilación del lípido A también puede variar, por ejemplo, P, P-P o P-PEtn.
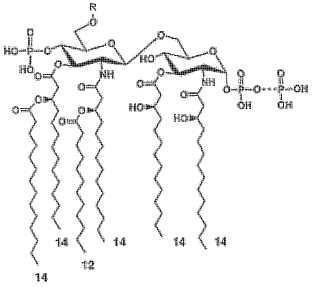
La figura 2 es una representación esquemática de de la región de lípido A de la molécula de LPS de Neisseria meningitidis, donde R es la región de oligosacáridos de núcleo de la molécula de LPS y los números en la parte de abajo de la figura se refieren a la longitud de cadena de las moléculas de ácidos grasos. La fosforilación del lípido A también puede variar, por ejemplo P, P-P o P-PEtn.
La figura 3 (a) es una representación esquemática del oligosacárido de núcleo de la molécula de LPS de Neisseria meningitidis.
La figura 3 (b) es una representación... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento de preparar una vacuna que comprende:
separar lipopolisacáridos de una bacteria de interés, en la que la bacteria está seleccionada del grupo que consiste en Neisseria meningitidis y Mannheimia haemolytica;
desesterificar el lipopolisacárido;
retirar al menos un ácido graso N-ligado del lipopolisacárido con una actividad amidasa aislada; y
conjugar el lipopolisacárido modificado con una molécula transportadora adecuada.
2. El procedimiento de acuerdo con la reivindicación 1 en el que la actividad de amidasa es a partir de un péptido que tiene al menos identidad del 70 % con la secuencia de aminoácidos según se expone bien en SEC ID N.º: 1 o bien en SEC ID N.º: 2 como se muestra en las figuras 5a y 5b, respectivamente.
3. El procedimiento de acuerdo con la reivindicación 1 en el que la actividad de amidasa es a partir de un péptido que tiene al menos el 80 % de identidad con la secuencia de aminoácidos según se expone bien en la SEC ID N.º: 1
o bien en la SEC ID N.º: 2.
4. El procedimiento de acuerdo con la reivindicación 1 en el que la actividad de amidasa es a partir de un péptido que tiene al menos identidad del 90 % con la secuencia de aminoácidos según se expone bien en la SEC ID N.º: 1 o bien en la SEC ID N.º: 2.
5. Un procedimiento de recuperar un lipopolisacárido modificado a partir de una bacteria de interés que comprende:
separar lipopolisacáridos de una bacteria de interés, en la que la bacteria está seleccionada del grupo que consiste en Neisseria meningitidis y Mannheimia haemolytica;
desesterificar la fase lipopolisacarídica;
retirar al menos un ácido graso N-ligado del lipopolisacárido con una actividad amidasa aislada; y
recuperar el LPS modificado.
6. El procedimiento de acuerdo con la reivindicación 5 en el que la actividad de amidasa es a partir de un péptido que tiene al menos identidad del 70 % con la secuencia de aminoácidos según se expone bien en la SEC ID N.º: 1 o bien en la SEC ID N.º: 2.
7. El procedimiento de acuerdo con la reivindicación 5 en el que la actividad de amidasa es a partir de un péptido que tiene al menos identidad del 80 % con la secuencia de aminoácidos según se expone bien en la SEC ID N.º: 1 o bien en la SEC ID N.º: 2.
8. El procedimiento de acuerdo con la reivindicación 5 en el que la actividad de amidasa es a partir de un péptido que tiene al menos identidad del 90 % con la secuencia de aminoácidos según se expone bien en la SEC ID N.º: 1 o bien en la SEC ID N.º: 2.
9. El procedimiento de acuerdo con la reivindicación 5 en el que el LPS modificado es soluble en agua, está Odeacilado y tiene al menos uno de los dos ácidos grasos N-ligados eliminado.
10. Una molécula de lipopolisacárido (LPS) mono-N-acilado-de-O-acilado aislada o purificada o una molécula de LPS de-N-acilado-de-O-acilado aislada o purificada a partir de una bacteria de interés conjugada a una proteína transportadora, en la que la bacteria está seleccionada del grupo que consiste en Neisseria meningitidis y Mannheimia haemolytica.
11. Uso del conjugado de acuerdo con la reivindicación 10 en la elaboración de un medicamento para la inmunización de individuos que tienen, o que son sospechosos de tener, o que están en riesgo de desarrollar una infección por la bacteria de interés.
Fig. 1. Fig. 2. Fig. 3a.
Fig. 3b
Lípido A
Fig. 3c.
Fig. 3d.
Lípido A
Lípido A
Fig. 4.
amidasa de ácidos grasos I (FAAI) amidasa de ácidos grasos II (FAAII)
Fig. 5b. Dd2 (637 aa con peso molecular 70, 282 daltons en el cromosoma 2)
Fig. 8. Fig. 8 continuación. Fig. 10. Fig. 12.
Fig. 16.
HIS 6X SITIO TC AMIDASA Dd1
Fig. 18.
Fig. 19.
Fig. 21.
Araquidonoil-p-nitroanilina P-nitroanilina Ácido araquidónico Tinción colorimétrica amarilla
()
11. 00 a 1 2 nm
Fig. 23.
47, 5 32, 5
Fig. 25. Fig. 27.
Fig. 29.
LPS-OH de galE de N.m./N-deacilación Sobrenadante de células privadas de nutrientes + LPS-OH
LPS-OH de 1003 lic1 lpsA de H.i./N-deacilación Sobrenadante de células privadas de nutrientes + LPS-OH
Fig. 31.
Fig. 33.
Fig. 35.
Tratamiento de Dictyostelium
Actividad de FAA I
Fig. 37.
Tratamiento de Dictyostelium
Actividad de FAA II
Fig. 38b Fig. 40. Fig. 42. Fig. 44. Fig. 45b.
Masa (m/z)
Fig. 47.
Carriles:
1: CRM
2: CRM activada
3: L3 galE-conj. purificado; Dictyostelium
% de suero de conejo
Patentes similares o relacionadas:
Diversificación de los oligosacáridos de la leche humana (HMO) o sus precursores, del 8 de Julio de 2020, de Glycom A/S: Un metodo de preparacion de una mezcla diversificada que comprende dos o mas oligosacaridos de la leche humana (HMO), el metodo comprende las etapas de […]
Método de producción de compuestos de inclusión de flavonoide, del 3 de Junio de 2020, de TAIYO KAGAKU CO., LTD.: Un método de producción de un compuesto de inclusión de flavonoide, que comprende una etapa de escisión que comprende tratar un flavonoide escasamente […]
Construcción de nuevas variantes de dextransacarasa DSR-S por ingeniería genética, del 6 de Mayo de 2020, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: 1. Una dextransacarasa que consiste en una secuencia que tiene el 90 %, el 95 % o el 98 % de similitud de secuencia con una secuencia de aminoácidos seleccionada del fragmento […]
Métodos para la degradación o la conversión de polisacáridos de la pared celular vegetal, del 6 de Mayo de 2020, de NOVOZYMES, INC.: Metodo para degradar o convertir los polisacaridos de la pared celular vegetal en uno o mas azucares, que comprende: tratar los polisacaridos de la pared celular vegetal con […]
Procedimiento para la purificación de hidrolizado de biomasa, del 29 de Abril de 2020, de CLARIANT INTERNATIONAL LTD.: Un procedimiento para la purificación de hidrolizado de biomasa que comprende las etapas a) Proporcionar un hidrolizado de biomasa, en el que el hidrolizado […]
Construcción de nuevas variantes de dextransacarasa DSR-S por ingeniería genética, del 22 de Abril de 2020, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: Una secuencia de nucleótidos que consiste en una secuencia de nucleótidos como se define en SEQ ID NO: 1 o la secuencia complementaria a la secuencia como […]
Transsialidasas de photobacterium mutadas, del 15 de Abril de 2020, de Glycom A/S: Una α2,6-transsialidasa que tiene una secuencia de aminoácidos que es por lo menos un 90% idéntica a la secuencia de aminoácidos de la SEQ ID […]
Exopolisacárido para el tratamiento y/o cuidado de la piel, mucosas, cabello y/o uñas, del 11 de Marzo de 2020, de LUBRIZOL ADVANCED MATERIALS, INC.: Uso del exopolisacárido de la cepa de las especies de Vibrio sp. con número de depósito CNCM I-4277, para mejorar la hidratación de la piel, mucosas, […]