Agentes reaccionantes de unión bioespecífica marcados con nuevos quelatos luminiscentes de lantánidos y su utilización.
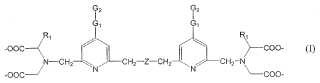
Quelato luminiscente de lantánido, caracterizado porque comprende un ion lantánido y un ligando quelante defórmula (I)
en la que
R1 se selecciona del grupo que consiste en H,
-COOH, -COO-, -CH2COOH y -CH2COO-;
G1 es un grupo que consiste en uno o dos restos, seleccionándose cada resto del grupo que consiste en etinodiílo(-C≡C-), etenileno (-CH≥CH-), fenileno, bifenileno, naftileno, piridileno, pirazinileno, pirimidinileno, piridazinileno,furileno, tienileno, pirrolileno, imidazolileno, pirazolileno, tiazolileno, isotiazolileno, oxazolileno, isoxazolileno,furazanileno, 1,2,4-triazol-3,5-ileno y oxadiazolileno;
G2 es un grupo para el acoplamiento a un agente reaccionante de unión bioespecífica que se selecciona del grupoque consiste en grupos amino, aminooxi, carbonilo, aldehído o mercapto, y formas activadas obtenidas de ellos;Z se selecciona del grupo que consiste en carboxialquilamina {-N[(CH2)nCOOH]- o -N[(CH2)nCOO-]-, en el que n ≥1, 2, 3, 4, 5 ó 6}, éter (-O-), tioéter (-S-), carbonilo (-CO-) y metilo no sustituido o sustituido (-CR2-), en el que elgrupo R2 se selecciona del grupo que consiste en H, metilo, etilo y carboxilalquilo [-(CH2)mCOOH o -(CH2)mCOO-,en el que m≥ 1, 2, 3, 4, 5 ó 6]; y
el ion lantánido se selecciona del grupo que consiste en europio(III), terbio(III), disprosio(III) y samario(III).
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E04396007.
Solicitante: DHR Finland Oy.
Nacionalidad solicitante: Finlandia.
Dirección: Biolinja 12 20750 Turku FINLANDIA.
Inventor/es: TAKALO, HARRI, ROSENBERG,JAANA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D401/12 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 401/00 Compuestos heterocíclicos que contienen dos o más heterociclos, que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, siendo al menos un ciclo de seis miembros con solamente un átomo de nitrógeno. › unidos por una cadena que contiene heteroátomos como enlaces de cadena.
- C07D401/14 C07D 401/00 […] › que contienen tres o más heterociclos.
- C07F5/00 C07 […] › C07F COMPUESTOS ACICLICOS, CARBOCICLICOS O HETEROCICLICOS QUE CONTIENEN ELEMENTOS DISTINTOS DEL CARBONO, HIDROGENO, HALOGENOS, OXIGENO, NITROGENO, AZUFRE, SELENIO O TELURO (porfirinas que contienen metal C07D 487/22; compuestos macromoleculares C08). › Compuestos que contienen elementos de los grupos 3 o 13 del sistema periódico.
- G01N33/533 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › con un marcador fluorescente.
PDF original: ES-2391952_T3.pdf
Fragmento de la descripción:
Agentes reaccionantes de unión bioespecífica marcados con nuevos quelatos luminiscentes de lantánidos y su utilización.
Campo de la invención
La presente invención se refiere a moléculas detectables que comprenden quelatos de lantánidos unidos a un agente reaccionante de unión bioespecífica, y a la utilización de dichas moléculas detectables en ensayos de unión a base de bioafinidad. La invención se refiere además a nuevos quelatos luminiscentes de lantánidos, útiles en la preparación de dichas moléculas detectables.
Antecedentes de la invención
Se usan aquí publicaciones y otros materiales para iluminar los antecedentes de la invención, y en particular se usan casos para proporcionar detalles adicionales respecto de la práctica.
En ensayos de unión específica, tales como, por ejemplo, inmunoensayos, ensayos de hibridación de ADN, ensayos de unión a receptores, y ensayos de unión celular, generalmente los analitos a medir están presentes a concentraciones muy bajas. Por lo tanto, se han desarrollado diversos compuestos marcadores que permiten que el agente reaccionante marcador se detecte y se cuantifique con sensibilidad elevada. En inmunoensayos y en ensayos de hibridación de ADN, es bien conocida la espectroscopía de luminiscencia resuelta en el tiempo que usa quelatos de lantánidos (por ejemplo Hemmilä, T. Stålberg, y P. Mottram (eds.) , “Bioanalytical Applications of Labelling Technologies”, Wallac, Turku, 1994 y D. Wild (eds) , “The Immunoassay Handbook”, Nature Publishing Group, 2001) . Los quelatos fotoluminiscentes (denominados en el contexto de esta memoria descriptiva simplemente como luminiscentes) estables de lantánidos también tienen otras aplicaciones, por ejemplo microscopía de fluorescencia y citometría. Por lo tanto, se ha realizado un número de intentos para desarrollar nuevos quelatos muy luminiscentes adecuados para esos tipos de aplicaciones fluorométricas resueltas en el tiempo. Estos incluyen, por ejemplo, quelatos estables compuestos de derivados de piridina (documentos US 4.920.195; US 4.801.722; US 4.761.481; US 5.571.897; US 5.859.215; Latva, M., Takalo, H., Mukkala, V. M., Matachescu, C., Rodriquez-Ubis,
J.C. y Kankare, J., 1997, J. Luminescence, 75, 149; Takalo, H., Hemmilä, I., Sutela, T. y Latva, M., 1996, Helv. Chim. Acta, 79, 789) , bipiridinas (documento US 5.216.134) , terpiridinas (documentos US 4.859.777, US 5.202.423, US 5.324.825) o diversos compuestos fenólicos (documentos US 4.670.572, US 4.794.191, IT 42508A/89) como grupos mediadores de la energía, y ácidos policarboxílicos como partes quelantes. Además, en las solicitudes de patentes y/o patentes, se han descrito diversos derivados de dicarboxilato (documentos US 5.032.677, US 5.055.578, US 4.772.563) , criptatos macrocíclicos (documentos US 4.927.923, WO 93/5049, EP 0 493 745) , calixarenos (Sato, N. y Shinkai, S., 1993, J. Chem. Soc. Perkin Trans. 2, 621; Steemers, F.J., Verboom, W., Reinboudt, D.N., van der Tol,
E.B. y Verhoeven, J.W., 1995, J. Am. Chem. Soc., 117, 9408) , conjugado de DTPA carbostril 124 (Selvin, P.R., Rana, T.M. y Hearst, J.E., 1994, J. Am. Chem. Soc., 116, 6029) y bases de Schiff macrocíclicas (documento EP 0 369 000) .
También se han descrito quelatos para ensayos de unión específica en, por ejemplo, los documentos EP 0 770 610; EP 0 649 020; EP 0 967 205; EP 1 152 010; WO 93/11433; Lemmetyinen et al. (2000) Luminescence 15, 341-350; Takalo et al. (1997) Helv. Chim. Acta 80, 372-387; Mukkala et al. (1997) J. Alloys & Compounds 225, 507-510; Karsilayan et al. (1997) Bioconj. Chem. 8, 71-75; Latva et al. (1997) J. Luminescence 75, 149-169; Hemmilä et al. (1997) J. Alloys & Compounds 249, 158-162; Takalo et al. (1994) Bioconj. Chem. 5, 278-282 y Mikola et al. (1995) Bioconj. Chem. 6, 235-241.
Es sabido que los quelatos luminiscentes de lantánidos se desactivan en una disolución acuosa. Cuando moléculas de agua se coordinan en la esfera interna de quelatos, la desactivación es un resultado de un proceso de decaimiento eficiente sin radiación que implica el acoplamiento de vibración del estado excitado del lantánido y la oscilación del OH. El proceso es aditivo con respecto al número de osciladores de OR, y por tanto el decaimiento de la luminiscencia está relacionado de forma inversa con el número de moléculas de agua unidas. Se han desarrollado diversos sistemas para evitar este fenómeno, tal como la utilización de detergentes y compuestos sinérgicos, la ut8ilización de concentración elevada de iones de flúor, la eliminación de agua mediante secado antes de la medición, la utilización de una matriz polimérica, o la medición de la luminiscencia en un disolvente orgánico o en óxido de deuterio. Una forma ideal para evitar la desactivación acuosa directa es usar agentes quelantes estables, preferiblemente nonadentados, que no permiten la coordinación de agua con el ion quelado. En los quelatos mencionados anteriormente, el ion de lantánido está normalmente coordinado a 7, 8 ó 9 heteroátomos, formando respectivamente un quelato hepta-, octa- o nonadentado. Los quelatos hepta- y octadentados contienen de dos a una moléculas de agua, y de este modo sufren la desactivación acuosa. Generalmente se supone que átomos de coordinación adicionales en quelatos nonadentados – que no tienen molécula de agua en la primera esfera de coordinación – no tienen ningún efecto positivo adicional con respecto a la desactivación acuosa.
Durante un proceso de transferencia de energía desde un ligando excitado a un ion de lantánido, la energía sufre un cruzamiento entre sistemas a uno de los estados de triplete del ligando. La siguiente etapa es una transición de la energía prohibida por spin, provocando la fosforescencia del ligando, o una transferencia de energía intramolecular al ion de lantánido. El decaimiento térmico, tal como, por ejemplo, el movimiento y rotación térmicos moleculares, es un proceso de desactivación no radioactiva conocido del estado de triplete mencionado. Los quelatos marcadores de lantánidos contienen normalmente un grupo funcional reactivo para acoplar el marcador a un agente reaccionante de
unión bioespecífica. De este modo, en una biomolécula marcada, el marcador puede rotar, y la desactivación no radioactiva del estado del triplete del ligando es un fenómeno posible.
La visión general es que varios grupos de unión radioactivos en una molécula marcadora provocan reacción cruzada y formación de los agregados de agente reaccionante de unión bioespecífica durante el proceso de marcaje, y de 10 este modo producen problemas de purificación y un menor rendimiento del material marcado.
Sumario de la invención
Un objetivo de esta invención es proporcionar un quelato luminiscente de lantánido mejorado, que comprende un ion 15 lantánido y un ligando quelante.
Otro objetivo de la presente invención es proporcionar una molécula detectable mejorada, que comprende un agente reaccionante de unión bioespecífica unido al quelato luminiscente de lantánido, útil para ensayos de unión específica a base de bioafinidad.
Todavía otro objetivo de la invención es proporcionar un procedimiento de marcaje mejorado de un agente reaccionante de unión bioespecífica usando el marcador de quelato luminiscente de lantánido.
De este modo, según un aspecto, esta invención proporciona un quelato luminiscente de lantánido que comprende 25 un ion lantánido y un ligando quelante de la fórmula (I)
en la que 30 a) R1 se selecciona del grupo que consiste en H, -COOH, -COO-, -CH2COOH y -CH2COO-;
b) G1 es un grupo que consiste en uno o dos restos, seleccionándose cada resto del grupo que consiste en etinodiílo (-C:C-) , etenileno (-CH=CH-) , fenileno, bifenileno, naftileno, piridileno, pirazinileno, pirimidinileno, 35 piridazinileno, furileno, tienileno, pirrolileno, imidazolileno, pirazolileno, tiazolileno, isotiazolileno, oxazolileno, isoxazolileno, furazanileno, 1, 2, 4-triazol-3, 5-ileno y oxadiazolileno;
c) G2 es un grupo para el acoplamiento a un agente reaccionante de unión bioespecífica que se selecciona del grupo que contiene grupos amino, aminooxi, carbonilo, aldehído o mercapto, o una forma activada obtenida de 40 ellos;
d) Z se selecciona del grupo que consiste en carboxialquilamina, éter, tioéter, carbonilo y metilo no sustituido o sustituido, en el que el grupo R2 se selecciona de un grupo que consiste en H, metilo,... [Seguir leyendo]
Reivindicaciones:
1. Quelato luminiscente de lantánido, caracterizado porque comprende un ion lantánido y un ligando quelante de fórmula (I)
en la que
R1 se selecciona del grupo que consiste en H, -COOH, -COO-, -CH2COOH y -CH2COO-;
G1 es un grupo que consiste en uno o dos restos, seleccionándose cada resto del grupo que consiste en etinodiílo (-C:C-) , etenileno (-CH=CH-) , fenileno, bifenileno, naftileno, piridileno, pirazinileno, pirimidinileno, piridazinileno, furileno, tienileno, pirrolileno, imidazolileno, pirazolileno, tiazolileno, isotiazolileno, oxazolileno, isoxazolileno,
furazanileno, 1, 2, 4-triazol-3, 5-ileno y oxadiazolileno;
G2 es un grupo para el acoplamiento a un agente reaccionante de unión bioespecífica que se selecciona del grupo que consiste en grupos amino, aminooxi, carbonilo, aldehído o mercapto, y formas activadas obtenidas de ellos;
Z se selecciona del grupo que consiste en carboxialquilamina {-N[ (CH2) nCOOH]- o -N[ (CH2) nCOO-]-, en el que n = 1, 2, 3, 4, 5 ó 6}, éter (-O-) , tioéter (-S-) , carbonilo (-CO-) y metilo no sustituido o sustituido (-CR2-) , en el que el grupo R2 se selecciona del grupo que consiste en H, metilo, etilo y carboxilalquilo [- (CH2) mCOOH o - (CH2) mCOO-, en el que m= 1, 2, 3, 4, 5 ó 6]; y
el ion lantánido se selecciona del grupo que consiste en europio (III) , terbio (III) , disprosio (III) y samario (III) .
2. Quelato de lantánido según la reivindicación 1, caracterizado porque G2 es una forma activada seleccionada del grupo que consiste en isocianato, isotiocianato, diazonio, bromoacetamido, yodoacetamido, ésteres reactivos, piridil2-ditio y 4-cloro-1, 3, 5-triazin-2-ilamino 6-sustituido.
3. Quelato de lantánido según la reivindicación 1, caracterizado porque el ligando quelante es {2, 2’, 2”, 2”’{[ (carboximetil) imino]bis (metilen) -bis{[4-[ (4-isotiocianato) fenil]etinil]piridin-6, 2diil}bis (metilenonitrilo) }tetraquis (acetato) }europio (III) .
4. Molécula detectable, caracterizada porque comprende un agente reaccionante de unión bioespecífica unido a un quelato luminiscente de lantánido que comprende un ion lantánido y un ligando quelante de fórmula (I)
en la que
R1 se selecciona del grupo que consiste en H, -COOH, -COO-, -CH2COOH y -CH2COO-;
G1 es un grupo que consiste en uno o dos restos, seleccionándose cada resto del grupo que consiste en etinodiílo
45 (-C:C-) , etenileno (-CH=CH-) , fenileno, bifenileno, naftileno, piridileno, pirazinileno, pirimidinileno, piridazinileno, furileno, tienileno, pirrolileno, imidazolileno, pirazolileno, tiazolileno, isotiazolileno, oxazolileno, isoxazolileno, furazanileno, 1, 2, 4-triazol-3, 5-ileno y oxadiazolileno;
G2 es un grupo para el acoplamiento a un agente reaccionante de unión bioespecífica que se selecciona del grupo que consiste en tiourea (-NH-CS-NH-) , aminoacetamida (-NH-CO-CH2-NH-) , amida (-NH-CO-, -CO-NH-, -NCH3-CO- y -CO-NCH3-) , tioéter alifático (-S-) , disulfuro (-S-S-) o 1, 3, 5-triazin-2, 4-diamina 6-sustituida;
Z se selecciona del grupo que consiste en carboxialquilamina {-N[ (CH2) nCOOH]- o -N[ (CH2) nCOO-]-, en el que n = 1, 2, 3, 4, 5 ó 6}, éter (-O-) , tioéter (-S-) , carbonilo (-CO-) y metilo no sustituido o sustituido (-CR2-) , en el que el grupo R2 se selecciona del grupo que consiste en H, metilo, etilo y carboxilalquilo [- (CH2) mCOOH o - (CH2) mCOO-, en el que m= 1, 2, 3, 4, 5 ó 6]; y
el ion lantánido se selecciona del grupo que consiste en europio (III) , terbio (III) , disprosio (III) y samario (III) .
5. Molécula detectable según la reivindicación 4, caracterizada porque el agente reaccionante de unión bioespecífica se selecciona del grupo que consiste en un anticuerpo, un antígeno, un ligando de receptor, una proteína de unión específica, una sonda de ADN y una sonda de ARN.
6. Molécula detectable según la reivindicación 4, caracterizada porque el quelato luminiscente de lantánido unido a un agente reaccionante de unión bioespecífica es {2, 2’, 2”, 2”’-{[ (carboximetil) imino]bis (metilen) -bis{[4-[ (4isotiocianato) fenil]etinil]piridin-6, 2-diil}bis (metilenonitrilo) }tetraquis (acetato) }europio (III) .
7. Procedimiento para llevar a cabo un ensayo de unión bioespecífica que usa una molécula detectable para un analito que se va a determinar, caracterizado porque dicha molécula detectable que comprende un agente reaccionante de unión bioespecífica unido a un quelato luminiscente de lantánido comprende un ion lantánido y un ligando quelante de fórmula (I)
en la que
R1 se selecciona del grupo que consiste en H, -COOH, -COO-, -CH2COOH y -CH2COO-;
G1 es un grupo que consiste en uno o dos restos, seleccionándose cada resto del grupo que consiste en etinodiílo (-C:C-) , etenileno (-CH=CH-) , fenileno, bifenileno, naftileno, piridileno, pirazinileno, pirimidinileno, piridazinileno, furileno, tienileno, pirrolileno, imidazolileno, pirazolileno, tiazolileno, isotiazolileno, oxazolileno, isoxazolileno, furazanileno, 1, 2, 4-triazol-3, 5-ileno y oxadiazolileno;
G2 es un grupo para el acoplamiento a un agente reaccionante de unión bioespecífica que se selecciona del grupo que consiste en tiourea (-NH-CS-NH-) , aminoacetamida (-NH-CO-CH2-NH-) , amida (-NH-CO-, -CO-NH-, -NCH3-CO- y -CO-NCH3-) , tioéter alifático (-S-) , disulfuro (-S-S-) o 1, 3, 5-triazin-2, 4-diamina 6-sustituida;
Z se selecciona del grupo que consiste en carboxialquilamina {-N[ (CH2) nCOOH]- o -N[ (CH2) nCOO-]-, en el que n = 1, 2, 3, 4, 5 ó 6}, éter (-O-) , tioéter (-S-) , carbonilo (-CO-) y metilo no sustituido o sustituido (-CR2-) , en el que el grupo R2 se selecciona del grupo que consiste en H, metilo, etilo y carboxilalquilo [- (CH2) mCOOH o - (CH2) mCOO-, en el que m= 1, 2, 3, 4, 5 ó 6]; y
45 el ion lantánido se selecciona del grupo que consiste en europio (III) , terbio (III) , disprosio (III) y samario (III) .
8. Procedimiento según la reivindicación 7, caracterizado porque el agente reaccionante de unión bioespecífica se selecciona del grupo que consiste en un anticuerpo, un antígeno, un ligando de receptor, una proteína de unión específica, una sonda de ADN o de ARN.
9. Procedimiento según la reivindicación 7, caracterizado porque el quelato luminiscente de lantánido unido a un agente reaccionante de unión bioespecífica es {2, 2’, 2”, 2”’-{[ (carboximetil) imino]bis (metilen) -bis{[4-
Patentes similares o relacionadas:
Compuestos heterocíclicos que activan AMPK y métodos de uso de los mismos, del 29 de Julio de 2020, de RIGEL PHARMACEUTICALS, INC.: Un compuesto que es N-((cis)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; N-((3S,4S)-1-(4-cianobencil)-3-fluoropiperidin-4-il)-6-(4-(4-metoxibenzoil)piperidin-1-carbonil)nicotinamida; […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Ureas cíclicas como inhibidores de ROCK, del 22 de Julio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de acuerdo con la Fórmula (I): **(Ver fórmula)** o un enantiómero, un diastereómero, un estereoisómero, un tautómero, una sal farmacéuticamente aceptable […]
Ureas asimétricas p-sustituidas y usos médicos de las mismas, del 22 de Julio de 2020, de Helsinn Healthcare SA: Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: una línea discontinua indica un enlace opcional; X es CH; […]
Formas en estado sólido de sales de Nilotinib, del 15 de Julio de 2020, de PLIVA HRVATSKA D.O.O: Una forma cristalina de fumarato de Nilotinib designada como Forma III, caracterizada por datos seleccionados de uno o más de los siguientes: a. un patrón de […]
Inhibidores de Bcl-2/Bcl-xL y su uso en el tratamiento de cáncer, del 15 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF MICHIGAN: Compuesto que tiene una estructura **(Ver fórmula)**
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]