USO DE UN COMPUESTO RECEPTOR DE CB1 EN CIERTAS PAUTAS DE DOSIFICACIÓN.
Procedimiento de tratamiento que usa un compuesto receptor de CB1 en ciertas pautas de dosificación.
La presente invención se refiere a un procedimiento de tratamiento que usa piperidin-1-ilamida del ácido 5-(4-cloro-fenil)-1-{2,4-dicloro-fenil)-4,5-dihidro-1H-pirazol-3-carboxílico como racemato o enantiómero (R) y (S) o sus mezclas en ciertas pautas de dosificación
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200802666.
Solicitante: LABORATORIOS DEL DR. ESTEVE, S.A..
Nacionalidad solicitante: España.
Provincia: BARCELONA.
Inventor/es: BUSCHMANN,HELMUT H., FISAS ESCASANY,MARIA ANGELES, VELA HERNANDEZ,JOSE,MIGUEL.
Fecha de Solicitud: 19 de Septiembre de 2008.
Fecha de Publicación: .
Fecha de Concesión: 1 de Septiembre de 2011.
Clasificación Internacional de Patentes:
- A61K31/454 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › conteniendo un ciclo de cinco eslabones con el nitrógeno como heteroátomo del ciclo, p. ej. pimozida, domperidona.
Clasificación PCT:
- A61K31/415 A61K 31/00 […] › 1,2-Diazoles.
- A61P3/04 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › Anorexiantes; Medicamentos para el tratamiento de la obesidad.
- A61P3/10 A61P 3/00 […] › para la hiperglucemia, p.ej. antidiabéticos.
- C07D231/06 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 231/00 Compuestos heterocíclicos que contienen ciclos de diazol-1,2 o diazol-1,2 hidrogenado. › que tienen un enlace doble entre miembros cíclicos o entre miembros cíclicos y no cíclicos.
Fragmento de la descripción:
Uso de un compuesto receptor de CB1 en ciertas pautas de dosificación.
La presente invención se refiere al uso de la piperidin-1-ilamida del ácido 5-(4-cloro-fenil)-1-(2,4-dicloro-fenil)-4,5-dihidro-1H-pirazol-3-carboxílico como racemato o enantiómero (R) y (S) o sus mezclas en ciertas pautas de dosificación.
Los cannabinoides son compuestos que se obtienen de la planta cannabis sativa que es conocida comúnmente como marihuana. El compuesto químico más activo de los cannabinoides de origen natural es tetrahidrocannabinol (THC), en particular
Estos cannabinoides de origen natural, así como sus análogos sintéticos promueven sus efectos fisiológicos a través de la unión a receptores específicos acoplados a G, los denominados receptores cannabinoides.
En la actualidad, se han identificado y clonado dos tipos característicos de receptores que se unen tanto a los cannabinoides naturales como sintéticos. Estos receptores, que se designan CB1 y CB2 están implicados en una diversidad de procesos fisiológicos y patofisiológicos en seres humanos y animales, por ejemplo, procesos relacionados con el sistema nervioso central, sistema inmunitario, sistema cardiovascular, sistema endocrino, sistema respiratorio, el tracto gastrointestinal o la reproducción, como se describe, por ejemplo, en Hollister, Pharm. Rev. 38, 1986, 1-20; Reny and Singha, Prog. Drug. Res., 36, 71-114, 1991; Consroe and Sandyk, en Marijuana/Cannabinoids, Neurobiology and Neurophysiology, 459, Murphy L. and Barthe A. Eds., CRC Press, 1992.
Por tanto, los compuestos que tienen una alta afinidad de unión por estos receptores cannabinoides y que son adecuados para modular estos receptores son útiles en la prevención y/o tratamiento de trastornos relacionados con los receptores cannabinoides.
En particular, el receptor CB1 está implicado en muchos trastornos diferentes relacionados con la ingesta de alimento tales como la bulimia o la obesidad, incluyendo obesidad asociada con diabetes tipo II (diabetes no dependiente de la insulina) y así, se pueden usar compuestos adecuados para regular este receptor en la profilaxis y/o tratamiento de estos trastornos.
También la dislipidemia, el síndrome metabólico (tanto en sus aspectos dependientes del peso o independientes del peso) y la diabetes tipo II han aumentado en importancia para la salud pública, en especial para los países desarrollados o en desarrollo, probablemente debido a un incremento estadísticamente notable en la proporción de miembros obesos o con sobrepeso en la población o en edad media.
Los compuestos de acuerdo con la fórmula (I), (Ia) o (Ib) (también conocidos como piperidin-1-ilamida del ácido 5-(4-cloro-fenil)-1-(2,4-dicloro-fenil)-4,5-dihidro-1H-pirazol-3-carboxílico como racemato y sus enantiómeros (S) y (R)) se describen conjuntamente con medios para su síntesis y su actividad biológica en las solicitudes WO 2005/077911 A1 (racemato), WO 2007/09686 A2 (enantiómero (S)) y WO 2007/09695 A1 (enantiómero (R)) respectivamente; incluyéndose el contenido de estas publicaciones en la presente memoria como referencia. Se demostró que estos compuestos eran ligandos de CB1 y/o compuestos con actividad antiobesidad y/o compuestos que tienen un efecto reductor sobre los niveles de triglicéridos en sangre en modelos in vivo. Así, estos compuestos de acuerdo con las fórmulas (I), (Ia) y (Ib) mostraron efectos claros que dieron a entender especialmente un gran potencial para el tratamiento o prevención de obesidad, dislipidemia, síndrome metabólico (tanto en sus aspectos dependientes del peso como independientes del peso) y/o diabetes tipo II.
No obstante, como un principio general incluso con estos compuestos seguros y eficaces, todavía es deseable reducir la cantidad de principio activo, el compuesto farmacéuticamente activo, usada con el fin de evitar los posibles efectos secundarios o sencillamente reducir la cantidad de principio activo que se consume, por ejemplo, por razones de ahorro de costes. Esto está además condicionado por el hecho de que el tratamiento de, por ejemplo, la obesidad o la reducción de la ingesta de alimentos con frecuencia se prolongan durante largos períodos de tiempo, alcanzándose normalmente el efecto deseado de forma relativamente rápida, seguido por una fase prolongada de estabilización del efecto. Así, sería muy deseable un tratamiento que uniera efectos más suaves al comienzo, pero que finalmente alcanzase el mismo efecto, mientras que al mismo tiempo usa menos cantidad de compuesto/principio activo.
Así, un objetivo de la presente invención fue proporcionar un medio para reducir la cantidad de principio activo a usar.
Dicho objetivo se consiguió mediante el uso de una cantidad farmacéuticamente eficaz de un principio activo seleccionado de al menos un compuesto de fórmula (I), (Ia) o (Ib) o mezclas de los mismos
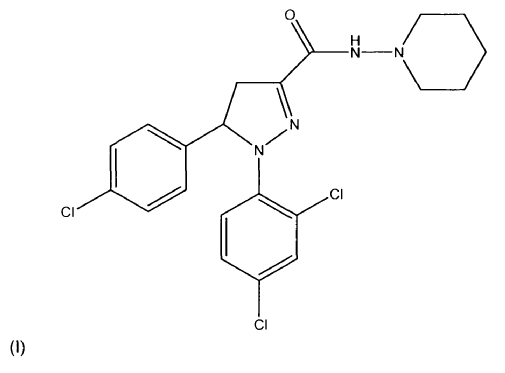
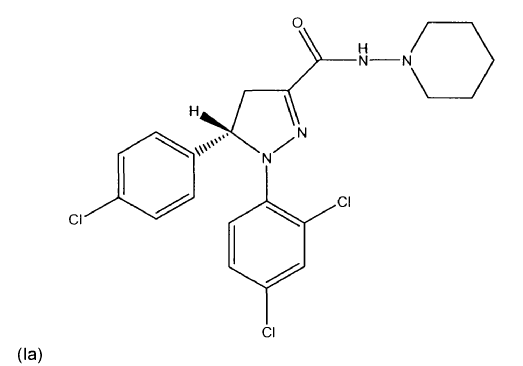
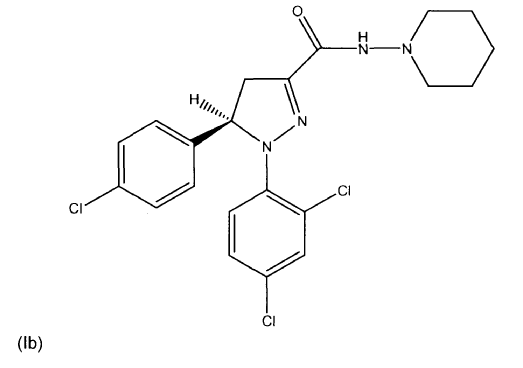
, opcionalmente en forma de uno o más de los polimorfos apropiados, en forma amorfa y/o de sus sales correspondientes y/o sus solvatos correspondientes,
para el tratamiento de obesidad, trastornos del apetito, dislipidemia, aumento de peso inducido por fármacos, síndrome metabólico o diabetes tipo II o para reducir la ingesta de alimentos y/o el peso corporal en un mamífero que lo necesite como una forma monodosis según un programa continuo que tiene un intervalo de dosificación de 6 veces a 1 vez por semana.
Con preferencia, este uso es para el tratamiento de obesidad; o preferiblemente es para el tratamiento de síndrome metabólico (dependiente o independiente del peso) o dislipidemia; o preferiblemente es para el tratamiento de diabetes tipo II; o preferiblemente es para reducir el peso corporal en un mamífero.
Se ha descubierto de forma sorprendente que una única dosis comparativamente baja de los compuestos de fórmula (I), (Ia) o (Ib) administrada con menos frecuencia que la forma de dosificación administrada una o dos veces al día usual, produce un efecto a largo plazo sobre el peso corporal. Así, una forma de dosificación del compuesto según la fórmula (I) administrada solo una vez cada dos días todavía produjo una reducción significativa del peso corporal en ratones al compararla con los animales tratados con vehículo después. Así, podría suponerse que siguiendo estas pautas de dosificación podría evitarse, reducirse o minimizarse cualquier efecto secundario esperado - en especial con el tratamiento de larga duración mientras que todavía se consigue y mantiene el efecto deseado finalmente.
"Forma monodosis" en el sentido de esta solicitud se define como cualquier formulación farmacéutica que comprende una cierta cantidad -opcionalmente variable pero preferiblemente constante- de principio(s) activo(s).
"Programa continuo" en el sentido de esta solicitud se define como una pauta terapéutica que describe un programa en curso de ciertos puntos de tiempo -medidos desde el primer tratamiento- en los que se debe aplicar una forma monodosis a un mamífero que lo necesita.
"Intervalo de dosificación" en el sentido de esta solicitud se define como el intervalo de tiempo entre dos aplicaciones diferentes de la forma monodosis.
El principio activo de acuerdo con la invención se puede someter a cualquier reducción del tamaño de partículas como molienda, molturación, reducción nanométrica o micronizaciones, o a complejación como, por ejemplo, complejación con ciclodextrinas o PEG.
Otro aspecto paralelo de la invención es el uso de una cantidad farmacéuticamente eficaz de un principio activo seleccionado de al menos un compuesto de fórmula (I), (Ia) o (Ib) o mezclas de los mismos
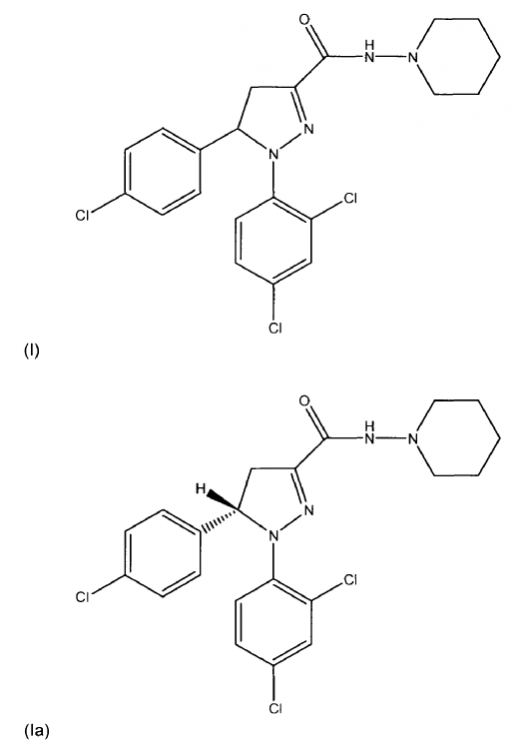
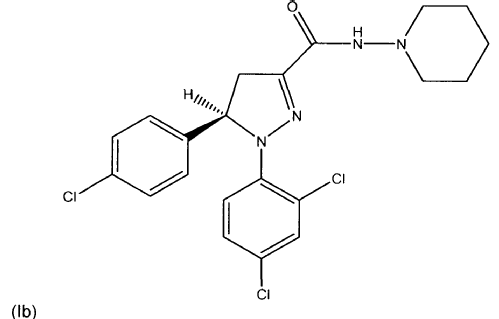
, opcionalmente en forma de uno o más de los polimorfos apropiados, en forma amorfa y/o de sus sales correspondientes y/o sus solvatos correspondientes,
en...
Reivindicaciones:
1. Uso de una cantidad farmacéuticamente eficaz de un principio activo seleccionado de al menos un compuesto de fórmula (I), (Ia) o (Ib) o mezclas de los mismos
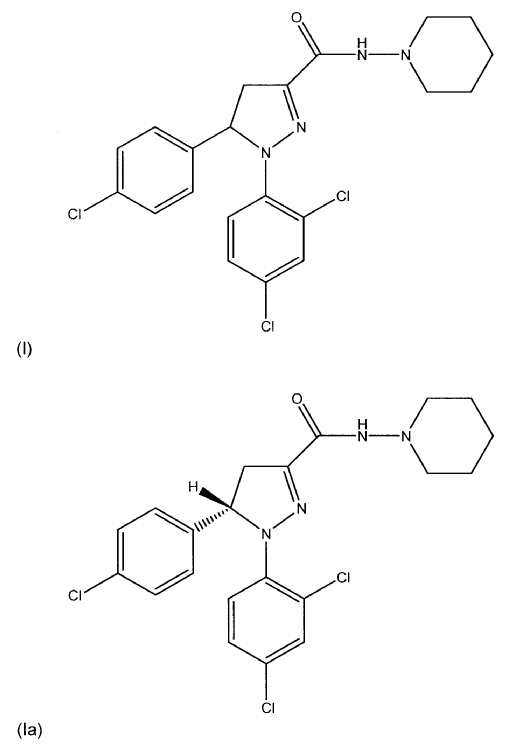
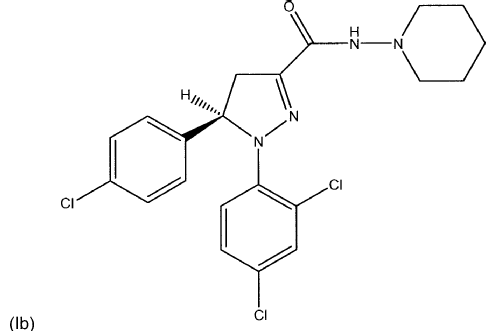
, opcionalmente en forma de uno o más de los polimorfos apropiados, en forma amorfa y/o de sus sales correspondientes y/o sus solvatos correspondientes,
en la fabricación de un medicamento para el tratamiento de obesidad, trastornos del apetito, dislipidemia, aumento de peso inducido por fármacos, síndrome metabólico o diabetes tipo II o para reducir la ingesta de alimentos y/o el peso corporal en un mamífero, en el que dicho medicamento se adapta para administración como una forma monodosis según un programa continuo que tiene un intervalo de dosificación de 6 veces a 1 vez por semana.
2. Uso según la reivindicación 1, caracterizado porque el intervalo de dosificación se selecciona del grupo constituido por dosificación una vez cada dos días, dosificación tres veces a la semana, dosificación una vez cada tres días, dosificación dos veces a la semana, dosificación una vez cada cuatro días, dosificación una vez cada cinco días, dosificación una vez cada seis días o dosificación una vez a la semana; con preferencia dosificación una vez cada dos días, dosificación tres veces a la semana, dosificación una vez cada tres días, dosificación dos veces a la semana o dosificación una vez cada cuatro días.
3. Uso de una cantidad farmacéuticamente eficaz de un principio activo seleccionado de al menos un compuesto de fórmula (I), (Ia) o (Ib) o mezclas de los mismos
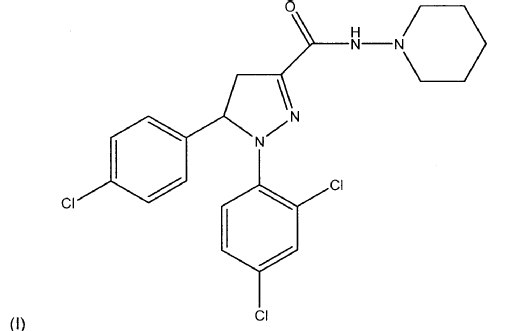
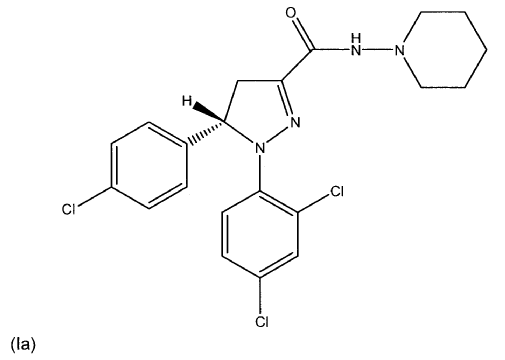
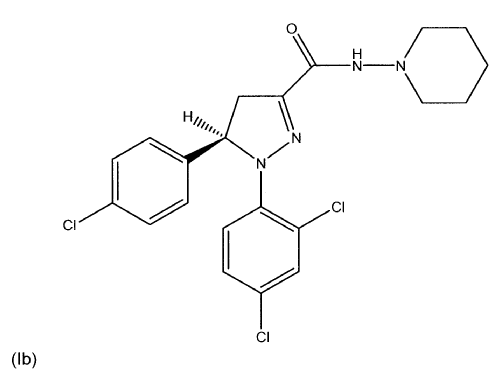
, opcionalmente en forma de uno o más de los polimorfos apropiados, en forma amorfa y/o de sus sales correspondientes y/o sus solvatos correspondientes,
en la fabricación de un medicamento para el tratamiento de obesidad, trastornos del apetito, dislipidemia, aumento de peso inducido por fármacos, síndrome metabólico o diabetes tipo II o para reducir la ingesta de alimentos y/o el peso corporal en un mamífero como una forma monodosis según un programa continuo que tiene una periodicidad de aproximadamente 6 veces cada semana a aproximadamente 1 vez por semana.
4. Uso según la reivindicación 2, caracterizado porque dicho programa continuo tiene una periodicidad de una vez cada 2, 3 ó 4 días o una vez cada 5, 6 ó 7 días, preferiblemente una vez cada 2, 3 ó 4 días.
5. Uso según cualquiera de las reivindicaciones 1 a 4, caracterizado porque la forma monodosis comprende el principio activo seleccionado de al menos uno de
• Piperidin-1-ilamida del ácido (rac)-5-(4-cloro-fenil)-1-(2,4-dicloro-fenil)-4,5-dihidro-1H-pirazol-3-carboxílico;
• Piperidin-1-ilamida del ácido (R)-5-(4-cloro-fenil)-1-(2,4-dicloro-fenil)-4,5-dihidro-1H-pirazol-3-carboxílico; o
• Piperidin-1-ilamida del ácido (S)-5-(4-cloro-fenil)-1-(2,4-dicloro-fenil)-4,5-dihidro-1H-pirazol-3-carboxílico,
• o mezclas de los mismos;
en una cantidad de 1 a 250 mg, preferiblemente 10 a 200 mg, más preferiblemente 15 a 150 mg.
6. Uso según cualquiera de las reivindicaciones 1 a 5, caracterizado porque la forma monodosis es adecuada para administrar 0,02 a 5 mg/kg, preferiblemente 0,2 a 4 mg/kg, o más preferiblemente 0,3 a 3 mg/kg, lo más preferiblemente 0,25 a 2,5 mg/kg del principio activo a dicho mamífero que lo necesita.
7. Uso según cualquiera de las reivindicaciones 1 a 6, caracterizado porque dicho mamífero es un animal de compañía tal como un gato o perro, o es un ser humano; preferiblemente porque dicho mamífero es un ser humano.
8. Uso según cualquiera de las reivindicaciones 1 a 7, caracterizado porque la monodosis está en forma de una composición farmacéutica seleccionada de
• una composición farmacéutica para aplicación oral,
• una composición farmacéutica para aplicación nasal,
• una composición farmacéutica para aplicación bucal,
• una composición farmacéutica para aplicación rectal, o
• una composición farmacéutica para aplicación vaginal, * o
• una composición farmacéutica para aplicación transdérmica,
• una composición farmacéutica para aplicación sistémica,
preferiblemente se selecciona de
• una composición farmacéutica para aplicación oral.
9. Uso según la reivindicación 8, caracterizado porque la composición farmacéutica se selecciona de
• un comprimido,
• una cápsula,
• un sobrecito,
• un polvo,
• un comprimido oblongo,
• un gel,
• una película,
• una miniesfera,
• un gránulo,
• un implante,
• un multiparticulado con gránulos comprimidos en un comprimido,
• un multiparticulado con gránulos introducidos en una cápsula,
• un multiparticulado con miniesferas comprimidas en un comprimido,
• un multiparticulado con miniesferas introducidas en una cápsula, o
• un supositorio, o
• una solución/dispersión inyectable
• un sistema transdérmico como un parche;
preferiblemente se selecciona de
• un comprimido,
• una cápsula,
• una miniesfera,
• un gránulo,
• un multiparticulado con gránulos comprimidos en un comprimido,
• un multiparticulado con gránulos introducidos en una cápsula,
• un multiparticulado con miniesferas comprimidas en un comprimido, o
• un multiparticulado con miniesferas introducidas en una cápsula,
10. Uso según cualquiera de las reivindicaciones 1 a 9, caracterizado porque el principio activo se selecciona de
a) Piperidin-1-ilamida del ácido (rac)-5-(4-cloro-fenil)-1-(2,4-dicloro-fenil)-4,5-dihidro-1H-pirazol-3-carboxílico;
preferiblemente en
• forma del polimorfo α;
• forma del polimorfo β;
• forma amorfa;
• forma de un solvato, preferiblemente un hidrato, más preferiblemente un monohidrato;
• la base libre; o
• una sal con un ácido con un pka
b) Piperidin-1-ilamida del ácido (R)-5-(4-cloro-fenil)-1-(2,4-dicloro-fenil)-4,5-dihidro-1H-pirazol-3-carboxílico,
preferiblemente en
• forma del polimorfo α;
• forma del polimorfo β;
• forma amorfa;
• forma de un solvato, preferiblemente un hidrato,
• la base libre;
• una sal con un ácido con un pka
c) Piperidin-1-ilamida del ácido (S)-5-(4-cloro-fenil)-1-(2,4-dicloro-fenil)-4,5-dihidro-1H-pirazol-3-carboxílico,
preferiblemente en
• forma de un polimorfo;
• forma amorfa;
• forma de un solvato, preferiblemente un hidrato,
• la base libre;
• una sal con un ácido con un pka
o
d) unas mezclas no racémicas de (b) y (c).
Patentes similares o relacionadas:
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]
Antagonistas del receptor p2x7 derivados de N-[2-(4-fenoxipiperidin-1-il)-2-(1,3-tiazol-5-il)etil]benzamida y N-[2-(4-benciloxipiperidin-1-il)-2-(1,3-tiazol-5-il)etil]benzamida sustituidas, del 15 de Julio de 2020, de AXXAM S.P.A: Un compuesto de la siguiente fórmula (I) o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** incluyendo cualquier forma estereoquímicamente […]
Forma sólida aislada de monohidrocloruro de anamorelina con baja proporción molar de cloruro:anamorelina, del 1 de Julio de 2020, de Helsinn Healthcare SA: Una forma sólida aislada de monohidrocloruro de anamorelina (también denominado 'monoclorhidrato de anamorelina'), de manera que el mencionado monohidrocloruro […]
Derivado de amina cíclica y uso farmacéutico del mismo, del 1 de Julio de 2020, de TORAY INDUSTRIES, INC.: Un derivado de amina cíclica representado por la siguiente fórmula general (I): **(Ver fórmula)** donde R1 representa un grupo alquiloxi que tiene de 1 a 3 átomos […]
Compuestos como antagonistas de CRTH2 y usos de los mismos, del 10 de Junio de 2020, de Sunshine Lake Pharma Co., Ltd (100.0%): Compuesto que tiene la fórmula (I) o estereoisómero, isómero geométrico, tautómero, N-óxido, hidrato, solvato o sal farmacéuticamente aceptable […]
Nuevos derivados de piperazina y piperidina, síntesis y uso de los mismos en la inhibición de la oligomerización de VDAC, la apoptosis y la disfunción mitocondrial, del 3 de Junio de 2020, de The National Institute for Biotechnology in the Negev Ltd: Compuesto de Fórmula general (Id): **(Ver fórmula)** en la que L2 es un grupo de enlace seleccionado del grupo que consiste en un alquilamidileno […]
Agonista de receptores de 5-HT4 para gastroparesia, del 3 de Junio de 2020, de RAQUALIA PHARMA INC: Una composición farmacéutica para su uso en el tratamiento de la gastroparesia que comprende una cantidad terapéuticamente eficaz de ácido 4-{[4-({[4-(2,2,2-trifluoroetoxi)-1,2-bencisoxazol-3-il]oxi}metil)piperidin-1-il]metil}tetrahidro-2H-piran-4-carboxílico […]
Derivados de 4-carboxamido-isoindolinona como inhibidores selectivos de PARP-1, del 27 de Mayo de 2020, de NERVIANO MEDICAL SCIENCES S.R.L.: Un compuesto de fórmula (I): **(Ver fórmula)** en el que: R es hidrógeno o flúor; y n, m, R1 y R2 tienen los significados siguientes: a) n es 0 y m es 0, 1, […]