PREPARACIONES PARA EL DIAGNÓSTICO DE LAS INFECCIONES CON HELICOBACTER PYLORI.
Preparación revestida para su utilización en la detección de infección por Helicobacter pylori,
que comprende: (i)una composición de núcleo, que comprende: 19 a 89 partes en peso de urea marcada con un isótopo del carbono, con relación a 100 partes en peso de la composición de núcleo, 10 a 80 partes en peso de un componente excipiente, con relación a 100 partes en peso de la composición de núcleo, y 0,01 a 1 partes en peso de un componente lubricante, con relación a 100 partes en peso de la composición de núcleo, comprendiendo el componente excipiente: (a)por lo menos un elemento seleccionado de entre el grupo constituido por lactosa, sacarosa y glucosa, (b)por lo menos un elemento seleccionado de entre el grupo constituido por celulosa cristalina, hidroxipropilcelulosa con baja sustitución, carboximetilcelulosa cálcica y croscarmelosa sódica, y (c)por lo menos un elemento seleccionado de entre el grupo constituido por almidón, carboximetilalmidón sódico, hidroxipropilalmidón, y almidón parcialmente pregelatinizado; y (ii)un agente de revestimiento, estando la composición de núcleo revestida con 0,1 a 5 partes en peso del agente de revestimiento, con relación a 100 partes en peso de la composición de núcleo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2001/004122.
Solicitante: OTSUKA PHARMACEUTICAL CO., LTD..
Nacionalidad solicitante: Japón.
Dirección: 9, KANDATSUKASA-CHO 2-CHOME CHIYODA-KU TOKYO 101-8535 JAPON.
Inventor/es: KAWASAKI, JUNICHI, OKAMURA, AKIO, NODA,ATSUNARI, TSUCHIYA,KYOKO, NISHIWAKI,SATOSHI, UNO,SHINICHIRO.
Fecha de Publicación: .
Fecha Solicitud PCT: 17 de Mayo de 2001.
Fecha Concesión Europea: 6 de Octubre de 2010.
Clasificación Internacional de Patentes:
- G01N33/569D4
Clasificación PCT:
- A61K47/02 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Compuestos inorgánicos.
- A61K51/04 A61K […] › A61K 51/00 Preparaciones que contienen sustancias radioactivas utilizadas para la terapia o para el examen in vivo. › Compuestos orgánicos.
- A61K9/28 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Grageas; Píldoras o comprimidos con revestimientos.
- A61K9/30 A61K 9/00 […] › Revestimientos orgánicos.
Clasificación antigua:
- A61K47/02 A61K 47/00 […] › Compuestos inorgánicos.
- A61K47/10 A61K 47/00 […] › Alcoholes; Fenoles; Sus sales, p. ej. glicerol; Polietilenglicoles [PEG]; Poloxámeros; Éteres alquílicos PEG/POE.
- A61K47/14 A61K 47/00 […] › Esteres de ácidos carboxílicos, p. ej. monoglicéridos de ácidos grasos, triglicéridos de cadenas medianas, parabenos o ésteres de ácidos grasos y de polietilenglicol (PEG).
- A61K47/26 A61K 47/00 […] › Hidratos de carbono, p. ej. alcoholes de azúcares, amino azúcares, ácidos nucleicos, mono-, di- u oligo-sacáridos; Sus derivados, p. ej. polisorbatos, ésteres de ácidos grasos sorbitano o glicirricina.
- A61K47/32 A61K 47/00 […] › Compuestos macromoleculares obtenidos por reacciones en las que intervienen solamente enlaces insaturados carbono-carbono, p. ej. carbómeros (resinas de carbopol).
- A61K47/36 A61K 47/00 […] › Polisacáridos; Sus derivados, p. ej. gomas o resinas, almidón, alginato, dextrina, ácido hialurónico, quitosano, inulina, agar o pectina.
- A61K47/38 A61K 47/00 […] › Celulosa; Sus derivados.
- A61K51/04 A61K 51/00 […] › Compuestos orgánicos.
- A61K9/30 A61K 9/00 […] › Revestimientos orgánicos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
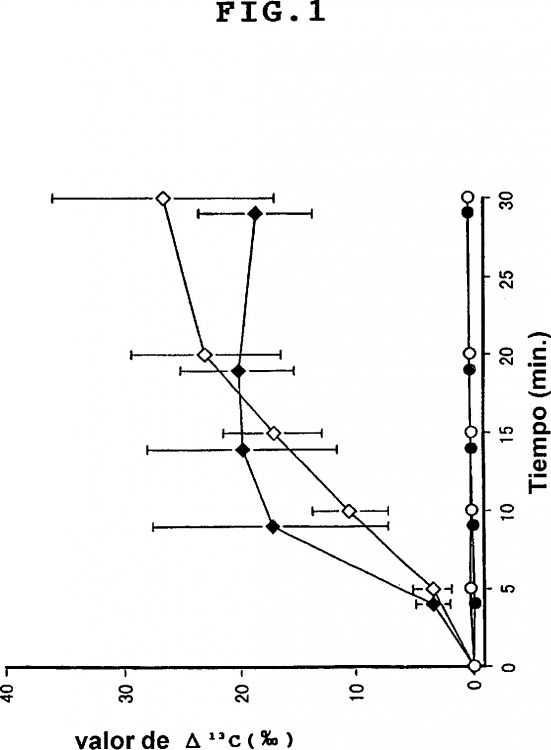
Fragmento de la descripción:
Preparaciones para el diagnóstico de las infecciones con Helicobacter pylori.
Campo de la invención
La presente invención se refiere a una preparación farmacéutica para utilización en el diagnóstico de una infección por Helicobacter pylori. Más particularmente, la invención se refiere a una forma de dosificación oral que encuentra aplicación en la prueba de la urea en la respiración, la cual es un método no invasivo de detección de Helicobacter pylori.
Descripción de la técnica relacionada
Desde el aislamiento y cultivo exitosos de Helicobacter pylori (en lo sucesivo denominada H. pylori) por Marshall et al. (Lancet, p. 1273-1275 (1983)), se han avanzado tanto perspectivas afirmativas como negativas sobre su papel etiológico. Recientemente, sin embargo, la infección por H. pylori ha reunido una gran cantidad de atención como causa principal o como cofactor en el comienzo de la gastritis, úlcera péptica y cáncer de estómago, que son la triada de enfermedades del aparato digestivo superior principales no sólo en Japón sino también fuera de Japón. En particular, la recomendación hecha por la NIH Consensus Conference (Bethesda, 1994) de que "la úlcera péptica en la que se ha verificado una infección por H. pylori, tanto si es una lesión primaria como una recurrente, requiere terapia de erradicación que suplemente medicación contra la secreción del ácido gástrico con antibacterianos" provocó bastante sensación en Japón, urgiendo a aquellos implicados a establecer un método exacto y rápido para el diagnóstico de la infección por H. pylori y la verificación de la erradicación de H. pylori.
La tecnología para detectar H. pylori en la mucosa gástrica se puede dividir en dos categorías principales, a saber, la invasiva que requiere una endoscopia (biopsia) (un método bacteriológico que implica el cultivo de aislados, un método histológico o inmunohistológico de detección, la prueba de ureasa, etc.), y el no invasivo. De ellos, se prefiere el no invasivo desde los puntos de vista de las cargas mentales y físicas sobre el paciente, idoneidad y seguridad.
Los dos métodos no invasivos representativos actualmente disponibles son un método serológico para el diagnóstico, que comprende determinar el nivel sérico de anticuerpos anti-H. pylori específicos, y la prueba de la urea en la respiración, que comprende administrar oralmente una urea marcada con un isótopo del carbono y determinar el dióxido de carbono marcado exhalado en el aire de la respiración (por ejemplo Sand, J., Gastroenterol, 1996, 31 (supl.) 214, p. 44-46; Gastraenteralogy, 1997, 113, s93-98; Gut, 1994, 35, p. 723-725; Aliment. Pharmacol. Ther. 1997, 11, p. 641-649; Gastraenteralogy, 1995, 109, p. 136-141).
Entre los métodos anteriores, el método serológico de diagnóstico, que se basa en la presencia de anticuerpos específicos, tiene el inconveniente de que, puesto que el estado positivo a anticuerpos del suero del hospedante persiste durante por lo menos 3 meses incluso después de la erradicación de H. pylori, aproximadamente 10-15% de los sujetos sometidos a ensayo dan respuestas de falso positivo y, como tal, no es adecuado para la confirmación de la eliminación bacteriana. Por lo tanto, recientemente se ha empleado ampliamente la prueba de la urea en la respiración, que no depende de la presencia de anticuerpos y es segura y no consume tiempo. Esta prueba se basa en la propiedad de H. pylori de producir una gran cantidad de la enzima ureasa. La ureasa normalmente no se produce en el cuerpo humano, y, por lo tanto, su detección indica que H. pylori, un productor de ureasa, existe en el estómago. De este modo, este método explota el fenómeno de que cuando la H. pylori productora de ureasa existe en el estómago del hospedante, la urea marcada ingerida por el hospedante se descompone y reacciona posteriormente con ácido gástrico de forma que la urea marcada se convierte en el dióxido de carbono marcado, el cual se exhala en el aire de la respiración (Lancet, p. 174-177 (1987)). Una ventaja adicional de esta prueba es que se puede evaluar la existencia de ureasa en una amplia región del estómago.
Sin embargo, el procedimiento convencional para esta prueba de la urea en la respiración implica la ingesta de una urea marcada isotópicamente en forma de una disolución acuosa, y, por lo tanto, diversas bacterias productoras de ureasa, residentes en la boca y la garganta, descomponen la urea ingerida en una etapa temprana tras la administración, presentando así un riesgo de dar una prueba de falso positivo en el diagnóstico de la infección por H. pylori. Para prevenir esta respuesta de falso positivo, es necesario que el sujeto del ensayo haga gárgaras en su garganta con agua inmediatamente después de la ingestión de una disolución acuosa de la urea marcada, para lavar la urea marcada que queda en la cavidad oral o para desinfectar la boca y la garganta antes de tiempo.
Sin embargo, tales tratamientos son gravosos no sólo para los sujetos del ensayo que sufren la prueba, sino también para el médico. Además, a fin de obtener un resultado preciso, el ruido de la detección debido a la descomposición de la urea por la flora bacteriana residente en y alrededor de la cavidad oral se debe de eliminar retrasando el tiempo de recogida de aire exhalado, con la desventaja consiguiente de una prolongación del procedimiento de ensayo.
Sumario de la invención
El objetivo de la presente invención consiste en proporcionar una formulación oral mejorada para una prueba de la urea en la respiración. Más particularmente, el objetivo de la invención consiste en proporcionar una preparación farmacéutica con la que se puede detectar y diagnosticar adecuadamente y de forma no invasiva una infección por H. pylori de la mucosa gástrica mediante la prueba de la urea en la respiración, y que está libre del riesgo de una prueba de falso positivo debido a la eliminación completa de la influencia de bacterias productoras de ureasa que habitan en la cavidad oral, la garganta y otros tejidos excepto en tubo digestivo.
Un objetivo adicional de la presente invención consiste en proporcionar una preparación farmacéutica con la que se puede detectar rápidamente sin demora de tiempo la presencia de H. pylori.
Para superar los inconvenientes anteriores de la prueba convencional de la urea en la respiración, se estudió exhaustivamente el desarrollo de una formulación farmacéutica que mostraría un comportamiento in vivo de manera que permanezca sin disolver en la cavidad oral, pero que, al entrar en el estómago, se disuelva rápidamente para permitir que la urea marcada se disperse rápidamente por todo el estómago. Como resultado, se descubrió que una formulación farmacéutica que muestra tal comportamiento in vivo favorable se puede proporcionar usando la sustancia activa, urea marcada, en combinación con un componente excipiente y un componente lubricante para preparar una composición de núcleo, y cubriendo esta composición de núcleo con un agente de revestimiento. De este modo, se confirmó que, cuando la preparación farmacéutica anterior se administra oralmente a un sujeto de ensayo, la sustancia activa alcanza el estómago sin ser afectada por las bacterias productoras de ureasa residentes en la cavidad oral, y se disuelve y dispersa rápidamente en el estómago sustancialmente sin estar sometida al retardo de la disolución por el revestimiento, y que, por lo tanto, esta preparación farmacéutica es un reactivo muy útil para el diagnóstico rápido y exacto de la infección por H. pylori. La presente invención se ha completado en base al hallazgo anterior.
La presente invención, por lo tanto, se refiere a las preparaciones farmacéuticas definidas en los siguientes párrafos (1)-(14) para la detección de infección por H. pylori según un protocolo de prueba de la urea en la respira- ción:
Reivindicaciones:
1. Preparación revestida para su utilización en la detección de infección por Helicobacter pylori, que comprende:
2. Preparación revestida según la reivindicación 1, en la que la proporción del agente de revestimiento es 0,3-5 partes en peso, sobre la base de 100 partes en peso de la composición de núcleo.
3. Preparación revestida según la reivindicación 1, en la que la proporción del agente de revestimiento es 0,5-3 partes en peso, sobre la base de 100 partes en peso de la composición de núcleo.
4. Preparación revestida según la reivindicación 1, que contiene 25-75% en peso de la urea marcada con un isótopo del carbono, 20-70% en peso del componente excipiente, y 0,05-0,8% en peso del componente lubricante, sobre la base de 100% en peso de la composición de núcleo.
5. Preparación revestida según la reivindicación 1, que contiene 30-70% en peso de la urea marcada con un isótopo del carbono, 35-65% en peso del componente excipiente, y 0,1-0,7% en peso del componente lubricante, sobre la base de 100% en peso de la composición de núcleo.
6. Composición revestida según la reivindicación 1, en la que la composición de núcleo contiene 10-450 partes en peso del componente excipiente y 0,01-6 partes en peso del componente lubricante, sobre la base de 100 partes en peso de la urea marcada con un isótopo del carbono.
7. Preparación revestida según la reivindicación 1, en la que la composición de núcleo contiene 50-150 partes en peso del componente excipiente y 0,1-5 partes en peso del componente lubricante, sobre la base de 100 partes en peso de la urea marcada con un isótopo del carbono.
8. Preparación revestida según la reivindicación 1, en la que el agente de revestimiento comprende un polímero soluble en agua y un plastificante.
9. Preparación revestida según la reivindicación 8, en la que el polímero soluble en agua es por lo menos un elemento seleccionado de entre el grupo constituido por pululano, dextrina, alginato de metal alcalino, hidroxipropilcelulosa, hidroxipropilmetilcelulosa, metilcelulosa y polivinilpirrolidona.
10. Preparación revestida según la reivindicación 8, en la que el plastificante es por lo menos un elemento seleccionado de entre el grupo constituido por alcohol polivinílico, polietilenglicol, citrato de trietilo, triacetina, glicerina concentrada, propilenglicol y polisorbato.
11. Preparación revestida según la reivindicación 1, en la que, como componente excipiente, la composición de núcleo contiene además por lo menos un elemento seleccionado de entre el grupo constituido por crospovidona, carboximetilalmidón cálcico, y polivinilpirrolidona.
12. Preparación revestida según la reivindicación 1, en la que, como componente lubricante, la composición de núcleo contiene por lo menos un elemento seleccionado de entre el grupo constituido por ácido esteárico, estearato de magnesio, estearato de calcio y aceite hidrogenado.
13. Preparación revestida según la reivindicación 1, en la que la composición de núcleo contiene lactosa, celulosa cristalina y almidón como componente excipiente y estearato de magnesio como componente lubricante, y el agente de revestimiento contiene hidroxipropilmetilcelulosa, polietilenglicol, óxido de titanio y talco.
14. Preparación revestida según la reivindicación 1, en la que la urea marcada con un isótopo del carbono es urea marcada con 13C.
15. Utilización de la preparación revestida según la reivindicación 1 para la preparación de un reactivo para la prueba de la urea en la respiración, para detectar una infección por Helicobacter pylori.
16. Utilización de la preparación revestida según la reivindicación 1 para la preparación de un reactivo para la prueba de la urea en la respiración para evaluar el efecto de la erradicación de Helicobacter pylori de una terapia de erradicación de Helicobacter pylori.
Patentes similares o relacionadas:
 CEBADORES, SONDAS, PROCEDIMIENTOS Y USOS DE LOS MISMOS PARA LA DETECCIÓN DE MYCOBACTERIIUM KANSASII, del 3 de Mayo de 2011, de WAKO PURE CHEMICAL INDUSTRIES, LTD: Un oligonucleótido específico de Mycobacterium kansasii para la detección de Mycobacterium kansasii que comprende una secuencia de nucleótidos […]
CEBADORES, SONDAS, PROCEDIMIENTOS Y USOS DE LOS MISMOS PARA LA DETECCIÓN DE MYCOBACTERIIUM KANSASII, del 3 de Mayo de 2011, de WAKO PURE CHEMICAL INDUSTRIES, LTD: Un oligonucleótido específico de Mycobacterium kansasii para la detección de Mycobacterium kansasii que comprende una secuencia de nucleótidos […]
MÉTODO DE DIAGNÓSTICO DE LAWSONIA INTRACELLULARIS, del 7 de Febrero de 2011, de BOEHRINGER INGELHEIM VETMEDICA GMBH: Método para el diagnóstico de infección por Lawsonia intracellularis preclínica o clínica, que comprende las siguientes etapas: a) detectar la unión específica de […]
CULTIVO DE LAWSONIA INTRACELLULARIS, VACUNAS ANTI-LAWSONIA INTRACELLULARIS Y AGENTES DE DIAGNOSTICO, del 9 de Febrero de 2010, de BOEHRINGER INGELHEIM VETMEDICA, INC.: Una vacuna para inducir una respuesta inmunitaria en bacterias L. intracellularis en un animal que comprende una cepa atenuada de L. intracellularis […]
Preparación externa líquida, del 29 de Julio de 2020, de HISAMITSU PHARMACEUTICAL CO. INC.: Una preparación tópica líquida, que comprende: agua; oxibutinina o una sal farmacéuticamente aceptable de la misma; y un éster de ácido dicarboxílico, […]
Preparaciones ácidas de insulina con estabilidad mejorada, del 15 de Julio de 2020, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Formulación farmacéutica que contiene insulina humana Gly(A21),Arg(B31),Arg(B32) y un tensioactivo, elegido de un grupo que contiene Tween 20® y Tween 80®; siendo […]
Composición a base de hidroxiapatita en polvo para el tratamiento del linfoma B o T, del 1 de Julio de 2020, de URODELIA: Composición para uso como autovacuna antitumoral para el tratamiento de linfomas B o T en un sujeto, que comprende un polvo de hidroxiapatita y/o de […]
Parche cutáneo adhesivo, del 3 de Junio de 2020, de HISAMITSU PHARMACEUTICAL CO. INC.: Un parche que comprende un respaldo y una capa adhesiva laminada sobre al menos una superficie del respaldo, donde la capa adhesiva contiene al menos uno […]
Sistema terapéutico transdérmico con fluencia de principio activo controlada, que contiene un óxido que reacciona de manera básica, del 20 de Mayo de 2020, de LTS LOHMANN THERAPIE-SYSTEME AG: Sistema terapéutico transdérmico, que comprende una capa trasera oclusiva, impermeable al principio activo, una matriz de una o múltiples capas […]