NUEVA QUITINASA DE ORIGEN BACTERIANO CON AMPLIO ESPECTRO FUNGICIDA.
Nueva quitinasa de origen bacteriano con amplio espectro fungicida.
La presente memoria describe una nueva secuencia de ADN que tiene una actividad promotora fuerte en bacterias y un método para expresar un gen que determina la síntesis de una quitinasa bacteriana de amplio espectro fungicida usando dicha secuencia. También describe un método para producir dicha quitinasa en bacterias usando la secuencia descrita, en particular, un método para producir el producto del gen deseado en gran cantidad en la célula bacteriana y obtenerlo secretado al exterior celular
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200802500.
Solicitante: CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC).
Nacionalidad solicitante: España.
Provincia: MADRID.
Inventor/es: PEREZ MELLADO,RAFAEL.
Fecha de Solicitud: 27 de Agosto de 2008.
Fecha de Publicación: .
Fecha de Concesión: 31 de Mayo de 2011.
Clasificación Internacional de Patentes:
- C12N9/24 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › actúan sobre compuestos glicosílicos (3.2).
Clasificación PCT:
- A01N63/02
- A61K38/47 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que actúan sobre compuestos glicosílicos (3.2), p. ej. celulosas, lactasas.
- A61P31/18 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › para el VIH.
- C12N15/75 C12N […] › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › para Bacillus.
- C12N9/24 C12N 9/00 […] › actúan sobre compuestos glicosílicos (3.2).
- C12P21/02 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › que tienen una secuencia conocida de varios aminoácidos, p. ej. glutation.
PDF original: ES-2343665_A1.pdf
Fragmento de la descripción:
Nueva quitinasa de origen bacteriano con amplio espectro fungicida.
Estado de la técnica
La quitina se encuentra ampliamente distribuida en la naturaleza, y de forma muy importante como polisacárido estructural en la pared celular de los hongos, llegando a alcanzar hasta un 16% del peso seco total en hongos filamentosos y basidiomicetos. Es un homopolímero insoluble en agua de carácter estructural formado por n repeticiones de N-acetil glucosamina unidas por enlaces β(1-4). También se encuentra en el exoesqueleto de artrópodos, cubierta de crustáceos, etc. Es uno de los polímeros más abundantes en la Naturaleza después de la celulosa.
La quitina es por tanto el compuesto más importante en el mantenimiento de la estructura de la pared fúngica, por lo que podría ser utilizado como blanco para la obtención de compuestos proteicos solubles de acción antifúngica.
La enzima conocida como quitinasa está presente en un amplio rango de organismos, particularmente microorganismos y frecuentemente de origen bacteriano, y su acción determina la hidrólisis del polímero de quitina impidiendo la viabilidad del hongo.
Entre los organismos que expresan quitinasa se encuentran virus, bacterias, hongos y plantas. La función de esta enzima en cada organismo es diversa, jugando importantes papeles fisiológicos y ecológicos: en invertebrados se requiere para la degradación parcial de sus antiguos exoesqueletos, en plantas como un mecanismo de defensa contra hongos patógenos, y en bacterias, para las funciones de nutrición y parasitismo, pudiéndose aplicar para el control de fitopatógenos en la agricultura. Hoy en día, la agricultura se ha hecho más vulnerable a las plagas de hongos debido, entre otras causas, a la escasa variación genética que presentan las plantas de cultivo a gran escala. Los hongos proliferan rápidamente, estimulados por el suelo rico en nutrientes y húmedo, ejerciendo un efecto devastador en los cultivos. No sólo afectan a la agricultura, el ser humano también puede ser un hospedador de estos patógenos oportunistas, particularmente cuando se encuentra en estados de inmunodepresión.
La quitinasa de Bacillus subtilis (EC 3.2.1.14) es una enzima de la familia 18 de la glicosil-hidrolasas que cataliza la degradación de la quitina. Bacillus subtilis es uno de los microorganismos con capacidad para secretar una gran variedad de enzimas extracelulares degradantes de polisacáridos, lo que hace que sea un microorganismo idóneo para la secreción de proteínas de interés comercial.
Las técnicas de ingeniería genética y biología molecular facilitan la sobreproducción de enzimas en microorganismos, lo que puede ser utilizado en los procesos de fermentación industrial para producir grandes cantidades de una enzima particular. Desde un punto de vista industrial, producir la mayor cantidad de una enzima determinada se hace necesario recurrir a las técnicas anteriormente citadas para sobreproducir la mayoría de las enzimas empleadas en esta industria.
Descripción
La cepa de Bacillus subtilis 168 presenta dentro de su genoma la secuencia SEQ ID 7, que a pesar de estar secuenciada, no tenía hasta la fecha descrita, ni asociada por homología a secuencias similares en otros genomas, ninguna función concreta. En la presente invención se determina la función de este gen concreto como codificante para una nueva quitinasa, aspecto principal de la presente invención.
La presente invención se refiere a una nueva enzima quitinasa codificada por Bacillus subtilis 168, a un método para producir dicha quitinasa y su uso como fungicida.
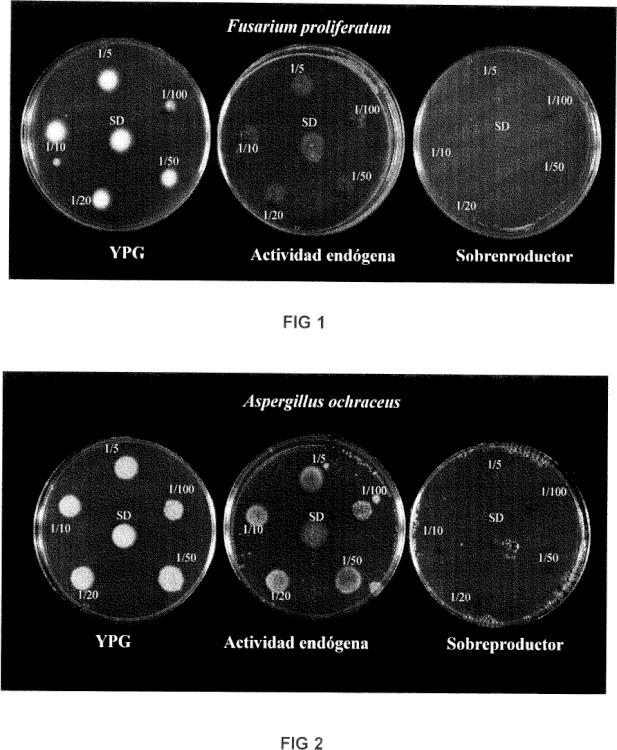
Por otro lado, se describe más adelante mediante ejemplos el efecto fungicida, tanto in vivo como in vitro, de la quitinasa de la presente invención sobre diferentes especies de hongos, demostrando la efectividad de la misma.
Por todo ello, un primer aspecto de la invención se refiere a un polipéptido codificado por un polinucleótido que presenta al menos un 70% de homología con SEQ ID 1, que presenta al menos un 80% de homología con SEQ ID 1, que presenta al menos un 90% de homología con SEQ ID 1 o que consiste esencialmente en SEQ ID 1. A partir de ahora nos referiremos a ella como polipéptido de la invención.
Un segundo aspecto de la invención se refiere a la construcción génica que comprende una secuencia polinucleotídica que codifica al polipéptido como se define en la reivindicación anterior y:
a. una secuencia polinucleotídica que comprende SEQ ID NO 2,
b. moléculas de ácido nucleico cuya cadena complementaria híbrida con la secuencia polinucleotídica de a), o
c. moléculas de ácido nucleico cuya secuencia difiere de a) y/o b) debido a la degeneración del código genético.
Un tercer aspecto de la invención plásmido recombinante que comprende:
- la construcción génica según la reivindicación anterior,
- el gen cat,
- el origen de replicación del plásmido pRMIcat de Escherichia coli y del plásmido pPCT2 para Bacillus subtilis,
- un gen repórter de promotores, y
- un gen de resistencia a kanamicina.
Otro aspecto de la invención se refiere al método de obtención del polipéptido de la invención que comprende introducir la construcción génica según la reivindicación 2 o el plásmido recombinante según la reivindicación 3, en una célula hospedante e incubar la célula hospedante según a) en un medio de cultivo adecuado.
Una realización preferida de dicho método además comprende purificar el polipéptido obtenido. En otra realización preferida la célula hospedadora se selecciona del grupo que comprende E. coli y B. subtilis.
Otro aspecto de la invención se refiere al uso del polipéptido de la invención para la preparación de un fármaco con actividad quitinasa.
Finalmente otro aspecto de la invención es el uso del polipéptido de la invención en la preparación de un fármaco con actividad fungicida.
Adicionalmente, se describe en la presente invención un método que permite la sobreproducción de proteínas de interés biológico, preferiblemente de forma extracelular, en este caso, la sobreproducción de la enzima de interés, polipéptido de la invención. Para ello, se utiliza un promotor específico. Este método de promoción de la expresión también puede ser utilizado para la expresión de otros genes de interés, mediante su inclusión en el plásmido recombinante descrito en la presente invención.
Específicamente, se describe un vector de expresión para sobreproducir proteínas regulado por un promotor de B. subtilis o para inducir la secreción de las proteínas al medio exterior, las células transformadas con este vector y el uso de las mismas para la sobreproducción de la enzima hidrolítica extracelular quitinasa.
El uso del promotor utilizado para la sobrexpresión no está limitado al gen para la quitinasa de B. subtilis, sino que permite expresar otras proteínas homologas o heterólogas ya que la utilización de la secuencia del promotor csn (SEQ ID NO 2) para la regulación de la expresión de genes de interés produce incrementos de los mismos en comparación con el uso de los propios promotores de estos genes.
En la presente invención se describe en detalle el método de elaboración del plásmido recombinante pCSN73 mediante la amplificación de la SEQ ID NO 3, utilizando cebadores específicos, preferentemente los cebadores que comprenden la SEQ ID NO 4 y la SEQ ID NO 5 y el ligado del fragmento de DNA amplificado con el plásmido lanzadera pNR2.
Así mismo se describe un método de elaboración de un plásmido que comprende la amplificación mediante cebadores específicos de la secuencia nucleotídica de B. subtilis que a su vez comprende la secuencia codificante para la proteína madura del gen yvbx y el terminador de la transcripción independiente del factor de terminación rho; la posterior digestión mediante endonucleasas del fragmento amplificado y del plásmido pCSN73; la purificación de los fragmentos obtenidos en la digestión; la desfoforilación de los extremos 5 P del plásmido; y el ligado de los fragmentos purificados. Preferentemente el método de elaboración del plásmido de la invención utiliza los cebadores que comprenden la SEQ ID NO 6 y la SEQ ID NO 7.
Dichos plásmidos se pueden utilizar en la transformación... [Seguir leyendo]
Reivindicaciones:
1. Polipéptido codificado por un polinucleótido que presenta al menos un 70% o un 80% o un 90% de homología con SEQ ID 1 o que consiste esencialmente en SEQ ID 1.
2. Construcción génica que comprende una secuencia polinucleotídica que codifica al polipéptido como se define en la reivindicación anterior y:
3. Plásmido recombinante que comprende:
4. Método de obtención de un polipéptido según la reivindicación 1 que comprende:
5. Método según la reivindicación anterior, que además comprende purificar el polipéptido obtenido.
6. Método según cualquiera de las reivindicaciones 4 a 5, en el que la célula hospedadora se selecciona del grupo que comprende E. coli y B. subtilis.
7. Uso de un polipéptido según la reivindicación 1 para la preparación de un fármaco con actividad quitinasa.
8. Uso de un polipéptido según la reivindicación 1 para la preparación de un fármaco con actividad fungicida.
Patentes similares o relacionadas:
Xilanasa mutante, método de fabricación y uso de la misma, y método para fabricar lignocelulosa sacarificada, del 29 de Julio de 2020, de MITSUI CHEMICALS, INC.: Una xilanasa mutante que comprende la secuencia de aminoácidos de la SEQ ID NO: 2 con una sustitución del resto de aminoácido en la posición 154 en la cual el resto de lisina […]
Métodos para controlar la producción de proteasas, del 1 de Julio de 2020, de ROAL OY: Una célula hospedadora que comprende al menos un gen cromosómico inactivado en donde el gen cromosómico inactivado comprende una secuencia de ácido nucleico que codifica un […]
POLIPÉPTIDO CON ACTIVIDAD XILANASA, SECUENCIA NUCLEOTÍDICA QUE LO CODIFICA, INGREDIENTE Y PROCESO QUE COMPRENDE DICHO INGREDIENTE PARA LA PREPARACIÓN DE UN PRODUCTO ALIMENTICIO, del 18 de Junio de 2020, de UNIVERSIDAD DE SANTIAGO DE CHILE: La presente invención se relaciona con un nuevo polipéptido con actividad xilanasa, la secuencia nucleotídica que lo codifica, un ingrediente que contiene dicho polipéptido, […]
Composiciones de galactosa alfa (1-3) galactosa, del 10 de Junio de 2020, de Janssen Biotech, Inc: Un método para producir una preparación de anticuerpos homogéneamente alfa-galactosilados produciendo una estructura de oligosacáridos alfa-galactosilados […]
Proteína, del 20 de Mayo de 2020, de Dupont Nutrition Biosciences ApS: Una enzima, en donde dicha enzima es una xilanasa GH10 o un fragmento de la misma, que tiene actividad xilanasa, comprendiendo dicha enzima los siguientes aminoácido en dos […]
Polipéptido degradador de carbohidratos y sus usos, del 13 de Mayo de 2020, de DSM IP ASSETS B.V.: Un polipéptido que tiene actividad como hemicelulasa que comprende la secuencia de aminoácidos indicada en SEQ ID NO: 32 o una secuencia de aminoácidos […]
Procedimiento para la hidrólisis de material lignocelulósico, en el que el hidrolizado se usa para la producción de hidrolasa microbiana, del 6 de Mayo de 2020, de CLARIANT INTERNATIONAL LTD.: Un procedimiento para la hidrólisis enzimática autosuficiente de material que contiene lignocelulosa, que comprende las etapas de: (a) someter un material que contiene lignocelulosa […]
Reticuladores químicos, del 22 de Abril de 2020, de AMICUS THERAPEUTICS, INC: Un método de realización de un péptido de direccionamiento lisosomal modificado que comprende: a. poner en contacto el factor de crecimiento similar […]