N-(5-ADAMANTANO-1-IL-METOXI-PENTIL)DESOXINOJIRIMICINA O UNA SAL FARMACÉUTICAMENTE ACEPTABLE DE LA MISMA PARA EL USO EN EL TRATAMIENTO DE LA RESISTENCIA A LA INSULINA.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/NL2004/000760.
Solicitante: GENZYME CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 153 SECOND AVENUE WALTHAM, MA 02451 ESTADOS UNIDOS DE AMERICA.
Inventor/es: AERTS,Johannes,Maria,Franciscus,Gerardus.
Fecha de Publicación: .
Fecha Solicitud PCT: 29 de Octubre de 2004.
Clasificación PCT:
- A61K31/445 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Piperidinas no condensadas, p. ej. piperocaína.
- A61P3/10 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › para la hiperglucemia, p.ej. antidiabéticos.
Clasificación antigua:
- A61K31/445 A61K 31/00 […] › Piperidinas no condensadas, p. ej. piperocaína.
- A61P3/10 A61P 3/00 […] › para la hiperglucemia, p.ej. antidiabéticos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre.
PDF original: ES-2357742_T3.pdf



Fragmento de la descripción:
N-(5-adamantano-1-il-metoxi-pentil)desoxinojirimicina o una sal farmacéuticamente aceptable de la misma para el uso en el tratamiento de la resistencia a la insulina.
Campo de la invención
La presente invención se refiere al uso de N-(5-adamantano-1-il-metoxi-pentil)desoxinojirimicina, o una sal farmacéuticamente aceptable de la misma, para la preparación de un medicamento para el tratamiento de la resistencia a la insulina en el que la síntesis de glucosilceramida y/o otros glicosfingolípidos tienen una función. La resistencia a la insulina crónica causa diabetes mellitus tipo II.
La incidencia de diabetes mellitus tipo II está aumentando espectacularmente. El defecto primario subyacente es una comprensión perjudicada de glucosa del flujo sanguíneo por músculo y tejido adiposo como el resultado de una sensibilidad reducida para movilizar los transportadores de GLUT4 a su superficie celular en respuesta a la insulina. Es ya conocido durante muchos años que concentraciones aumentadas del palmitato de ácido graso se asocian con homeóstasis de glucosa aberrante. No obstante, el mecanismo molecular por el que la lipotoxicidad causa la aparición y progresión de la diabetes es poco comprendido. Una comprensión ulterior en esta materia por lo tanto ayudará a mejorar/desarrollar medicamentos para tratar la resistencia a la insulina y la diabetes mellitus tipo II.
Mecanismo molecular de lipopatogénesis
Las actividades de investigación en glicoesfingolípidos y diabetes mellitus tipo II en el Departamento de Bioquímica del Centro Académico Médico/Universidad de Amsterdam han llevado recientemente a una nueva comprensión inesperada en la lipopatogénesis de la diabetes mellitus tipo II. El mecanismo subyacente está descrito en detalle más debajo.
Función de glicoesfingolípidos en la resistencia a la insulina adquirida
Una función está supuesta para (glico)esfingolípidos en la patogénesis de resistencia a la insulina. Este pensamiento proviene del hecho ignorado de que el palmitato es el bloque de construcción esencial de la fracción de ceramida en esfingolípidos: el primer paso de su biosíntesis implica la transferencia de palmitato a serina, catalizado por serina palmitoiltransferasa, véase figura 1. El índice de síntesis de esfingolípidos en el hígado es altamente dependiente de la concentración de palmitato. De manera importante, esto podría ser experimentalmente confirmado para células musculares cultivadas (células de músculo liso, mioblastos): la adición de 0.1, 0.5, 1.0 mM de palmitato en el medio de cultivo condujo a aumentos proporcionales en la síntesis de glicoesfingolípidos, como fue revelado por incorporación aumentada de serina radiomarcada en estas estructuras.
Este descubrimiento incitó un examen más detallado de la posibilidad de que en realidad los (glico)esfingolípidos median la lipotoxicidad en los músculos subyacente a la resistencia a la insulina. Ha sido destacado recientemente que GM3 (el gangliósido más simple en la superficie de la célula, véase figura 2) puede perjudicar la señalización de insulina. En este aspecto se observa que la concentración de GM3 en la superficie de la célula parece regular la absorción de glucosa en respuesta a la insulina interfiriendo negativamente con multi-agrupamiento de receptores de insulina. Por otra parte, concentraciones altas de GM3 se asocian con movilización reducida de GLUT4 a la superficie celular. Recíprocamente, la reducción de GM3 se asocia con una sensibilidad de insulina mejorada (véase Yamishita et al. Proc Natl Acad Sci USA (2003) 100, 3445-9 Enhanced insulin sensitivity in mice lacking ganglioside GM3; Tagami et al. (2002) J Biol Chem 277, 3085-92. El gangliósido GM3 participa en las condiciones patológicas de resistencia a la insulina). Postulamos que en condiciones de obesidad, los niveles de palmitato son elevados de manera crónica y que por lo tanto la formación de glicoesfingolípidos en adipocitos al igual que células musculares ocurrirá a índices aumentados, favoreciendo la resistencia a la insulina. La conexión entre concentración aumentada de palmitato en músculo como fuerza impulsora para la síntesis de glicoesfingolípidos local (incluyendo GM3) y resistencia a la insulina (véase figura 3) no ha sido aún reconocida por otros.
Papel crucial de la glucosilceramida sintasa
Se descubrió además que la concentración de GM3 y otros gangliósidos en la superficie celular depende de la actividad de la glucosilceramida sintasa (la síntesis de glucosilceramida), la etapa limitadora del índice en la síntesis de gangliósidos (véase figura 3). Esta enzima cataliza la formación de glucosilceramida de ceramida y UDP-glucosa. Los valores de Km de ambos de sus sustratos (ceramida y UDP-glucosa) están en la gama fisiológica. Mostramos que la glucosilceramida sintasa es una enzima reguladora clave respecto a la sensibilidad de insulina. Aumentos en su actividad han sido proporcionados y observados previamente en respuesta a citoquinas inflamatorias (TNF-alfa), hormonas esteroides, ácido graso saturado, e infección vírica (véase figura 4). Se ha descubierto ahora sorprendentemente que los cambios en la síntesis de glicosfingolípidos tienen un impacto en la promoción de resistencia a la insulina que puede finalmente desarrollarse en diabetes mellitus tipo II. Este descubrimiento de que la lipopatogénesis impacta en la resistencia a la insulina muestra que la inhibición de la actividad de la glucosilceramida sintasa ejerce un efecto provechoso anti-hiperglicémico.
Resumen de la invención
Nuevo uso de inhibidores basados en iminoazucar
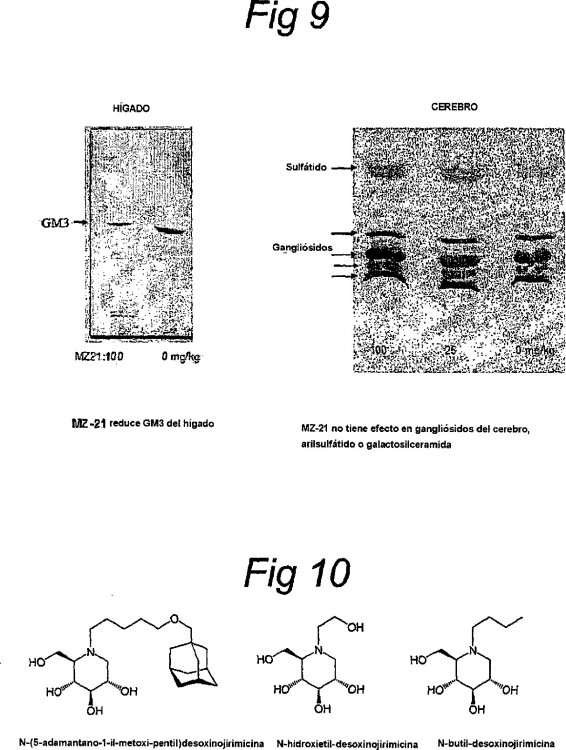
Se ha vuelto evidente que las desoxinojirimicinas, una categoría particular de iminoazúcares, son agentes adecuados para reducir la síntesis glicosfingolípidos por la inhibición de la síntesis de glucosilceramida. Además, la experiencia práctica ha sido obtenida con la seguridad de administración de iminoazucar en seres humanos.
Por consiguiente, la presente invención se refiere al uso de un inhibidor de glucosilceramida sintasa, dicho inhibidor siendo N-(5-adamantano-1-il-metoxi-pentil)desoxinojirimicina, para la preparación de un medicamento para el tratamiento de resistencia a la insulina.
La glucosilceramida sintasa no es la única enzima que se inhibe por desoxinojirimicinas. De hecho varias enzimas "procesadoras de glucosa" en la superficie celular y en varios compartimentos intracelulares se inhiben por las desoxinojirimicinas (véase Butters et al. Chem. Rev. (2000), 100: 4683-96). Las consecuencias de administración de desoxinojirimicinas in vivo no siempre se correlacionan con la potencia in vitro contra las enzimas diana, debido a la accesibilidad diferente del fármaco a compartimentos diferentes de la célula. Por ejemplo n-butil-desoxinojirimicina es un glicano potente que corta el inhibidor de α-glucosidasa in vitro (sub-μM Ki) y sólo un inhibidor modesto de glucosilceramida sintasa (síntesis de glicoesfingolípido es inhibida sólo un 20-30% por 100 mg de TID n-butil-desoxinojirimicina). Sin embargo, debido a la accesibilidad superior de la enzima última al fármaco (el dominio catalítico de glucosilceramida sintasa está enfrente del citosol, mientras que las α-glucosidasas residen en el ER). N-butil-desoxinojirimicina ha sido recientemente registrada para el tratamiento de la enfermedad de Gaucher de tipo 1 basado en su capacidad para inhibir la biosíntesis de glicoesfingolípidos. Así la evaluación in vivo es esencial para establecer en qué medida son significantes las actividades inhibitorias potenciales de las desoxinojirimicinas.
Un inhibidor adecuado debería tener un valor IC50 in vivo para glucosilceramida sintasa inferior a 1 mM, como determinado por una medición in vivo de la actividad de glucosilceramida sintasa utilizando células cultivadas como se describe en los ejemplos. Preferiblemente el IC50 es inferior a 0.5 mM, más preferiblemente inferior a 0.1 mM e incluso más preferiblemente inferior a 0.05 mM.
Se prefiere que el inhibidor de glucosilceramida sintasa inhiba otras enzimas lo menos posible. En este contexto en particular las enzimas intestinales son de relevancia ya que inhibidores potentes de glicosidasas intestinales pueden causar dolencias intestinales severas y pueden no ser muy bien toleradas por muchos individuos. Así se prefiere que el derivado de desoxinojirimicina no sea un inhibidor potente de sucrosa intestinal, maltasa y/o lactasa.... [Seguir leyendo]
Reivindicaciones:
1. Uso de N-(5-adamantano-1-il-metoxi-pentil)desoxinojirimicina, o una sal farmacéuticamente aceptable de la misma, para la preparación de un medicamento para el tratamiento de resistencia a la insulina.
2. Uso según la reivindicación 1 donde N-(5-adamantano-1-il-metoxipentil)desoxinojirimicina, o una sal farmacéuticamente aceptable de la misma es un inhibidor de glucosilceramida sintasa.
3. Uso según la reivindicación 1 o 2 donde el medicamento es para el tratamiento de diabetes mellitus tipo II.
4. Uso según la reivindicación 1 - 3 donde el medicamento debe ser administrado por vía oral.
Patentes similares o relacionadas:
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Triple combinación de antagonistas del receptor 5-HT6 puros, inhibidores de la acetilcolinesterasa y antagonista del receptor NMDA, del 15 de Julio de 2020, de SUVEN LIFE SCIENCES LIMITED: Una combinación que comprende un antagonista del receptor 5-HT6 puro, un inhibidor de la acetilcolinesterasa y un antagonista del receptor NMDA, en el que el antagonista […]
Combinación de agonistas inversos del receptor de histamina-3 con inhibidores de acetilcolinesterasa, del 24 de Junio de 2020, de SUVEN LIFE SCIENCES LIMITED: Una combinación que comprende un agonista inverso del receptor de histamina-3 y un inhibidor de acetilcolinesterasa; en donde el agonista inverso del receptor de histamina-3 […]
Compuestos inhibidores de la acetilcolinesterasa y agonistas de los receptores serotoninérgicos 5HT4, con efecto paramnesiante, sus procedimientos de preparación y composiciones farmacéuticas que los contienen, del 10 de Junio de 2020, de Université de Caen: Compuesto de fórmula general (I): **(Ver fórmula)** en la que: X representa un átomo de hidrógeno, o un átomo de halógeno […]
Nuevos derivados de piperazina y piperidina, síntesis y uso de los mismos en la inhibición de la oligomerización de VDAC, la apoptosis y la disfunción mitocondrial, del 3 de Junio de 2020, de The National Institute for Biotechnology in the Negev Ltd: Compuesto de Fórmula general (Id): **(Ver fórmula)** en la que L2 es un grupo de enlace seleccionado del grupo que consiste en un alquilamidileno […]
Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular, del 27 de Mayo de 2020, de Global Blood Therapeutics, Inc: Un compuesto de Fórmula (I): **(Ver fórmula)** o un tautómero o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento […]
Composición farmacéutica en comprimido que comprende bilastina, del 27 de Mayo de 2020, de Alfred E. Tiefenbacher (GmbH & Co. KG): Una composición farmacéutica en forma de comprimido, que comprende a) una forma cristalina de bilastina, en donde la forma cristalina tiene picos característicos a 6,53, […]
Nuevas composiciones para prevenir y/o tratar trastornos degenerativos del sistema nervioso central, del 27 de Mayo de 2020, de AMICUS THERAPEUTICS, INC: Un compuesto de Fórmula III: **(Ver fórmula)** en donde: R1 es C(R2)(R3)(R4); R2 es hidrógeno, -OH o halógeno; R3 es hidrógeno, -OH, halógeno o -CH3; […]