MÉTODO PARA LA EXPRESIÓN RECOMBINANTE DE UN POLIPÉPTIDO.
Método para la producción recombinante de un polipéptido heterólogo en una célula huésped eucariótica que comprende un plásmido de expresión,
caracterizado porque: a) el plásmido de expresión comprende, en dirección 5' a 3', aa) un promotor, ab) un ácido nucleico codificante de un primer polipéptido que es una secuencia de señal, la secuencia de aminoácidos del cual se selecciona de la Tabla 1 dependiendo de los primeros dos aminoácidos del segundo polipéptido seleccionados de manera que los primeros dos aminoácidos del segundo polipéptido sean idénticos a los primeros dos aminoácidos de las secuencias de aminoácidos de la región FR1 de inmunoglobulina que sigue naturalmente, ac) un ácido nucleico codificante de un segundo polipéptido que comprende: i) un ácido nucleico codificante de dicho polipéptido heterólogo, ii) un ácido nucleico codificante de un conector, iii) un ácido nucleico codificante de un fragmento de inmunoglobulina que comprende por lo menos los dominios constantes de una cadena de una inmunoglobulina, ad) una región 3' no traducida que comprende una señal de poliadenialción, b) el plásmido de expresión se introduce en una célula huésped eucariótica, c) la célula huésped se cultiva bajo condiciones adecuadas para la expresión del segundo polipéptido, d) el segundo polipéptido se recupera del medio de cultivo
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/010067.
Solicitante: F. HOFFMANN-LA ROCHE AG.
Nacionalidad solicitante: Suiza.
Dirección: GRENZACHERSTRASSE 124 4070 BASEL SUIZA.
Inventor/es: KOPETZKI, ERHARD.
Fecha de Publicación: .
Fecha Solicitud PCT: 19 de Octubre de 2006.
Clasificación PCT:
- C07K19/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Péptidos híbridos (Inmoglobulinas híbridas compuestas solamente de inmoglobulinas C07K 16/46).
- C12N15/62 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Secuencias de ADN que codifican proteínas de fusión.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2361188_T3.pdf
Fragmento de la descripción:
La presente invención se refiere a un método para la expresión de un polipéptido en células eucarióticas.
Antecedentes de la invención
Los sistemas de expresión para la producción de polipéptidos recombinantes son bien conocidos del estado de la técnica y se describen en, por ejemplo, Marino M.H., Biopharm. 2:18-33, 1989; Goeddel D.V. et al., Methods Enzymol. 185:3-7, 1990; Wurm F. y Bernard A., Curr. Opin. Biotechnol. 10:156-159, 1999. Los polipéptidos para la utilización en aplicaciones farmacéuticas preferentemente se producen en células de mamífero tales como células CHO, células NS0, células Sp2/0, células COS, células HEK, células BHK y similares. Los elementos esenciales de un plásmido de expresión son una unidad de propagación plásmido procariótico, por ejemplo para E. coli, que comprende un origen de replicación y un marcador de selección, un marcaodr de selección eucariótico, y uno o más casetes de expresión para la expresión del gen o genes estructurales de interés, comprendiendo cada uno un promotor, un gen estructural y un terminador de transcripción, incluyendo una señal de poliadenilación. Para la expresión transitoria en células de mamífero, puede incluirse un origen de replicación de mamífero tal como Ori de SV40 ó OriP. Como promotor, puede seleccionarse un promotor constitutivo o inducible. Para la transcripción optimizada, puede incluirse una secuencia de Kozak en la región 5' no traducida. Para el procesamiento del ARNm, en particular el corte y empalme del ARNm y la terminación de la transcripción, pueden incluirse señales de corte y empalme del ARNm, dependiendo de la organización del gen estructural (organización exón/intrón), así como una señal de poliadenilación.
La expresión de un gen se lleva a cabo en forma de expresión transitoria o permanente. El polipéptido o polipéptidos de interés en general son polipéptidos secretados y por lo tanto contienen una extensión N-terminal (también conocida como secuencia de señal), que resulta necesaria para el transporte/secreción del polipéptido a través de la célula hacia el medio extracelular.
En general, la secuencia de señal puede derivarse de cualquier gen codificante de un polipéptido secretado. En el caso de que se utilice una secuencia de señal heteróloga, preferentemente es una secuencia que resulta reconocida y procesada (es decir, cortada por una peptidasa de señal) por la célula huésped. Para la secreción en levaduras, por ejemplo, la secuencia de señal nativa de un gen heterólogo que debe expresarse puede sustituirse por una secuencia de señal de levadura homóloga derivada de un gen secretado, tal como la secuencia de señal de invertasa de levadura, el líder de factor alfa (incluyendo los líderes de factor α de Saccharomyces, Kluyveromyces, Pichia y Hansenula, estando el segundo descrito en la patente US nº 5.010.182), la secuencia de señal de la fosfatasa ácida, o la secuencia de señal de la glucoamilasa de C. albicans (patente EP nº 0 362 179). En la expresión en células de mamífero, la secuencia de señal nativa de la proteína de interés resulta satisfactoria, aunque pueden resultar adecuadas otras secuencias de señal de mamífero tales como las secuencias de señal de polipéptidos secretados de la misma especie o de especies relacionadas, por ejemplo para inmunoglobulinas de origen humano o murino, así como secuencias de señal secretoria víricas, por ejemplo la secuencia de señal de la glucoproteína D del herpes simplex. El fragmento de ADN codificante de dicho presegmento se liga en el mismo marco de lectura al fragmento de ADN codificante de un polipéptido de interés.
En la patente WO nº 98/28427, se informa de una proteína de fusión preparada genética o químicamente que comprende la región Fc de inmunoglobulina, un derivado o análogo fusionado con la parte N-terminal de la proteína OB. Una molécula quimérica, es decir, una fusión de anticuerpo o una proteína de fusión, que comprende una secuencia importada de proteína carboxi-terminal y una región cargo amino-terminal se presenta en la patente WO nº 03/035892.
En la patente US nº 2003/0049227 se informa de un método para la inducción de una respuesta inmunológica citocida contra un tumor en un mamífero mediante la administración de una inmunocitoquina, que es una proteína de fusión que comprende una parte inmunoglobulina aminoterminal y una parte citoquina carboxi-terminal.
La patente WO nº 01/16437 informa de una proteína fusionada recombinante soluble que es estable en el sistema circulatorio de mamífero, que comprende un polipétido que contiene un sitio de reconocimiento para una molécula diana, tal como un sitio receptor del complemento, y que se encuentra unida en el extremo N-terminal de una cadena de inmunoglobulina. Se informa de una proteína de fusión constituida de un anticuerpo y un péptido que presenta una actividad biológica en la patente US nº 2003/0103984.
En la patente US nº 2004/0033511, se informa de una proteían de fusión de anticuerpo-citoquina y en la patente US nº 2004/0180035, de un inmunoconjugado de anticuerpo-citoquina. Se informa de una inmunotoxina que comrpende gelonina y un anticuerpo en la patente WO nº 94/26910. Perlman et al. (Perlman D., J. Mol. Biol. 167:391-409, 1983) informan de un sitio y secuencia de reconocimiento putativo de peptidasa de señal en péptidos de señal eucarióticos y procarióticos. Se informa del efecto de los cambios de péptido de señal sobre el procesamiento extracelular de la estreptoquinasa de Escherichia coli en Pratap J. y Dikshit K.L., Mol. Gen. Genet. 258:326-333, 1998.
Descripción resumida de la invención
La presente invención comprende un método para la producción recombinante de un polipéptido heterólogo en una célula huésped eurcariótica, que comrpende un plásmido de expresión, en el que el plásmido de expresión comprende, en una dirección 5' a 3', a) un promotor, b) un ácido nucleico codificante de un primer polipéptido que es una secuencia d señal, cuya secuencia de aminoácidos se selecciona de la Tabla 1 dependiendo de los primeros dos aminoácidos del segundo polipéptido, seleccionados de manera que los primeros dos aminoácidos del segundo polipéptido sean idénticos a los primeros dos aminoácidos de las secuencias de aminoácidos de la región FR1 de inmunoglobulina que sigue naturalmente, c) un ácido nucleico codificante de un segundo polipéptido que comprende un ácido nucleico codificante del polipéptido heterólogo, un ácido nucleico codificante de una molécula conectora, y un ácido nuclieco codificante de un fragmento de inmunoglobulina que comrpende por lo menos los dominios constantes de una cadena de una inmunoglobulina, y d) una región 3' no traducida que comprende una señal de poliadenilación. El método comrpende aemás la introducción del plásmido de expreión en una célula huésped eucariótica que se cultiva bajo condiciones adecuadas para la expresión del segundo polipéptido y se recupera el segundo polipéptido del medio de cultivo.
En una realización de la invención, el ácido nuclieco codificante del segundo polipéptido contiene en posición 5' respecto al ácido nucleico codificante del polipéptido heterólogo un ácido nucleico adicional codificante de un único aminoácido o un dipéptido, o el péptido de secuencia de aminoácidos QIWNN (SEC ID nº 472) o un fragmento del mismo.
En otra realización, el fragmento de inmunolgobulina se obtiene de una IgG o de una IgE.
En una realización adicional, la célula eucariótica es una célula de mamífero, especialmente una célula CHO, una célula NS0, una célula Sp2/0, una célula COS, una célula K562, una célula BHK, una célula PER.C6 o una célula HEK.
En todavía otra realización, la molécula conectora es un péptido o polipéptido seleccionado de entre el grupo que consiste de las secuencias SEC ID nº 06, 07, 08, 09, 10, 139, 140, 554, 555, 556 y 557.
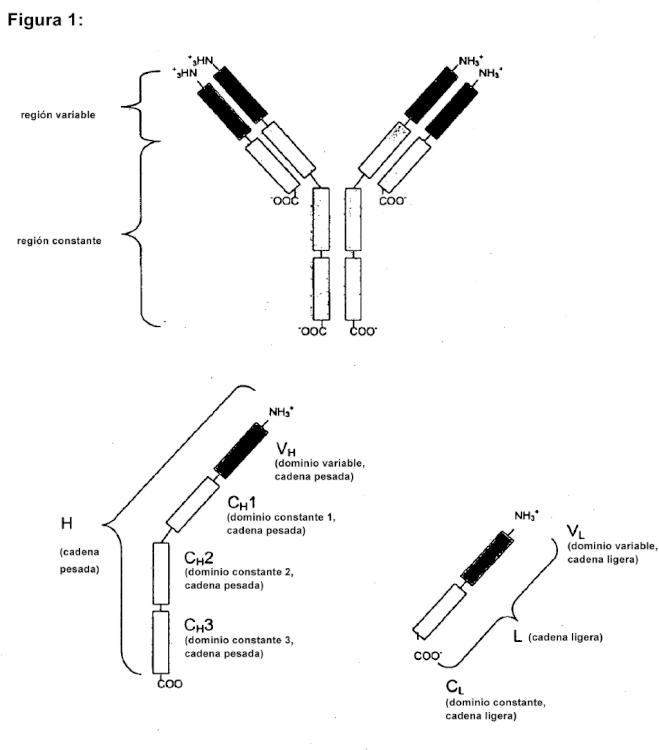
En otra realización, el fragmento de inmunogloublina comprende el dominio constante carboxi-terminal de una cadena pesada o ligera de una inmunoglobulina natural o sintética, es decir, el dominio CH1, la región bisagra, el dominio CH2, el dominio CH3 de una cadena pesada, o el dominio CL de una cadena ligera. Además, el fragmento de inmunoglobulina comprende un fragmento de dominio variable.
En otra realización, el fragmento de domino variable es un dominio variable de una cadena pesada o ligera de inmunoglobulina en la que uno a seis aminoácidos del dominio variable han sido... [Seguir leyendo]
Reivindicaciones:
1. Método para la producción recombinante de un polipéptido heterólogo en una célula huésped eucariótica que comprende un plásmido de expresión, caracterizado porque:
a) el plásmido de expresión comprende, en dirección 5' a 3', aa) un promotor, ab) un ácido nucleico codificante de un primer polipéptido que es una secuencia de señal, la secuencia de aminoácidos del cual se selecciona de la Tabla 1 dependiendo de los primeros dos aminoácidos del segundo polipéptido seleccionados de manera que los primeros dos aminoácidos del segundo polipéptido sean idénticos a los primeros dos aminoácidos de las secuencias de aminoácidos de la región FR1 de inmunoglobulina que sigue naturalmente, ac) un ácido nucleico codificante de un segundo polipéptido que comprende:
i) un ácido nucleico codificante de dicho polipéptido heterólogo, ii) un ácido nucleico codificante de un conector, iii) un ácido nucleico codificante de un fragmento de inmunoglobulina que comprende por lo menos los dominios constantes de una cadena de una inmunoglobulina,
ad) una región 3' no traducida que comprende una señal de poliadenialción,
b) el plásmido de expresión se introduce en una célula huésped eucariótica, c) la célula huésped se cultiva bajo condiciones adecuadas para la expresión del segundo polipéptido, d) el segundo polipéptido se recupera del medio de cultivo.
2. Método según la reivindicación 1, caracterizado porque dicho segundo polipéptido comprende, tras el polipéptido heterólogo, un conector, y tras el conector, un fragmento de inmunoglobulina a modo de parte carboxi-terminal del segundo polipéptido.
3. Método según la reivindicación 1 ó 2, caracterizado porque el segundo polipéptido contiene, en posición 5' respecto al ácido nucleico codificante de dicho polipéptido heterólogo, un ácido nucleico adicional codificante de un único aminoácido o un dipéptido o el péptido QIWNN (SEC ID nº 472) o un fragmento de los mismos.
4. Método según cualquiera de las reivindicaciones 1 a 3, caracterizado porque el fragmento de inmunogloublina se obtiene a partir de una IgG o de una IgE.
5. Método según cualquiera de las reivindicaciones 1 a 4, caracterizado porque la célula eucariótica es una célula de mamífero.
6. Método según la reivindicación 5, caracterizado porque la célula de mamífero es una célula CHO, NS0, Sp2/0, COS, K562, BHK, PER.C6 ó HEK.
7. Método según cualquiera de las reivindicaciones 1 a 6, caracterizado porque el conector es un péptido o polipéptido seleccionado de entre el grupo que consiste de las secuencias SEC ID nº 06, 07, 08, 09, 10, 139, 140, 554, 555, 556 y 557.
8. Método según cualquiera de las reivindicaciones 1 a 7, caracterizado porque el fragmento de inmunoglobulina comprende:
a) el dominio CH1, CH2, CH3 y la región bisagra de una cadena pesada de inmunoglobulina o el dominio CL de una cadena ligera de inmunoglobulina, y b) un fragmento de un dominio variable de cadena pesada o ligera de inmunoglobulina.
9. Método según cualquiera de las reivindicaciones 1 a 7, caracterizado porque el fragmento de inmunoglobulina comprende únicamente dominios constantes.
10. Plásmido que comprende, en dirección 5' a 3':
a) un promotor, 144
b) un ácido nucleico codificante de un primer polipéptido que es una secuencia de señal, la secuencia de aminoácidos del cual se seleccionan de la Tabla 1 dependiendo de los primeros dos aminoácidos del segundo polipéptido seleccionados de manera que los primeros dos aminoácidos del segundo polipéptido sean idénticos a los primeros dos aminoácidos de las secuencias de aminoácidos de la región FR1 de inmunoglobulina que sigue naturalmente, c) un ácido nucleico codificante de un segundo polipéptido que comprende:
i) un ácido nucleico codificante de un polipéptido heterólogo, ii) un ácido nucleico codificante de un conector, iii) un ácido nucleico codificante de un fragmento de inmunoglobulina que comprende por lo menos los dominios constantes de una cadena de una inmunoglobulina,
d) una región 3' no traducida que comprende una señal de poliadenilación.
11. Kit para la preparación de un plásmido para la expresión de un polipéptido heterólogo en una célula eucariótica que comprende un plásmido que comprende, en dirección 5' a 3':
a) un promotor, b) un ácido nucleico codificante de un primer polipéptido que es una secuencia de señal, cuya secuencia de aminoácidos se selecciona de entre el grupo que consiste de las secuencias SEC ID nº 36, 37, 319, 320, 321, 322, 323, 324, 325, 326, 327, 328 y 329, c) un ácido nucleico codificante de un segundo polipéptido que comprende:
i) un ácido nucleico codificante de un péptido QIWNN (SEC ID nº 472) o una fracción N-terminal del mismo que comprende por lo menos el dipéptido QI, ii) un sitio de clonación que comprende por lo menos un sitio de corte de restricción, iii) un ácido nucleico codificante de un conector seleccionado de entre el grupo que consiste de las secuencias SEC ID nº 06, 07, 08, 09, 10, 139, 140, 554, 555, 556 y 557, iv) un ácido nucleico codificante de un fragmento de inmunoglobulina, que comprende por lo menos los dominios constantes de una cadena de una inmunoglobulina.
d) una región 3' no traducida que comprende una señal de poliadenilación.
Patentes similares o relacionadas:
Cadena ligera de enteroquinasa modificada, del 22 de Julio de 2020, de NOVO NORDISK A/S: Un análogo de la cadena ligera de la enteroquinasa bovina que comprende una secuencia de aminoácidos establecida en la SEQ ID NO: 1, en donde dicho análogo comprende […]
Detección de interacciones proteína a proteína, del 15 de Julio de 2020, de THE GOVERNING COUNCIL OF THE UNIVERSITY OF TORONTO: Un método para medir cuantitativamente la fuerza y la afinidad de una interacción entre una primera proteína de membrana o parte de la misma y una […]
Métodos y composiciones para ingeniería genómica, del 3 de Junio de 2020, de Sangamo Therapeutics, Inc: Una pareja de nucleasas de dedo de zinc (ZFN) que comprende una ZFN izquierda y una ZFN derecha, comprendiendo cada ZFN un dominio de escisión […]
Métodos y composiciones para escisión dirigida y recombinación, del 20 de Mayo de 2020, de Sangamo Therapeutics, Inc: Un método in vitro para la escisión selectiva de un gen HLA clase I, un gen HLA que codifica una proteína de clase 1 del Complejo de Histocompatibilidad Mayor (MHC) […]
Antígenos de coagulasa estafilocócica y métodos para su uso, del 13 de Mayo de 2020, de UNIVERSITY OF CHICAGO: Una composición inmunógena que comprende al menos dos dominios 1-2 de coagulasa estafilocócica diferentes, en donde cada uno de los al menos dos dominios […]
Reconocimiento de unión a diana celular mediante un agente bioactivo usando transferencia de energía de resonancia de bioluminiscencia intracelular, del 6 de Mayo de 2020, de PROMEGA CORPORATION: Un sistema de ensayo que comprende: (a) una biblioteca de agentes bioactivos, cada uno de los cuales está fijado a un fluoróforo; (b) una diana celular fusionada a […]
Etiqueta de epítopo y método de detección, captura y/o purificación de polipéptidos etiquetados, del 15 de Abril de 2020, de ChromoTek GmbH: Péptido epítopo aislado que tiene de 12 a 25 aminoácidos, en donde la secuencia de aminoácidos comprende una secuencia según se define en SEQ ID NO: 32 (X1X2RX4X5AX7SX9WX11X12), […]
Utilización diagnóstica de un polipéptido de fusión que comprende una proteína vírica y un enzima MGMT, del 15 de Abril de 2020, de INSTITUT PASTEUR: Utilización in vitro de un polipéptido de fusión que comprende una proteína vírica y i) el enzima 6-metilguanina-ADN-metiltransferasa (MGMT, EC 2.1.1.63) o un homólogo […]