USO DEL GEN NCBSR4 PARA EL DIAGNOSTICO Y PREVENCION DE LA NEOSPOROSIS Y COMO MARCADOR PARA EL ANALISIS DE LA PATOGENIA.
Uso del gen NcBSR4 para el diagnóstico y prevención de la neosporosis y como marcador para el análisis de la patogenia.
La presente invención se refiere al uso del gen NcBSR4 y la proteína NcBSR4, los vectores de expresión y las células hospedadoras que los contengan, para el diagnóstico y la prevención de la neosporosis y, como marcador específico de la fase de bradizoíto de N. caninum, para el análisis de la patogenia o de la eficacia de las vacunas frente al establecimiento de la infección crónica en el hospedador intermediario. También se refiere al uso del promotor del gen NcBSR4 para la expresión de genes heterólogos que permite el estudio de los mecanismos moleculares que determinan la conversión de estadio de taquizoíto a bradizoíto y a la inversa.
Además, la presente invención se refiere al desarrollo de anticuerpos monoclonales y sueros policlonales monoespecíficos frente a la proteína NcBSR4 y su forma recombinante, que representan una alternativa para el diagnóstico serológico de la neosporosis y de la infección crónica por N. caninum en los tejidos animales
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200601262.
Solicitante: UNIVERSIDAD COMPLUTENSE DE MADRID.
Nacionalidad solicitante: España.
Provincia: MADRID.
Inventor/es: ORTEGA MORA,LUIS MIGUEL, FERNANDEZ GARCIA,AURORA, RISCO CASTILLO,VERONICA, AGUADO MARTINEZ,ADRIANA.
Fecha de Solicitud: 17 de Mayo de 2006.
Fecha de Publicación: .
Fecha de Concesión: 28 de Mayo de 2010.
Clasificación Internacional de Patentes:
- C07K14/44 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de protozoos.
- G01N33/569B
Clasificación PCT:
- C07K14/44 C07K 14/00 […] › de protozoos.
- C12N15/30 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican proteínas de protozoos, p. ej. Plasmodium, Trypanosoma, Eimeria.
- G01N33/569 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para microorganismos, p. ej. protozoarios, bacterias, virus.
Fragmento de la descripción:
Uso del gen NcBSR4 para el diagnóstico y prevención de la neosporosis, y como marcador para el análisis de la patogenia.
Objeto de la invención
La presente invención se establece en el campo de la sanidad animal y se refiere, según se expresa en el enunciado de esta memoria descriptiva, al diagnóstico, análisis de la patogenia y la prevención de la enfermedad producida por el parásito protozoo Neospora caninum. De forma más concreta la invención se relaciona con la molécula polinucleotídica correspondiente al gen NcBSR4 de N. caninum, su RNA mensajero y el antígeno que codifica, NcBSR4, siendo éste una proteína específica del estadio de bradizoíto, así como los oligonucleótidos, los vectores recombinantes, las células hospedadoras transformadas, y las proteínas expresadas de forma recombinante, el uso de éstos como reactivos para el diagnóstico de la enfermedad, su aplicación al desarrollo de técnicas moleculares que permitan estudiar la patogenia de la enfermedad, además de su utilidad para la producción de vacunas.
Antecedentes
La neosporosis
N. caninum es un parásito protozoo perteneciente al phylum Apicomplexa que incluye otros parásitos patógenos importantes como Toxoplasma gondii con el que guarda mucha relación. N. caninum está descrito desde 1989 como agente productor de aborto y mortalidad neonatal en el ganado bovino (Thilsted and Dubey. 1989. J. Vet. Diagn. Invest. 1, 205-209), aunque es capaz de infectar a un amplio espectro de especies de mamíferos (Dubey J. P. 2003. Korean J Parasitol. 41, 1-16; Moore D. P. 2005. Vet. Parasitol. 127, 87-97).
La neosporosis bovina está considerada como una enfermedad parasitaria de distribución cosmopolita y una de las causas más frecuentes de fallo reproductivo (Dubey J. P. 2003. J. Parasitol. 89, S42-S56). La manifestación clínica más importante de la infección en las hembras gestantes es el aborto y generalmente tiene lugar entre el tercer y noveno mes de gestación, siendo más frecuente en torno a los 5-6 meses. Los terneros congénitamente infectados que nacen vivos pueden presentar problemas neuromusculares, aunque lo más frecuente es el nacimiento de terneros clínicamente sanos (Buxton et al. 2002. Trends Parasitol. 18, 546-552). Así mismo, la neosporosis puede afectar a los perros, hospedadores definitivos, aunque pueden actuar también como hospedadores intermediarios, donde produce polimiositis, encefalitis, parálisis y puede causar la muerte (Lindsay and Dubey. 1989. J. Parasitol. 75, 163-165; Buxton et al. 2002. Trends Parasitol. 18, 546-552).
Como T. gondii, N. caninum tiene un ciclo de vida que comprende tres estadios (Dubey and Lindsay 1996. Vet. Parasitol. 67, 1-59; Basso et al. 2001. J. Parasitol. 87, 612-618). Los esporozoítos infectan al hospedador intermediario por ingestión de los ooquistes eliminados por el hospedador definitivo que esporulan en el medio ambiente. En el hospedador intermediario se desarrollan dos fases intracelulares distintas: los taquizoítos, de replicación rápida y responsables de la fase aguda de la infección, y los bradizoítos, la forma de multiplicación lenta del parásito dando lugar a quistes tisulares localizados fundamentalmente en el sistema nervioso central. Estos bradizoítos permanecen latentes en los quistes de los tejidos hasta su reactivación (Antony and Williamson. 2001. New Zeal. Vet. J. 49, 42-47; Buxton et al. 2002. Trends Parasitol. 18, 546-552). Diversos estudios en T. gondii y N. caninum indican que la diferenciación de taquizoíto a bradizoíto en estos parásitos es un fenómeno inducido por estrés, aunque no se conocen con exactitud los mecanismos moleculares que determinan el paso de una fase del ciclo a otra. Así mismo, se ha sugerido una implicación de la respuesta inmune en la latencia y la reactivación de la infección en animales infectados de forma crónica (Lyons et al., 2002, Trends Parasitol. 18, 198-201).
Antígenos de N. caninum
En lo que se refiere a la comparación de la composición antigénica entre el taquizoíto y el bradizoíto de N. caninum, la información disponible hasta el momento es escasa, hecho que contrasta con los estudios realizados en T. gondii, donde son varios los antígenos específicos de estadio identificados y caracterizados.
En N. caninum se han identificado antígenos específicos del taquizoíto o compartidos por ambos estadios (Fuchs et al. 1998. J. Parasitol. 84, 753-758; Lee et al. 2004. J. Vet. Sci. 5, 139-145; Shin et al. 2004. Proteomics 4, 3600-3609; Shin et al. 2005. Vet. Parasitol. 134, 41-52). Entre estos antígenos se han descrito dos proteínas de superficie, NcSAG1 (Hemphill et al. 1997. Parasitology 115, 371-380), específica de taquizoíto, cuyo gen fue clonado por Howe et al. (1998. Infect. Immun. 66, 5322-5328) y NcSRS2 (Hemphill et al. 1996. Parasitol. Res. 82, 497-504), que se expresa de forma conjunta en los taquizoítos y en los bradizoítos. Se han identificado tres proteínas de micronemas, NcMIC3 (Sonda et al. 2000. Mol. Biochem. Parasitol. 108, 39-51), NcMIC1 (Keller et al. 2002. Infect. Immun. 70, 3187-3198), presentes en ambos estadios, y NcMIC4 (Keller et al. Infect. Immun. 2004. 72, 4791-4800), identificada a partir de taquizoítos. Así mismo, se han incluido en el banco de genes dos secuencias de Neospora denominadas NcMIC10 y NcMIC11, que podrían codificar dos proteínas de micronemas, ya que sus secuencias presentan una homología elevada con las secuencias que codifican las proteínas de T. gondii TgMIC10 y TgMIC11, respectivamente. Otros genes que han sido donados son NcGRA6 y NcGRA7, que codifican proteínas de gránulos densos del taquizoíto de N. caninum (Lally et al.1996. Clin. Diagn. Lab. Immunol. 3, 275-279). Además de estas proteínas de gránulos densos, se han descrito otras denominadas NcNTPasa-I (Asai et al. 1998. Exp. Parasitol. 90, 277-285), NcGRA2 (Ellis et al. 2000. Parasitology 120 (Pt 4), 383-390) y NcGRA1 (Lee et al. 2003. Proteomics 3, 2339-2350). Las proteínas NcGRA1, NcGRA2, y NcGRA7 se localizan no sólo en la fase de taquizoíto sino en la pared de los quistes producidos in vitro (Vonlaufen et al. 2004. 72, 576-83). Así mismo, se ha descrito recientemente un antígeno de 56 kDa presente en el complejo apical de varios estadios de desarrollo del parásito (Jenkins et al. 2004. J. Parasitol. 90, 660-663). En base a varios de estos antígenos se han desarrollado diversos ELISAs recombinantes para el diagnóstico de la infección por N. caninum (revisado en: Ortega-Mora et al. 2006. Acta Parasitol. 51, 1-14).
Finalmente, se han clonado tres genes que expresan enzimas en N. caninum: NcSUB1 que expresa una serin-proteasa de 65 kDa, localizada en los micronemas del taquizoíto (Louie and Conrad. 1999. Mol. Biochem. Parasitol. 103, 211-223; Louie et al. 2002. J. Parasitol. 88, 1113-1119); un gen que codifica una superóxido dismutasa (Fe-SOD) que se expresa en ambos estadios del parásito, taquizoítos y bradizoítos (Cho et al. 2004. J. Parasitol. 90, 278-85) y el gen que codifica una disulfuro isomerasa (NcPDI) específica del taquizoíto e implicada en la interacción del parásito con la célula hospedadora (Naguleswaran et al. 2005. Int J Parasitol. 35, 1459-1472).
En relación con los antígenos específicos del bradizoíto de N. caninum tan sólo el gen NcSAG4 ha sido identificado, clonado y caracterizado recientemente (WO2005053505). Sin embargo, en T. gondii sí se han descrito diversos genes que expresan antígenos específicos de bradizoíto entre los cuales destacan varios de superficie como TgSAG4 (Ödberg-Ferragut et al.1996. Mol. Biochem. Parasitol. 82, 237-244) y TgBSR4 (Knoll LJ, Boothroyd JC. 1998. Mol. Cell. Biol. 18, 807-814).
Diagnóstico de la neosporosis
Para el diagnóstico de la neosporosis bovina los datos epidemiológicos y la historia clínica son muy importantes y pueden orientar, pero siempre es necesaria la confirmación mediante el diagnóstico laboratorial (Anderson et al. 2000. Anim Reprod Sci. 60-61,417-431). Para ello es recomendable tanto el examen del feto abortado como la serología materna. En este sentido se plantean dos problemas principales en el diagnóstico de la neosporosis bovina: el criterio diagnóstico y las técnicas utilizadas en el feto abortado y, por otro lado, el diagnóstico de la infección y/o enfermedad en el animal...
Reivindicaciones:
1. Molécula polinucleotídica caracterizada por la secuencia de nucleótidos SEQ ID NO: 13 que contiene el gen NcBSR4 de Neospora caninum.
2. Molécula polinucleotídica según reivindicación 1 caracterizada porque codifica la proteína antigénica NcBSR4 de Neospora caninum (SEQ ID NO: 14).
3. Molécula polinucleotídica según reivindicación 1 caracterizada por la secuencia comprendida entre el nucleótido 1084 y el 2195 de la secuencia SEQ ID NO: 13.
4. Molécula polinucleotídica seleccionada del conjunto de secuencias constituido por (a) el gen NcBSR4 de Neospora caninum, caracterizado por SEQ ID NO: 13, (b) secuencias homólogas al gen NcBSR4 que codifican el antígeno NcBSR4 y (c) fragmentos del gen NcBSR4 que codifican polipéptidos que conservan las características antigénicas de NcBSR4.
5. Procedimiento para el diagnóstico in vitro de la infección crónica por N. caninum a partir de tejidos o fluidos de animales infectados caracterizado por la detección de las moléculas polinucleotídicas según las reivindicaciones 1 a 4 mediante su amplificación enzimática basada en la reacción PCT o RT-PCR, su hibridación in situ con sondas de DNA o cualquier otro método de detección de los ácidos nucleicos.
6. Procedimiento para el diagnóstico de la infección crónica por N. caninum según la reivindicación 5 caracterizado por el uso de oligonucleótidos-cebadores y/o sondas elegidos del conjunto constituido por las secuencias SEQ ID NO: 1 (R1BSR4), SEQ ID NO: 2 (R2BSR4), SEQ ID NO: 3 (F1BSR4), SEQ ID NO: 4 (F2BSR4), SEQ ID NO: 5 (NcESTF), SEQ ID NO: 6 (NcESTR), SEQ ID NO: 7 (FNCEST5), SEQ ID NO: 8 (RNCEST3), SEQ ID NO: 9 (FBamHNcBSR4), SEQ ID NO: 10 (RHindIIINcBSR4), SEQ ID NO: 11 (NcBSR4F3) y SEQ ID NO: 12 (NcBSR4R3).
7. Vector recombinante caracterizado porque comprende una secuencia de nucleótidos definida según las reivindicaciones 1 a 4.
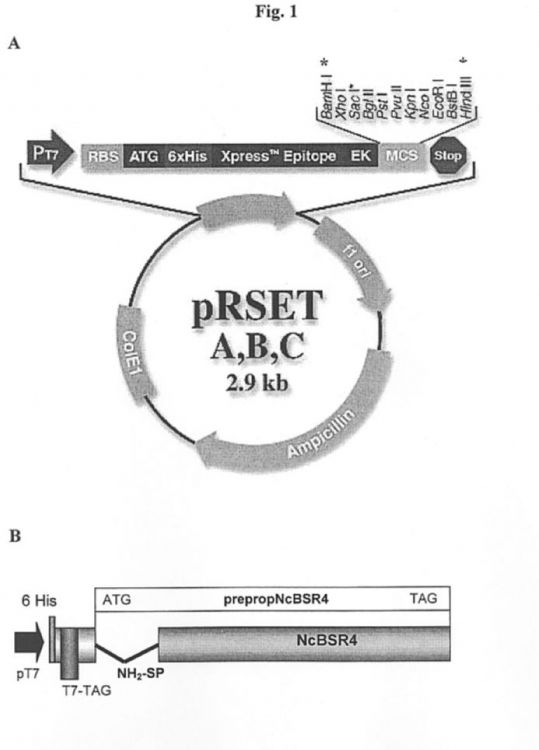
8. Vector recombinante caracterizado porque comprende la molécula polinucleotídica según la reivindicación 3 y el plásmido pRSET-C.
9. Células eucariotas hospedadoras transfectadas con los vectores recombinantes de la reivindicación 7.
10. Células procariotas hospedadoras transformadas con los vectores recombinantes de la reivindicación 7 u 8.
11. Un polipéptido purificado o aislado seleccionado de (a) la proteína antigénica NcBSR4 de N. caninum, caracterizada por la secuencia de aminoácidos SEQ ID NO: 14; (b) secuencias modificadas química o enzimáticamente derivadas de secuencias homólogas a la de la proteína NcBSR4 (SEQ ID NO: 14) que conservan sus características antigénicas; (c) polipéptidos derivados de NcBSR4 (SEQ ID NO: 14) que conservan sus características antigénicas; o (d) proteínas recombinantes que comprenden la proteína NcBSR4 (SEQ ID NO: 14) o polipéptidos derivados de NcBSR4 (SEQ ID NO: 14) que conservan sus características antigénicas.
12. Procedimiento para el diagnóstico serológico de la infección crónica por N. caninum caracterizado por el uso de anticuerpos monoclonales o suero policlonal específico frente a proteínas y/o polipéptidos según la reivindicación 11 mediante inmunohistoquímica, inmunofluorescencia o cualquier otro método basado en la detección de dichas proteínas y/o polipéptidos por el citado suero.
13. Procedimiento para el diagnóstico serológico de la infección crónica por N. caninum caracterizado por la detección de las proteínas y/o polipéptidos según la reivindicación 11 mediante enzimoinmunoanálisis (ELISA), radioinmunoanálisis (RIA), inmunoblot o cualquier otro método basado en la capacidad antigénica de dichos polipéptidos.
14. Procedimiento para el diagnóstico serológico de la infección crónica por N. caninum según la reivindicación 13 caracterizado por la detección de las proteínas y/o polipéptidos según la reivindicación 11 mediante un ELISA de competición.
15. Una composición inmunogénica que comprenda: (a) un polipéptido según la reivindicación 11, (b) un a molécula polinucleotídica según las reivindicaciones 1 a 4; (c) un vector recombinante según la reivindicación 7; (d) unas células hospedadoras transfectadas según las reivindicaciones 9; (e) unas células hospedadoras transformadas según las reivindicaciones 10, formulada como vacuna contra la neosporosis.
16. Una composición inmunogénica según la reivindicación 15, que comprenda un adyuvante o una o varias citoquinas.
17. Un método de preparación de una composición inmunogénica que comprenda una combinación de (a) un polipéptido según la reivindicación 11; (b) una molécula polinucleotídica que contenga una secuencia que codifique un polipéptido según la reivindicación 11; (c) un vector recombinante según la reivindicación 7; (d) unas células hospedadoras transfectadas según las reivindicaciones 9; (e) unas células hospedadoras transformadas según las reivindicaciones 10, formulada como vacuna contra la neosporosis.
18. Un kit de vacunación para mamíferos contra la neosporosis que comprenda un contenedor que incluya una composición inmunogénica formulada según reivindicaciones 15 y 16.
Patentes similares o relacionadas:
Cepas mutantes de neospora y sus usos, del 9 de Octubre de 2019, de Bio-Sourcing: Cepa mutante de Neospora caninum en la que la función de la proteína NcMIC3 se suprime mediante la deleción de todo el gen ncmic3.
Adyuvante nuevo, del 25 de Abril de 2018, de Laboratorios LETI, S.L: Molécula de ácido nucleico representada por una secuencia de nucleótidos seleccionada del grupo que consiste en: i. Secuencias de nucleótidos que codifican un polipéptido […]
Molécula para tratar un trastorno inflamatorio, del 7 de Marzo de 2018, de Laboratorios LETI, S.L: Molécula de ácido nucleico capaz de inducir una respuesta antiinflamatoria para uso como medicamento, donde dicha molécula de ácido nucleico […]
Protozoo modificado que expresa al menos dos proteínas variables de superficie (VSP), vacuna que lo comprende, procedimientos, usos y métodos, del 31 de Enero de 2018, de CONSEJO NACIONAL DE INVESTIGACIONES CIENTIFICAS Y TECNICAS (CONICET) (33.3%): Protozoo parásito modificado Giardia en el que el gen Dicer, el gen ARN-polimerasa ARN-dependiente (RdRP) o ambos han sido silenciados mediante ingeniería genética, comprendiendo […]
UNA VACUNA CONTRA LA INFECCIÓN POR TRYPANOSOMA CRUZI, del 9 de Noviembre de 2017, de BAEREMAECKER, Carlos: Una composición de vacuna contra la infección por Trypanosoma cruzi que comprende, al menos, una proteína mutante trans-sialidasa de Trypanosoma cruzi (SEQ 1) y, […]
Mutantes con inactivación condicional de un receptor de tipo sortilina en parásitos apicomplejos y usos de los mismos, del 25 de Octubre de 2017, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE: Una construcción de ácido nucleico, que comprende: (i) una secuencia que comprende de 100 a 10000 pb, ventajosamente de 150 a 4000 pb, más ventajosamente de 1000 […]
Proteínas de fusión y su uso en el diagnóstico y tratamiento de la leishmaniasis, del 15 de Marzo de 2017, de INFECTIOUS DISEASE RESEARCH INSTITUTE: Un polipéptido de fusión aislado que comprende dos o más antígenos de Leishmania seleccionados del grupo que consiste en K26, K39, y K9, en el que el antígeno […]
Composiciones farmacéuticas que comprenden un polipéptido que comprende al menos un motivo CXXC y antígenos heterólogos y usos de las mismas, del 7 de Diciembre de 2016, de CENTRE NATIONAL DE LA RECHERCHE SCIENTIFIQUE (CNRS): Vacuna frente a un antígeno que comprende : - un antígeno unido a un polipéptido heterólogo para el antígeno, en la que polipéptido es una proteína de superficie […]