PROCEDIMIENTO MEJORADO PARA LA PREPARACION DE ACIDOS AMINOMETILCICLOALCANACETICOS.
Procedimiento para la preparación de gabapentina de fórmula 1
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IN2002/000224.
Solicitante: HIKAL LTD.
Nacionalidad solicitante: India.
Dirección: 6, NAWAB BUILDING, 327, DR. D N ROAD FORT,400001 MUMBAI.
Inventor/es: KUPPUSWAMY,NAGARAJAN,HIKAL R & D CENTRE, HARIHARAN,SIVARAMAKRISHNAN,HIKAL R & D CENTRE, MARIADAS,ARULSELVAN,HIKAL R & D CENTRE.
Fecha de Publicación: .
Fecha Concesión Europea: 13 de Enero de 2010.
Clasificación Internacional de Patentes:
- C07C227/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 227/00 Preparación de compuestos que contienen grupos amino y carboxilo unidos a la misma estructura carbonada. › por reacciones que implican a los grupos amino o carboxilo, p. ej. hidrólisis de ésteres o de amidas, por formación de haluros, de sales o de ésteres.
- C07C227/38 C07C 227/00 […] › Separación; Purificación; Estabilización; Empleo de aditivos (separación de isómeros ópticos C07C 227/34).
Clasificación PCT:
- C07C227/42 C07C 227/00 […] › Cristalización.
- C07C229/28 C07C […] › C07C 229/00 Compuestos que contienen grupos amino y carboxilo unidos a la misma estructura carbonada. › siendo saturada la estructura carbonada y conteniendo ciclos.
Clasificación antigua:
- C07C227/42 C07C 227/00 […] › Cristalización.
- C07C229/28 C07C 229/00 […] › siendo saturada la estructura carbonada y conteniendo ciclos.
Fragmento de la descripción:
Procedimiento mejorado para la preparación de ácidos aminometilcicloalcanacéticos.
Antecedentes
Esta invención se refiere a un procedimiento mejorado para la preparación de ácidos aminometilcicloalcanacéticos. Esta invención se refiere, en particular, a un procedimiento mejorado para la preparación de gabapentina (que es conocido químicamente como ácido 1-aminometil-1-ciclohexanacético), que es un agente bien conocido, útil para el tratamiento de la epilepsia y otras enfermedades cerebrales. En la serie química de los ácidos 1-aminometilcicloalcan-1-acéticos, la gabapentina, que es el ácido 1-aminometil-1-ciclohexanacético, ha sido desarrollada como medicamento que tiene propiedades anticonvulsivas.
La gabapentina tiene la fórmula 1 que se muestra a continuación
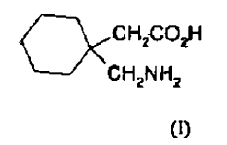
Las patentes USA nº 4024175 y nº 4087 54 y la patente alemana nº 2460891 dan a conocer este compuesto, su procedimiento de preparación y sus utilizaciones.
Las patentes mencionadas describen varios procedimientos para la preparación de gabapentina y compuestos similares a la fórmula general 2 que se indica a continuación.
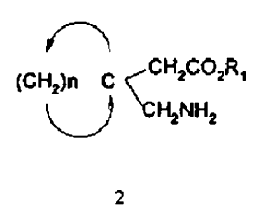
en la que R1 es un átomo de hidrógeno, o un radical alquilo inferior, y n es un entero con un valor de 4 a 6 y comprendiendo además sus sales farmacéuticamente aceptables.
Los procedimientos que se dan a conocer en estas patentes se basan en métodos conocidos utilizados para la preparación de aminas primarias. De manera especifica, estos procedimientos comportan la reacción de Curtius de monoésteres de ácido cicloalcandiacético, reacción de Hoffmann de monoamidas de ácido cicloalcandiacético o la reagrupación de Lossen de los ésteres de sulfonato del ácido 1-carboximetilcicloalcanacetohidroxámico.
En una variación de la reagrupación de Lossen, el procedimiento puede ser llevado a cabo sobre la O-sulfoniloxicicloalcan-1,1-(N-hidroxi)imidadiacética (patente USA nº 4152326, y patente de Canadá nº 1085420). Estos procedimientos pasan por un isocianato o uretano que puede ser convertido en el ácido 1-aminometilcicloalcan-1-acético deseado por hidrólisis ácida o básica. El clorhidrato del aminoácido es aislado a partir del hidrolizado por evaporación de agua.
En particular, en las patentes USA nº 4024175 y nº 4087544 y la patente alemana nº 2460891, el ácido monometilciclohexan-1-acético es transformado en la azida que se descompone (reacción de Curtius) en tolueno hirviendo. El isocianato resultante se hidroliza con ácido clorhídrico en solución acuosa. La solución resultante se evapora hasta sequedad para proporcionar el clorhidrato del ácido 1-aminometilciclohexan-1-acético, que es convertido en gabapentina con una resina de intercambio iónico básica.
En las mismas patentes, la monoamida del ácido 1,1-ciclopentandiacético es tratada con hipobromito sódico en solución acuosa a -10 grados, y la solución es calentada, a continuación, a 60 grados durante 2 horas. A continuación, se acidifica con ácido clorhídrico 12N y se evapora en vacío. El residuo se extrae con etanol y la solución se etanol de evapora proporcionando clorhidrato del ácido 1-aminometilciclopentan-1-acético del cual se obtiene el aminoácido libre por paso a través de una resina de intercambio iónico básica.
En la patente USA nº 4152326, la imida del ácido N-(p-toluensulfoniloxi)-1,1-ciclohexandiacético es calentada con una solución acuosa de hidróxido sódico al 10% (reagrupación de Lossen) a 100 grados, y la solución resultante es acidificada con ácido clorhídrico concentrado y evaporada a sequedad. El residuo es digerido con etanol y filtrado, y el filtrado es evaporado en vacío para conseguir bencensulfonato de gabapentina. El tratamiento de este material con el intercambiador iónico básico IR-45 en forma -OH proporciona la gabapentina.
En los años siguientes se han solicitado patentes referentes a otras rutas que comportan la hidrólisis de 2-azaspiro(4,5)decan-3-ona de fórmula 3, conocida convencionalmente como gabalactama, aislada por primera vez por Sircar (J. Ind. Chem. Soc., 1928,5,549; chem. Abstracts, 1929,23,818) con ácido clorhídrico 1:1
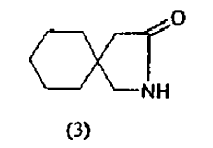
(Las patentes USA nº 5091567, nº 5068413, la patente europea 414263; la solicitud de patente WO 9914184A1) para conseguir gabapentina en forma de sal clorhidrato.
Por lo tanto, en la patente USA nº 5068413 y en la patente europea nº 414263 A2, la gabalactama es mezclada 1:1 con ácido clorhídrico y sometida a ebullición en reflujo a 108 grados C durante 6 horas, siendo enfriada y diluida con agua. La mezcla es extraída con cloruro de metileno para eliminar la lactama no disuelta. La solución acuosa es evaporada a sequedad en vacío y el residuo es lavado con acetona para proporcionar clorhidrato de gabapentina como parte insoluble.
En la patente USA nº 5091567, la gabalactama es hidrolizada de manera similar con ácido clorhídrico para proporcionar el clorhidrato de gabapentina.
En la solicitud de patente WO nº 9914184A1, la lactama de fórmula 3 es hidrolizada con una mezcla de ácido clorhídrico 6N y dioxano en reflujo durante 4 horas. La solución es evaporada a sequedad y el residuo es cristalizado a partir de metanol-acetato de etilo-heptano para conseguir el clorhidrato de gabapentina.
En otras dos patentes (patentes USA nº 4956473 y nº 4958644), la lactama de fórmula 3, que tiene un grupo carbetoxi adicional, es sintetizada e hidrolizada con ácido clorhídrico 1:1 con la eliminación simultanea del grupo carbotoxi para conseguir el clorhidrato de gabapentina.
En la patente USA nº 4958044, una solución de dimetil éster del ácido (1-ciano cicloexil) malónico en etanol es hidrogenada a 10 bares de presión de hidrógeno y a 90 grados C sobre 3 g de níquel de Raney durante 4,5 horas. La solución es filtrada y el filtrado es evaporado para proporcionar 2-aza-(4-metoxi-carbonil)espiro(4,5)decan-3-ona(carbetoxi gabalactama). Esta se mezcla con ácido clorhídrico al 20% y se mezcla en reflujo durante 24 horas. Esta solución es evaporada a sequedad y el residuo es manipulado para conseguir clorhidrato de gabapentina.
También se han descrito otros métodos para sintetizar gabapentina directamente sin la intervención de gabalactama o clorhidrato de gabapentina. En las patentes USA nos 5095148, 5135455, 5136091, 5149870 y en la patente de Canadá nº 203217, el benzil éster del ácido (1-ciano ciclohexil)acético es hidrogenado en metanol utilizando un 5% de rodio sobre carbono como catalizador a 10 bares de presión de hidrógeno durante 23 horas a temperatura ambiente. El filtrado de la mezcla como concentración del filtrado y dilución con etanol proporciona gabapentina con un rendimiento del 27%.
En las patentes USA nos 5132451, 5319135 y 6294690, el ácido 1-cianociclohexanoacético es hidrogenado en metano a una temperatura ambiente durante 2 horas utilizando un 15% de rodio sobre carbono como catalizador conteniendo un 1% de paladio. La mezcla es filtrada y el filtrado es concentrado. La adición de isopropanol y la agitación a 0-5 grados durante 24 horas proporciona la gabapentina. En la patente europea nº 414262B1, se hidrogena el ácido 1- cianociclohexanacético sobre níquel de Raney para producir gabapentina.
En la patente USA nº 6294690, se somete el benzonitrilo a una reducción de Birch con litio y amoníaco líquido y los intermediarios de reducción retenidos con etilbromoacetato. El producto resultante es hidrolizado a ácido (1-ciano ciclohexan-2,5-dienil)acético que es hidrogenado en hidróxido amónico metabólico durante 3,5 horas a 50 grados C y 50 psi de presión de hidrógeno sobre un catalizador de carbón con 5% de paladio. La mezcla es filtrada y el filtrado es concentrado para conseguir gabapentina en crudo.
La solicitud WO nº 2000039074 describe la síntesis de gabapentina por hidrogenación de bencil o difenilmetil éster del ácido 1-nitrometilciclohexildiacético.
Con gran diferencia, el procedimiento más ampliamente utilizado para la preparación de gabapentina es la eliminación de HCl de su sal clorhidrato. Esto ha sido conseguido de diferentes...
Reivindicaciones:
1. Procedimiento para la preparación de gabapentina de fórmula 1

que comprende:
(i) preparar una solución acuosa de clorhidrato de gabapentina en agua con una proporción de una parte en peso del clorhidrato de gabapentina con respecto a 0,5-3 partes en peso de agua;
(ii) preparar una solución acuosa de hidróxido sódico o potásico en una concentración del orden de 40-50% p/p;
(iii) añadir de 0,08 a 0,3 partes en peso de la solución obtenida en la fase (ii) a 1,5-4 partes en peso de la solución obtenida en la fase (i) a una temperatura en un rango de 0 a 20 grados C en forma de una solución resultante;
(iv) calentar la solución resultante gradualmente a una temperatura en un rango de 50-90 grados C;
(v) enfriar gradualmente la solución resultante a una temperatura en un rango de 0 a 15 grados C para obtener un precipitado;
(vi) dejar reposar el precipitado durante un periodo de tiempo comprendido entre 0,5 y 8 horas a una temperatura en el rango de 0 a 15 grados C;
(vii) separar el precipitado de su licor madre por métodos convencionales; y
(viii) recristalizar el precipitado a partir de una mezcla de alcohol isopropílico (IPA), metanol y agua para conseguir gabapentina con una pureza superior al 99,5% y otro licor madre.
2. Procedimiento, según la reivindicación 1, en el que la cantidad de clorhidrato de gabapentina y agua utilizada en la fase (i) tiene una proporción entre 0,5 y 2,5 de agua con respecto a 1 parte del clorhidrato de gabapentina.
3. Procedimiento, según la reivindicación 1, en el que la solución de hidróxido sódico o potásico utilizada puede encontrarse en una concentración en un rango de 40-50% p/p en agua.
4. Procedimiento, según la reivindicación 1, en el que la temperatura utilizada en la etapa (iii) es de 10-20 grados C.
5. Procedimiento, según la reivindicación 1, en el que la temperatura utilizada en la etapa (iv) es de 50-70 grados C.
6. Procedimiento, según la reivindicación 1, en el que la temperatura utilizada en la etapa (v) se encuentra entre 5 y 15 grados C.
7. Procedimiento, según la reivindicación 1, en el que el tiempo utilizado para el reposo del precipitado en la etapa (vi) es de 0,5 a 3 horas.
8. Procedimiento, según la reivindicación 1, en el que la separación de gabapentina en la etapa (vii) se efectúa por filtrado.
9. Procedimiento, según la reivindicación 1, que comprende además el tratamiento de los licores madre obtenidos en las etapas (vii) y (viii) con una solución acuosa de hidróxido sódico en una concentración comprendida entre el 5 y el 20% a una temperatura comprendida entre 80 y 100 grados C, y la extracción con un disolvente orgánico para obtener gabalactama de fórmula 3.

10. Procedimiento, según la reivindicación 9, en el que la concentración de hidróxido sódico puede ser comprendida entre el 10 y el 20% y la temperatura puede variar entre 80 y 85 grados C.
11. Procedimiento, según la reivindicación 9, en el que el disolvente orgánico es seleccionado entre el grupo que consiste en tolueno, dicloruro de etileno, dicloruro de metileno y hexano.
Patentes similares o relacionadas:
Proceso para la preparación de un complejo de gadobenato dimeglumina en forma sólida, del 22 de Octubre de 2013, de Bracco Imaging SPA: Un proceso para la preparación de una forma sólida de un compuesto gadobenato dimeglumina,de fórmula :**Fórmula** comprendiendo el secado por pulverización […]
Oligoelemento en polvo, procedimiento y dispositivo para su fabricación, del 13 de Septiembre de 2013, de Pancosma S.A. (100.0%): Complejo organometalico hidrosoluble de glicina con un metal, en el que la glicina tiene un enlace con el metalpor los dos oxigenos de su grupo carbonilo, siguiendo la […]
Proceso y dispositivo para la fabricación de complejos organometálicos en polvo, del 25 de Julio de 2012, de Pancosma S.A. (100.0%): Proceso de fabricacion de un complejo organometalico cristalino en polvo a partir de aminoacidoshidrosolubles que comprende las siguientes […]
Disoluciones acuosas de alta concentración de N,N-dialquilglicina y procedimiento para la producción de las mismas, del 25 de Abril de 2012, de KAO CORPORATION: Una disolución acuosa de alta concentración de una N, N-dialquilglicina, producida a partir de una sal de metal alcalino de N, N-dialquilglicina como material […]
RECUPERACION DE UN AMINOACIDO., del 16 de Junio de 1999, de AECI LIMITED: UN METODO PARA RECUPERAR UN AMINOACIDO DESEADO TAL COMO UNA LLISINA DE UNA SOLUCION ACUOSA QUE CONTIENE EL AMINOACIDO DESEADO E IMPUREZAS, QUE INCLUYE […]
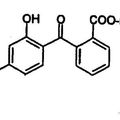 PROCEDIMIENTO PARA LA OBTENCION DE ESTERES DEL ACIDO 2-(4-N,N-DIALQUILAMINO-2-HIDROXIBENZOIL)BENZOICO, del 16 de Febrero de 2008, de BASF SE: Procedimiento para la obtención del éster de n-hexilo del ácido 2-(4-N, N-dietilamino-2-hidroxibenzoil)benzoico de la fórmula Ia mediante […]
PROCEDIMIENTO PARA LA OBTENCION DE ESTERES DEL ACIDO 2-(4-N,N-DIALQUILAMINO-2-HIDROXIBENZOIL)BENZOICO, del 16 de Febrero de 2008, de BASF SE: Procedimiento para la obtención del éster de n-hexilo del ácido 2-(4-N, N-dietilamino-2-hidroxibenzoil)benzoico de la fórmula Ia mediante […]
PROCEDIMIENTO PARA LA OBTENCION DE AMINOACIDOS CICLICOS., del 16 de Marzo de 2007, de MENADIONA, S.L.: Procedimiento para la obtención de aminoácidos cíclicos. La presente invención se refiere a un procedimiento para obtener aminoácidos cíclicos sustancialmente […]
Mezclas de agentes quelantes y procedimiento de fabricación de dichas mezclas, del 6 de Mayo de 2020, de BASF SE: Mezcla que comprende (A) Del 90 al 99,9% en peso de una mezcla de enantiómeros L y D del ácido metilglicildiacético (MGDA) o de sus respectivas sales […]