METODO ENZIMATICO PARA PRODUCIR ALFA-D-GLUCOSILGLICEROL (2-O-GLICERIL-ALFA-D-GLUCOPIRANOSIDA).
Método para producir 2-O-gliceril-a-D-glucopiranosida (aGG) a partir de un donador de glucosilo y un aceptor de glucosilo que comprende las etapas de:
- proporcionar una sacarosa fosforilasa (EC 2.4.1.7)
- incubar dicha sacarosa fosforilasa con una mezcla que comprende sacarosa como donador de glucosilo y glicerol como aceptor de glucosilo y
- aislamiento y/o purificación de 2-O-gliceril-a-D-glucopiranosida
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/AT2007/000448.
Solicitante: TECHNISCHE UNIVERSITAT GRAZ
FORSCHUNGSHOLDING TU GRAZ GMBH.
Nacionalidad solicitante: Austria.
Dirección: RECHBAUERSTRASSE 12,8010 GRAZ.
Inventor/es: GODL,CHRISTIANE, SAWANGWAN,THORNTHAN, NIDETZKY,BERND, MULLER,MARIO.
Fecha de Publicación: .
Fecha Concesión Europea: 24 de Marzo de 2010.
Clasificación Internacional de Patentes:
- A23L1/236D
- A61K8/60A
- A61Q19/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61Q USO ESPECIFICO DE COSMETICOS O DE PREPARACIONES SIMILARES PARA EL ASEO. › Preparaciones para el cuidado de la piel.
- A61Q19/10 A61Q […] › A61Q 19/00 Preparaciones para el cuidado de la piel. › Preparaciones para la limpieza o el baño.
- C12P19/44 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 19/00 Preparación de compuestos que contienen radicales sacárido (ácido cetoaldónico C12P 7/58). › Preparación de O-glucósidos, p. ej. glucósidos.
Clasificación PCT:
- C12P19/44 C12P 19/00 […] › Preparación de O-glucósidos, p. ej. glucósidos.
Fragmento de la descripción:
Método enzimático para producir a-D-glucosilglicerol (2-O-gliceril-a-D-glucopiranosida).
La presente invención se refiere a métodos para producir a-D-glucosilglicerol (2-O-gliceril-a-D-glucopiranosida).
Los hidratos de carbono simples y complejos rigen una diversa gama de funciones celulares, entre las que se incluyen el almacenamiento de energía, la estructura de la pared celular, la interacción y señalización célula-célula, las interacciones huésped-patógeno y la glicosilación de proteínas. También tienen una función como osmolitos y moléculas pequeñas de estilos de vida extremos. Las glicosiltransferasas (GTs) son enzimas responsables de la síntesis de glucosidos en la naturaleza, mientras que las glicosilhidrolasas (GHs) han sido evolucionadas para degradarlas. Entre las clases GT y GH, las glucósido fosforilasas (GPs) son especiales en varios sentidos. GPs catalizan la fosforolisis de a y ß-D-glicósidos, principalmente glicósidos (Glc-OR) incluyendo disacáridos y oligo- o polisacáridos de diversos grados de polimerización. La transferencia de glucosilo a fosfato (Pi) está favorecida termodinámicamente in vivo porque el fosfato normalmente está presente en un gran exceso con respecto a a-D-glucosa-1-fosfato (Glc-1-P). No obstante, las constantes de equilibrio termodinámico (Keq) de las reacciones catalizadas por GP son intermedias a los valores Keq para la reacción de GTs (Keq <<1) y GHs (Keq>>1). Los valores Keq favorables relativamente y el hecho de que los azúcares fosfo-activados sean menos caros que los activados por nucleótido, requeridos por la mayoría de las GTs, hacen que GPs sean unos biocatalizadores interesantes para la síntesis estéreo- y regioespecífica de glicósidos.
Recientemente se dedica una atención cada vez mayor hacia nuevos a-D-glicósidos, en particular, a-D-glucosil glicerilo (2-O-gliceril-a-D-glucopiranosida, aGG) para la cual se están desarrollando actualmente diversas aplicaciones. aGG funciona como un soluto compatible en microorganismos que proporciona cierta protección contra las tensiones producidas por altas concentraciones de sal, calor y radiación de UV. aGG es supuestamente útil como edulcorante alternativa en productos alimenticios debido a su baja cariogenicidad y su bajo valor calórico en comparación con la sacarosa. Por otra parte, se está estudiando aGG y sus derivados como productos terapéuticos en enfermedades causadas por un plegamiento fallido de proteínas y en terapia contra el cáncer. En cosmética aGG se puede emplear como agente anti envejecimiento y compuesto para regular la hidratación.
aGG se puede producir a través de métodos químicos, así como métodos enzimáticos. Los métodos químicos pueden implicar varios compuestos de partida como maltitol, isomaltosa, trehalulosa, etc. (ver, v.g., Takenaka F. y cols., Biosci. Biotechnol. Biochem. (2000) 64: 378-385). Las enzimas que catalizan la síntesis de aGG pueden implicar a-glucosidasa (Takenaka F. y Uchiyama H. Biosci. Biotechnol. Biochem. (2000) 64: 1821-1861), ciclodextrin glucanotransferasa (Nakano H. y cols., J. Biosci. Bioeng. (2003) 95: 583-588), glucosil-glicerolfosfato sintasa (Marin K. y cols., J. Bacteriol (1998) 180:4843-4849) y glucosidasa vegetal II (Kaushal GP y cols., Arch. Biochem. Biophys (1989) 272:481-487). Todos los procedimientos actuales para la síntesis de aGG presentan una o más de las siguientes desventajas cruciales: múltiples etapas de reacción (incluyendo activación, protección y desprotección); síntesis que requiere un trabajo y una elaboración intensivas; un bajo rendimiento y productividad; una baja economía atómica, tiempos de reacción prolongados. En consecuencia, no se ha desarrollado ningún proceso industrial para la producción de aGG y el producto no está disponible en el mercado.
La síntesis química de aGG natural esteréoquímicamente puro no es factible técnicamente debido a procedimientos extremadamente laboriosos y aun rendimiento bajo. La síntesis microbiana de aGG ha sido demostrado pero la productividad es escasa. La síntesis enzimática de aGG utilizando transglucosilación a través de a-glucosidasas es una posibilidad que ha sido descrita, pero el principal inconveniente del proceso es la errónea regioselectividad de las enzimas conocidas, que prefieren el grupo hidroxi primario en lugar de secundario de glicerol. La mezcla producto sintetizada a través de a-glucosidasas contiene solamente un 30% de aGG natural correcta, lo que requiere un esfuerzo sustancial para aislar el producto.
La síntesis microbiana de aGG actualmente no es un proceso maduro, sobre todo cuando se tiene en cuenta el rendimiento de aGG ya que no permite la producción de aGG como un producto químico en masa. Las concentraciones de producto que se pueden obtener son muy bajas (v.g., 29 mg/l; Roder y cols., FEMS Microbiol. Lett. (2005) 243: 219-226) y también la productividad (
JP 0509 1891 se refiere a un proceso para obtener componentes de azúcar que se comparan con una fracción de glucosa y una fracción de alcohol de azúcar unidos por reacción de sacarosa o ácido glucosa-1-fosfórico y un alcohol de azúcar en presencia de sacarosa fosforilasa.
En la publicación de Kitao S. y cols. (Biotec. Biochem. 56(1992): 2011-2014) se describe la transferencia de glucosa a varios aceptores por incubación de sacarosa fosforilasa con glucosa-1-fosfato y dichos aceptores de glucosa.
JP 2001/245690 A se refiere a un método para producir glicósidos y oligosacáridos utilizando una glucosidasa, en particular ß-galactosidasa.
El objeto de la presente invención consiste en proporcionar un método enzimático para la producción de aGG estéreoquímicamente puro en un alto rendimiento superando los inconvenientes de los métodos conocidos en la técnica. Asimismo, el método deberá permitir preferiblemente el uso de sustratos económicos.
Por consiguiente, la presente invención se refiere a un método para producir 2-O-gliceril-a-D-glucopiranosida (aGG) a partir de un donador de glucosilo y un aceptor de glucosilo que comprende las etapas de:
- proporcionar una sacarosa fosforilasa (EC 2.4.1.7)
- incubar dicha sacarosa fosforilasa con una mezcla que comprende sacarosa como donador de glucosilo y glicerol como aceptor de glucosilo y aislar y/o purificar 2-O-gliceril-a-D-glucopiranosida.
Sacarosa fosforilasa (SPasa; EC 2.4.1.7) cataliza la conversión de sacarosa y fosfato en D-fructosa y Glc 1-P. SPasa también ha sido aislada a partir de una serie de fuentes bacterianas. Los genes que codifican SPasa han sido clonados a partir de diferentes bacterias y han sido expresados heterólogamente (Kawasaki H y cols., Biosci. Biotech. Biochem. (1996) 60: 322-324; Kitao S. y Nakano E. J. Ferment. Bioeng. (1992) 73: 179-184; van den Broek LAM y cols. Appl. Microbiol. Biotechnol. (2004) 65: 219-227). De acuerdo con la clasificación basada en secuencias sistemáticas de glucosil hidrolasas (GH) y glicosil transferasas (GT) (Coultinho PM y cols., J. Mol. Biol. (2003) 328:307-317; Henrissat B. Biochem. J. (1999) 280:309-316) SPasa pertenece a la familia GH13 (Clan GH-H), denominada frecuentemente como la familia a-amilasa. La estructura tridimensional de SPasa desde Bifidobacterium adolescentis ha sido resuelta recientemente, revelando un plegamiento de barril (ß/a) 8 y un sitio catalítico en el que dos grupos carboxilato probablemente cumplen el papel de un nucleófilo (Asp 192) y un ácido/base general (Glu232).
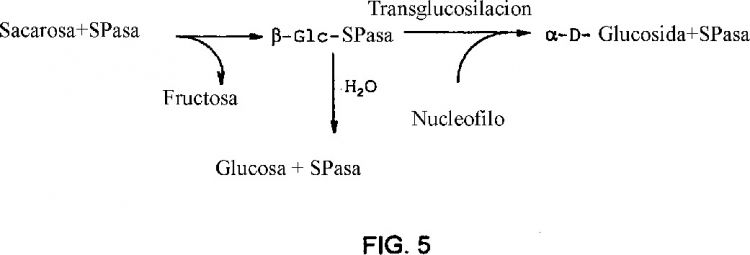
La reacción de SPasa prosigue con retención neta de la configuración anomérica y tiene lugar a través de un mecanismo de desplazamiento doble que implica dos etapas de inversión en la configuración: segmentación de la unión carbono-oxígeno del donador glucosilo y formación de un producto intermedio ß-glucosilo-enzima (ß-Glc-E) covalente; y la reacción del producto intermedio con fosfato para producir Glc 1-P. En una reacción lateral, el producto intermedio ß-Glc-E puede ser interceptado por agua, llevando a hidrólisis. La conversión hidrolítica de sacarosa es irreversible, pero prosigue casi dos órdenes de magnitud más lenta que la reacción fosforolítica. SPasa también cataliza las reacciones de transglucosilación que tienen lugar en competencia con la hidrólisis y de esta manera el producto intermedio ß-Glc-E es atacado por nucleófilos externos y se producen nuevos a-D-glicósidos.
Los estudios bioquímicos han demostrado que SPasa es estrictamente específica para transferir una...
Reivindicaciones:
1. Método para producir 2-O-gliceril-a-D-glucopiranosida (aGG) a partir de un donador de glucosilo y un aceptor de glucosilo que comprende las etapas de:
- proporcionar una sacarosa fosforilasa (EC 2.4.1.7)
- incubar dicha sacarosa fosforilasa con una mezcla que comprende sacarosa como donador de glucosilo y glicerol como aceptor de glucosilo y
- aislamiento y/o purificación de 2-O-gliceril-a-D-glucopiranosida.
2. Un método según la reivindicación 1, caracterizado porque la mezcla comprende un donador de glucosilo adicional seleccionado del grupo que consiste en a-D-glucosa-1-fosfato, a-D-glucosa-1-fluoruro y mezclas de ellos.
3. Método según la reivindicación 1 ó 2, caracterizado porque la sacarosa fosforilasa es de origen microbiano, preferiblemente de origen bacteriano.
4. Un método según la reivindicación 3, caracterizado porque la sacarosa fosforilasa bacteriana se obtiene de Agrobacterium vitis, Bifidobacterium adolescentis, Bifidobacterium longum, Escherichia coli, Escherichia coli 06, Lactobacilus acidophilus, Lactobacilus delbrueckii subsp. lactis, Leuconostoc mesenteroides, Listeria monocytogenes, Pseudomonas putrefaciens, Pseudomonas saccharophila, Rhodopirellula baltica, Shewanella baltica, Shewanella frigidimarina, Solibacter usitatus, Streptococcus mutans y/o Synechococcus sp.
5. Método según cualquiera de las reivindicaciones 1 a 4, caracterizado porque la sacarosa fosforilasa se produce por recombinación como proteína de longitud completa, o un fragmento catalíticamente activo de la misma, o una proteína de fusión.
6. El método según cualquiera de las reivindicaciones 1 a 5, caracterizado porque se inmoviliza la sacarosa fosforilasa antes de la etapa de incubación sobre un soporte.
7. El método según la reivindicación 6, caracterizado porque dicho soporte es un soporte sólido, preferiblemente un polímero, más preferiblemente un polímero acrílico, en particular, un copolímero de metacrilamida, N,N'-metilen-bis(acrilamida) y un monómero que lleva grupos oxirano.
8. El método según la reivindicación 6 ó 7, caracterizado porque el soporte es una resina de cromatografía, seleccionada preferiblemente del grupo que consiste en una resina de cromatografía de intercambio aniónico, una resina de cromatografía de intercambio de cationes, una resina de cromatografía de afinidad y una resina de cromatografía de interacción hidrófoba.
9. El método según cualquiera de las reivindicaciones 1 a 8, caracterizado porque la incubación se lleva a cabo a un valor de pH de 4 a 10, preferiblemente de 5 a 9, más preferiblemente de 6 a 8, en particular de 7, y/o durante al menos 15 minutos, preferiblemente, durante al menos 60 minutos, más preferiblemente durante al menos 3 horas, siendo más preferible incluso durante al menos 5 horas.
10. El método según cualquiera de las reivindicaciones 1 a 9, caracterizado porque la incubación se lleva a cabo a una temperatura comprendida entre 10 y 50ºC, preferiblemente de 15 a 40ºC, más preferiblemente a una temperatura de 30ºC.
11. El método según cualquiera de las reivindicaciones 1 a 10, caracterizado porque la mezcla comprende un donador de glucosilo en una concentración comprendida entre 0,01 y 3 moles/l, preferiblemente entre 0,05 y 2 moles/l, más preferiblemente entre 0,1 y 1,5 moles/l, y/o glicerol en una concentración comprendida entre 0,01 y 10 moles/l, preferiblemente, entre 0,05 y 5 moles/l, más preferiblemente entre 0,1 y 3 moles/l, siendo incluso más preferible entre 0,1 y 1,5 moles/l.
12. El método según cualquiera de las reivindicaciones 1 a 11, caracterizado porque la relación de glicerol a donador de glucosilo en la mezcla oscila entre 0,1:1 y 10:1, preferiblemente entre 0,5: 1 y 5:1, más preferiblemente entre 1:1 y 3:1.
13. El método según cualquiera de las reivindicaciones 1 a 12, caracterizado porque se aísla a-D-glucosilglicerol por cromatografía por elución sobre carbono activo en un rendimiento de 55%, preferiblemente 70%, más preferiblemente 85%.
14. El método según cualquiera de las reivindicaciones 1 a 13, caracterizado porque la sacarosa fosforilasa se obtiene a partir de Leuconostoc mesenteroides y se inmoviliza en un polímero acrílico, en particular, un copolímero de metacrilamida, N,N'-metilen-bis(acrilamida) y un polímero que lleva grupos oxirano, incubándose la sacaroasa fosforilasa inmovilizado con sacarosa como donador de glucosilo.
15. El método según la reivindicación 1 para producir una mezcla que contiene a-D-glucosilglicerol y fructosa que comprende las etapas de:
- proporcionar una sacarosa fosforilasa (EC 2.4.1.7),
- incubar dicha sacarosa fosforilasa con una mezcla que comprende sacarosa y glicerol como aceptor de glucosilo y
- aislar y/o purificar la mezcla de a-D-glucosilglicerol y fructosa.
Patentes similares o relacionadas:
Potenciador de la conservación, del 29 de Julio de 2020, de DSM IP ASSETS B.V.: Una composición tópica que comprende fitantriol y eritrulosa.
Uso de un compuesto que comprende al menos una función nucleófila para la captura de compuestos de carbonilo que resultan de la reacción entre uno o más compuestos que constituyen el sebo y el ozono, del 22 de Julio de 2020, de L'OREAL: Compuestos A que tienen una o más funciones nucleófilas FA capaces de reaccionar con uno o más compuestos carbonílicos B que resultan de la reacción entre uno o más compuestos […]
Procedimiento de preparación de una composición tópica a base de células vegetales desdiferenciadas e inducidas en cultivo in vitro, del 15 de Julio de 2020, de Naolys Sarl: Procedimiento de preparación de una composición de uso tópico que comprende un material derivado de células vegetales de una especie seleccionada entre […]
Analógicos biaromáticos de vitamina D, del 15 de Julio de 2020, de DSM IP ASSETS B.V.: Compuesto según la fórmula (I) **(Ver fórmula)** en la que · X e Y son ambos -CH2-, o uno de X e Y es -CH2- y el otro es -O-; y · R1 es un grupo metilo […]
Compuestos que presentan actividad antioxidante contra radicales libres y actividad anti-inflamatoria, y las correspondientes composiciones farmacéuticas o cosméticas para cuidado de la piel, del 8 de Julio de 2020, de GIULIANI S.P.A.: Un compuesto que tiene la fórmula general (I): **(Ver fórmula)** donde R = H, CH2-OH, CH2-O-CO-CH3, CH2-O-CO-Ph (Ph = fenilo) R' = H, CH2-O-CO-CH3, […]
Composición tópica que comprende extractos de boldo y de reina de los prados, destinada a un animal, y sus aplicaciones, del 6 de Julio de 2020, de Virbac SA: Composición tópica para animales, caracterizada por que comprende en un medio fisiológicamente aceptable extractos de boldo Peumus boldus y extractos de reina […]
Composiciones farmacéuticas para uso tópico basadas en ácido hialurónico sulfatado como promotor de absorción de la piel, del 1 de Julio de 2020, de FIDIA FARMACEUTICI S.P.A.: Una composición farmacéutica para uso tópico que contiene ácido hialurónico sulfatado como promotor de absorción de la piel de diclofenaco, ketoprofeno, ibuprofeno […]
Uso de principios activos refrescantes fisiológicos y agentes que contienen tales principios activos, del 17 de Junio de 2020, de Symrise AG: Procedimiento no terapéutico para la modulación in-vitro del receptor de mentol frío TRPM8, en el que se lleva a contacto el receptor con al menos un modulador, que se selecciona […]