METODO DE TRATAMIENTO QUE UTILIZA CONJUGADOS LIGANDO-INMUNOGENO.
Composición farmacéutica en una forma de dosificación parenteral que comprende cantidades terapéuticamente eficaces de un conjugado ligando-inmunógeno,
en el que el inmunógeno activa un receptor de tipo toll, en el que el inmunógeno es un nucleótido y en el que el ligando es ácido fólico u otro ligando de unión a receptor de folato y un portador farmacéuticamente aceptable para los mismos, caracterizada porque la composición comprende además IL-2, IL-4, IL-10, IL-11, IL-12, IL-15, IL-18, o combinaciones de las mismas
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US02/30546.
Solicitante: PURDUE RESEARCH FOUNDATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 3000 KENT AVENUE,WEST LAFAYETTE, IN 47906.
Inventor/es: LOW, PHILIP, STEWART, LU,YINGJUAN.
Fecha de Publicación: .
Fecha Concesión Europea: 16 de Diciembre de 2009.
Clasificación Internacional de Patentes:
- A61K31/711 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Acidos desoxirribonucleicos naturales, es decir conteniendo unicamente 2'-desoxirribosas unidas a la adenina, la guanina, la citosina o la timina y teniendo enlaces 3'-5' fosfodiester.
- A61K47/48H4S
Clasificación PCT:
- A61K47/48
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
Clasificación antigua:
- A61K31/00 A61K […] › Preparaciones medicinales que contienen ingredientes orgánicos activos.
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- A61K39/395 A61K […] › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61K39/40 A61K 39/00 […] › bacterianos.
- A61K39/42 A61K 39/00 […] › virales.
- A61K48/00 A61K […] › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
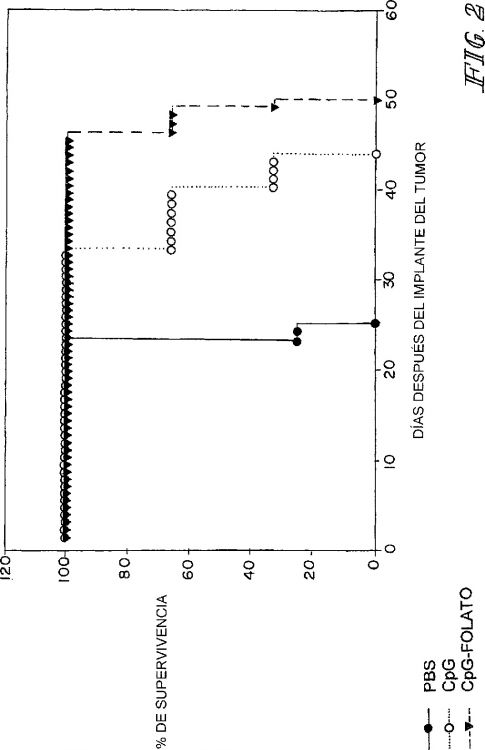
Fragmento de la descripción:
Método de tratamiento que utiliza conjugados ligando-inmunógeno.
Sector de la invención
La presente invención se refiere a una composición farmacéutica para su utilización en el tratamiento de estados patológicos caracterizados por la existencia de poblaciones de células patogénicas. Más particularmente, se administran complejos ligando-inmunógeno dirigidos a células a un huésped patológico, opcionalmente en combinación con un estimulador del sistema inmune, para aumentar y/o redirigir las respuestas inmunes del huésped a las células patogénicas.
Antecedentes y características de la invención
El sistema inmune de los mamíferos proporciona un medio para el reconocimiento y la eliminación de células tumorales, otras células patogénicas y la invasión de patógenos exógenos. Aunque el sistema inmune proporciona normalmente una línea fuerte de defensa, existen aún muchos casos en los que las células cancerosas, otras células patogénicas, o agentes infecciosos, eluden una respuesta inmune del huésped y proliferan o persisten con la patogenicidad concomitante del huésped. Se han desarrollado agentes quimioterapéuticos y terapias con radiación para eliminar neoplasmas replicantes. Sin embargo, la mayoría de los agentes quimioterapéuticos, si no todos, disponibles actualmente y los regímenes de terapia con radiación presentan efectos secundarios adversos ya que no sólo trabajan para destruir células cancerosas, sino también afectan a células huésped normales, tales como células del sistema hematopoyético. Además, los agentes quimioterapéuticos tienen una eficacia limitada en casos en los que se desarrolla resistencia del huésped al fármaco.
Los patógenos exógenos también pueden proliferar en un huésped evitando una respuesta inmune competente o cuando el sistema inmune del huésped se ha comprometido por terapias con fármacos o por otros problemas de salud. Aunque se han desarrollado muchos compuestos terapéuticos, muchos patógenos son o se vuelven resistentes a dichos agentes terapéuticos. La capacidad de las células cancerosas y los organismos infecciosos de desarrollar resistencia a los agentes terapéuticos, y los efectos secundarios adversos de los fármacos anticáncer disponibles actualmente, destacan la necesidad de desarrollar nuevas terapias específicas para poblaciones de células patogénicas con una toxicidad menor para el huésped.
Los investigadores han desarrollado protocolos terapéuticos para destruir células cancerosas dirigiendo compuestos citotóxicos específicamente a dichas células. Estos protocolos utilizan toxinas conjugadas a ligandos que se unen a receptores únicos para las células cancerosas o sobreexpresadas por éstas en un intento por minimizar la liberación de la toxina a células normales. Utilizando esta estrategia, se han desarrollado ciertas inmunotoxinas que consisten en anticuerpos dirigidos a receptores específicos en células patogénicas, estando los anticuerpos unidos a toxinas, tales como ricina, exotoxina de Pseudomonas, toxina de la difteria y el factor de necrosis tumoral. Estas inmunotoxinas reconocen células tumorales que transportan los receptores específicos reconocidos por el anticuerpo (Olsnes, S., Immunol. Today, 10, págs. 291-295, 1989; Melby, E.L., Cancer Res., 53 (8), págs. 1755-1760, 1993; Better, M.D., Publicación PCT No. WO 91/07418, publicada el 30 de mayo de 1991).
Otra estrategia para el reconocimiento selectivo de poblaciones de células cancerosas o patógenos exógenos en un huésped es aumentar la respuesta inmune del huésped contra las células patogénicas, evitando de este modo la necesidad de administrar compuestos que también pueden mostrar una toxicidad independiente para el huésped. Una estrategia divulgada para la inmunoterapia es la de unir anticuerpos, por ejemplo, anticuerpos multiméricos diseñados genéticamente, a la superficie de la célula tumoral para expresar la región constante de los anticuerpos en la superficie celular e inducir, de este modo, la citólisis de la célula tumoral mediante diversos procesos mediados por el sistema inmune (De Vita, V.T., Biologic Therapy of Cancer (Terapia biológica del cáncer), 2a ed. Philadelphia, Lippincott, 1995; Soulillou, J.P., patente de Estados Unidos No. 5.672.486). Sin embargo, esta estrategia se ha complicado por las dificultades en la definición de antígenos específicos para tumores. Otra estrategia que depende de la competencia inmune del huésped es dirigir un anticuerpo anti-receptor de células T o anticuerpos anti-receptor Fc a las superficies de células tumorales para promover la unión directa de las células inmunes a los tumores (Kranz, D. M., patente de Estados Unidos No. 5.547.668). También se ha descrito una estrategia basada en vacunas que depende de una vacuna que comprende antígenos fusionados a citoquinas, modificando la citoquina la inmunogenicidad del antígeno de la vacuna y, de este modo, estimulando la respuesta inmune al agente patogénico (Pillai, S., Publicación PCT No. WO 91/11146, publicada el 7 de febrero de 1991). Este método depende de la modulación indirecta de la respuesta inmune descrita. Otra estrategia para la citólisis de poblaciones de células no deseadas utiliza IL-1 o fragmentos de Fab de globulina anti-timocito unida a antígenos para eliminar las células T no deseadas; sin embargo, en base a los datos experimentales descritos, el método parece eliminar sólo el 50% de la población de células reconocidas y da lugar a una citólisis no específica in vivo (es decir, el 50% de los linfocitos de la sangre periférica que no son células T también mueren (Pouletty, P., Publicación PCT No. WO 97/37690, publicada de 16 de octubre de 1997). De este modo, aún existe una necesidad significativa de terapias dirigidas al tratamiento de estados patológicos caracterizados por la existencia de poblaciones de células patogénicas en un huésped afectado.
La inmunidad se puede clasificar como inmunidad innata o adaptativa, siendo la inmunidad adaptativa mediada por las células T y las células B que muestran especificidad y memoria. La respuesta inmune innata es una respuesta inmediata que puede ser mediada por células fagocíticas, células citolíticas naturales, células T, y otras células, y el sistema complemento. Las células fagocíticas, tales como monocitos/macrófagos y células dendríticas (células que presentan antígenos), llevan a cabo funciones duales que incluyen la eliminación y la degradación de agentes infecciosos o antígenos exógenos y la presentación de los componentes de los patógenos ingeridos a células T intactas en el contexto de autoantígenos MHC o de tipo MHC. Las células T intactas reconocen el antígeno exógeno en el contexto de antígenos MHC o de tipo MHC y se diferencian en células TH1 o TH2 maduras que, a continuación, pueden inducir la inmunidad adaptativa.
Las células inmunes que median en la inmunidad innata son capaces de distinguir entre agentes propios y agentes patogénicos mediante la utilización de receptores en la superficie de estas células que reconocen motivos conservados en los patógenos que no están presentes en eucariotas superiores. Una de dichas clases de receptores es la familia de receptores de tipo toll que se conservan entre insectos y humanos y se identificaron por primera vez en Drosophila.
La familia de receptores de tipo toll contiene, como mínimo, diez miembros (TLRs 1-10) y los receptores de tipo toll están presentes en la superficie de monocitos/macrófagos y células dendríticas. Los receptores de tipo toll se activan a través del reconocimiento de motivos conservados en los patógenos, pero no se sabe si la activación tiene lugar a través de la unión directa del motivo conservado al receptor de tipo toll o a través de la unión a un receptor de acceso que interacciona con el receptor de tipo toll. La activación de los receptores de tipo toll da lugar a la secreción de citoquinas y la inducción de una respuesta inmune innata en la que las células T intactas se diferencian en células TH1 o TH2. De este modo, los receptores de tipo toll pueden proporcionar una unión crítica entre el reconocimiento inmune innato y la posterior activación de la inmunidad adaptativa.
Las moléculas capaces de activar los receptores de tipo toll pueden ser componentes de agentes patogénicos, tales como dipéptido muramilo, LPS, lipopéptidos, lipoproteínas, peptidoglicano, ácido lipoteicoico, lipoarabinomanano, y Zymosan (un preparado de pared celular de levadura), o pueden ser otras moléculas endógenas a un huésped, tal como fibronectina o proteína de choque térmico. Estas...
Reivindicaciones:
1. Composición farmacéutica en una forma de dosificación parenteral que comprende cantidades terapéuticamente eficaces de un conjugado ligando-inmunógeno, en el que el inmunógeno activa un receptor de tipo toll, en el que el inmunógeno es un nucleótido y en el que el ligando es ácido fólico u otro ligando de unión a receptor de folato y un portador farmacéuticamente aceptable para los mismos, caracterizada porque la composición comprende además IL-2, IL-4, IL-10, IL-11, IL-12, IL-15, IL-18, o combinaciones de las mismas.
2. Composición farmacéutica, según la reivindicación 1, que comprende además IL-2, IL-4, IL-10, IL-11, IL-12, IL-15, IL-18, o combinaciones de las mismas, en combinación con IFN-a o IFN-?.
3. Composición farmacéutica en una forma de dosificación parenteral que comprende cantidades terapéuticamente eficaces de un conjugado ligando-inmunógeno, en el que el inmunógeno activa un receptor de tipo toll, en el que el inmunógeno es un nucleótido y en el que el ligando es ácido fólico u otro ligando de unión a receptor de folato y un portador farmacéuticamente aceptable para los mismos, caracterizada porque la composición comprende además IL-2, IL-4, IL-10, IL-11, IL-12, IL-15, IL-18, IFN-a, IFN-?, GM-CSF, o combinaciones de las mismas.
4. Composición farmacéutica, según las reivindicaciones 1 a 3, en la que el ligando se conjuga al inmunógeno a través de una unión que comprende un enlace covalente, iónico o de hidrógeno.
5. Composición farmacéutica, según cualquiera de las reivindicaciones anteriores, en la que el inmunógeno es un nucleótido CpG.
6. Composición farmacéutica, según cualquiera de las reivindicaciones anteriores, en una forma de dosificación de liberación prolongada parenteral.
7. Utilización de una composición farmacéutica en una forma de dosificación parenteral que comprende cantidades terapéuticamente eficaces de un conjugado ligando-inmunógeno y en el que el inmunógeno activa un receptor de tipo toll y en el que el inmunógeno es un nucleótido y en el que el ligando es ácido fólico u otro ligando de unión a receptor de folato, en la preparación de un medicamento para el tratamiento del cáncer, caracterizado porque el medicamento comprende además IL-2, IL-4, IL-10, IL-11, IL-12, IL-15, IL-18, o combinaciones de las mismas.
8. Utilización, según la reivindicación 6, en la que el medicamento comprende además IL-2, IL-4, IL-10, IL-11, IL-12, IL-15, IL-18, o combinaciones de las mismas, en combinación con IFN-a o IFN-?.
9. Utilización de una composición farmacéutica en una forma de dosificación parenteral que comprende cantidades terapéuticamente eficaces de un conjugado ligando-inmunógeno, en el que el inmunógeno activa un receptor de tipo toll y en el que el inmunógeno es un nucleótido y en el que el ligando es ácido fólico u otro ligando de unión a receptor de folato, en la preparación de un medicamento para el tratamiento del cáncer, caracterizado porque el medicamento comprende además IL-2, IL-4, IL-10, IL-11, IL-12, IL-15, IL-18, IFN-a, IFN-?, GM-CSF, o combinaciones de las mismas.
10. Utilización, según las reivindicaciones 7 a 9, en la que el ligando se conjuga al inmunógeno a través de una unión que comprende un enlace covalente, iónico o de hidrógeno.
11. Utilización, según las reivindicaciones 7 a 10, en la que el inmunógeno es un nucleótido CpG.
12. Utilización, según cualquiera de las reivindicaciones anteriores 7 a 11, en la que el medicamento es una forma de dosificación de liberación prolongada parenteral.
13. Composición farmacéutica, según las reivindicaciones 1-6, en una forma de dosificación parenteral que comprende cantidades terapéuticamente eficaces de un conjugado ligando-inmunógeno para su utilización en la activación de un receptor de tipo toll, en el que el inmunógeno es un nucleótido y en el que el ligando es ácido fólico u otro ligando de unión a receptor de folato y un portador farmacéuticamente aceptable para los mismos, en combinación con IL-2, IL-4, IL-10, IL-11, IL-12, IL-15, IL-18, IFN-a, IFN-?, GM-CSF, o combinaciones de las mismas.
Patentes similares o relacionadas:
Péptido para inducir regeneración de tejido y uso del mismo, del 4 de Marzo de 2020, de StemRIM Inc: Un péptido que consiste en una porción de una proteína HMGB1 y tiene una actividad de estimulación de la migración de una célula, donde dicho péptido consiste en una cualquiera […]
Moléculas de unión a ligando y usos de las mismas, del 25 de Diciembre de 2019, de Vegenics Pty Limited: Una molécula de unión a ligando que comprende un polipéptido de unión a ligando fusionado a un fragmento de dominio constante de inmunoglobulina, comprendiendo […]
Compuestos inhibitorios dirigidos a conexina 43 y sus métodos de uso en el tratamiento del trauma ocular de la córnea, del 4 de Septiembre de 2019, de Ocunexus Therapeutics, Inc: Un compuesto de inhibición de conexina 43 que inhibe, en su totalidad o en parte, la expresión o actividad de una conexina 43 para su uso en un método para tratar un sujeto […]
Composiciones de SYN3 y métodos, del 12 de Junio de 2019, de MERCK SHARP & DOHME CORP: Una composicion farmaceutica liofilizada que comprende N-(3-colamidopropil)-N-(3(actobionamidopropil))-colamida (SYN3), hidroxipropil-beta-ciclodextrina (HPßCD) y un sistema […]
Métodos y composiciones farmacéuticas para el tratamiento de fibrosis quística, del 10 de Junio de 2019, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un oligonucleótido que comprende una secuencia de ácido nucleico seleccionada del grupo que consiste en SEQ ID NO: 1, SEQ ID NO: 2 y SEQ ID NO: 3, en donde dicho […]
Agente para la profilaxis y el tratamiento de infecciones víricas, del 8 de Mayo de 2019, de Secarna Pharmaceuticals GmbH & Co. KG: Agente para la profilaxis y el tratamiento de infecciones víricas causadas por picornavirus, caracterizado por el hecho de que comprende al menos una ADNzima […]
Ácido nucleico antisentido, del 26 de Abril de 2019, de National Center of Neurology and Psychiatry: Un oligómero antisentido que se selecciona de un grupo que consiste en de (a) a (c) a continuación, o una sal o hidrato farmacéuticamente aceptable […]
Ácido poli(beta málico) con tripéptido colgante Leu-Leu-Leu para la administración eficaz del fármaco citoplasmático, del 25 de Abril de 2019, de CEDARS-SINAI MEDICAL CENTER: Una molécula de administración de fármacos que comprende un andamio molecular de ácido polimálico unido covalentemente a uno o más módulos […]