MEDIOS PARA CULTIVO CELULAR.
Procedimiento de producción de un polvo de medio nutritivo aglomerado,
un polvo de complemento de medio aglomerado, un polvo de subgrupo de medio nutritivo aglomerado o un polvo de tampón aglomerado, comprendiendo el procedimiento:
aglomerar un polvo de medio nutritivo, polvo de complemento de medio, polvo de subgrupo de medio nutritivo o polvo de tampón, con un disolvente que comprende al menos un lípido disuelto en el mismo,
suministrar el disolvente al menos un lípido para su incorporación en el polvo de medio nutritivo, polvo de complemento de medio, polvo de subgrupo de medio nutritivo o polvo de tampón, y
en el que el al menos un lípido se compleja con una ciclodextrina
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US02/38230.
Solicitante: LIFE TECHNOLOGIES CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 5791 VAN ALLEN WAY,CARLSBAD, CA 92008.
Inventor/es: FIKE,RICHARD, RADOMINSKI,ROBERT, DADEY,BARBARA, HASSETT,RICHARD.
Fecha de Publicación: .
Fecha Concesión Europea: 31 de Marzo de 2010.
Clasificación Internacional de Patentes:
- C12N5/00M
Clasificación PCT:
- C12N5/02 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Propagación de células individuales o de células en suspensión; Su conservación; Medios de cultivo para este fin.
Clasificación antigua:
- C12N5/02 C12N 5/00 […] › Propagación de células individuales o de células en suspensión; Su conservación; Medios de cultivo para este fin.
Fragmento de la descripción:
Medios para cultivo celular.
Campo de la invención
La presente invención se refiere de forma general a células, medios nutritivos, complementos de medios, subgrupos de medios y formulaciones tampón. Específicamente, la presente invención proporciona formulaciones de medio nutritivo en polvo seco, particularmente formulaciones de medio de cultivo celular, que comprenden todos los factores nutritivos necesarios que facilitan el cultivo in vitro de las células, y a procedimientos de producción de estas formulaciones de medios. La presente invención se refiere específicamente a procedimientos que incorporan lípidos y/u otros componentes escasamente solubles en disolventes inorgánicos o polares tales como agua. La invención también se refiere a procedimientos de producción de complementos de medios en polvo seco, tales como sueros en polvo seco (por ejemplo, suero bovino fetal) con ingredientes complementarios tales como lípidos u otros ingredientes útiles para soportar el cultivo celular. La invención también se refiere a formulaciones tampón en polvo seco que producen condiciones iónicas y de pH particulares tras la rehidratación. La invención también se refiere a procedimientos de preparación de medios nutritivos, complementos de medios (particularmente sueros en polvo seco), subgrupos de medios y formulaciones tampón en polvo seco estériles preparados con aditivos solubles en disolventes orgánicos o apolares. La invención también se refiere a medios nutritivos, complementos de medios, subgrupos de medios, formulaciones tampón en polvo seco y células preparadas mediante los procedimientos de la invención. La presente invención también se refiere a kits y procedimientos para el cultivo de células procariotas y eucariotas que usan estos medios nutritivos, complementos de medios, subgrupos de medios y formulaciones tampón en polvo seco.
Antecedentes de la invención
Medios de cultivo celular
Los medios de cultivo celular proporcionan nutrientes para mantener y/o hacer crecer células en un entorno controlado, artificial e in vitro. Las características y composiciones de los medios de cultivo celular varían dependiendo de los requisitos celulares particulares y cualquier función para la que se cultivan las células. Los parámetros importantes incluyen osmolalidad, pH y formulaciones de nutrientes. El entorno normal de una célula en cultivo es un medio acuoso en el que se disuelven o suspenden los nutrientes y otros componentes del cultivo. Es especialmente ventajosa la incorporación de cantidades útiles de lípidos u otros componentes que son sólo escasamente solubles en agua.
Se han utilizado formulaciones de medios para cultivar una serie de tipos de células incluyendo células animales, vegetales y bacterianas. Las células cultivadas en medios de cultivo catabolizan los nutrientes disponibles y producen sustancias biológicas útiles tales como anticuerpos monoclonales, hormonas, factores de crecimiento, virus, factores antigénicos, enzimas, citocinas y similares. Tales productos tienen aplicaciones industriales y/o terapéuticas y, con la llegada de la tecnología del ADN recombinante, pueden modificarse células mediante ingeniería para que produzcan grandes cantidades de estos productos. Por tanto, la capacidad para cultivar células in vitro no sólo es importante para el estudio de la fisiología celular, sino que también es necesaria para la producción de sustancias útiles que no pueden obtenerse de otra manera por medios rentables.
Las formulaciones de medios de cultivo celular se han documentado bien en la bibliografía y una serie de medios están disponibles comercialmente. En los primeros trabajos de cultivo celular, las formulaciones de los medios se basaron en la composición química y las propiedades fisicoquímicas (por ejemplo, osmolalidad, pH, etc.) de la sangre y se denominaron "soluciones fisiológicas" (Ringer, S., J. Physiol. 3:380-393 (1880); Waymouth, C., En: Cells and Tissues in Culture, Vol. 1, Academic Press, Londres, págs. 99-142 (1965); Waymouth, C., In Vitro 6:109-127 (1970)). Sin embargo, las células en diferentes tejidos de organismos multicelulares, por ejemplo, plantas, invertebrados incluyendo insectos, vertebrados incluyendo peces y mamíferos están expuestos a diferentes microentornos con respecto a la presión parcial de oxígeno/dióxido de carbono y las concentraciones de nutrientes, vitaminas y oligoelementos; por consiguiente, el cultivo in vitro satisfactorio de diferentes tipos celulares con frecuencia requerirá el uso de diferentes formulaciones de medios. Los componentes típicos de los medios de cultivo celular incluyen aminoácidos, sales orgánicas e inorgánicas, vitaminas, metales traza, azúcares, lípidos y ácidos nucleicos, cuyos tipos y cantidades pueden variar dependiendo de los requisitos particulares de un tipo de célula o tejido dado y el fin al que se aplica la célula. Con frecuencia, particularmente en composiciones de medios complejos, los problemas de estabilidad dan como resultado productos tóxicos y/o menores concentraciones eficaces de los nutrientes requeridos, limitando de ese modo la vida funcional de los medios de cultivo. Por ejemplo, la glutamina es un constituyente de casi todos los medios que se usan en el cultivo de células de mamíferos in vitro. La glutamina se descompone espontáneamente en ácido pirrolidona-carboxílico y amoniaco. La velocidad de degradación puede estar influenciada por las condiciones iónicas y de pH pero en los medios de cultivo celular, con frecuencia no puede evitarse la formación de estos productos de degradación. (Tritsch et al., Exp. Cell Res. 28:360-364 (1962)).
Wang et al. (In Vitro 14(8):715-722 (1978)) han demostrado que se producen fotoproductos tales como peróxido de hidrógeno, que son letales para las células, en el medio de Eagle modificado por Dulbecco (DMEM). La riboflavina y el triptófano o la tirosina son componentes necesarios para la formación de peróxido de hidrógeno durante la exposición a la luz. Dado que la mayoría de los medios de cultivo para mamíferos contienen riboflavina, tirosina y triptófano, es probable que se produzcan fotoproductos tóxicos en la mayoría de los medios de cultivo celular.
Para evitar estos problemas, los investigadores preparan los medios "cuando es necesario", y evitan el almacenamiento a largo plazo de los medios de cultivo. Los medios disponibles comercialmente, normalmente en forma de polvo seco, son una alternativa conveniente a preparar los medios desde cero, es decir, añadiendo cada nutriente individualmente, y también evitan algunos de los problemas de estabilidad asociados con los medios líquidos. Sin embargo, sólo está disponible un número limitado de medios de cultivo comerciales, a excepción de aquellas formulaciones a medida suministradas por el fabricante.
Los líquidos (medios acuosos) con frecuencia se complementan con concentrado lipídico, por ejemplo, el lípido Lipid Concentrate (100X), disponible de GIBCO de Invitrogen Corporation, Carlsbad, California. Convencionalmente los medios en polvo no podían contener eficazmente componentes que no fueran fácilmente solubles en agua, el disolvente más común utilizado para la reconstitución. Por tanto, después de que se reconstituya un polvo para formar un medio, frecuentemente se añaden componentes adicionales con una pequeña cantidad de disolvente orgánico tal como alcoholes (por ejemplo, metanol, etanol, glicoles, etc.), éteres (por ejemplo, MEK), cetonas (por ejemplo, acetona), DMSO, etc. Estos disolventes deben usarse con moderación ya que generalmente provocan efectos tóxicos o indeseados en las células que están cultivándose. La toxicidad y la solubilidad interaccionan limitando la cantidad del componente deseado que puede añadirse al cultivo.
Aunque las formulaciones de medios en polvo seco pueden aumentar la vida útil de almacenamiento de algunos medios, existen varios problemas asociados con los medios en polvo seco, especialmente en la aplicación a gran escala. La producción de grandes volúmenes de medios requiere instalaciones de almacenamiento para los medios de polvo seco, por no mencionar las cocinas especializadas para los medios necesarias para mezclar y pesar los componentes de nutrientes. Debido a la naturaleza corrosiva de los medios de polvo seco, los tanques de mezclado deben sustituirse periódicamente.
Normalmente, las formulaciones de medios de cultivo celular se complementan con una gama de aditivos, incluyendo componentes indefinidos tales como suero bovino fetal (FBS) (por ejemplo, al 10-20%, 5-10%, 1-5%, 0,1-1% v/v) o extractos o hidrolizados...
Reivindicaciones:
1. Procedimiento de producción de un polvo de medio nutritivo aglomerado, un polvo de complemento de medio aglomerado, un polvo de subgrupo de medio nutritivo aglomerado o un polvo de tampón aglomerado, comprendiendo el procedimiento:
aglomerar un polvo de medio nutritivo, polvo de complemento de medio, polvo de subgrupo de medio nutritivo o polvo de tampón, con un disolvente que comprende al menos un lípido disuelto en el mismo,
suministrar el disolvente al menos un lípido para su incorporación en el polvo de medio nutritivo, polvo de complemento de medio, polvo de subgrupo de medio nutritivo o polvo de tampón, y
en el que el al menos un lípido se compleja con una ciclodextrina.
2. Procedimiento según la reivindicación 1, en el que la ciclodextrina es ß-metilciclodextrina.
3. Procedimiento según cualquier reivindicación anterior, en el que la aglomeración comprende aglomeración en lecho fluidizado.
4. Procedimiento según cualquier reivindicación anterior, en el que el disolvente está en fase líquida.
5. Procedimiento según cualquier reivindicación anterior, en el que el lípido está en forma de una sal.
6. Procedimiento según cualquier reivindicación anterior, en el que el lípido tiene uno o más grupos hidroxilo.
7. Procedimiento según cualquier reivindicación anterior, en el que el disolvente es una mezcla.
8. Procedimiento según la reivindicación 7, en el que la mezcla es una mezcla de líquidos.
9. Procedimiento según la reivindicación 7 o la reivindicación 8, en el que la mezcla comprende al menos un disolvente polar.
10. Procedimiento según la reivindicación 7 o la reivindicación 8, en el que la mezcla comprende al menos un disolvente apolar.
11. Procedimiento según la reivindicación 7 o la reivindicación 8, en el que la mezcla comprende al menos un disolvente orgánico.
12. Procedimiento según la reivindicación 7 o la reivindicación 8, en el que la mezcla comprende un 20%-95% de disolvente orgánico.
13. Procedimiento según la reivindicación 7, en el que la mezcla comprende al menos un disolvente seleccionado del grupo constituido por: (a) al menos un disolvente polar; y (b) al menos un disolvente orgánico o al menos un disolvente apolar.
14. Procedimiento según la reivindicación 13, en el que la mezcla comprende los disolventes en razón del 1% al 99% de (a) el al menos un disolvente polar con (b) el al menos un disolvente orgánico o el al menos un disolvente apolar.
15. Procedimiento según la reivindicación 14, en el que la mezcla comprende un 40-60% del al menos un disolvente orgánico o del al menos un disolvente apolar.
16. Procedimiento según la reivindicación 14, en el que la mezcla comprende un 50% de (a) el al menos un disolvente polar y el 50% de (b) el al menos un disolvente orgánico o el al menos un disolvente apolar.
17. Procedimiento según la reivindicación 7, en el que la mezcla comprende agua y al menos un disolvente seleccionado del grupo constituido por dimetilsulfóxido, alcoholes, éteres y cetonas.
18. Procedimiento según la reivindicación 8, en el que la mezcla comprende agua y alcohol.
19. Procedimiento según la reivindicación 8 ó 18, en el que la mezcla comprende agua y etanol.
20. Procedimiento según la reivindicación 7, en el que la mezcla comprende al menos un disolvente seleccionado del grupo constituido por dimetilsulfóxido, alcoholes, éteres y cetonas.
21. Procedimiento según la reivindicación 20, en el que la mezcla comprende aproximadamente un 40-60% de etanol.
22. Procedimiento según la reivindicación 20, en el que la mezcla comprende aproximadamente un 50% de etanol.
23. Procedimiento según la reivindicación 7, en el que el disolvente comprende una mezcla de al menos dos disolventes seleccionados del grupo constituido por disolventes apolares y disolventes orgánicos.
24. Procedimiento según la reivindicación 1, en el que el disolvente es agua.
25. Procedimiento según la reivindicación 1, en el que la ciclodextrina se disuelve en agua, y después se añade una mezcla de lípido/alcohol a la disolución de ciclodextrina, antes de la aglomeración.
26. Procedimiento según cualquier reivindicación anterior, en el que el suministro se lleva a cabo en condiciones que comprenden al menos una de temperatura controlada, humedad controlada y presión parcial controlada del/de los disolvente(s).
27. Procedimiento según cualquier reivindicación anterior, en el que el lípido se selecciona del grupo constituido por ácido linoleico, ácido lipoico, ácido araquidónico, ácido palmítico, ácido oleico, ácido palmitoleico, ácido esteárico, ácido mirístico, ácido linolénico, fosfatidiletanolamina, fosfatidilcolina, esfingomielina, cardiolipina, vitamina A, vitamina E, vitamina K, prostaglandina y un esterol.
28. Procedimiento según la reivindicación 27, en el que dicho esterol es un esterol vegetal o uno animal.
29. Procedimiento según la reivindicación 27, en el que el esterol es colesterol.
30. Polvo de medio nutritivo aglomerado, polvo de complemento de medio aglomerado, polvo de subgrupo de medio nutritivo aglomerado o polvo de tampón aglomerado, preparados según el procedimiento de las reivindicaciones 1-27.
31. Polvo según la reivindicación 30 que tiene una formación de polvo fino reducida en comparación con un polvo de medio nutritivo no aglomerado.
32. Polvo según la reivindicación 30 que tiene una solubilidad más completa en comparación con un polvo de medio nutritivo no aglomerado.
33. Polvo según la reivindicación 30 que tiene menos material insoluble en comparación con un polvo de medio nutritivo no aglomerado.
34. Polvo según la reivindicación 30 que tiene una disolución más rápida en comparación con un polvo de medio nutritivo no aglomerado.
35. Polvo según la reivindicación 30, en el que el polvo de medio nutritivo está libre de suero.
36. Polvo según la reivindicación 30, en el que el polvo de medio nutritivo está libre de componentes de mamíferos.
37. Polvo según la reivindicación 30, en el que el polvo de medio nutritivo está libre de componentes animales.
38. Procedimiento de cultivo de una célula que comprende: (a) reconstituir el polvo aglomerado según cualquiera de las reivindicaciones 30 a 37 con un disolvente para formar una disolución líquida; y (b) poner en contacto la célula con la disolución líquida en condiciones que favorecen el cultivo de la célula.
39. Procedimiento según la reivindicación 38, en el que la célula es una célula seleccionada del grupo constituido por célula bacteriana, célula de insectos, célula de levaduras, célula de nematodos, célula de aves, célula de anfibios, célula de reptiles y célula de mamíferos.
40. Procedimiento según la reivindicación 38, en el que la célula es una célula de mamíferos.
41. Procedimiento según la reivindicación 40, en el que la célula de mamíferos se selecciona del grupo constituido por una célula CHO, una célula COS, una célula VERO, una célula BHK, una célula AE-1, una célula SP2/0, una célula L5.1, una célula PerC6, una célula 293 y una célula de hibridoma.
42. Procedimiento según la reivindicación 40, en el que la célula de mamíferos es una célula humana.
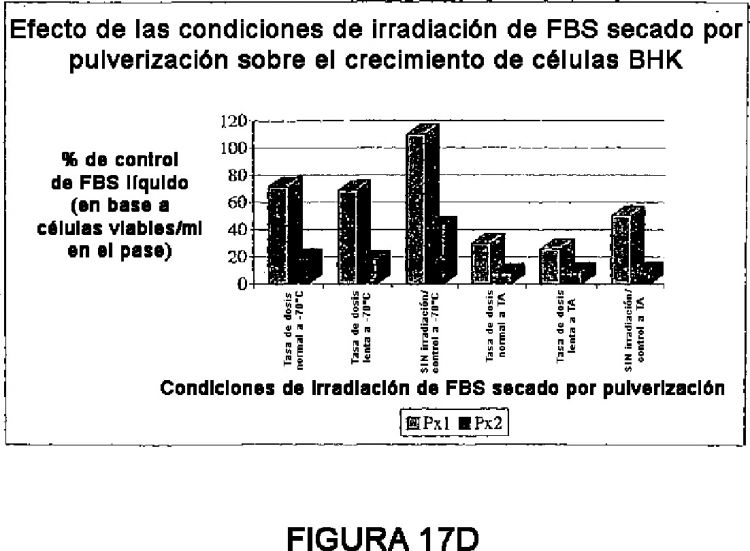
43. Procedimiento según cualquiera de las reivindicaciones 38 a 42 en el que el crecimiento de la célula a los 3, 4, 7, 10, 14, 28, 30, 60 ó 90 días es del 50%-120% en comparación con el crecimiento de la célula en el mismo momento en un medio líquido con lípido añadido.
Patentes similares o relacionadas:
COMPOSICIÓN PARA LA CREACIÓN, REGENERACIÓN Y REPARACIÓN TISULAR MEDIANTE UN IMPLANTE BIOLÓGICO QUE PORTA CÉLULAS ENRIQUECIDO CON CONCENTRADO DE PLAQUETAS Y COMPLEMENTOS, del 12 de Diciembre de 2011, de GORROCHATEGUI BARRUETA, ALBERTO: La composición incorpora, junto al concentrado de plaquetas que aporta fibrinógeno y concentraciones de factores de crecimiento plaquetarios (PDGFs), otras concentraciones […]
 ALIMENTACION RESTRINGIDA DE GLUCOSA PARA EL CULTIVO DE CELULAS ANIMALES, del 7 de Septiembre de 2010, de WYETH LLC: Método de cultivo celular para el control de la producción de ácido láctico a niveles reducidos en un cultivo celular alimentado por lotes, […]
ALIMENTACION RESTRINGIDA DE GLUCOSA PARA EL CULTIVO DE CELULAS ANIMALES, del 7 de Septiembre de 2010, de WYETH LLC: Método de cultivo celular para el control de la producción de ácido láctico a niveles reducidos en un cultivo celular alimentado por lotes, […]
 PROCEDIMIENTO PARA EL CULTIVO DE CELULAS PARA LA PRODUCCION DE SUBSTANCIAS, del 2 de Junio de 2010, de F. HOFFMANN-LA ROCHE AG: Procedimiento para el cultivo de células de mamíferos para la producción de substancias, caracterizado porque, se cultivan unas células de mamíferos que producen una substancia, […]
PROCEDIMIENTO PARA EL CULTIVO DE CELULAS PARA LA PRODUCCION DE SUBSTANCIAS, del 2 de Junio de 2010, de F. HOFFMANN-LA ROCHE AG: Procedimiento para el cultivo de células de mamíferos para la producción de substancias, caracterizado porque, se cultivan unas células de mamíferos que producen una substancia, […]
Composiciones para la supresión de la formación de inhibidores contra el factor VIII en pacientes con hemofilia A., del 22 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Una composición que comprende material vegetal liofilizado que comprende al menos un fragmento de FVIII conjugado con la subunidad B de la toxina […]
Estimulación de la vía wnt en la reprogramación de células somáticas, del 20 de Mayo de 2020, de WHITEHEAD INSTITUTE FOR BIOMEDICAL RESEARCH: Un método de reprogramación de una célula somática de mamífero, que comprende: (a) poner en contacto la célula somática de mamífero con un activador de la vía Wnt seleccionado […]
 Irradiación de glóbulos rojos y almacenamiento anaeróbico, del 29 de Abril de 2020, de Hemanext Inc: Un método para almacenar glóbulos rojos que comprende:
empobrecimiento de oxígeno u oxígeno y dióxido de carbono de los glóbulos rojos, produciendo así glóbulos […]
Irradiación de glóbulos rojos y almacenamiento anaeróbico, del 29 de Abril de 2020, de Hemanext Inc: Un método para almacenar glóbulos rojos que comprende:
empobrecimiento de oxígeno u oxígeno y dióxido de carbono de los glóbulos rojos, produciendo así glóbulos […]
Ceramidasa y diferenciación celular, del 22 de Abril de 2020, de MOUNT SINAI SCHOOL OF MEDICINE: Un método in vitro para mejorar el fenotipo de una población de condrocitos, dicho método comprende: seleccionar una población de condrocitos de mamífero que […]
Medios de perfusión, del 1 de Abril de 2020, de Coherus Biosciences, Inc: Un método para la fabricación de una proteína que comprende la etapa de producir la proteína mediante el cultivo celular por perfusión de células […]