LIGANDOS DE AFINIDAD DE UNION A ANTICUERPOS.
Material de soporte sólido teniendo inmovilizado covalentemente sobre el mismo un ligando de afinidad,
comprendiendo dicho ligando uno o más grupo(s) funcional(es) hidrofóbico(s) y uno o más grupo(s) funcional(es) catiónico(s),
donde al menos un grupo funcional hidrofóbico está separado de al menos un grupo funcional catiónico por una distancia a través de enlaces de entre 5 Å y 20 Å,
donde dicho ligando consiste en menos de 5 residuos y tiene un peso molecular de entre 120 Da y 1.000 Da; y
donde el ligando comprende o consiste en 3 residuos unidos covalentemente, X1-X2-X3, donde dichos residuos unidos covalentemente también están unidos covalentemente al enlazador L de la entidad L-PM, donde PM es el material de soporte sólido,
donde X1 es un aminoácido natural o no natural en una configuración D y/o L, o un residuo de ácido carboxílico comprendiendo un grupo aromático opcionalmente sustituido,
donde X2 es un aminoácido natural o no natural en una configuración D y/o L, o un residuo de ácido carboxílico comprendiendo un grupo aromático opcionalmente sustituido, con la condición de que X2 no sea un residuo de treonina, y
donde X3 es un aminoácido natural o no natural en una configuración D y/o L, o un residuo de ácido carboxílico
comprendiendo un grupo aromático opcionalmente sustituido,
donde al menos uno de X1, X2 y X3 comprende un grupo funcional catiónico, y
donde al menos uno de X1, X2 y X3 comprende un grupo funcional hidrofóbico,
donde X1 se selecciona de L-Arg, D-Lys, D-Phe, D-Pro, INA, PPC, DBHBA, 3HBA, 4HBA y SAA;
donde X2 se selecciona de L-Arg, L-Asn, D-Leu, D-Lys, D-Phe, D-Pro, L-Pro, AIB, AHX, INA, NLE y PPC; y
donde X3 se selecciona de L-Arg, L-Asn, D-Lys, D-Phe, D-Pro, L-Pro y PPC
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/DK2005/000828.
Solicitante: NOVO NORDISK A/S.
Nacionalidad solicitante: Dinamarca.
Dirección: NOVO ALLE 1,2880 BAGSVAERD.
Inventor/es: AMBROSIUS, DOROTHEE, JOHANNSEN,IB, MICHAEL,ROICE, RAMOS GALLEGO,MONICA, NOTHELFER,FRANZ, JACOBI,ALEXANDER.
Fecha de Publicación: .
Fecha Concesión Europea: 17 de Marzo de 2010.
Clasificación Internacional de Patentes:
- C07K1/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › Cromatografía de afinidad o técnicas análogas basadas en procesos de absorción selectiva.
- C07K16/06A
- G01N33/543F
Clasificación PCT:
- C07K5/08 C07K […] › C07K 5/00 Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados. › Tripéptidos.
- C07K5/10 C07K 5/00 […] › Tretapéptidos.
- G01N33/543 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › con un soporte insoluble para la inmovilización de compuestos inmunoquímicos.

Fragmento de la descripción:
Ligandos de afinidad de unión a anticuerpos.
Campo de la invención
La presente invención se refiere a ligandos de afinidad unidos covalentemente a un material de soporte sólido, tal como una matriz de polímero, y usos de los mismos en la purificación y/o el aislamiento de biomoléculas, tales como proteínas, en particular anticuerpos, tales como anticuerpos monoclonales. Los ligandos de afinidad comprenden dos dominios diferentes o grupos funcionales: (i) un dominio hidrofóbico y (ii) un dominio catiónico.
Antecedentes de la invención
La cromatografía de afinidad habilita selectiva y reversiblemente sustancias biológicas de adsorción, tales como anticuerpos monoclonales, para una sustancia de enlace complementaria, tal como un ligando de afinidad inmovilizado en un material de soporte sólido contenido en una columna de afinidad.
Las columnas de afinidad frecuentemente contienen un material de soporte sólido, normalmente una matriz de polímero porosa, a la cual se une covalentemente un ligando adecuado directamente o mediante un enlazador. Una muestra conteniendo sustancias biológicas con una afinidad por el ligando puede ponerse en contacto con el ligando de afinidad inmovilizado covalentemente al material de soporte sólido bajo condiciones de enlace favorables que promueven un enlace específico entre el ligando y las sustancias biológicas con una afinidad por el ligando. La columna puede lavarse posteriormente con un regulador de pH para eliminar el material no enlazado, y en otra etapa las sustancias biológicas con una afinidad por el ligando pueden eluirse y obtenerse en una forma purificada o aislada. Por consiguiente, el ligando debería exhibir preferiblemente características de enlace específicas y reversibles para la sustancia biológica, tales como un anticuerpo, el cual se desee purificar o aislar.
Los anticuerpos tienen una o más copias de una unidad en forma de Y, compuesta por cuatro cadenas de polipéptidos. Cada Y contiene dos copias idénticas de una cadena "pesada", y dos copias idénticas de una "cadena ligera", llamadas así por sus pesos moleculares relativos.
Los anticuerpos pueden dividirse en cinco clases: IgG, IgM, IgA, IgD y IgE, en base al número de unidades Y y al tipo de cadena pesada. La cadena pesada determina la subclase de cada anticuerpo. Las cadenas pesadas de IgG, IgM, IgA, IgD, e IgE se conocen como gamma, mu, alfa, delta, y epsilon, respectivamente. Las cadenas ligeras de cualquier anticuerpo pueden clasificarse o bien como de tipo kappa (?) o lambda (?) (una descripción de las características moleculares del polipéptido).
Para aplicaciones farmacéuticas, el anticuerpo más frecuentemente usado es IgG el cual puede dividirse en tres partes, dos regiones F(ab) y una región Fc, por la papaina de la enzima proteolítica, o en dos partes, una región F(ab')2 y una región Fc por la pepsina de la enzima proteolítica.
Las regiones F(ab) comprenden los "brazos" del anticuerpo, los cuales son críticos para la enlace de antígenos. La región Fc comprende la "cola" del anticuerpo y juega un papel en la respuesta inmunitaria, al igual que sirve como un "asa" útil para manipular el anticuerpo durante algunos procedimientos inmunoquímicos. El número de regiones F(ab) en el anticuerpo, se corresponde con su subclase, y determina la "valencia" del anticuerpo (dicho en términos generales, el número de "brazos" con los cuales el anticuerpo puede enlazar su antígeno).
El término "anticuerpo" significa una inmunoglobulina, producida sintéticamente o bien de forma natural o parcial o completa. Todos los fragmentos y derivados de los mismos que mantienen la capacidad de enlace específica también se incluyen en el término. Son fragmentos típicos FC, FAB, cadena pesada, y cadena ligera. El término también engloba cualquier polipéptido con un dominio de enlace homólogo o ampliamente homólogo, tal como al menos un 95% idéntico en comparación con la secuencia de aminoácidos, para un dominio de enlace de inmunoglobulina. Estos polipéptidos pueden derivarse de fuentes naturales, o producirse sintéticamente de forma parcial o completa. Un anticuerpo puede ser monoclonal o policlonal. El anticuerpo puede ser un elemento de cualquier clase de inmunoglobulina, incluyendo cualquiera de las clases humanas: IgG, IgM, IgA, IgD, e IgE. Los derivados de la clase IgG, no obstante, se prefieren en una forma de realización de la presente invención.
El término "fragmento de anticuerpo" se refiere a cualquier derivado de un anticuerpo que tenga menos que su longitud completa. Preferiblemente, el fragmento de anticuerpo retiene al menos una parte significante de la capacidad de enlace específica del anticuerpo en toda su longitud. Ejemplos de fragmentos de anticuerpos incluyen, pero no se limitan a, Fab, Fab', F(ab')2, scFv, FV, diacuerpo de dsFv, y fragmentos de Fd. El fragmento de anticuerpo puede producirse por cualquier medio. Por ejemplo, el fragmento de anticuerpo puede producirse enzimáticamente o químicamente por fragmentación de un anticuerpo intacto o puede producirse de manera recombinante a partir de un gen codificando la secuencia del anticuerpo parcial. De forma alternativa, el fragmento de anticuerpo puede producirse sintéticamente de forma completa o parcial. El fragmento de anticuerpo puede ser opcionalmente un fragmento de anticuerpo monocatenario. De forma alternativa, el fragmento puede comprender cadenas múltiples que se enlacen juntas, por ejemplo, por enlaces de disulfuro. El fragmento también puede opcionalmente ser un complejo multimolecular. Un fragmento de anticuerpo funcional típicamente comprenderá al menos aproximadamente 50 aminoácidos y más típicamente comprenderá al menos aproximadamente 200 aminoácidos.
Los "Fvs monocatenarios" (scFvs) son fragmentos de anticuerpo recombinantes que consisten sólo en la cadena ligera variable (VL) y la cadena pesada variable (VH) conectadas covalentemente la una a la otra por un enlazador del polipéptido. Tanto el dominio VL como VH pueden ser el dominio aminoterminal. El enlazador de polipéptidos puede tener una longitud y una composición variables mientras los dos dominios variables estén ligados sin interferencia estérica importante. Típicamente, los enlaces están compuestos principalmente por extensiones de glicina y residuos de serina con algún ácido glutámico o residuos de lisina intercalados para solubilidad. Los "diacuerpos" son scFvs diméricos. Los componentes de los diacuerpos típicamente tienen enlaces peptídicos más cortos que la mayoría de scFvs y muestran una preferencia para asociarse como dímeros. Un fragmento "Fv" es un fragmento de anticuerpo que consiste en un dominio VH y un dominio VL mantenidos juntos por interacciones no covalentes. El término "dsFv" se utiliza en este caso para referirse a un FV con un enlace de disulfuro creado genéticamente intermolecular para estabilizar el par VH - VL. Un fragmento "F(ab')2" es un fragmento de anticuerpos esencialmente equivalente al obtenido a partir de inmunoglobulinas (típicamente IgG) por digestión con una pepsina enzimática a un pH 4.0-4.5. El fragmento puede producirse de forma recombinante. Un fragmento "Fab" es un fragmento de anticuerpo esencialmente equivalente al obtenido por reducción del puente o puentes de disulfuro que unen las dos partes de cadena pesada en el fragmento F(ab')2. El fragmento Fab' puede producirse recombinantemente. Un fragmento "Fab" es un fragmento de anticuerpo esencialmente equivalente al obtenido mediante la digestión de inmunoglobulinas (típicamente IgG) con la papaína enzimática. El fragmento Fab puede producirse recombinantemente. El segmento de cadena pesada del fragmento Fab es la parte de Fd. Una región "Fc" es una región constante de una clase particular de anticuerpo.
El enlace entre antígenos y anticuerpos depende de enlaces de hidrógeno, enlaces hidrofóbicos, fuerzas electroestáticas, y fuerzas van der Waals. Estos son todos enlaces de una naturaleza débil no covalente, puesto que algunas asociaciones entre un antígeno y un anticuerpo pueden ser bastante fuertes. Por consiguiente, la constante de afinidad para la enlace antígeno-anticuerpo puede abarcar una gama amplia, extendiéndose desde menos de 105 mol-1 a más de 1012 mol-1. Las constantes de afinidad están afectadas por la temperatura, el pH y el solvente. Además de una afinidad de un anticuerpo por un ligando, la estabilidad global de un complejo de ligando-anticuerpo también se determina por la valencia del antígeno...
Reivindicaciones:
1. Material de soporte sólido teniendo inmovilizado covalentemente sobre el mismo un ligando de afinidad, comprendiendo dicho ligando uno o más grupo(s) funcional(es) hidrofóbico(s) y uno o más grupo(s) funcional(es) catiónico(s),
donde al menos un grupo funcional hidrofóbico está separado de al menos un grupo funcional catiónico por una distancia a través de enlaces de entre 5 Å y 20 Å,
donde dicho ligando consiste en menos de 5 residuos y tiene un peso molecular de entre 120 Da y 1.000 Da; y
donde el ligando comprende o consiste en 3 residuos unidos covalentemente, X1-X2-X3, donde dichos residuos unidos covalentemente también están unidos covalentemente al enlazador L de la entidad L-PM, donde PM es el material de soporte sólido,
donde X1 es un aminoácido natural o no natural en una configuración D y/o L, o un residuo de ácido carboxílico comprendiendo un grupo aromático opcionalmente sustituido,
donde X2 es un aminoácido natural o no natural en una configuración D y/o L, o un residuo de ácido carboxílico comprendiendo un grupo aromático opcionalmente sustituido, con la condición de que X2 no sea un residuo de treonina, y
donde X3 es un aminoácido natural o no natural en una configuración D y/o L, o un residuo de ácido carboxílico
comprendiendo un grupo aromático opcionalmente sustituido,
donde al menos uno de X1, X2 y X3 comprende un grupo funcional catiónico, y
donde al menos uno de X1, X2 y X3 comprende un grupo funcional hidrofóbico,
donde X1 se selecciona de L-Arg, D-Lys, D-Phe, D-Pro, INA, PPC, DBHBA, 3HBA, 4HBA y SAA;
donde X2 se selecciona de L-Arg, L-Asn, D-Leu, D-Lys, D-Phe, D-Pro, L-Pro, AIB, AHX, INA, NLE y PPC; y
donde X3 se selecciona de L-Arg, L-Asn, D-Lys, D-Phe, D-Pro, L-Pro y PPC.
2. Material de soporte sólido teniendo inmovilizado covalentemente sobre el mismo un ligando de afinidad, comprendiendo dicho ligando uno o más grupo(s) funcional(es) hidrofóbico(s) y uno o más grupo(s) funcional(es) catiónico(s),
donde al menos un grupo funcional hidrofóbico se separa de al menos un grupo funcional catiónico por una distancia a través de enlaces de entre 5 Å y 20 Å,
donde dicho ligando consiste en menos de 5 residuos y tiene un peso molecular de entre 120 Da y 1.000 Da; y
donde el ligando de afinidad comprende o consiste en los residuos unidos covalentemente X1-X2-X3, donde opcionalmente X1, X2 y/o X3, se enlaza con un residuo de enlazador, L; y
donde
el residuo X1 se selecciona del grupo que consiste en Arg, Phe, PPC, DBHBA, SAA, DAP, DAB, (DBHBA)2-DAP, (MDCA)2-DAP, DPBBA, DBBA, PCAA, DPPAA, Trp, TMPPA, y DBHPA,
el residuo X2 se selecciona del grupo que consiste en Arg, Asn, Leu, Lys, Phe, Pro, PPC, DAP, DAB, His, Trp, Tyr, y Ser, y
el residuo X3 se selecciona del grupo que consiste en Arg, Asn, Pro, PPC, Asp, Orn, y (1H2NA)Dap.
3. Material de soporte sólido que tiene inmovilizado covalentemente sobre el mismo un ligando de afinidad, comprendiendo dicho ligando uno o más grupo(s) funcional(es) hidrofóbico(s) y uno o más grupo(s) funcional(es) catiónico(s),
donde al menos un grupo funcional hidrofóbico se separa de al menos un grupo funcional catiónico por una distancia a través de enlaces de entre 5 Å y 20 Å,
donde dicho ligando consiste en 3 residuos seleccionados del grupo que consiste en D-Leu; D-Lys; D-Phe; D-Pro; L-Arg; L-Asn; L-Pro; Ahx; Aib; DBHBA; INA; Nle; PPC; SAA; 3HBA y 4HBA, y tiene un peso molecular de entre 120 Da y 1.000 Da.
4. Material de soporte sólido según cualquiera de las reivindicaciones 1 y 2 y 3, donde dicha resina de afinidad tiene una capacidad de enlace mayor que 5 mg de anticuerpo monoclonal por ml de resina de afinidad.
5. Material de soporte sólido según cualquiera de las reivindicaciones precedentes, donde el ligando comprende o consiste en uno o más de:
D-Phe-(L)Arg-(L)Arg,
L-Arg-D-Phe-(L)Arg,
PPC-D-Pro-(L)Arg,
PPC-D-Leu-PPC,
INA-D-Phe-PPC,
PPC-AIB-PPC,
L-Arg-(L)Arg-D-Phe,
PPC-(L)Arg-D-Pro,
D-Pro-PPC-(L)Arg,
L-Arg-D-Pro-PPC,
D-Lys-INA-(L)Arg,
INA-(L)Arg-D-Lys,
PPC-AHX-PPC,
PPC-Nle-PPC,
SAA-(L)Arg-(L)Pro,
SAA-(L)Pro-(L)Arg,
DBHBA-(L)Arg-(L)Asn,
DBHBA-(L)Asn-(L)Arg,
3HBA-(L)Arg-(L)Pro,
3HBA-(L)Pro-(L)Arg,
4HBA-(L)Arg-(L)Pro, y
4HBA-(L)Pro-(L)Arg,
6. Material de soporte sólido según cualquiera de las reivindicaciones 1-4, donde el ligando es uno seleccionado del grupo que consiste en
H2N-(D)Phe-(L)Arg-(L)Arg-Gly-OH,
H2N-(L)Arg-(D)Phe-(L)Arg-Gly-OH,
HN-PPC-(D)Pro-(L)Arg-Gly-OH,
DBBA-(L)His-(L)Arg-Gly-OH,
DBBA-His-Arg-Gly-OH,
DBBA-His-Arg-Arg-Gly-OH,
DPPBA-(L)Phe-(L)Arg-Gly-OH,
PCAA-(L)Phe-(L)Arg-Gly-OH,
DPPBA-(L)Lys-(L)Arg-Gly-OH,
SAA-(L)Arg-(L)Pro-Gly-OH,
SAA-(L)Pro-(L)Arg-Gly-OH,
DBHBA-(L)Arg-(L)Asn-Gly-OH,
DBHBA-(L)Asn-(L)Arg-Gly-OH,
DPPBA-(L)Trp-(L)Arg-Gly-OH,
(MDCA)2 DAP-(L)Arg-(L)Orn-Gly-OH,
(MDCA)2 DAP-(L)Arg-(L)Asp-Gly-OH,
DPPAA-(L)Phe-(L)Arg-Gly-OH,
DPPAA-PPC-(L)Arg-Gly-OH,
DBHBA-(D)Phe-(D)Arg-Gly-OH,
DPPAA-(D)Tyr-(D)Arg-Gly-OH,
(DPPA)2 DAP-(L)Arg-(L)Orn-Gly-OH,
(DBHBA)2 DAP-(L)Arg-(L)Arg-Gly-OH,
DBHBA-DAP-Arg-Gly-OH,
DBHBA-DAP-Arg-Arg-Gly-OH,
(DBHBA)2 DAP-Arg-Gly-OH,
(DBHBA)2 DAP-Arg-Arg-Gly-OH,
TMPPA-(L)Trp-(L)Arg-Gly-OH, y
DBHPA-(L)Arg-(L)Orn-Gly-OH.
7. Material de soporte sólido según cualquiera de las reivindicaciones 1-4, donde el ligando es uno seleccionado del grupo que consiste en
D-Phe-(L)Arg-(L)Arg-Gly,
L-Arg-D-Phe-(L)Arg-Gly,
PPC-D-Pro-(L)Arg-Gly,
PPC-D-Leu-PPC-Gly,
INA-D-Phe-PPC-Gly,
PPC-AIB-PPC-Gly,
L-Arg-(L)Arg-D-Phe-Gly,
PPC-(L)Arg-D-Pro-Gly,
D-Pro-PPC-(L)Arg-Gly,
L-Arg-D-Pro-PPC-Gly,
D-Lys-INA-(L)Arg-Gly,
INA-(L)Arg-D-Lys-Gly,
PPC-AHX-PPC-Gly,
PPC-Nle-PPC-Gly,
SAA-(L)Arg-(L)Pro-Gly,
SAA-(L)Pro-(L)Arg-Gly,
DBHBA-(L)Arg-(L)Asn-Gly,
DBHBA-(L)Asn-(L)Arg-Gly,
3HBA-(L)Arg-(L)Pro-Gly,
3HBA-(L)Pro-(L)Arg-Gly,
4HBA-(L)Arg-(L)Pro-Gly, y
4HBA-(L)Pro-(L)Arg-Gly.
8. Material de soporte sólido según cualquiera de las reivindicaciones precedentes, donde el ligando se selecciona del grupo que consiste en DBBA-(L)His-(L)Arg-Gly-OH y (DBHBA)2-DAP-(L)Arg-(L)Arg-Gly-OH.
9. Método para el aislamiento de anticuerpos o derivados de los mismos, incluyendo el método las etapas de (i) proporcionar un material de soporte sólido teniendo inmovilizado covalentemente sobre el mismo un ligando de afinidad tal y como se define en cualquiera de las reivindicaciones 1-8, (ii) proporcionar una muestra conteniendo un anticuerpo con una afinidad por dicho ligando, (iii) poner en contacto dicho ligando con dicha muestra conteniendo dicho anticuerpo, (iv) enlazar selectivamente dicho anticuerpo cuando dicho anticuerpo está contenido en dicha muestra y (v) aislar selectivamente dicho anticuerpo cuando dicho anticuerpo está contenido en dicha muestra.
Patentes similares o relacionadas:
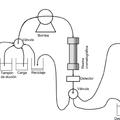 Purificación de proteínas, del 29 de Julio de 2020, de UCB Biopharma SRL: Un proceso para la purificación de una proteína de interés a partir de una mezcla que comprende las etapas de
a) en un ciclo de cromatografía operativo, […]
Purificación de proteínas, del 29 de Julio de 2020, de UCB Biopharma SRL: Un proceso para la purificación de una proteína de interés a partir de una mezcla que comprende las etapas de
a) en un ciclo de cromatografía operativo, […]
Membranas para cromatografía formadas por reacciones de polimerización clic de tiol-eno o tiol-ino, del 10 de Junio de 2020, de Merck Millipore Ltd: Un material compuesto, que comprende: un miembro de soporte, que comprende una pluralidad de poros que se extienden a través del miembro de […]
Un procedimiento de cromatografía de reparto débil, del 6 de Mayo de 2020, de WYETH LLC: Un procedimiento de recuperación de un producto purificado de un fluido de carga que incluye una o más impurezas, que comprende las etapas de: hacer pasar el fluido […]
Procedimiento de purificación de polipéptidos, del 22 de Abril de 2020, de CSL LIMITED: Procedimiento de purificación de un polipéptido de interés por cromatografía de intercambio catiónico en el que un compuesto químico se añade en una concentración de al menos […]
Etiqueta de epítopo y método de detección, captura y/o purificación de polipéptidos etiquetados, del 15 de Abril de 2020, de ChromoTek GmbH: Péptido epítopo aislado que tiene de 12 a 25 aminoácidos, en donde la secuencia de aminoácidos comprende una secuencia según se define en SEQ ID NO: 32 (X1X2RX4X5AX7SX9WX11X12), […]
Matriz de cromografía de afinidad, del 25 de Marzo de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES SOCIETE ANONYME: Matriz de cromatografía de afinidad, en forma de gel, que comprende unas partículas de polímero sobre las cuales se injerta al menos un oligosacárido […]
Sistema de tampón para purificación de proteína, del 26 de Febrero de 2020, de GLAXOSMITHKLINE LLC: Un sistema de cromatografía que comprende: (i) un sistema de tampón de múltiples componentes libre de cloruro de sodio para la purificación de una […]
Proteína mutante, del 19 de Febrero de 2020, de Cytiva BioProcess R&D AB: Una proteína de unión a inmunoglobulina que se une a regiones de una molécula de inmunoglobulina distintas de las regiones determinantes de […]