PROCEDIMIENTO PARA LA PREPARACION DEL 14BETA-HIDROXI-BACATINA III-1,14-CARBONATO.
Procedimiento para la preparación de 14ß-hidroxi-1,14-carbonato-bacatina III, que comprende:
a. tratar la 7-Boc-13-cetobacatina III de fórmula
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP02/08007.
Solicitante: INDENA S.P.A..
Nacionalidad solicitante: Italia.
Dirección: VIALE ORTLES, 12,20139 MILANO.
Inventor/es: BOMBARDELLI, EZIO, FONTANA, GABRIELE, BATTAGLIA,ARTURO I.C.O.C.E.A, GUERRINI,ANDREA I.C.O.C.E.A, BALDELLI,ELENORA.
Fecha de Publicación: .
Fecha Concesión Europea: 5 de Mayo de 2010.
Clasificación Internacional de Patentes:
- C07D305/14 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 305/00 Compuestos heterocíclicos que contienen ciclos de cuatro miembros que tienen un átomo de oxígeno como único heteroátomo del ciclo. › condensados con ciclos o sistemas cíclicos carbocíclicos.
- C07D493/08 C07D […] › C07D 493/00 Compuestos heterocíclicos que contienen átomos de oxígeno como únicos heteroátomos del ciclo en el sistema condensado. › Sistemas puenteados.
Clasificación PCT:
- A61K31/335 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen el oxígeno como único heteroátomo de un ciclo, p. ej. fungicromina.
- C07D305/14 C07D 305/00 […] › condensados con ciclos o sistemas cíclicos carbocíclicos.
Clasificación antigua:
- A61K31/335 A61K 31/00 […] › que tienen el oxígeno como único heteroátomo de un ciclo, p. ej. fungicromina.
- C07D305/14 C07D 305/00 […] › condensados con ciclos o sistemas cíclicos carbocíclicos.
Fragmento de la descripción:
Procedimiento para la preparación del 14ß-hidroxi-bacatina III-1,14-carbonato.
La presente invención se refiere a un procedimiento para la preparación de 14ß-hidroxi-1,14-carbonato-bacatina III. El producto obtenido con el procedimiento de la invención puede usarse en la preparación de derivados de taxano novedosos con actividad antitumoral.
Los taxanos son una de las clases más importantes de agentes antitumorales desarrollados en los últimos años. El paclitaxel es un complejo de diterpeno obtenido de la corteza de Taxus brevifolia y se considera uno de los principales medicamentos para el tratamiento del cáncer. Actualmente, está llevándose a cabo una extensa búsqueda de derivados de taxano novedosos que tienen actividad farmacológica superior y un perfil farmacocinético mejorado. Un enfoque específico se refiere a derivados de bacatina III modificados de manera diversa con respecto a la estructura original. Ejemplos de dichos compuestos se representan mediante los derivados de 14ß-hidroxi-bacatina III dados a conocer en los documentos US 5705508, WO 97/43291, WO 96/36622. Actualmente, los derivados de 1,14-carbonato de 14ß-hidroxi-desacetilbacatina III se preparan partiendo del precursor 14ß-hidroxi-desacetilbacatina III, que es un compuesto natural que puede obtenerse en pequeñas cantidades mediante extracción de las hojas de Taxus wallichiana, tal como se da a conocer en el documento EP 559019. Hay una gran necesidad de procedimientos novedosos para la preparación fácil, eficaz, de grandes cantidades de 14ß-hidroxi-1,14-carbonato-bacatina III, y por tanto los derivados de la misma.
Se ha encontrado ahora que puede prepararse 14ß-hidroxi-bacatina III-1,14-carbonato con un procedimiento partiendo de 13-cetobacatina III, compuesto que puede obtenerse fácilmente a partir de 10-desacetilbacatina III, que a su vez puede aislarse fácilmente en grandes cantidades de las hojas de Taxus baccata, a diferencia de 14ß-hidroxi-bacatina III.
Por tanto, la invención se refiere a un procedimiento para la preparación de 14ß-hidroxi-bacatina III-1,14-carbonato que comprende las siguientes etapas:
a. tratar la 7-Boc-13-cetobacatina III de fórmula

con agentes oxidantes y bases adecuados, para dar 7-Boc-13-ceto-14-hidroxi-bacatina III:
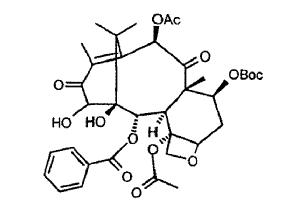
b. carbonatar los grupos hidroxilo 1 y 14 para dar 14ß-hidroxi-7-Boc-13-ceto-bacatina III-1,14-carbonato:
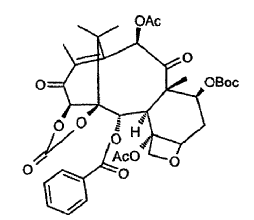
c. reducir la cetona en la posición 13 y escindir el grupo protector en 7 o viceversa.
La 13-cetobacatina III de partida está convenientemente protegida en la posición 7 con un grupo protector adecuado, preferiblemente terc-butoxicarbonilo (Boc). La etapa a) se lleva a cabo mediante tratamiento con una base adecuada, en particular t-butóxido de potasio (t-BuOK) o bis(trimetilsilil)amida de potasio (KHMDS). La reacción puede llevarse a cabo a de -40 a -78ºC. Los disolventes adecuados para esta reacción son éteres, tales como tetrahidrofurano o dietil éter, en particular en mezcla con hexametilfosforamida (HMPA) o 1,3-dimetil-3,4,5,6-tetrahidro-2(1H)pirimidinona (DMPU). Entonces se trata el enolato con un agente oxidante, tal como derivados de oxaziridina (en particular N-bencenosulfonilfeniloxaziridina, N-bencenosulfonil-m-nitrofeniloxaziridina y canforsulfoniloxaziridina) para proporcionar el derivado de 13-ceto-14-hidroxi-bacatina III 7-protegida.
Entonces se lleva a cabo la etapa b) mediante tratamiento con un agente de carbonilación (por ejemplo carbonildiimidazol o fosgeno) en las condiciones descritas habitualmente en la bibliografía, para proporcionar el derivado de 1,14-carbonato. La reacción puede llevarse a cabo convenientemente en disolventes inertes, preferiblemente disolventes clorados o éteres, en presencia de una base (preferiblemente piridina o trietilamina), a una temperatura que oscila desde -40ºC hasta temperatura ambiente. La reacción puede llevarse a cabo tanto para el material de partida puro como para el producto bruto de la etapa anterior.
La reducción del carbonilo en la posición 13 de la etapa c) se lleva a cabo fácilmente con borohidruro de tetrabutilamonio en etanol a una temperatura que oscila habitualmente desde -20 hasta -50ºC, y se completa en el plazo de 2-6 horas. La reacción también puede llevarse a cabo en metanol, isopropanol, o en una mezcla de metanol y tetrahidrofurano. El agente reductor puede usarse en cantidad estequiométrica, aunque preferiblemente se usa un exceso de hidruro. La reducción también puede efectuarse con otros hidruros, preferiblemente borohidruro de litio, borohidruro de sodio, triacetoxiborohidruro de sodio, en las condiciones conocidas en la técnica.
La protección en la posición 7 se elimina en condiciones que dependen del grupo protector usado. Por ejemplo, si el grupo protector en la posición 7 es terc-butoxicarbonilo, la hidrólisis con el ácido fórmico puede usarse satisfactoriamente.
La 13-cetobacatina III de partida puede prepararse fácilmente según uno de los dos siguientes procedimientos.
Se oxida selectivamente 10-desacetil-bacatina III en la posición 13 con ozono para dar 13-ceto-10-desacetil-bacatina III. La oxidación puede llevarse a cabo en disolventes alcohólicos o clorados, en particular metanol o cloruro de metileno, a una temperatura que oscila desde -78 hasta temperatura ambiente. Entonces se acetila de manera regioselectiva 13-ceto-10-desacetil-bacatina III para dar 13-ceto-bacatina III.
Alternativamente, puede obtenerse 13-ceto-bacatina III mediante oxidación de bacatina III o bien natural o bien que puede obtenerse mediante acetilación regioselectiva de 10-desacetilbacatina III. La oxidación puede llevarse a cabo con ozono, o también con dióxido de manganeso en disolventes apróticos tales como cloruro de metileno, a temperaturas que oscilan desde 0ºC hasta 60ºC, más preferiblemente a temperatura ambiente.
Los procedimientos de la invención se resumen en el siguiente esquema:
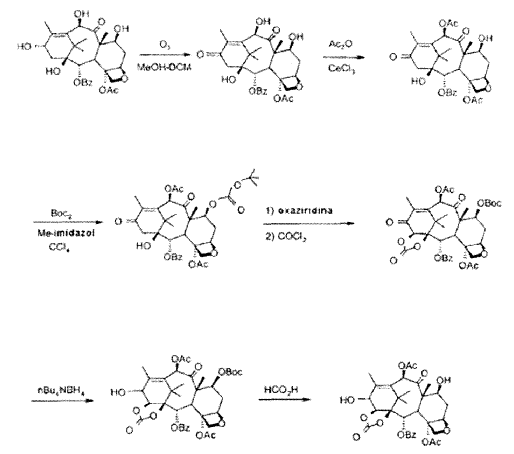
Los siguientes ejemplos ilustran adicionalmente la invención.
Las abreviaturas usadas son las siguientes:
AcOEt = acetato de etilo; TES = trietilsililo; TESCl = cloruro de trietilsililo; DCM = diclorometano, THF = tetrahidrofurano, HMPA = hexametilfosforamida, DMPU = 1,3-dimetil-3,4,5,6-tetrahidro-2(1H)pirimidinona.
Ejemplo 1
10-Desacetil-13-ceto-bacatina III
Se disolvió 10-desacetil-bacatina III (3 g, 5 mmol) en DCM-MeOH 1:1 (250 ml) y se enfrió hasta -78ºC. Se burbujeó una corriente de ozono (1,4 g/ml) a través de la disolución hasta que desapareció el material de partida (2 h). Se sustituyó la corriente de ozono por nitrógeno. Entonces se trató la disolución con sulfuro de dimetilo (1 ml) y piridina (1 ml), se eliminó el disolvente mediante evaporación y se disolvió el producto bruto en EtOAc (100 ml) y se lavó con HCl 0,1 N y hielo. Tras la eliminación del disolvente mediante evaporación, se obtuvo el producto del título con un rendimiento del 90%.
Ejemplo 2
13-Ceto-bacatina III
Se disolvió bacatina III (150 g, 0,25 mol) en acetona (1,43 l). Se añadió el dióxido de manganeso disponible comercialmente (450 g) en tres partes con fuerte agitación. Tras haber desaparecido el producto de partida (4 h) se filtró la suspensión y se eliminó el disolvente mediante evaporación. Se suspendió el producto bruto en EtOAc (100 ml) y se sometió a reflujo durante 1 h, entonces se añadió c-Hex (100 ml). Se obtuvo el compuesto del título de aguas madre, tras la evaporación del disolvente, como un sólido blanco (140 g, 95%).
Ejemplo 3
7-Boc-13-ceto-bacatina III
Una disolución de 13-ceto-bacatina III (1,1 g, 1,9 mmol) en cloruro de metileno (0,5 ml) se disolvió en tetracloruro de carbono (14 ml) a temperatura ambiente. Entonces se añadieron 1-metilimidazol (35 ml, 0,282 mmol) y Boc2O (1,026 g, 4,7 mmol) con fuerte agitación. Se dejó la disolución con agitación a 20ºC durante 18 horas. Después de esto, se sustituyó el disolvente por acetona (5 ml), se vertió la disolución en agua (5 ml) y...
Reivindicaciones:
1. Procedimiento para la preparación de 14ß-hidroxi-1,14-carbonato-bacatina III, que comprende:
a. tratar la 7-Boc-13-cetobacatina III de fórmula
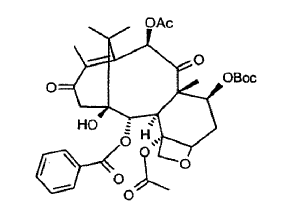
con agentes oxidantes y bases adecuados, para dar 7-Boc-13-ceto-14-hidroxi-bacatina III:
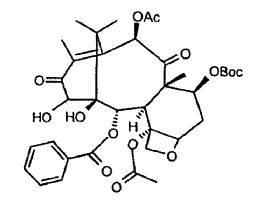
b. carbonatar los grupos hidroxilo 1 y 14 para dar 14ß-hidroxi-7-Boc-13-ceto-bacatina III-1,14-carbonato:
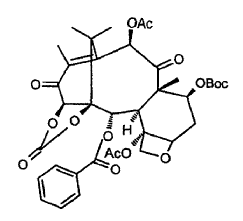
c. reducir la cetona en la posición 13 y escindir el grupo protector en 7.
2. Procedimiento según la reivindicación 1, en el que la etapa a) se lleva a cabo mediante tratamiento con t-butóxido de potasio o bis(trimetilsilil)amida de potasio a una temperatura de desde -40 hasta -78ºC en éteres en mezcla con hexametilfosforamida (HMPA) o 1,3-dimetil-3,4,5,6-tetrahidro-2(1H)pirimidinona (DMPU), en presencia de derivados de oxaziridina.
3. Procedimiento según la reivindicación 2, en el que el derivado de oxaziridina se selecciona de N-bencenosulfonilfeniloxaziridina, N-bencenosulfonil-m-nitrofeniloxaziridina y canforsulfoniloxaziridina.
4. Procedimiento según una cualquiera de las reivindicaciones 1 a 3, en el que la etapa b) se lleva a cabo mediante tratamiento con un carbonildiimidazol o fosgeno en disolventes clorados en presencia de una base a temperaturas que oscilan desde -40ºC hasta temperatura ambiente.
5. Procedimiento según una cualquiera de las reivindicaciones 1 a 4, en el que la etapa c) se lleva a cabo mediante tratamiento con un hidruro a una temperatura de desde -20 hasta -50ºC.
6. Procedimiento según la reivindicación 5, en el que el hidruro se selecciona de borohidruro de tetrabutilamonio, borohidruro de tetraetilamonio, borohidruro de sodio, borohidruro de litio, triacetoxiborohidruro de sodio y la reacción se lleva a cabo en etanol, metanol, isopropanol, o en una mezcla de metanol y tetrahidrofurano.
7. Procedimiento según una cualquiera de las reivindicaciones 1 a 6, en el que se prepara 13-ceto-bacatina III protegida en el hidroxilo en 7 mediante acetilación selectiva del hidroxilo 10 seguida por oxidación del hidroxilo 13 y protección del hidroxilo 7.
8. Procedimiento según la reivindicación 7, en el que se obtiene 13-ceto-bacatina III mediante acetilación selectiva de desacetilbacatina III en 10 con anhídrido acético seguida por oxidación con dióxido de manganeso en disolventes apróticos a 0ºC-60ºC o mediante oxidación de bacatina III con ozono.
9. Compuesto 7-Boc-13-ceto-14-hidroxi-bacatina III, de fórmula
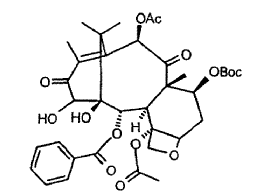
como producto intermedio novedoso.
10. Compuesto 14ß-hidroxi-7-Boc-13-ceto-bacatina III-1,14-carbonato, de fórmula:

como producto intermedio novedoso.
11. Compuesto 14ß-hidroxi-7-Boc-13-hidroxi-bacatina-III-1,14-carbonato, de fórmula:
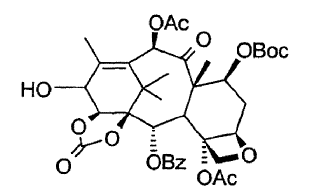
como producto intermedio novedoso.
Patentes similares o relacionadas:
Reactivos de merilformilo sustituido y procedimiento de uso de los mismos para modificar propiedades fisicoquímicas y/o farmacocinéticas de compuestos, del 15 de Enero de 2020, de Sphaera Pharma Pte. Ltd: Un compuesto farmacéutico modificado, que se selecciona entre el grupo que consiste en: - Compuesto n.º 295: yoduro de 1-(acetoximetil)-4-((4-etoxi-3-(1-metil-7-oxo-3-propil-4,7-dihidro-1H-pirazolo[4,3- […]
Forma cristalina de cabazitaxel y proceso para la preparación de la misma, del 17 de Junio de 2019, de FRESENIUS KABI ONCOLOGY LIMITED: Una forma cristalina 1 de cabazitaxel, que se caracteriza por un patrón de difracción de polvo de rayos X (XRD), determinado con una radiación de Cu Kα, que […]
Procedimientos para la preparación de carbazitaxel que implican la sililación en C(7)-OH y C(13)-OH o solo la sililación en C(7)-OH, del 14 de Mayo de 2019, de FRESENIUS KABI ONCOLOGY LIMITED: Un procedimiento para la preparación de cabazitaxel (I),que comprende las etapas de: a) tratar 10-desacetilbacatina de fórmula (III)**Fórmula** […]
Preparación de tesetaxel y compuestos relacionados y los compuestos intermedios de síntesis correspondientes, del 29 de Marzo de 2019, de Odonate Therapeutics, LLC: Un método de fabricación de un compuesto taxano que comprende acoplar un precursor de la cadena lateral de taxano a un grupo hidroxilo C13 del […]
Procedimiento para la preparación de cabazitaxel y sus compuestos intermedios, del 20 de Marzo de 2019, de Intas Pharmaceuticals Limited: Procedimiento para preparar cabazitaxel (I) que comprende una etapa de: reacción de un compuesto de fórmula (II)**Fórmula** donde X representa H o cadena lateral de […]
Derivados de taxano solubles en agua y sus usos, del 20 de Febrero de 2019, de Jiangsu Nhwaluokang Pharmaceutical Research and Development Co., Ltd: Un derivado de taxano soluble en agua de fórmula general (I-1), (I-2) o (I-3): **Fórmula** en donde, R1 es H o metilo; R2 es H, metilo […]
Formas de estado sólido de cabazitaxel y procesos de preparación de las mismas, del 8 de Marzo de 2017, de Teva Pharmaceuticals International GmbH: La forma cristalina III de cabazitaxel, solvato de 2-propanol, caracterizada por los datos seleccionados de: (a) un patrón de difracción de rayos X en polvo que […]
Un proceso mejorado para la preparación de derivados de taxano, del 11 de Enero de 2017, de EMCURE PHARMACEUTICALS LIMITED: Un proceso para la preparación de derivados de taxano que comprende las etapas: i) formar una mezcla de reacción de un derivado de taxano y una sal metálica […]