HIDROLIZADO DE CARTILAGO AVIAR, PROCEDIMIENTO DE PREPARACION Y SUS USOS.
Hidrolizado de cartílago aviar caracterizado porque:
a) comprende:
- 45% a 70% en peso de colágeno de tipo II hidrolizado,
- 9% a 15% en peso de sulfato de condroitina,
- 0,5% a 2% en peso de ácido hialurónico;
b) entre todos los aminoácidos:
- la valina representa 2,7% a 3,3%,
- la isoleucina representa 2,0% a 2,4%,
- la fenilalanina representa 2,2% a 2,6%,
- la lisina representa 3,8% a 4,2%,
- el triptófano representa 0,4% a 0,6%,
- la hidroxiprolina representa 5,5% a 8,7%,
- la hidroxilisina representa 0,7% a 1,8%,
- la relación molar entre hidroxiprolina e hidroxilisina está comprendida entre 5,0 y 8,0;
c) el peso molecular medio de su fracción peptídica está comprendido entre 500 y 1000 Daltons
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/053850.
Solicitante: DIANA NATURALS.
Nacionalidad solicitante: Francia.
Dirección: CABINET REGIMBEAU 20, RUE DE CHAZELLES,75847 PARIS CEDEX 17.
Inventor/es: VOULAND,ERIC, BERGER,CELINE.
Fecha de Publicación: .
Fecha Concesión Europea: 3 de Marzo de 2010.
Clasificación Internacional de Patentes:
- A23J1/10 NECESIDADES CORRIENTES DE LA VIDA. › A23 ALIMENTOS O PRODUCTOS ALIMENTICIOS; SU TRATAMIENTO, NO CUBIERTO POR OTRAS CLASES. › A23J COMPOSICIONES A BASE DE PROTEINAS PARA LA ALIMENTACION; TRATAMIENTO DE PROTEINAS PARA LA ALIMENTACION; COMPOSICIONES A BASE DE FOSFATIDOS PARA LA ALIMENTACION. › A23J 1/00 Preparación de composiciones a base de proteínas para la alimentación; Apertura de huevos en grandes cantidades y separación de la yema de la clara. › a partir pelos, plumas, cuernos, pieles, cuero, huesos o similares.
- A23L1/305A
- A23L1/305B
- A61K31/728 A […] › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Acido hialurónico.
- A61K31/737 A61K 31/00 […] › Polisacáridos sulfatados, p. ej. sulfato de condroitina, sulfato de dermatano (A61K 31/727 tiene prioridad).
- A61K35/32 A61K […] › A61K 35/00 Preparaciones medicinales que contienen sustancias de constitución indeterminada o sus productos de reacción. › Huesos; Osteocitos; Osteoblastos; Tendones; Tenocitos; Dientes; Odontoblastos; Cartílago; Condrocitos; Membrana sinovial.
- A61K38/01 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Proteínas hidrolizadas; Sus derivados.
- A61K38/39 A61K 38/00 […] › Péptidos del tejido conectivo, p. ej. colágeno, elastina, laminina, fibronectina, vitronectina, globulina insoluble en frío [CIG].
- C07K14/78 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Péptidos del tejido conectivo, p. ej. colágeno, elastina, laminina, fibronectina, vitronectina, globulina insoluble en frío (CIG).
Clasificación PCT:
- A61K35/32 A61K 35/00 […] › Huesos; Osteocitos; Osteoblastos; Tendones; Tenocitos; Dientes; Odontoblastos; Cartílago; Condrocitos; Membrana sinovial.
- A61K38/39 A61K 38/00 […] › Péptidos del tejido conectivo, p. ej. colágeno, elastina, laminina, fibronectina, vitronectina, globulina insoluble en frío [CIG].
- C07K14/78 C07K 14/00 […] › Péptidos del tejido conectivo, p. ej. colágeno, elastina, laminina, fibronectina, vitronectina, globulina insoluble en frío (CIG).
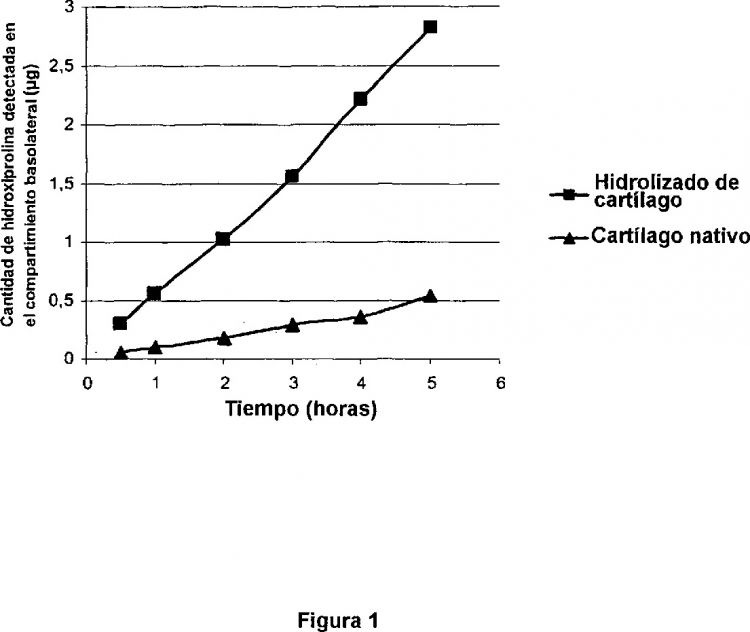
Fragmento de la descripción:
Hidrolizado de cartílago aviar, procedimiento de preparación y sus usos.
La presente invención se refiere a un hidrolizado de cartílago aviar que comprende 45% a 70% en peso de colágeno de tipo II hidrolizado, 9% a 15% en peso de sulfato de condroitina, 0,5% a 2% en peso de ácido hialurónico; con una composición de aminoácidos que contiene 2,7% a 3,3% de valina, 2,0% a 2,4% de isoleucina, 2,2% a 2,6% de fenilalanina, 3,8% a 4,2% de lisina, 0,4% a 0,6% de triptófano, 5,5% a 8,7% de hidroxiprolina, 0,7% a 1,8% de hidroxilisina, y en la que la relación molar entre hidroxiprolina e hidroxilisina está comprendida entre 5,0 y 8,0; y en el que el peso molecular medio de la fracción peptídica está comprendido entre 500 y 1000 Daltons. La invención también se refiere a un procedimiento para preparar dicho hidrolizado y su uso como un complemento alimentario y/o como un medicamento, particularmente para el tratamiento o prevención de artralgias.
Los cartílagos son tejidos altamente complejos encontrados en muchos órganos humanos y animales. De este modo, los cartílagos se pueden tomar del tabique nasal, la laringe, la tráquea arterial, los bronquios, las superficies articulares, el cartílago epifisario de huesos largos, el punto xifoide del esternón, etc.
Los cartílagos están compuestos de muchas moléculas usadas como ingredientes activos en alimentos dietéticos de seres humanos y animales, en farmacopea humana y veterinaria, o en cosmetología. Algunas de las moléculas más conocidas incluyen colágenos, hexosaminas y glucosaminoglucanos (sulfato de condroitina, sulfato de queratano, ácido hialurónico).
En particular, se ha sugerido que el colágeno de tipo II hidrolizado, el sulfato de condroitina y el ácido hialurónico que forman parte de los constituyentes de las articulaciones se podrían usar para el tratamiento de artralgias. La artralgia se trata convencionalmente mediante fármacos antiinflamatorios no esteroideos (NSAID) y posiblemente fármacos antálgicos, pero estos tratamientos sintomáticos a menudo están acompañados de efectos secundarios y por lo tanto sería útil tener tratamientos que pudiesen atenuar de manera secundaria el dolor y mejorar la motricidad, por medio de la acción prolongada en las articulaciones.
La mayoría de estas moléculas se han extraído durante muchos años del cartílago de ganado vacuno. Sin embargo, desde la aparición de la encefalopatía espongiforme bovina (BSE), las industrias alimentarias, farmacéuticas y cosméticas se han preocupado por la posible contaminación de estos extractos por los priones responsables de BSE, que no son inactivados por calor y son difíciles de detectar.
El uso de esqueletos de condrictios podría ser una solución de sustitución para productos derivados de bóvidos. Pero las fuentes marinas tienen límites cuantitativos, económicos y medioambientales. Por lo tanto, sería útil encontrar otra fuente de cartílago a partir de animales comunes reconocidos por estar libres de enfermedades priónicas. Las aves de corral domésticas (pollos, pavos, patos, pintada, codorniz, palomas) satisfacen estos criterios de seguridad sanita- ria.
La patente US nº 6.025.327 describe un material derivado de cartílago de esternón de pollo, que comprende colágeno de tipo II hidrolizado con un peso molecular medio de alrededor de 1500 a alrededor de 2500 Daltons. La patente US nº 6.323.319 describe un procedimiento para obtener el material en la patente US nº 6.025.327.
La patente US nº 6.780.841 describe un hidrolizado de colágeno de tipo II capaz de inducir la formación de cartílago en un individuo, obteniéndose dicho hidrolizado a partir de cartílago de esternón de pollo, que comprende por lo menos 20% de sulfato de condroitina despolimerizado, por lo menos 10% de ácido hialurónico y con un peso molecular medio de 5.500 a aproximadamente 1000 Daltons.
No se presentan resultados que demuestren tal actividad de formación de cartílago, reducción de artralgias o aumento de la movilidad en un individuo. Además, la patente US nº 6.780.841 establece específicamente que las proporciones de sulfato de condroitina despolimerizado y ácido hialurónico son esenciales, y que se prefieren enormemente las proporciones más elevadas posibles, sugiriendo así que un producto que comprende pequeñas cantidades de sulfato de condroitina despolimerizado y ácido hialurónico sería ineficaz in vivo para inducir la formación de cartílago, reducir la artralgia o incrementar la movilidad en un individuo.
Además, las tres patentes US nº 6.025.327, US nº 6.323.319 y US nº 6.780.841 describen hidrolizados preparados únicamente a partir de cartílago de esternón de pollo, tomándose precauciones particularmente cuidadosas para evitar incluir cualquier hueso, apartándose todo cartílago de articulación a un lado para evitar el riesgo de incluir fragmentos óseos. Estas tres patentes indican muy claramente que las precauciones a tomar para el material bruto muy específico usado son cruciales para la pureza del producto final para evitar la contaminación por colágeno de tipo I o III y de este modo permitir la proporción más elevada posible de proteoglucanos.
El hecho de que no se use cartílago distinto del cartílago de esternón conduce inevitablemente a una eficiencia total en hidrolizado mucho menor que si se usa otro cartílago. Además, las precauciones especiales a tener en cuenta complican gravemente el uso del proceso de preparación del material bruto, y en particular dan como resultado que sea imposible usarlo a escala industrial.
Por lo tanto, sería deseable tener un hidrolizado de cartílago de aves de corral, particularmente un hidrolizado de cartílago de pollo, capaz de inducir la formación de cartílago, reducir la artralgia o incrementar la movilidad en un individuo, y que se pueda obtener mediante un procedimiento de preparación apropiado para uso industrial.
A diferencia de lo que se sugiere en las patentes US nº 6.025.327, nº 6.323.319 y nº 6.780.841, se ha demostrado que es posible obtener una biodisponibilidad in vitro y una eficacia in vivo satisfactorias en pacientes que sufren artralgia, con un hidrolizado de cartílago de pollo que comprende proporciones significativamente menores de sulfato de condroitina despolimerizado y ácido hialurónico, teniendo también dicho hidrolizado un peso molecular medio significativamente menor y una composición de aminoácidos significativamente diferente. Además, tal hidrolizado que tiene una buena eficacia in vivo se puede obtener usando un procedimiento mejorado que conduce a ganancias particularmente apreciables en términos de eficacia, coste y tiempo.
En particular, el hidrolizado desarrollado por los inventores se obtiene a partir de un material bruto que contiene todo cartílago recuperable de un cadáver de pollo, y no exclusivamente a partir del esternón. El material bruto usado es una mezcla compuesta de 70% a 100% en peso de hueso (incluyendo el esternón) y cartílago de articulación, y 0% a 30% en peso de cartílago de esternón. Este material bruto se puede obtener sin tener que usar todas las precauciones esenciales descritas en las patentes US nº 6.025.327, nº 6.323.319 y nº 6.780.841, y por lo tanto se puede producir industrialmente. La eficacia global por cadáver de pollo es también mucho mayor.
Además, el procedimiento para obtener el hidrolizado desarrollado por los inventores es significativamente más rápido que el procedimiento descrito en las patentes US nº 6.025.327, nº 6.323.319 y nº 6.780.841. No incluye una etapa para la incubación del material bruto en agua, y la duración de la etapa de hidrólisis es más corta.
Finalmente, a diferencia del procedimiento descrito en las patentes US nº 6.025.327, nº 6.323.319 y nº 6.780.841, la etapa de esterilización en el procedimiento para obtener el hidrolizado desarrollado por los inventores se lleva a cabo al final del protocolo, lo que permite una mejor seguridad sanitaria.
Por lo tanto, la invención se refiere a un hidrolizado de cartílago aviar caracterizado porque:
Reivindicaciones:
1. Hidrolizado de cartílago aviar caracterizado porque:
2. Hidrolizado según la reivindicación 1, caracterizado porque se prepara a partir de una mezcla de hueso y cartílago de articulación (70%-100% en peso) y posiblemente cartílago de esternón (0%-30% en peso).
3. Procedimiento para preparar un hidrolizado de cartílago aviar según la reivindicación 1 ó 2, que comprende:
4. Hidrolizado según la reivindicación 1 ó 2, u obtenido usando el procedimiento según la reivindicación 3, para uso como un complemento alimentario.
5. Hidrolizado según la reivindicación 1 ó 2, u obtenido usando el procedimiento según la reivindicación 3, para uso como un medicamento.
6. Hidrolizado según la reivindicación 1 ó 2, u obtenido usando el procedimiento según la reivindicación 3, para uso como un medicamento para el tratamiento o prevención de artralgia.
7. Hidrolizado según la reivindicación 6, caracterizado porque el origen de artralgia es degeneración de cartílago relacionada con la edad, esfuerzo excesivo de las articulaciones debido a la práctica intensa de un deporte, o esfuerzo excesivo de las articulaciones debido a obesidad.
Patentes similares o relacionadas:
Composiciones que comprenden una proteína de fusión de VIP-ELP para su uso en el tratamiento de fibrosis quística, del 29 de Julio de 2020, de Phasebio Pharmaceuticals, Inc: Una composición farmacéutica que comprende una proteína de fusión que comprende un péptido intestinal vasoactivo (VIP) y uno o más péptidos de tipo elastina (ELP), que […]
Péptido basado en colágeno tipo II alfa-1 útil para el tratamiento de una enfermedad de la superficie ocular, del 15 de Julio de 2020, de EYEBIO KOREA: Un péptido que consiste en una secuencia de aminoácidos representada por SEQ ID NO: 1.
Matrices de soporte derivadas de TN3 específicas para CD40L y sus métodos de empleo, del 1 de Julio de 2020, de Viela Bio, Inc: Una matriz de soporte de Tenascina 3 (Tn3) que comprende dos subunidades monoméricas específicas para CD40L, conectadas en tándem, donde la subunidad […]
Composiciones para el uso en métodos para el tratamiento de heridas, trastornos y enfermedades de la piel, del 18 de Marzo de 2020, de KRYSTAL BIOTECH, INC: Una composicion farmaceutica que comprende: a) un virus del herpes simple (HSV) con replicacion defectuosa que comprende un genoma del virus […]
Composición de bebida para mejorar la piel, del 18 de Marzo de 2020, de Bottled Science Limited: Una composición de bebida que comprende colágeno y vitamina C, o un derivado de la misma y metil sulfonil metano, en la que dicho colágeno está presente en una […]
Composición farmacéutica para prevenir o tratar los ojos secos, del 29 de Enero de 2020, de EYEBIO KOREA: Una composición farmacéutica para su uso en la prevención o el tratamiento del ojo seco, la composición farmacéutica comprende, como componente activo, un péptido […]
Métodos y composiciones para la condrogénesis in vitro e in vivo, del 18 de Diciembre de 2019, de Lineage Cell Therapeutics, Inc: Una composición que comprende una línea celular progenitora embrionaria clonal para su uso en un método in vivo de generación de cartílago, comprendiendo la composición: […]
Composición secada por pulverización que comprende un extracto de fruto de acerola, colágeno de tipo II hidrolizado y condroitín sulfato, del 30 de Octubre de 2019, de Paninkret Chemisch-Pharmazeutisches Werk GmbH: Método para preparar una composición secada por pulverización que comprende un extracto de fruto de acerola y colágeno hidrolizado, comprendiendo el método las etapas […]