EVALUACION DE DAÑO NEURONAL A PARTIR DE MUESTRAS DE SANGRE.
Un método para detectar una lesión neuronal en un sujeto, comprendiendo el método los pasos de:
(a) poner en contacto una muestra de sangre, suero o plasma obtenida del sujeto con un anticuerpo que se une específicamente a NF-H en la muestra;
(b) detectar la presencia o cantidad de NF-H en la muestra; y
(c) correlacionar la presencia o cantidad de NF-H en la muestra con la lesión neuronal
Tipo: Resumen de patente/invención. Número de Solicitud: W04009114US.
Solicitante: UNIVERSITY OF FLORIDA RESEARCH FOUNDATION, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 223 GRINTER HALL,GAINESVILLE, FL 32611.
Inventor/es: SHAW,GERRY, PIKE,BRIAN,R, TULI,SONAL,S.
Fecha de Publicación: .
Fecha Concesión Europea: 19 de Agosto de 2009.
Clasificación Internacional de Patentes:
- C07K16/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
- G01N33/68V2
Clasificación PCT:
- C07K16/18 C07K 16/00 […] › contra materiales animales o humanos.
- G01N33/68 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que intervienen proteínas, péptidos o aminoácidos.
Clasificación antigua:
- A61B1/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › Instrumentos para proceder al examen médico de las cavidades o conductos del cuerpo por inspección visual o fotográfica, p. ej. endoscopios (examen de las cavidades o conductos del cuerpo utilizando ondas ultrasónicas, sónicas o infrasónicas A61B 8/12; instrumentos endoscópicos para la toma de muestras celulares o para biopsias A61B 10/04; con fines quirúrgicos A61B 17/00; instrumentos quirúrgicos endoscópicos A61B 17/94; instrumentos quirúrgicos que utilizan un haz láser dirigido a lo largo o a través de un conducto flexible A61B 18/22 ); Dispositivos de iluminación al efecto (para los ojos A61B 3/00).
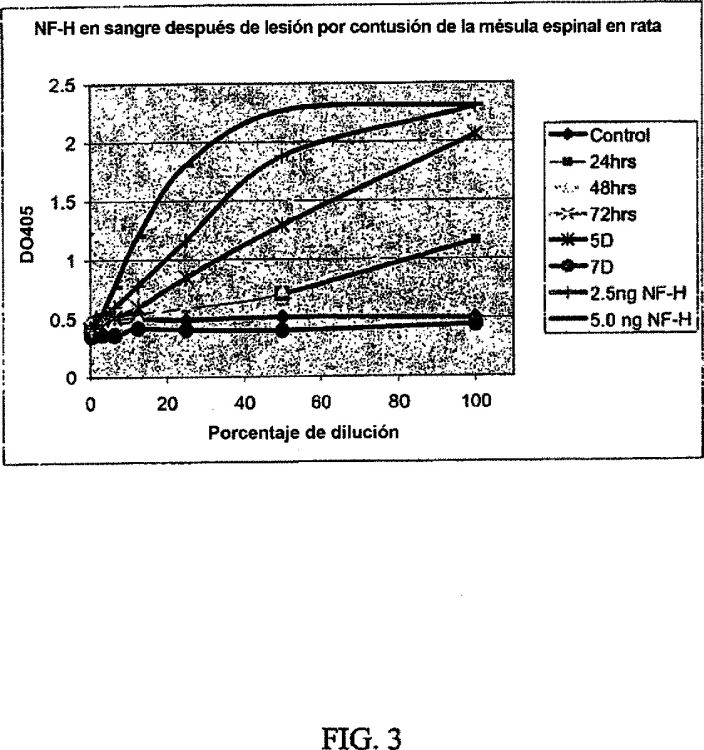
Fragmento de la descripción:
Evaluación de daño neuronal a partir de muestras de sangre.
Declaración respecto a la investigación patrocinada federalmente
Esta invención se realizó con ayuda del gobierno de los Estados Unidos con la subvención número DAMD17-01-0765 concedida por el Ejercito de los Estados Unidos, y la subvención número AA012151-02 concedida por los Institutos Nacionales de Salud. El gobierno de los Estados Unidos puede tener ciertos derechos en la invención.
Campo de la invención
La invención se refiere en general a los campos de la biología y la medicina. Más en particular, la invención se refiere a detectar daño a las células neuronales analizando una muestra biológica para la proteína H de neurofilamentos (NF) liberada de las neuronas dañadas.
Antecedentes
En los últimos años se ha enfocado mucho interés en la detección de proteínas marcadoras específicas en sangre para diagnosticar con rapidez varios tipos de daños y enfermedades. Esos denominados biomarcadores, cuando se estudian en detalle, tienen el potencial de proporcionar el diagnóstico rápido y sencillo de una variedad de daños y enfermedades. Por ejemplo, durante muchos años se ha sabido que la presencia del antígeno polipeptídico de tejido (TPA) en suero humano es un biomarcador útil para varias formas de carcinoma, y que el nivel de expresión de TPA se correlaciona negativamente con el pronóstico del cáncer. TPA se identificó inicialmente produciendo antisueros contra los residuos insolubles de tumores humanos extraídos, y la presunción a partir de los primeros trabajos fue que los componentes de TPA serían proteínas específicas de tumor (Bjorklund, B, Antibiot. Chemother. 22:16-31, 1978). Sin embargo, estudios posteriores indicaron que TPA era realmente un complejo de queratinas 8, 18 y 19 parcialmente degradadas, que son componentes abundantes del citoesqueleto de células epiteliales normales en diferenciación así como de células de carcinoma (Weber et al., Embo. J. 3:2707-2714, 1984). Aparentemente las células de carcinoma que se dividen con rapidez liberan algunos de sus componentes citoplásmicos al suero donde son de alguna manera resistentes a las proteasas séricas y de este modo se pueden detectar mediante pruebas inmunológicas apropiadas. Por lo tanto, los individuos con carcinomas del tipo apropiado tienen cantidades mucho mayores de estos fragmentos proteicos circulantes que los individuos normales. Puesto que el nivel de expresión de TPA en suero refleja fielmente la carga de células de carcinoma, las determinaciones de TPA tienen valor tanto de diagnóstico como de pronóstico. Otro ejemplo de este tipo de planteamiento es el seguimiento del infarto de miocardio, en el que se miden los niveles de creatina quinasa cardiaca y troponina I cardiaca. El contenido en suero de estas proteínas, liberadas de las células cardiacas dañadas, proporciona información médicamente útil que va en el tamaño del infarto que tiene valor pronóstico. Estos tipos de descubrimientos y muchos otros establecen el principio de que las proteínas normales de las células se pueden expresar a niveles mucho más altos en suero en ciertos tipos específicos de daños y enfermedades, y su detección inmunológica puede ser de uso diagnóstico y de pronóstico.
Aunque las enfermedades asociadas con lesión neuronal son una preocupación sanitaria principal en todo el mundo, no se ha encontrado un biomarcador específico fiable y conveniente de lesión neuronal, incluso aunque tal marcador tenga una gran utilidad científica y clínica potencial (Ingebrigtsen y Romner, J. Trauma 52:798-808, 2002). Se han descrito algunos marcadores potenciales de lesión cerebral pero todos tienen desventajas. Por ejemplo, estudios previos han propuesto que S100-ß, enolasa específica de neuronas (NSE) (Persson et al., Stroke 18:911-918, 1987) y más recientemente productos de degradación de la espectrina (SBP, Pike et al., J Cereb Blood Flow Metab 24:98-106, 2004) en muestras biológicas podían ser útiles para medir la lesión cerebral. Sin embargo ni S100-ß ni los SBP son específicos para el daño neuronal o incluso del sistema nervioso. La enolasa específica de neuronas parece más prometedora, ya que se expresa en grandes cantidades solo en neuronas, pero no se ha usado ampliamente tal vez porque la NSE es una proteína relativamente inestable. La proteína asociada a microtúbulos (MAP) tau también se ha propuesto como un biomarcador de lesión neuronal (Zemlan et al., J Neurochem 72:741-750, 1999). Sin embargo, no es una proteína particularmente abundante y también se expresa en células no neuronales (por ejemplo, células gliales astrocíticas reactivas (Togo y Dickson, Acta Neuropathol. 104:398-402, 2002)). Por lo tanto existe una necesidad para un ensayo de diagnóstico rápido y fiable que se pueda usar para evaluar de forma conveniente el daño neuronal. Tal ensayo sería útil para evaluar el daño neuronal en animales de experimentación y para controlar los efectos de fármacos que pueden ser neuroprotectores en estos animales. Tal ensayo sería particularmente útil si se pudiera detectar la molécula relevante en sangre más que líquido cefalorraquídeo (LCR), ya que obtener sangre no es solo rutinario en contextos de investigación y médicos, sino que también es mucho más fácil, menos agresivo y potencialmente menos peligroso que obtener LCR. El biomarcador potencial sería particularmente útil si se pudiera detectar en sangre a las pocas horas del traumatismo, ya que esto permitiría que se usara en el servicio de urgencias para controlar víctimas humanas de accidentes con lesión neuronal potencial en la médula espinal o el cerebro. Es difícil determinar cuánta lesión neuronal se ha producido en víctimas de accidentes usando la actual tecnología de rayos X, TAC e IRM. La detección y cuantificación de un biomarcador de lesión neuronal puede tener por lo tanto un considerable valor de diagnóstico y pronóstico en seres humanos.
Hu Y-Y et al. "Elevated levels of phosphorylated neurofilament proteins in cerebrospinal fluid of Alzheimer disease patients", Neuroscience Letters, Limerick, IE, vol. 320, no. 3, 8 de marzo de 2002, pp. 156-160, divulgan que los niveles de NF-H/M no fosforiladas y NF-L son significativamente mayores en pacientes con enfermedad de Alzheimer y demencia vascular. Además divulgan que un nivel aumentado de NF-H/M fosforilada y NF-L sola también está ligado a la enfermedad de Alzheimer y usan un ELISA sándwich para subunidades de NF, incluyendo NF-H, en líquido cefalorraquídeo.
Hashimoto Ryota et al., "Quantitative analysis of neurofilament proteins in Alzheimer brain by enzyme linked immunosorbent assay system", Psychiatry and Clinical Neurosciences, vol. 53, no. 5, Octubre 1999, pp. 587-591, describen la detección de dos subunidades de NF (L y H) en cerebro con Alzheimer e informan de que la NF-H fosforilada aumenta en los cerebros.
Skuoen J S et al., "Protein markers in cerebrospinal fluid in experimental nerve root injury. A study of slow-onset chronic compression effects or the biochemical effects of nucleus pulposus on sacral nerve roots", Spine, 1 Nov. 1999, vol. 24, no. 21, 1 Noviembre 1999 (01-11-1999), pp. 2195-2200, describen que se usó un ELISA sándwich para demostrar que los niveles de NF-L están aumentados en líquido cefalorraquídeo después de lesión neuronal traumática (compresión de la raíz nerviosa).
Compendio
La solicitud se refiere al descubrimiento de que una lesión al tejido del sistema nervioso central (SNC) tales como la médula espinal o el cerebro en un animal de experimentación produce la liberación de proteínas que se originan en los NF que se pueden detectar en líquidos biológicos tales como sangre y LCR del animal. La presencia de estas proteínas derivadas de NF se puede detectar usando ensayos que utilizan anticuerpos que se unen específicamente a NFDP (proteínas y péptidos derivados de NF) particulares. Puesto que la expresión de los NF está completamente restringida a neuronas, la medida de las NFDP proporciona una manera de detectar de forma específica e inequívoca el daño neuronal.
Los NF están compuestos predominantemente de tres proteínas subunidades, es decir NF-L, NF-M, NF-H, con cantidades más pequeñas de dos proteínas más, a-internexina y periferina (Shaw, 1998 Neurofilaments. Nueva York: Springer). Cuando las neuronas se dañan las subunidades de los NF, que normalmente se encuentran en filamentos estables de 10 nm de diámetro, se rompen a componentes solubles bajo la influencia de varias enzimas endógenas, tales como las calpaínas, catepsinas, caspasas y otras. Estas...
Reivindicaciones:
1. Un método para detectar una lesión neuronal en un sujeto, comprendiendo el método los pasos de:
- (a) poner en contacto una muestra de sangre, suero o plasma obtenida del sujeto con un anticuerpo que se une específicamente a NF-H en la muestra;
- (b) detectar la presencia o cantidad de NF-H en la muestra; y
- (c) correlacionar la presencia o cantidad de NF-H en la muestra con la lesión neuronal.
2. El método de la reivindicación 1, en donde el paso (b) de detectar la presencia o cantidad de NF-H comprende realizar un inmunoensayo seleccionado del grupo que consiste en inmunotransferencia, ELISA, radioinmunoensayo, inmunodifusión e inmunoprecipitación.
3. El método de la reivindicación 2, en donde el paso (b) de detectar la presencia o cantidad de NF-H en la muestra comprende realizar un ELISA.
4. Uso de un kit para detectar una lesión neuronal en un sujeto mediante el método según cualquiera de las reivindicaciones anteriores, comprendiendo el kit:
- (a) un sustrato sólido;
- (b) al menos un anticuerpo que se une específicamente a NF-H;
- (c) un agente para detectar la unión del al menos un anticuerpo a NF-H; e
- (d) instrucciones para usar el kit para detectar lesión neuronal en un sujeto.
5. El uso de la reivindicación 4, en donde el agente para detectar la unión del al menos un anticuerpo a NF-H comprende una molécula de sustrato cromogénico.
Patentes similares o relacionadas:
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Terapia basada en anticuerpos de la amiloidosis por transtiretina (TTR) y anticuerpos de origen humano para ese propósito, del 22 de Julio de 2020, de Neurimmune Holding AG: Un anticuerpo anti-transtiretina (TTR) de origen humano o un fragmento de unión a antígeno del mismo, que es capaz de unirse a especies de TTR mutadas, mal plegadas, […]
Polipéptidos biparatópicos antagonistas de la señalización WNT en células tumorales, del 15 de Julio de 2020, de Boehringer Ingelheim International GmbH & Co. KG: Un polipéptido que se une específicamente a LRP5 o LRP6, que comprende - un primer dominio variable individual de inmunoglobulina seleccionado del grupo de dominios […]
PTPRS y proteoglicanos en enfermedad autoinmune, del 15 de Julio de 2020, de LA JOLLA INSTITUTE FOR ALLERGY AND IMMUNOLOGY: Una proteína recombinante no enzimática que comprende una secuencia de aminoácidos de un dominio extracelular de PTPRS, donde la proteína comprende tanto el dominio 1 (Ig1) […]
Redirectores de células T específicas de antígenos, del 1 de Julio de 2020, de THE JOHNS HOPKINS UNIVERSITY: Una nanoparticula que comprende en su superficie: (A) un anticuerpo que se une especificamente a un antigeno de celula diana o epitopo del mismo; y (B) un resto […]
Anticuerpos scFv que pasan las capas epitelial y/o endotelial, del 1 de Julio de 2020, de ESBATech, an Alcon Biomedical Research Unit LLC: Un anticuerpo monocatenario (scFv) que comprende: (a) un dominio variable de la cadena ligera (VL) que tiene tres regiones CDR de VL no […]
Moléculas de unión con cadena J modificada, del 24 de Junio de 2020, de IGM BIOSCIENCES, INC: Una molécula de unión que comprende un anticuerpo de IgM, IgA, IgG/IgM o IgG/IgA con una cadena J modificada, donde la cadena J modificada comprende una cadena […]
Terapia de combinación para tratamiento de enfermedad, del 24 de Junio de 2020, de Mereo BioPharma 5, Inc: Un anticuerpo antagonista del ligando 4 tipo delta (DLL4) para su uso en un procedimiento para tratar el cáncer, inhibir el crecimiento tumoral, mejorar […]