COMPOSICIONES ANESTESICAS LIPOSOMICAS DE LIBERACION SOSTENIDA.
Una composición farmacéutica que comprende un anestésico amida encapsulado en un liposoma multivesicular,
comprendiendo dicho liposoma multivesicular anestésico amida; al menos un ácido seleccionado del grupo constituido por un ácido mineral diprótico, un ácido mineral triprótico y un polihidroxi carboxilato o combinaciones de los mismos; un componente lipídico que comprende al menos un lípido anfipático y al menos un lípido neutro que carece de un grupo de cabeza hidrófilo; y, opcionalmente, un colesterol y/o un esterol vegetal
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US98/19583.
Solicitante: DEPOTECH CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 10450 SCIENCE CENTER DRIVE,SAN DIEGO, CA 92121.
Inventor/es: KIM, SINIL, KIM,TAEHEE, MURDANDI,SHARAD.
Fecha de Publicación: .
Fecha Concesión Europea: 7 de Abril de 2010.
Clasificación Internacional de Patentes:
- A61K31/167 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo el átomo de nitrogeno de un grupo carboxiamida unido directamente al ciclo aromático, p. ej. lidocaina, paracetamol.
- A61K31/40 A61K 31/00 […] › que tienen ciclos con cinco eslabones con un nitrógeno como único heteroátomo de un ciclo, p. ej. sulpirida, succinimida, tolmetina, buflomedil.
- A61K31/445 A61K 31/00 […] › Piperidinas no condensadas, p. ej. piperocaína.
- A61K9/00M5
- A61K9/127 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Liposomas.
- A61K9/127B2
Clasificación PCT:
- A61K9/127 A61K 9/00 […] › Liposomas.
Clasificación antigua:
- A61K9/127 A61K 9/00 […] › Liposomas.
Fragmento de la descripción:
Composiciones anestésicas liposómicas de liberación sostenida.
Antecedentes de la invención
La presente invención se refiere a formulaciones liposómicas de compuestos tales como fármacos. Más particularmente, la presente invención se refiere a procedimientos de encapsular anestésicos en liposomas multivesiculares con una eficiencia elevada y tasas de liberación sostenidas in vivo.
Normalmente, la duración de la acción de un anestésico local tras su administración es suficientemente larga como para cubrir el dolor infligido durante la mayoría de los procedimientos quirúrgicos. No obstante, la duración de la acción no es lo bastante larga como para cubrir la mayoría del dolor posquirúrgico o el dolor producido por muchos procedimientos diagnósticos invasivos o por lesiones. La infusión continua o la infiltración repetida de un anestésico local en una herida quirúrgica, "puerto" diagnóstico o punto de lesión no es práctica. Por tanto, una formulación de liberación sostenida de un anestésico local sería útil para el tratamiento del dolor, especialmente a la luz de las tendencias actuales de cirugías ambulatorias y centros de atención de emergencia. Deseablemente, dichas formulaciones también son útiles en el dolor traumático y diagnóstico.
En la literatura se han descrito varios enfoques para desarrollar formulaciones de liberación sostenida de anestésicos locales. Por ejemplo, microesferas de polímero de ácido poliláctico-co-glicólico que contienen bupivacaína y dexametasona han producido una duración prolongada de la anestesia local. También se ha demostrado que formas cristalinas de anestésicos locales tienen una duración prolongada de la acción. Se ha demostrado que bupivacaína lipófila sin base incorporada en las membranas de liposomas multilaminares y liposomas unilaminares grandes cargados con un gradiente de protones tienen una eficacia que dura de 6 a 11 horas.
Se están desarrollando liposomas multivesiculares (LMV) como sistema de liberación de fármacos de liberación sostenida basado en lípidos para la liberación local, regional o sistémica del fármaco. Se ha demostrado la liberación sostenida de muchos fármacos estables en agua encapsulados en LMV en modelos con animales por las vías de administración intratecal, subcutánea, intraperitoneal y epidural, así como en pacientes humanos mediante las vías intracerebroventricular, intratecal, subcutánea y epidural. En un ensayo clínico de fase III, multicéntrico y aleatorizado de una formulación de LMV del agente citotóxico citarabina se ha demostrado que esta formulación es más eficaz que la citarabina libre en el tratamiento del carcinoma leptomeningial.
Los LMV se definen como liposomas que contienen múltiples cámaras no concéntricas dentro de cada partícula de liposoma, que se asemejan a una matriz "de tipo espuma". Dichas partículas se deben distinguir de las vesículas multilaminares (VML), también conocidas como liposoma multilaminar, que contienen múltiples cámaras concéntricas dentro de cada partícula de liposoma. Otra partícula distinta es la vesícula unilaminar (VUL), también conocida como liposoma unilaminar, que incluye un único compartimento acuoso interno. La presente invención se refiere a LMV. La técnica anterior describe la preparación de LMV (Kim y coI., Biochim. Biophys. Acta 728, 339-348, 1983).
Muchas de las sustancias catiónicas biológicamente activas usadas en las técnicas de encapsulación en LMV se usan como sales de ácidos minerales monopróticos (por ejemplo, como sales de clorhidrato). La técnica anterior (documento WO 9 703 652) ha usado dichas sales de ácidos minerales monopróticos disponibles habitualmente de sustancias catiónicas biológicamente activas para su encapsulación en liposomas sin realizar ninguna modificación en una sal de ácido mineral diprótico o triprótico. La técnica anterior también ha usado ácidos orgánicos, tales como ácidos cítrico o glutámico, para efectuar la encapsulación.
Resumen de la invención
La invención proporciona anestésicos locales encapsulados en liposomas multivesiculares (LMV), es decir vesículas lipídicas que tienen múltiples cámaras acuosas internas no concéntricas que tienen membranas internas distribuidas en forma de red a lo largo del LMV. Las cámaras contienen ácidos que son eficaces para permitir la encapsulación de ciertos anestésicos y para modular la velocidad de liberación de los anestésicos encapsulados. La invención también proporciona procedimientos para fabricar dichas composiciones y para proporcionar anestesia local a los sujetos mediante la administración de las composiciones.
La técnica anterior ha usado sales monopróticas disponibles habitualmente (por ejemplo clorhidrato o glutámico) de compuestos biológicamente activos. Esto ha tenido como resultado formulaciones inaceptables para encapsular las sustancias biológicamente activas en LMV o una eficiencia de encapsulación muy baja. La invención es el resultado del sorprendente hallazgo de que la inclusión de la forma de base libre de los compuestos anestésicos solubilizados con ácido fosfórico, o la conversión de las sales clorhidrato disponibles habitualmente de los compuestos anestésicos en sales fosfato (sal de ácido mineral triprótico) o sulfato (sal de ácido mineral diprótico) para su inclusión en LMV tiene como resultado una considerablemente mejora en la eficiencia de la encapsulación así como una liberación sostenida en medio biológicamente relevante. También se incluyen los ácidos orgánicos polialcohólicos, tales como ácido glucurónico o glucónico, en los que dicho ácido está co-encapsulado con anestésicos para ayudar en la encapsulación y efectuar la liberación sostenida del anestésico. Sorprendentemente, los ácidos orgánicos polialcohólicos son superiores a los ácidos orgánicos no polialcohólicos, y dan composiciones con una elevada eficiencia de encapsulación y liberación sostenida del anestésico. Los ácidos orgánicos polialcohólicos mejoran considerablemente la encapsulación del anestésico y la aceptabilidad de la formulación. Las sales sulfato y una serie de otras sales requieren la inclusión de dichos ácidos para formar formulaciones aceptables.
Cuando el anestésico encapsulado se administra en forma de una única dosis intracutánea o subcutánea, la duración o la anestesia y la semivida del fármaco en el punto de inyección local aumentan en comparación con la inyección del anestésico sin encapsular. La dosis máxima tolerada del anestésico encapsulado también está considerablemente aumentada en la formulación liposómica con respecto a la inyección del anestésico sin encapsular.
El principal uso para la invención es para fabricar formulaciones de liberación sostenida de sustancias biológicamente activas que tienen elevadas velocidades de difusión a través de las membranas de bicapa lipídica. El uso de sales de ácidos minerales tanto dipróticos como tripróticos de sustancias biológicamente activas y la co-encapsulación de ácidos orgánicos polialcohólicos permite que estos fármacos difíciles de encapsular se encapsulen con facilidad y se liberen lentamente.
Otras características y ventajas de la invención serán evidentes a partir de la siguiente descripción detallada y a partir de las reivindicaciones.
Breve descripción de las figuras
La figura 1A es un gráfico que muestra el efecto anestésico (número de falta de respuesta a seis punciones en función del tiempo tras una única dosis intracutánea de fosfato de bupivacaína encapsulada en LMV que contiene diferentes concentraciones de bupivacaína.
La figura 1B es un gráfico que muestra el efecto anestésico (número de faltas de respuesta a seis punciones en función del tiempo tras una única dosis intracutánea de clorhidrato de bupivacaína no encapsulado a diferentes concentraciones.
La figura 2 es un gráfico que muestra una comparación de la duración de la anestesia para las formulaciones de las figuras 1A (fosfato de bupivacaína encapsulada en LMV, círculos rellenos) y 1B (clorhidrato de bupivacaína no encapsulado, círculos vacíos) cuantificada mediante el "tiempo hasta la mitad de la respuesta máxima (R3)" (eje de ordenadas) frente a la concentración de la dosis administrada (eje de abscisas).
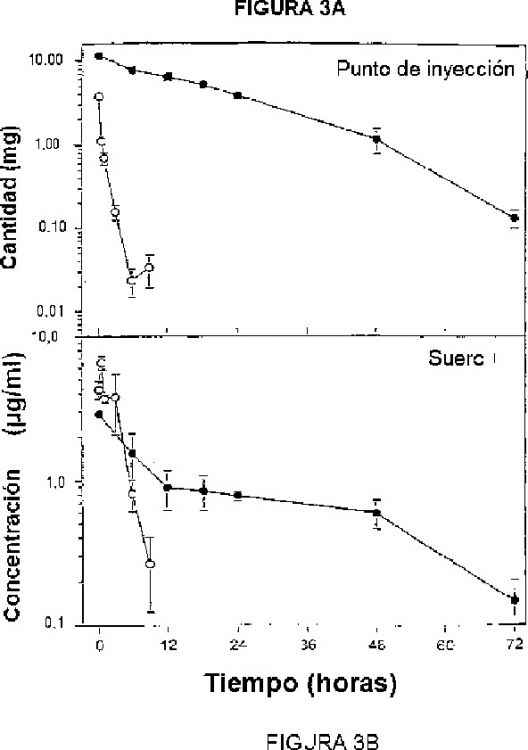
La figura 3A es un gráfico que muestra la cantidad total de bupivacaína (mg) que queda en un punto de inyección hasta 72 horas después de una única dosis intracutánea de fosfato de bupivacaína encapsulada en LMV (círculos rellenos) o clorhidrato...
Reivindicaciones:
1. Una composición farmacéutica que comprende un anestésico amida encapsulado en un liposoma multivesicular, comprendiendo dicho liposoma multivesicular anestésico amida; al menos un ácido seleccionado del grupo constituido por un ácido mineral diprótico, un ácido mineral triprótico y un polihidroxi carboxilato o combinaciones de los mismos; un componente lipídico que comprende al menos un lípido anfipático y al menos un lípido neutro que carece de un grupo de cabeza hidrófilo; y, opcionalmente, un colesterol y/o un esterol vegetal.
2. La composición de la reivindicación 1, en la que el ácido es un ácido mineral triprótico.
3. La composición de la reivindicación 2, en la que el ácido mineral triprótico es ácido fosfórico.
4. La composición de la reivindicación 1, en la que dicho al menos un lípido anfipático se selecciona del grupo constituido por dierucoilfosfatidilcolina y dipalmitoilfosfatidilglicerol.
5. La composición de la reivindicación 1, en la que dicho al menos un lípido anfipático comprende dierucoilfosfatidilcolina.
6. La composición de la reivindicación 1, en la que dicho al menos un lípido anfipático comprende dipalmitoilfosfatidilglicerol.
7. La composición de la reivindicación 1, en la que dicho al menos un lípido neutro comprende tricaprilina.
8. La composición de la reivindicación 1, en la que el anestésico amida se selecciona del grupo constituido por bupivacaína, mepivacaína, ropivacaína, lidocaína, pirrocaína, prilocaína, sus estereoisómeros y combinaciones de los mismos.
9. La composición de la reivindicación 1, en la que el anestésico amida es bupivacaína.
10. La composición de la reivindicación 1, en la que el lípido anfipático se proporciona en mezcla con colesterol.
11. La composición de la reivindicación 1, en la que el ácido es ácido fosfórico, dicho al menos un lípido anfipático comprende dierucoilfosfatidilcolina y/o dipalmitoilfosfatidilglicerol, dicho al menos un lípido neutro comprende tricaprilina, dicho anestésico amida es bupivacaína.
12. La composición de la reivindicación 8, en la que el anestésico amida tiene la estructura siguiente:
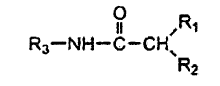
en la que R1 es una alquilamina secundaria o terciaria o una alquilenamina secundaria o terciaria, R2 es hidrógeno, alquilo o alquileno que además se une a R1, R3 es un sustituyente fenilo alquilsustituido.
13. La composición de la reivindicación 12, en la que R1 y R2 forman un sustituyente seleccionado del grupo constituido por N-alquilpiperidina y N-alquilpirrolidina.
14. La composición de la reivindicación 12, en la que R3 es un sustituyente 2,6-dimetilfenilo.
Patentes similares o relacionadas:
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Triple combinación de antagonistas del receptor 5-HT6 puros, inhibidores de la acetilcolinesterasa y antagonista del receptor NMDA, del 15 de Julio de 2020, de SUVEN LIFE SCIENCES LIMITED: Una combinación que comprende un antagonista del receptor 5-HT6 puro, un inhibidor de la acetilcolinesterasa y un antagonista del receptor NMDA, en el que el antagonista […]
Combinación de agonistas inversos del receptor de histamina-3 con inhibidores de acetilcolinesterasa, del 24 de Junio de 2020, de SUVEN LIFE SCIENCES LIMITED: Una combinación que comprende un agonista inverso del receptor de histamina-3 y un inhibidor de acetilcolinesterasa; en donde el agonista inverso del receptor de histamina-3 […]
Compuestos inhibidores de la acetilcolinesterasa y agonistas de los receptores serotoninérgicos 5HT4, con efecto paramnesiante, sus procedimientos de preparación y composiciones farmacéuticas que los contienen, del 10 de Junio de 2020, de Université de Caen: Compuesto de fórmula general (I): **(Ver fórmula)** en la que: X representa un átomo de hidrógeno, o un átomo de halógeno […]
Nuevos derivados de piperazina y piperidina, síntesis y uso de los mismos en la inhibición de la oligomerización de VDAC, la apoptosis y la disfunción mitocondrial, del 3 de Junio de 2020, de The National Institute for Biotechnology in the Negev Ltd: Compuesto de Fórmula general (Id): **(Ver fórmula)** en la que L2 es un grupo de enlace seleccionado del grupo que consiste en un alquilamidileno […]
Compuestos de benzaldehído sustituidos y métodos para su uso en el aumento de la oxigenación tisular, del 27 de Mayo de 2020, de Global Blood Therapeutics, Inc: Un compuesto de Fórmula (I): **(Ver fórmula)** o un tautómero o una sal farmacéuticamente aceptable del mismo, para su uso en el tratamiento […]
Composición farmacéutica en comprimido que comprende bilastina, del 27 de Mayo de 2020, de Alfred E. Tiefenbacher (GmbH & Co. KG): Una composición farmacéutica en forma de comprimido, que comprende a) una forma cristalina de bilastina, en donde la forma cristalina tiene picos característicos a 6,53, […]
Nuevas composiciones para prevenir y/o tratar trastornos degenerativos del sistema nervioso central, del 27 de Mayo de 2020, de AMICUS THERAPEUTICS, INC: Un compuesto de Fórmula III: **(Ver fórmula)** en donde: R1 es C(R2)(R3)(R4); R2 es hidrógeno, -OH o halógeno; R3 es hidrógeno, -OH, halógeno o -CH3; […]