Producción mejorada de cefalosporina.
Una cepa de Penicillium productora de cefalosporina que ha adquirido la capacidad de producir cefalosporinasdespués de haber sido transformada con un gen que codifica expandasa,
y opcionalmente después de sertransformada además con un gen que codifica hidroxilasa, una hidroxilasa y una acetiltransferasa, o con unahidroxilasa y una acetiltransferasa y una O-carbamoil transferasa, siendo capaz dicho Penicillium de producirderivados N-acilados de 7-ADCA, 7-ADAC, 7-ACA y de ácido 7-amino-3-carbamoil-oximetil-3-cefem-4-carboxílico,respectivamente, caracterizada por que ha sido transformada con un gen CefT heterólogo que codifica una proteínaCefT que es una proteína implicada en el transporte de un compuesto cefalosporínico desde el interior delmicroorganismo productor de cefalosporina hacia el exterior del microorganismo productor de cefalosporina, y con loque la relación de la capacidad de producción de cefalosporina de la cepa de Penicillium transformada con el genCefT heterólogo en comparación con la capacidad de producción de cefalosporina de la cepa de Penicillium notransformada con el gen CefT heterólogo es al menos 1,2.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/051755.
Solicitante: DSM Sinochem Pharmaceuticals Netherlands B.V.
Nacionalidad solicitante: Países Bajos.
Dirección: Alexander Fleminglaan 1 2613 AX Delft PAISES BAJOS.
Inventor/es: BOVENBERG, ROELOF, ARY, LANS, DRIESSEN,ARNOLD,JACOB,MATTIEU, VAN DEN BERG,MARCO ALEXANDER, HANS,MARCUS, NIJLAND,JEROEN GERBEN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D501/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › Compuestos heterocíclicos que contienen sistemas cíclicos tia-5 aza-1 biciclo [4.2.0] octano, es decir, compuestos que contienen un sistema cíclico de fórmula: , p. ej. cefalosporinas; Estando estos sistemas cíclicos adicionalmente condensados, p. ej. condensados en posición 2, 3 con heterociclos que contienen oxígeno, nitrógeno o azufre.
- C12N15/81 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › para levaduras.
- C12P35/06 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 35/00 Preparación de compuestos que contienen un sistema cíclico 5-tia, 1-aza biciclo [4.2.0] octano, p. ej. cefalosporina. › Cefalosporina C; Sus derivados.
- C12R1/645 C12 […] › C12R SISTEMA DE INDEXACION ASOCIADO A LAS SUBCLASES C12C - C12Q, RELATIVO A LOS MICROORGANISMOS. › C12R 1/00 Microorganismos. › Hongos.
PDF original: ES-2423454_T3.pdf
Fragmento de la descripción:
Producción mejorada de cefalosporina La presente invención se refiere a la producción fermentativa de una cefalosporina en un microorganismo.
El hongo filamentoso Penicillium chr y sogenum es un productor natural de antibióticos !-lactámicos, tales como penicilina G. En las últimas décadas, las capacidades de producción de penicilina G mejoraron enormemente mediante mejora de la cepa clásica, dando como resultado cepas de producción industrial poderosas. Recientemente, por medio de manipulación mediante ingeniería genética de la ruta metabólica, se integraron con éxito varias rutas para la producción de cefalosporina en las cepas de producción de penicilina, en particular Penicillium chr y sogenum. En el documento EP-A-0532341, se transformó Penicillium chr y sogenum con el gen cefE de Streptomyces clavuligerus que codifica una expandasa que permite a la cepa transformada producir adipil-7-ADCA (ácido adipil-7-amino-3-metil-3-cefem-4-carboxílico) cuando se cultiva en presencia del precursor ácido adípico. En el documento EP-A-0540210, además del gen cefE de Streptomyces clavuligerus, se transformó Penicillium chr y sogenum con un gen de hidroxilasa cuyo producto de expresión convierte la cadena lateral de 3metilo de adipil-7-ADCA en 3-hidroximetilo, para dar ácido adipil-7-aminodesacetilcefalosporánico (adipil-7-ADAC) ; en otro ejemplo, en el documento EP-A-0540210, Penicillium chrisogenum, ya transformado con genes que codifican expandasa e hidroxilasa, se transforma adicionalmente con un gen de acetiltransferasa cuyo producto de expresión convierte la cadena lateral 3-hidroximetílica en la cadena lateral 3-acetiloximetílica para dar adipil-7-ACA. En el documento WO 2004/106347, una cepa de Penicillium chr y sogenum se ha transformado con genes que codifican una expandasa, una hidroxilasa y una enzima O-carbamoil transferasa, dando como resultado ácido adipil-7-amino3-carbamoiloximetil-3-cefem-4-carboxílico.
Las cepas industriales de Penicillium chr y sogenum se han seleccionado por su capacidad para producir y segregar grandes cantidades de una variedad de compuestos beta-lactámicos, en particular penicilina G y penicilina V, en el medio de cultivo. Varias líneas de prueba indican que la secreción de beta-lactama es un proceso activo, posiblemente vía proteínas de transporte. Durante las últimas etapas de tales procesos de fermentación, se encuentran títulos extremadamente elevados de beta-lactama en fermentaciones a escala industrial. El documento WO 01/32904 describe varios polipéptidos transportadores ABC que están implicados en la secreción de penicilina G. La potenciación de la actividad transportadora ABC dio como resultado una secreción potenciada del compuesto beta-lactámico.
La producción de moléculas de cefalosporina en hospedantes de producción recombinante no cefalosporínicos naturalmente, tales como las cepas de Penicillium explicadas aquí anteriormente, todavía plantea varios problemas. Por ejemplo, el nivel de secreción de los compuestos deseados es todavía relativamente bajo y se debe de incrementar a fin de ser tanto técnica como económicamente más atractivo. La tasa de producción de cefalosporinas producidas en P. chr y sogenum estará limitada debido al hecho de que los transportadores de penicilina, es decir, los polipéptidos transportadores ABC, tendrán una baja afinidad por el compuesto cefalosporínico. Se ha sugerido en el documento WO 01/32904 que esto se podría superar clonando uno o más polipéptidos transportadores ABC homólogos, a partir de productores naturales de cefalosporina tales como Acremonium chr y sogenum usando los polinucleótidos que codifican los transportadores ABC descritos en el documento WO 01/32904.
El hongo filamentoso Acremonium chr y sogenum es un productor natural de cefalosporinas tales como cefalosporina C. En una cepa particular de este hongo, Acremonium chr y sogenum C10, se ha identificado recientemente un gen CefT que codifica una proteína de la bomba de eflujo putativa y, al mismo tiempo, aumenta significativamente la producción de cefalosporina C (Ullán et al. (2002) Mol. Genet. Genomics, 267, 673-683; Liras y Martin (2006) International Microbiology 9, 9-19; Martin et al. (2005) Curr. Opinion Microbiol. 8, 282-293) . La secuencia nucleotídica del gen CetT se ha depositado en la base de datos nucleotídica del National Center for Biotechnology Information con el número de acceso (locus) AJ487683. El NCBS se puede acceder en INTERNET en www.ncbi.nlm.nih.gov, y la secuencia nucleotídica del gen CefT en http://www.ncbi.nlm.nih.gov/entrez/viewer.fcgi?db=nucleotide&val=21214008. A partir de la secuencia de aminoácidos de la proteína codificada por el CefT, los autores concluyeron que es una proteína transmembránica puesto que tiene 12 segmentos transmembránicos (TMS) y contiene los motivos A, B, C, D2 y G característicos del grupo de 12 TMS del antiportador fármaco:H+ de la superfamilia de facilitadores principales. La proteína CefT confiere resistencia a ciertos ácidos orgánicos tóxicos, incluyendo ácido isovalérico y ácido fenilacético, como se concluyó a partir del hecho de que estos ácidos fueron tóxicos a una cepa de Acremonium en la que la CefT se inactivó. La sobreexpresión del gen homólogo CefT dio como resultado una producción mejorada de cefalosporina C en Acremonium chr y sogenum. Este no fue el caso cuando se usó una forma truncada del gen CefT. Sin embargo, la inactivación específica del gen CefT no afectó a la producción de cefalosporina C en Acremonium chr y sogenum, lo que sugiere que hay sistemas redundantes implicados en la exportación de cefalosporina en Acremonium chr y sogenum.
La proteína CefT de Acremonium chr y sogenum C10 no pertenece a la familia de transportadores ABC. La comparación de la secuencia de aminoácidos de la proteína CefT de Acremonium chr y sogenum C10 (Ullán et al (2002) ) con cualquier secuencia de aminoácidos de los transportadores ABC descritos en el documento WO
01/32904 revela que la proteína CefT no tiene ninguna homología con las proteínas transportadoras ABC (es decir, <25%) .
La expresión “gen CefT” se refiere a un gen que codifica una proteína CefT, es decir, una proteína implicada en el transporte de un compuesto cefalosporínico desde el interior del microorganismo productor de cefalosporina hacia el exterior del microorganismo productor de cefalosporina. Un ejemplo de tal gen CefT de la cepa Acr y monium chr y sogenum C10 se puede encontrar en Ullán et al (2002) , que también describe la secuencia de aminoácidos de la proteína CefT codificada por el gen CefT.
La expresión “gen CefT heterólogo” significa que el gen CefT se puede obtener de cualquier microorganismo hospedante y se usa para transformar un microorganismo productor de cefalosporina, con la condición de que el microorganismo hospedante adecuado del que deriva el gen CefT no sea la misma especie que el microorganismo productor de cefalosporina transformado con el gen CefT.
La expresión “gen CefT homólogo” significa que el gen CefT se obtiene de cualquier microorganismo hospedante adecuado y se usa para transformar un microorganismo productor de cefalosporina, con la condición de que el microorganismo hospedante adecuado del que deriva el gen CefT sea la misma especie que el microorganismo productor de cefalosporina transformado con el gen CefT. La transformación de la cepa Acr y monium chr y sogenum C10 con un gen CefT homólogo que se origina de la misma cepa Acr y monium chr y sogenum C10 ha sido descrita por Ullán et al. (2002) .
El término “homología” se refiere a la identidad de la secuencia de un primer gen, proteína o enzima con la secuencia de un segundo gen, proteína o enzima. A lo largo de esta descripción, el grado de homología se expresa como un porcentaje de identidad con un gen, proteína o enzima de referencia. La determinación de estas homologías se puede llevar a cabo por métodos conocidos por el experto, por ejemplo usando la secuencia proteica de la proteína de referencia como “secuencia de interrogación” para llevar a cabo una búsqueda frente a bases de datos públicas para, por ejemplo, identificar otros miembros de la familia o secuencias relacionadas. Tales búsquedas se pueden llevar a cabo usando programas BLAST (versión 2.2) usando los parámetros por defecto del programa respectivo. Véase, por ejemplo, http://www.ncbi.nlm.nih.gov.
En un primer aspecto, la presente invención proporciona un microorganismo productor de cefalosporina caracterizado por que se ha transformado con un gen CefT heterólogo y con lo que el microorganismo transformado tiene una capacidad productora de cefalosporina mejorada en comparación con el microorganismo... [Seguir leyendo]
Reivindicaciones:
1. Una cepa de Penicillium productora de cefalosporina que ha adquirido la capacidad de producir cefalosporinas después de haber sido transformada con un gen que codifica expandasa, y opcionalmente después de ser transformada además con un gen que codifica hidroxilasa, una hidroxilasa y una acetiltransferasa, o con una 5 hidroxilasa y una acetiltransferasa y una O-carbamoil transferasa, siendo capaz dicho Penicillium de producir derivados N-acilados de 7-ADCA, 7-ADAC, 7-ACA y de ácido 7-amino-3-carbamoil-oximetil-3-cefem-4-carboxílico, respectivamente, caracterizada por que ha sido transformada con un gen CefT heterólogo que codifica una proteína CefT que es una proteína implicada en el transporte de un compuesto cefalosporínico desde el interior del microorganismo productor de cefalosporina hacia el exterior del microorganismo productor de cefalosporina, y con lo que la relación de la capacidad de producción de cefalosporina de la cepa de Penicillium transformada con el gen CefT heterólogo en comparación con la capacidad de producción de cefalosporina de la cepa de Penicillium no transformada con el gen CefT heterólogo es al menos 1, 2.
2. Un microorganismo productor de cefalosporina según la reivindicación 1, caracterizado por que el gen CefT heterólogo que codifica una proteína CefT que es una proteína implicada en el transporte de un compuesto cefalosporínico desde el interior del microorganismo productor de cefalosporina hacia el exterior del microorganismo productor de cefalosporina deriva de Acremonium, preferiblemente de Acremonium chr y sogenum, lo más preferible de Acremonium chr y sogenum C10, o es un homólogo de dicho gen CefT que codifica una proteína CefT con una identidad de más de 30% en base a la proteína cuando se compara con la proteína CefT de Acremonium chr y sogenum C10.
3. Un método para la construcción de una cepa de Penicillium según cualquiera de las reivindicaciones 1-2, que comprende las etapas de:
a. Aislar el gen CefT de un hospedante adecuado; y
b. Transformar la cepa de Penicillium productora de cefalosporina con el gen CefT aislado en la etapa a,
con la condición de que el hospedante y el microorganismo productor de cefalosporina no sea el mismo organismo.
4. Un procedimiento para la producción de una cefalosporina, que comprende cultivar la cepa de Penicillium productora de cefalosporina según cualquiera de las reivindicaciones 1-2.
5. Un procedimiento según la reivindicación 4, en el que la cefalosporina se selecciona del grupo que consiste en los derivados N-acilados de 7-ADCA, 7-ACA, 7-ACCA y de ácido 7-amino-3-carbamoil-oximetil-3-cefem-4-carboxílico.
Patentes similares o relacionadas:
Proceso para la producción de compuestos 3-alquenilcefem, del 10 de Mayo de 2017, de OTSUKA CHEMICAL CO., LTD.: Un proceso para la preparación del ácido 7-amino-3-[(E/Z)-2-(4-metiltiazol-5-il)vinil]-3-cefem-4-carboxílico de fórmula y una sal de un metal alcalino del […]
Sales de clorhidrato de un compuesto antibiótico, del 20 de Enero de 2016, de Theravance Biopharma Antibiotics IP, LLC: Un compuesto de fórmula I:**Fórmula** en el que x está en el intervalo de 1 a 2.
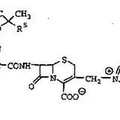 Compuestos de cefem, del 1 de Abril de 2015, de ASTELLAS PHARMA INC.: Un compuesto de la fórmula [I]: (Ver fórmula) en la que R 1 es alquilo C1-C6, hidroxialquilo (C1-C6) o haloalquilo (C1-C6), y R 2 es hidrógeno o un grupo protector amino, […]
Compuestos de cefem, del 1 de Abril de 2015, de ASTELLAS PHARMA INC.: Un compuesto de la fórmula [I]: (Ver fórmula) en la que R 1 es alquilo C1-C6, hidroxialquilo (C1-C6) o haloalquilo (C1-C6), y R 2 es hidrógeno o un grupo protector amino, […]
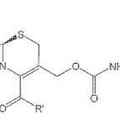 Compuesto de cefem, del 10 de Abril de 2013, de DSM Sinochem Pharmaceuticals Netherlands B.V: Un compuesto de cef-3-em caracterizado por la fórmula [I]
o una sal o éster del mismo,
en el que R se selecciona del grupo que consiste […]
Compuesto de cefem, del 10 de Abril de 2013, de DSM Sinochem Pharmaceuticals Netherlands B.V: Un compuesto de cef-3-em caracterizado por la fórmula [I]
o una sal o éster del mismo,
en el que R se selecciona del grupo que consiste […]
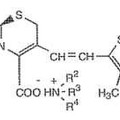 Compuestos de 3-alquenilcefem y procedimiento para su producción, del 16 de Mayo de 2012, de OTSUKA CHEMICAL CO., LTD.: Un compuesto de 3-alquenilcefem de fórmula **Formula**
en la que R1 es bencilo o fenoximetilo, R2, R3 y R4 son iguales o diferentes, siendo cada uno de ellos un […]
Compuestos de 3-alquenilcefem y procedimiento para su producción, del 16 de Mayo de 2012, de OTSUKA CHEMICAL CO., LTD.: Un compuesto de 3-alquenilcefem de fórmula **Formula**
en la que R1 es bencilo o fenoximetilo, R2, R3 y R4 son iguales o diferentes, siendo cada uno de ellos un […]
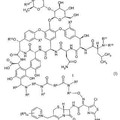 Antibióticos entrecruzados de glucopéptidos y cefalosporinas, del 2 de Mayo de 2012, de THERAVANCE, INC.: Un compuesto con la fórmula I:
O una sal farmacológicamente aceptable del mismo, en el que R1 es -Ya- (W) n-Yb-; R2 es hidrógeno o un alquilo C1-6; cada R3 se […]
Antibióticos entrecruzados de glucopéptidos y cefalosporinas, del 2 de Mayo de 2012, de THERAVANCE, INC.: Un compuesto con la fórmula I:
O una sal farmacológicamente aceptable del mismo, en el que R1 es -Ya- (W) n-Yb-; R2 es hidrógeno o un alquilo C1-6; cada R3 se […]
Procesos para producir compuestos de 3-cefem, del 18 de Abril de 2012, de OTSUKA KAGAKU KABUSHIKI KAISHA: Un proceso para preparar un compuesto de 3-halogenometilcefem de la fórmula o una sal del mismo en la que X1 es un átomo de halógeno, caracterizado por que […]
PROCEDIMIENTO PARA LA PREPARACIÓN DE CEFOTETÁN, del 2 de Noviembre de 2011, de ACS DOBFAR S.P.A.: Procedimiento para la obtención de cefotetán purificado, de fórmula (l) **Fórmula** que contiene no más del 0,2% del tautómero de fórmula (ll) **Fórmula** […]