Direccionamiento a células de cáncer usando nanopartículas.
Una nanopartícula furtiva específica de diana que comprende:
una matriz polimérica y un agente terapéutico;
donde la matriz polimérica comprende un polímero no funcionalizado que comprende un copolímero de ácido poliláctico y polietilenglicol o poli(ácido láctico-co-ácido glicólico) y polietilenglicol; y
un polímero conjugado con un ligando unido covalentemente a un ligando PSMA de bajo peso molecular;
donde el ligando PSMA de bajo peso molecular es de Fórmulas I, II, III o IV:^**Fórmula**
y sus enantiómeros, estereoisómeros, rotámeros, tautómeros, diastereómeros o racematos;
donde
m y n son cada uno, independientemente, 0, 1, 2 o 3; p es 0 o 1;
R1, R2, R4 y R5 se seleccionan cada uno, independientemente, del grupo que consiste en alquilo sustituido o no sustituido, arilo sustituido o no sustituido y cualquier combinación de estos; y
R3 es H o alquilo C1-6;
y donde R1, R2, R4 y R5 comprenden un punto de unión a la nanopartícula.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11186037.
Solicitante: BIND Therapeutics, Inc.
Inventor/es: ZALE,STEPHEN,E, ALI,Mir Mukkaram.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/337 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos de cuatro eslabones, p. ej. taxol.
- A61K9/14 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › en estado especial, p. ej. polvos (microcápsulas A61K 9/50).
- A61K9/48 A61K 9/00 […] › Preparaciones en cápsulas, p. ej. de gelatina, de chocolate.
- A61K9/51 A61K 9/00 […] › Nanocápsulas.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
- B82B1/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B82 NANOTECNOLOGIA. › B82B NANOESTRUCTURAS FORMADAS POR MANIPULACION DE ATOMOS O MOLECULAS INDIVIDUALES, O COLECCIONES LIMITADAS DE ATOMOS O MOLECULAS COMO UNIDADES DISCRETAS; SU FABRICACION O TRATAMIENTO. › Nanoestructuras formadas por manipulación de átomos o moléculas individuales, o colecciones limitadas de átomos o moléculas como unidades discretas.
PDF original: ES-2510396_T3.pdf


Fragmento de la descripción:
Direccionamiento a células de cáncer usando nanopartículas Campo de la invención
La presente invención se refiere en general a composiciones farmacéuticas que comprenden nanopartículas furtivas específicas de diana útiles en el tratamiento del cáncer.
Antecedentes
La administración de un fármaco a un paciente con liberación controlada del principio activo ha sido un área de investigación activa durante décadas y se ha visto alimentada por los muchos desarrollos recientes en la ciencia de polímeros. Además, pueden diseñarse sistemas poliméricos de liberación controlada para proporcionar un nivel de fármaco en el intervalo óptimo a lo largo de un periodo de tiempo más prolongado que otros procedimientos de administración de fármacos, aumentando de este modo la eficacia del fármaco y minimizando los problemas con la conformidad del paciente.
Se han desarrollado partículas biodegradables como vehículos de liberación sostenida usados en la administración de fármacos de pequeño tamaño molecular, proteínas y fármacos peptfdicos y ácidos nucleicos. Los fármacos se encapsulan típicamente en una matriz polimérica que es biodegradable y biocompatible. A medida que se degrada el polímero y/o a medida que el fármaco difunde hacia afuera del polímero, el fármaco se libera en el cuerpo.
El direccionamiento de sistemas poliméricos de liberación controlada (por ejemplo, dirigidos a un tejido o tipo celular particular o dirigidos a un tejido enfermo específico pero no a tejido normal) es deseable porque reduce la cantidad de fármaco presente en los tejidos del cuerpo que no están fijados como objetivo. Esto es particularmente importante cuando se trata una afección tal como el cáncer, en la que es deseable que se administre una dosis citotóxica del fármaco a células cancerosas sin destruir el tejido no canceroso circundante. El direccionamiento de fármacos eficaz debería reducir los efectos secundarios indeseables y a veces potencialmente mortales comunes en la terapia anticancerosa. Además, el direccionamiento puede permitir que los fármacos alcancen ciertos tejidos que de otro modo serían incapaces de alcanzar sin una nanopartícula dirigida.
Por consiguiente, existe la necesidad de desarrollar sistemas de administración que puedan administrar niveles terapéuticos de fármaco para tratar enfermedades tales como el cáncer, al tiempo que reduzcan también los efectos secundarios en el paciente.
Sumario de la invención
Continúa existiendo la necesidad de composiciones útiles en el tratamiento o la prevención o la mejora de uno o más síntomas de cáncer, particularmente cánceres que expresan antfgeno de membrana específico de próstata (PSMA), incluyendo, pero sin limitación, cáncer de próstata, cáncer pulmonar no microcítico, carcinoma colorrectal y lioblastoma, y tumores sólidos que expresan PSMA en la neovasculatura tumoral. En un aspecto, la invención proporciona una nanopartícula furtiva, que comprende:
una matriz polimérica y un agente terapéutico;
donde la matriz polimérica comprende un polímero no funcionalizado que comprende un copolfmero de ácido poliláctico y polietilenglicol o poli(ácido láctico-co-ácido glicólico) y polietilenglicol; y
un polímero conjugado con un ligando unido covalentemente a un ligando PSMA de bajo peso molecular;
donde el ligando PSMA de bajo peso molecular es de Fórmulas I, II, III o IV:
I
II
III
y su enantiómeros, estereoisómeros, rotámeros, tautómeros, diastereómeros o racematos;
donde
m y n son cada uno independientemente 0, 1, 2 o 3; p es 0 o 1;
R1, R2, R4 y R5 se seleccionan cada uno, independientemente, del grupo que consiste en alquilo sustituido o no sustituido, arilo sustituido o no sustituido, y cualquier combinación de estos; y
R3 es H o alquilo C1-6,
y donde R1, R2, R4 y R5 comprenden un punto de unión a la nanopartfcula.
En otra realización de la nanopartfcula furtiva específica de diana de la invención, el ligando PSMA de bajo peso molecular tiene un peso molecular inferior a 1000 g/mol.
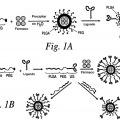
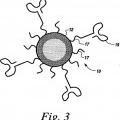
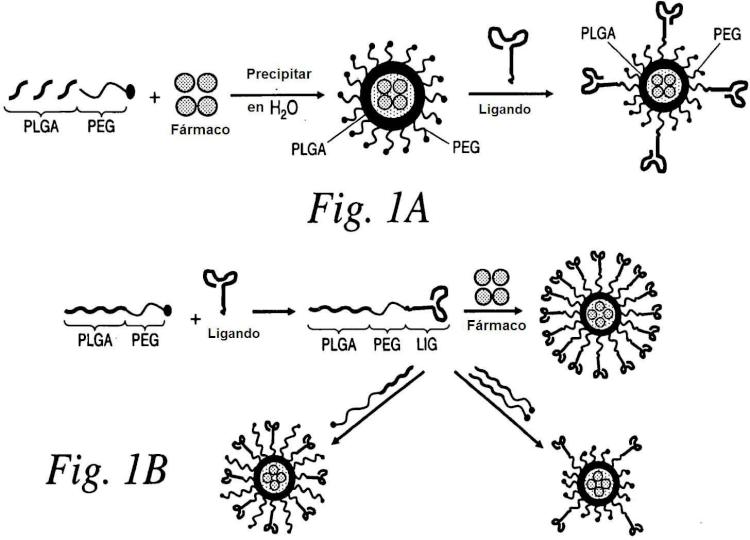
En la nanopartfcula furtiva específica de diana de la invención, la nanopartfcula comprende una matriz polimérica, donde la matriz polimérica comprende un polímero no funcionalizado que comprende un copolímero de PLA y PEG o PLGA y PEG, y un polímero conjugado con un ligando unido a un ligando PSMA de Fórmula I, II, III o IV. En otra realización, la matriz polimérica comprende PLGA o PLA y un copolímero de PLGA o PLA y PEG.
Una porción de la matriz polimérica comprende un polímero conjugado con un ligando comprende un polímero conjugado con un ligando unido covalentemente al ligando PSMA de bajo peso molecular. En una realización, el polímero conjugado con un ligando comprende un copolímero de ácido poliláctico y polietilenglicol o poli(ácido láctico-co-ácido glicólico) y polietilenglicol. En otra realización, la matriz polimérica está unida covalentemente al ligando PSMA de bajo peso molecular a través del extremo libre de PEG. En otra realización más, la matriz polimérica está unida covalentemente al ligando PSMA de bajo peso molecular a través de un grupo carboxilo en el extremo libre de PEG. En otra realización más, la matriz polimérica está unida covalentemente al ligando PSMA de bajo peso molecular a través de un grupo funcional maleimida en el extremo libre de PEG.
En otro aspecto, la invención proporciona una composición farmacéutica que comprende una pluralidad de nanopartículas furtivas específicas de diana como las que se definen en la presente.
En otro aspecto, la invención proporciona una composición farmacéutica de la invención para su uso en el tratamiento del cáncer. En una realización, la composición farmacéutica es para su uso en el tratamiento de un tumor sólido prostético o no prostético. En otra realización, la composición farmacéutica es para su uso en el tratamiento de un tumor sólido prostético o no prostético en el que se expresa PSMA en la neovasculatura tumoral. En otra realización, la composición farmacéutica es para su uso en el tratamiento del cáncer de próstata, carcinoma pulmonar no microcítico, carcinoma colorrectal o glioblastoma.
En una realización de la composición farmacéutica de la invención, la nanopartfcula tiene una cantidad de resto de dirección eficaz para el tratamiento del cáncer de próstata en un sujeto que lo necesite. En otra realización, la nanopartfcula tiene una cantidad de resto de dirección eficaz para el tratamiento de tumores sólidos que expresan PSMA en la neovasculatura tumoral en un sujeto que lo necesite. En otra realización más, el ligando de PSMA de bajo peso molecular tiene una K¡ de entre 0,5 nM y 10 nM.
En una realización de la composición farmacéutica de la invención, la nanopartfcula tiene una cantidad de agente terapéutico eficaz para el tratamiento del cáncer de próstata en un sujeto que lo necesite. En otra realización, la nanopartícula tiene una cantidad de agente terapéutico eficaz para el tratamiento de tumores sólidos que expresan PSMA en la neovasculatura tumoral en un sujeto que lo necesite.
En otra realización de la composición farmacéutica de la invención, la nanopartícula tiene una proporción de polímero unido a ligando respecto a polímero no funcionalizado eficaz para el tratamiento del cáncer de próstata. En otra realización, los polímeros de la matriz polimérica tienen un peso molecular eficaz para el tratamiento del cáncer de próstata. En otra realización más, la nanopartícula tiene una carga superficial eficaz para el tratamiento del cáncer de próstata.
En otra realización de la composición farmacéutica de la invención, dicho sistema es adecuado para el tratamiento específico de diana de una enfermedad o trastorno y la administración de un agente terapéutico. En otra realización, la nanopartícula comprende además un agente terapéutico. En una realización, el agente terapéutico se asocia con la superficie de, se encapsula en el interior de, se rodea por o se dispersa a través de la nanopartfcula. En otra realización más, el agente terapéutico se encapsula en el interior del núcleo hidrófobo de la nanopartícula. En realizaciones particulares, el agente terapéutico se selecciona del grupo que consiste en mitoxantrona y docetaxel.
En otro aspecto, la invención proporciona la composición farmacéutica de la invención para su uso en un método de tratamiento del cáncer de próstata en un sujeto que lo necesite. En una realización, la composición farmacéutica se administra directamente a la próstata de un sujeto. En otra realización más, la composición farmacéutica... [Seguir leyendo]
Reivindicaciones:
1. Una nanopartícula furtiva específica de diana que comprende: una matriz polimérica y un agente terapéutico;
donde la matriz polimérica comprende un polímero no funcionalizado que comprende un copolímero de ácido poliláctico y polietilenglicol o pol¡(ác¡do láctico-co-ácido glicólico) y polietilenglicol; y
un polímero conjugado con un ligando unido covalentemente a un ligando PSMA de bajo peso molecular;
donde el ligando PSMA de bajo peso molecular es de Fórmulas I, II, III o IV:
i n in iv
y sus enantiómeros, estereoisómeros, rotámeros, tautómeros, diastereómeros o racematos; donde
m y n son cada uno, Independientemente, 0, 1, 2 o 3;
p es 0 o 1;
R1, R2, R4 y R5 se seleccionan cada uno, independientemente, del grupo que consiste en alquilo sustituido o no sustituido, arilo sustituido o no sustituido y cualquier combinación de estos; y
R3 es H o alquilo C1-6;
y donde R1, R2, R4 y R5 comprenden un punto de unión a la nanopartícula.
2. La nanopartícula furtiva específica de diana de la reivindicación 1, donde el ligando PSMA de bajo peso molecular tienen un peso molecular menor de 1000 g/mol.
3. La nanopartícula furtiva específica de diana de cualquiera de las reivindicaciones 1-2, donde el polímero conjugado con un ligando comprende un copolímero de ácido poliláctico y polietilenglicol o polijácido láctico-co-ácido glicólico) y polietilenglicol.
4. La nanopartícula furtiva específica de diana de la reivindicación 13, donde el polímero conjugado con un ligando está unido covalentemente al ligando PSMA de bajo peso molecular a través de un grupo carboxilo o un grupo funcional maleimida en el extremo libre de PEG.
5. La nanopartícula furtiva específica de diana de cualquiera de las reivindicaciones 1-4, donde el agente terapéutico es docetaxel.
6. La nanopartícula furtiva específica de diana de cualquiera de las reivindicaciones 1-5, donde R1, R2, R4 y R5 son cada uno, independientemente, alquilo C1-6 o fenllo, o cualquier combinación de alquilo C1-6 o fenilo, que están independientemente sustituidos una o más veces con OH, SH, NH2 o C02H, y donde el grupo alquilo puede estar interrumpido por N(H), S u O.
7. La nanopartícula furtiva específica de diana de cualquiera de las reivindicaciones 1-6, donde el ligando
| PSMA de bajo peso molecular es | ||
| f?1 | O | co2h |
| HOjC-l | X | irC02H |
| H H | N | |
| H | H |
y sus enantiómeros, estereoisómeros, rotámeros, tautómeros, diastereómeros o racematos; donde R1 es alquilo C1- 6 o fenilo, o cualquier combinación de alquilo C1-6 o fenilo, independientemente sustituido una o más veces con OH, SH, NH2 o C02H, donde el grupo alquilo puede estar interrumpido por N(H), S u O, y donde R1 comprende un punto de unión covalente a la nanopartícula.
8. La nanopartícula furtiva específica de diana de cualquiera de las reivindicaciones 1-6, donde el polímero
conjugado con un ligando es representado por:
o ch3 o r o
O O z nnr;_
O
J y
R
CH3
O CH3
° Y^°if' 'W-Y'
O
,Ra
`R1 O
z H02C-L X Jt~C02H
iríl B h
o 9 «£»
y
O o
z
co2h
co2h
donde R1, R2, R3, R4 y R5 tienen las definiciones descritas para las Fórmulas I, II, III o IV en la reivindicación 1 o 6, y donde R7 y Rg son grupos alquilo, Rs es un enlace de tipo éster o amida, X = fracción molar de 0 a 1, Y = fracción molar de 0 a 0.5, X+Y = de 20 a 1720 y Z = de 25 a 455.
9. La nanopartícula furtiva específica de diana de cualquiera de las reivindicaciones 1-8, donde el polímero conjugado con un ligando es representado por:
o ch3 o
CH O O
O
O J y
co2h
R° o S
h°2c^nAn^co2h
H H H H
donde Ri es alquilo C1-6 o fenilo, o cualquier combinación de alquilo C1-6 o fenilo, Independientemente sustituido una o más veces con OH, SH, NH2 o C02H, donde el grupo alquilo puede estar Interrumpido por N(H), S u O; R7 y Rg son grupos alquilo; R8 es un enlace de tipo áster o amida, X = fracción molar de 0 a 1, Y = fracción molar de 0 a 0.5, X+Y = de 20 a 1720 y Z = de 25 a 455.
10. La nanopartícula furtiva específica de diana de la reivindicación 9, donde X es una fracción molar de 1 e Y es una fracción molar de 0.
11. La nanopartícula furtiva específica de diana de las reivindicaciones 9 o 10, donde el polímero conjugado con un ligando es representado por:
R,*'
| - | |
| o | |
| CH3 0 | 0 |
r2.
O
°'R^NH
ho2c
o
donde R-i y R3 son grupos alquilo, y R2 es un grupo áster o amida.
12. La nanopartícula furtiva específica de diana de una cualquiera de las reivindicaciones 1-4 o 6-11, en la que el agente terapéutico se selecciona del grupo que consiste en agentes quimioterápicos tales como doxorubicina, gemcitabina, daunorubicina, procarbazina, mitomicina, citarabina, etopósido, metotrexato, 5-fluorouracilo, vinblastina, vincristina, bleomicina, paclitaxel, docetaxel, aldesleucina, asparaginasa, busulfán, carboplatino, cladribina, camptotecina, CPT-1.1, 10-hidroxi-7-etilcamptotecina, dacarbazina, S-l capecitabina, ftorafur, 5desoxiflurouridina, UFT, eniluracilo, desoxicitidina, 5-azacitosina, 5-azadesoxicitosina, alopurinol, 2-cloroadenosina, trimetrexato, aminopterina, metilen- 10-desazaaminopterina, oxaplatino, picoplatino, tetraplatino, satraplatino, platino-DACH, ormaplatino, CI-973, JM-216 y análogos de los mismos, epirubicina, 9-am¡nocamptotec¡na, 10,11- metilendioxicamptotecina, 9-nitrocamptotecina, TAS 103, vindesina, mostaza de L-fenilalanina, ifosfamida, mafosfamida, perfosfamida, trofosfamida carmustina, semustina, epotilonas A-E, tomudex, 6-mercaptopurina, 6- tioguanina, amsacrina, fosfato de etopósido, karenitecina, aciclovir, valaciclovir, ganciclovir, amantadina, rimantadina, lamivudina, zidovudina, bevacizumab, trastuzumab, rituximab y 5-fluorouracilo y combinaciones de los mismos, o un ARNip.
13. La nanopartícula furtiva específica de diana de una cualquiera de las reivindicaciones 16 o 6-11, en la que el agente terapéutico se selecciona del grupo que consiste en mitoxantrona y docetaxel.
14. Una composición farmacéutica que comprende una pluralidad de nanopartículas especificas de diana como se define en cualquiera de las reivindicaciones 1-13.
15. Una composición farmacéutica de la reivindicación 14, para su uso en el tratamiento del cáncer.
16. La composición farmacéutica para el uso de la reivindicación 15, para su uso en el tratamiento de un tumor 5 sólido prostético o no prostético.
17. La composición farmacéutica para el uso de la reivindicación 16, para su uso en el tratamiento de un tumor sólido prostético o no prostético en el que se expresa PSMA en la neovasculatura tumoral.
18. La composición farmacéutica para el uso de la reivindicación 15, para su uso en el tratamiento del cáncer de próstata, carcinoma pulmonar no microcítico, carcinoma colorrectal o glioblastoma.
19. Una nanopartícula furtiva específica de diana que comprende un agente terapéutico y un compuesto de
fórmula:
F¡7
| - 0 ch3 | 0 |
| 'A'V | °^'o-^y/ |
| o> n X O | O L J > X |
| ------1 O O X *____I | - O |
| ''° T'°n | |
| 1----- O X u 1 O | O |
co2h
H H H H
y 9 Wn
co2h co2h
(OR* )p ' "
O CH3 u
VoV^W
ch3 o
o HS^>o^^co2h
'K0'^t0vR^R4/ C02H
O CH,
ch3 o.o L J H
o o
co2h
donde R1, R2, R3, R4 y R5 tienen las mismas definiciones descritas para las Fórmulas I, II, III o IV en la reivindicación 1 o 6, y donde R7 y R9 son grupos alquilo, R8 es un enlace de tipo éster o amida, X = fracción molar de 0 a 1, Y = fracción molar de 0 a 0.5, X+Y = de 20 a 1720 y Z = de 25 a 455.
20. La nanopartícula furtiva específica de diana de la reivindicación 19, donde el compuesto es de fórmula:
Patentes similares o relacionadas:
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Profármacos de gemcitabina, del 29 de Julio de 2020, de NuCana plc: Una formulación farmacéutica que comprende gemcitabina-[fenil-benzoxi-L-alaninil)]-(S)-fosfato 3: **(Ver fórmula)** o una sal o solvato […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Complejos de agentes terapéuticos de base vírica y poli(beta-amino-ésteres) modificados, del 29 de Julio de 2020, de Sagetis Biotech, SL: Un complejo de un agente terapéutico de base vírica con un polímero de fórmula I: **(Ver fórmula)** donde cada L1 y L2 están seleccionados […]
Compuestos de alquinilbenceno heterocíclicos, y composiciones médicas y usos de los mismos, del 29 de Julio de 2020, de Guangzhou Healthquest Pharma Co., Ltd: Un compuesto de alquinilbenceno heterocíclico que tiene la fórmula (I) y una sal farmacéuticamente aceptable, o estereoisómero del mismo, **(Ver […]
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.